第二节、水中无机污染物的迁移转化
电子教案与课件:《环境化学》课件 6 水中无机物的迁移转化

Free template from
• 水和氧化物胶体对重金属离子有较强的专属吸附作用,这种吸附作用 发生在胶体双电层的Stern层中,被吸附的金属离子进入Stern层后, 不能被通常提取交换性阳离子的提取剂提取,只能被亲和力更强的金 属离子取代。
• 表 水合氧化物对金属离子的专属吸附与非专属吸附的区别
2021/2/20
Free template from
• 1)、矿物微粒和黏土矿物
• 天然水中常见矿物微粒为石英、长石、云 母及黏土矿物等硅酸盐矿物。
• 天然水中具有显著胶体化学特性的微粒是 黏土矿物。主要为铝或镁的硅酸盐。
2021/2/20
Free template from
了水中主要溶质的性质。一个厌氧性湖泊。其湖下层的元 素都将以还原形态存在:碳还原成-4价形成CH4;氮形成 NH+4;硫形成H2S;铁形成可溶性Fe2+。而表层水由于可以 被大气中的氧饱和。成为相对氧化性介质,如果达到热力 学平衡时,上述元素将以氧化态存在:碳形成CO2;氮形 成NO-3;铁形成Fe(OH)3沉淀;硫形成SO2-4.显然这种变化 对水生生物和水质影响很大。
2021/2/20
Free template from
• 5)、其他
• 湖泊中的藻类,污水中的细菌、病毒,废 水排出的表面活性剂、油滴等,也都有类 似的胶体化学表现,起类似的作用。
2021/2/20
Free template from
2021/2/20
Free template from
氧化还原
2021/2/20
Free template from
• 氧化还原平衡对水环境中污染物的迁移转化具有重要意义。 水体中氧化还原的类型。速率和平衡,在很大程度上决定
环境化学教案 第三节水中无机污染物的迁移转化(氧化还原2)
由此反应可知,当有机物进入天然水后,水体中溶解氧的含量会迅速降低。如果有机物的数量非常多的话,可以使水体中溶解氧全部被消耗掉,甚至可以使水体转换成为沼泽。在水中,NH4+只有被氧化成NO3-后,氮才能被藻类利用。
例2求被大气氧所饱合的中性天然水的pE值。
解:该体系溶解氧起决定电势作用,溶解氧的氧化还原反应为:
pE=pE0+ [H+]
已知:pE0=20.75
pH=7 [H+]=10-7
将已知条件代入pE的表达式,得:pE=13.58。该体系pE值较高,是一个氧化性体系。
例3求微生物作用产生甲烷的中性厌氧水的pE值及溶解氧的分压
天然水是一个非常复杂的混合体系,其中存在着众多的氧化剂和还原剂。其中常见的氧化剂包括溶解氧、Mn(IV)、Fe(III)、和S(VI),常见的还原剂包括有机物、Mn(II)、Fe(II)、S(-II)。当我们要求得某种天然水的pE值时,首先需要确定哪种物质起决定电势作用,然后根据起决定电势作用物质的氧化还原反应,求得体系的pE值。一般的天然水体中起决定电势作用的物质是溶解氧,当有机物含量非常高时,则有机物起决定电势作用。铁和锰起决定电势作用的情况则比较少见。下面我们来看两种极端情况下体系的pE值。
pE=-4.13
将已知条件代入pE的表达式,得: =3.0×10-72atm。
由此可见该体系中溶解氧的分压非常低,一般水体中的溶解氧的分压均超过此值。由于天然水的pE值随水中溶解氧的减少而降低,因此表层水pE值较高,底层水pE值较低。
例3:从湖水中取出深层水,其PH=7.0,含溶解氧浓度0.32mg/L,请计算PE和Eh。(KH=1.26*10-8[mol/(L·Pa)]
无机污染物迁移、转化和归宿

无机污染物进入河流中的迁移、转化和归宿对无机污染物而言,特别是重金属和准金属等污染物,一旦进入水环境,均不能被生物降解,而其他大部分无机污染物经过分解,转化形态之后可以组成生物细胞的成分而被彻底利用,包括无机元素与金属元素。
无机污染物(以重金属为主体)主要是以简单的离子、络离子或可溶性分子的形式在水环境中通过一系列物理化学作用,如溶解--沉淀作用、氧化--还原作用、水解作用、络合和螯合作用、吸附--解吸作用等实现的迁移和转化,参与和干扰各种环境化学过程和物质循环过程。
重金属(Hg、Cd等)在迁移过程中可富集于底泥,成为长期潜在的有害污染源或通过食物链富集。
污染物在迁移转化的过程中,主要受污染物自身的理化性质以及外界环境的物理化学条件和自然地理条件影响。
简单的内部因素可主要为组成化合物的能力、形成不同价位离子的能力、水解能力、形成络合物的能力和被胶体吸附的能力。
一般来说,由共价键结合的污染物容易进行气迁移;由离子键结合容易进行水迁移。
外部因素主要指环境的酸碱环境、氧化还原条件、交替种类以及数量和性质等。
如酸性环境有利于钙、锶、钡、锌、镉等迁移;碱性环境则有利于硒、钼和五价钒的迁移。
氧化条件有利于铬、钒、硫的迁移;还原环境有利于铁、锰等的迁移。
从微生物的角度以及水体溶解氧的情况(水体复氧及耗氧)来分析无机污染物进入河流的迁移转化问题,我们需要考虑到,在河流表层部分,溶解氧较充足,处于较高的氧化还原电位,主要存在好养性微生物,其元素将以氧化态存在,碳成为CO2,氮成为NO3-,铁成为Fe(OH)3沉淀,硫成为SO42-;在中间部分,溶解氧相对较少,是一个兼型层,兼有氧化和还原作用,主要由兼性微生物生存;在底层,水体处于还原环境,其元素都将以还原形态存在,碳还原成CH4,氮形成NH4+,硫形成H2S,铁形成可溶性Fe2+。
在相应微生物作用下,完成相应元素的物质循环。
综上分析,污染物的转化,往往与迁移相伴进行,并且实现污染物迁移的途径是彼此相互作用的,是一个统一体,并不能将其独立开来,对于自净体系而言,无机污染物迁移转化的过程较为复杂,下图简以说明。
【环境化学】第3.2章 水环境化学——水中无机污染物的配合作用

总反应:Zn2++2NH3→Zn(NH3)22+ β2 总反应:Zn2++3NH3→Zn(NH3)32+ β3 总反应:Zn2++4NH3→Zn(NH3)42+ β4
逐级稳定常数:K1、 K2 、 K3 、 K4 累积稳定常数: β1 、 β2 、 β3 、 β4 累积稳定常数与逐级稳定常数的关系
设:α={ 1+ β1 [OH-]+ β2 [OH-]2+ β3[OH-]3 + β4 [OH-]4 }
得:[Me]T= [Me2+]·α
11
第三章/第二节/2.5 配合作用
2.5.4 金属配合物
一、羟基对金属离子的配合作用
2. 各种羟基配合物占金属总量的百分数φ 各种羟基配合物的比例
φ0= [Me2+] / [Me]T =1/ α φ1= [Me(OH)+] / [Me]T = {β1[Me2+][OH-] }/ [Me]T = β1[OH-] / α = φ0 β1[OH-] φ2 = [Me(OH)2] / [Me]T = φ0 β2[OH-] 2 φ3 = [Me(OH)3-] / [Me]T = φ0 β3[OH-] 3 φ4 = [Me(OH)42-] / [Me]T = φ0 β4[OH-]4
Hum
COO O
Fe
OH (H2O)-x-1
+ H+
[ Hum
COO O
Fe
OOHH(H2O)x-2]+2H+
在低pH时,从腐植质的酸性基团中置换出一个质子。 在高pH时,则从金属水合物中的水分子中释放出一个质子。
20
第三章/第二节/2.5 配合作用
第11讲水中有机污染物的迁移转化

Kp=Koc[0.2(1-wf)wocs+wfwocf]
其中,Wf—细颗粒的质量分数(d<50um) wocs—粗颗粒组分的有机碳含量 wocf—细颗粒组分的有机碳含量
第11讲水中有机污染物的迁移转化
憎水有机物的Koc与辛醇-水分配系数的关系
Koc =0.63 Kow Kow—辛醇-水分配系数,即化学物质在辛醇中和水中的 浓度比
第11讲水中有机污染物的迁移转化
三、水解反应速度 ❖ 通常有机物的水解是一级反应
❖ 半衰期与有机物属性、温度、 pH有关,与有机物 初始浓度无关.
第11讲水中有机污染物的迁移转化
水解速率与pH的关系
❖ Mabey等把水解速率归纳为
◎酸性催化过程 ◎碱性催化过程 ◎中性催化过程
❖ 水解速率为三个催化过反应速度的和:
❖ 有机物在沉积物与水之间的分配
Kp —分配系数(与沉积物中有机质浓度有关) cT —总有机物浓度(μg/L) cs —沉积物中有机物浓度(μg/kg) cw —溶解在溶液中的有机物浓度(μg/L) cp —沉积物浓度(kg/L)
第11讲水中有机污染物的迁移转化
标化分配系数Koc
Koc=Kp/Xoc Xoc—沉积物中有机碳的质量分数。 对非极性有机物,Koc与沉物性质无关
式中: αw——有机毒物可溶解相分数 c,cT—有机物溶解相中的浓度和 表示化学物质在气—液相达到平衡时,溶解 于水相的浓度与气相中化学物质浓度(或分压 力)有关: p=KHcw
式中:p—污染物在大气中的平衡分压,Pa; cw——污染物在水中平衡浓度,mol/m3; KH——亨利定律常数, Pa·m3/mol。
❖ Kow和溶解度的关系
E-第三章第一讲

以上属于封闭的水溶液体系的情况,,没 有考虑溶解性CO2与大气交换过程,因 而实际上,根据气体交换动力学, CO2 在气液界面的平衡时间需数日。因此, 若所考虑的溶液反应在数小时之内完成, 就可应用封闭体系固定碳酸化合态总量 的模式加以计算。反之,如果所研究的 过程是长时期的,例如一年期间的水质 组成,则认为CO2与水是处于平衡状态, 可以更近似于真实情况。
②CO2的溶解度
25℃时水中[CO2]的值可以用亨利定律来计算。 已知干空气中CO2 的含量为0.0314%(体积), 水在250C时蒸汽压为0.03167×105pa,CO2 的 亨利定律常数是3.34×10-7mol/(L· Pa)(25℃), 则CO2在水中的溶解度为: PCO2=(1.0130-0.03167)×105×3.14×10-4 =30.8Pa [CO2]=3.34×10-7×30.8=1.O28×10-5mol/L
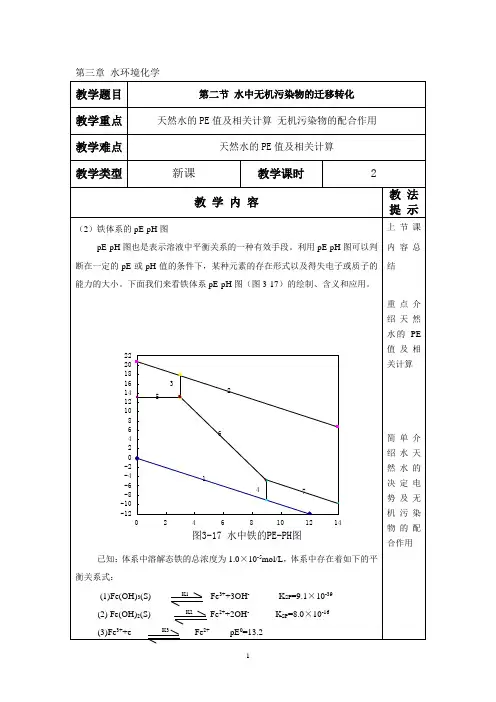
假如存在固体Fe(OH)3(s),则 Fe(OH)3(s)+3H+→ Fe3++3H2O [Fe3+]/[H+]3=9.1×103 在pH=7时: [Fe3+]=9.1×103×(1.0×10-7)3=9.1×10-18mol/L 将这个数值代人上面的方程式中,即可得出其他 各形态的浓度: [Fe(OH)2+]=8.1×10-14mol/L [Fe(OH)2+]=4.5×10-10mol/L [Fe2(OH)24+]=1.O2×10-23mol/L 很明显,在近于中性的天然水溶液中,水合铁离 子的浓度可以忽略不计。
氧在水中的溶解度与水的温度、氧在水中的 分压及水中含盐量有关。氧在1.0130×105Pa、 250C和水中的溶解度,可按下面步骤计算。 首 先 从 表 3-2 可 查 出 水 在 250C 的 蒸 汽 压 为 0.03167×105pa,由 于干 空 气中 氧的 含 量为 20.95%,所以氧的分压为: pO2=(1.0130-0.03167)×105×0.2095 =0.2056×105pa 代入亨利定律可求出氧在水中的摩尔浓度为: [O2(aq)]= KH·G p =1.26×10-8×0.2056×105 =2.6×10-4mol/L 氧的分子量为32,因此其溶解度为8.32mg/L。
第三章 水中无机污染物的迁移转化
氧:30%~35%, 氢:4%~6%, 氮:2%~4%
富里酸 :
碳和氮:44%~50%和1%~3%。氧:44%~50%
(不同地区和不同来源的腐殖质其分子量组成和元素组成都有区别)
腐殖质结构特点: 腐殖质结构特点
苯环、羧基、醇基和酚基
14
富里酸结构式
15
水环境中的配位作用--腐殖质配合作用 腐殖质配合作用
天然水、污水的氧化天然水、污水的氧化-还原反应
----微生物催化反应 ---电子迁移+质子迁移 氧化-还原反应缓慢 还原反应缓慢) (氧化 还原反应缓慢)
pE---pH 天然水体的 pE--pH 图
氧化还原体系,H+或OH¯参与转移。 pE除了与氧化态和还原态浓度有关外,受体系pH的影响,可以 用pE-pH 图来表示。 pE -pH 图可显示水中各形态的稳定范围及边界线。
胶体微粒吸附高分子电解质而凝聚。 聚合物具有链状分子,可以同时吸附在若干个胶体微粒上,在微 粒之间架桥粘结,使它们聚集成团。
(7)无机高分子的絮凝 (8)絮团卷扫絮凝 (9ห้องสมุดไป่ตู้颗粒层吸附絮凝 10) (10)生物絮凝
藻类、细菌等具有胶体性质,带电荷,发生凝聚。 胶体性质,带电荷,发生凝聚。 胶体性质
7
9
水体环境的氧化-还原作用
--污染物氧化还原转化 --污染物氧化还原转化 1. 2. 3. 4. 重金属 氮化物 硫 砷
砷可能存在的形态:H3AsO3、H2AsO3-、H3AsO4、H2AsO4-、 HAsO42-,最主要的是以H2AsO4-和HAsO42-五价形态存在。 pH< 4酸性水体,可能存在H3AsO4和AsO+ pH> l2.5碱性水体,还可能存在AsO43-,甚至HAsO32-及AsO33-形态
第11讲_水中有机污染物的迁移转化
13、He who seize the right moment, is the right man.谁把握机遇,谁就心想事成 。21.7.1521.7.1500:37:3000:37:30Jul y 15, 2021
❖
14、谁要是自己还没有发展培养和教 育好, 他就不 能发展 培养和 教育别 人。2021年7月 15日星 期四上 午12时 37分30秒00:37:3021.7.15
(2) 光量子产率与直接光解速率
❖ 一个分子被活化是由体系吸收光子进行的。 ❖ 分子被活化后,它可能进行光反应,也可能通过光辐射
的形式进行“去活化”再回到基态
(2) 光量子产率与直接光解速率
❖ 进行光化学反应的光子占吸收总光子数之比,称 为光量子产率(Φ)。
生成或破坏给定物种的摩尔数 体系吸收光子的摩尔数
❖ 当污染物在水中的浓度很低时,光被污染物吸收的平均 速率( I’αλ)为:
已知I Id (110Ld ) Is (110Ls ) j —单位转换系数,当I 的单
I ' I
E c
j( Ec)
I
E c
j
位为光子/cm2·s分子,C 的单位为mol/L时,
既, I ' K c,
K
E I
j
j=6.02×10-20
ci
KLc K g pc KL KHKg
Fz
KL (c ci )
KL (c
KLc K g pc KL KHKg
)
1
c pc KH Kg
KH 1 KL
KV
(c
c*)
其中, 1 1 1 , KV KL K g KH
c* Pc KH
图 双膜理论示意图
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
于晶格中离子的同晶替代造成的,例如硅氧四面体中的Si4+被
Al3+所取代,或者铝氢氧八面体中的Al3+被Mg2+所取代等,都会 产生这种永久负电荷。另一部分为可变电荷,主要随着环境pH
的改变而发生改变,原因是 Si-OH中的H+ 在碱性溶液中的离解。
Si-OH+OH-=Si-O-+H2O。
特征:这种吸附是一种可逆反应,能够迅速达到平衡。 不受温度影响,酸碱条件下均可进行,其交换吸附能力 与溶质的性质、浓度及吸附剂性质等有关。对于那些具 有可变电荷表面的胶体,当体系pH高时,也带负电荷并
n
以lgG对lgc作图可得一直线。lgk为截距,因此, k值是c=1时的吸附 1
n 量,它可以大致表示吸附能力的强弱。
浓度增长的强度。
该等温线不能给出饱和吸附量。 L型等温式为:G=G0c/(A+c)
为斜率,它表示吸附量随
式中:G0——单位表面上达到饱和时间的最大吸附量; A——常数。 G对c作图得到一条双曲线,其渐近线为G=G0,即当c→∞时,G→G0。 在等温式中A为吸附量达到时溶液的平衡浓度。 转化为:1/G = 1/G0 + (A/G0)(1/c)
1 以G
1 对 作图,同样得到一直线。 c
等温线在一定程度上反映了吸附剂与吸附物的特性,其形式在许
多情况下与实验所用溶质浓度区段有关。当溶质浓度甚低时,可能在 初始区段中呈现H型,当浓度较高时,曲线可能表现为F型,但统一起 来仍属于L型的不同区段。 影响吸附作用的因素有以下几种: 首先是溶液pH值对吸附作用的影响。在一般情况下,颗粒物对重金 属的吸附量随pH值升高而增大。当溶液pH超过某元素的临界pH值时, 则该元素在溶液中的水解、沉淀起主要作用。吸附量(G)与pH、平衡 浓度(C)之间的关系可用下式表示:G = A· C· 10BpH式中:A、B—常数。
第二节、水中无机污染物的迁移转化
一、颗粒物与水之间的迁移 二、水中胶体颗粒物聚集的基本原理和方式 三、溶解和沉淀 四、氧化—还原
五、配合作用
无机污染物,特别是重金属和准金属等污染物,一旦进入 水环境,不能被生物降解;
主要通过吸附 —解吸、沉淀 —溶解、氧化 —还原、配合作 用、胶体形成等一系列物理化学作用进行迁移转化,参与和 干扰各种环境化学过程和物质循环过程; 最终以一种或多种形式长期存留在环境中,造成永久性的 潜在危害。 重点介绍重金属污染物在水环境中迁移转化的基本原理。
锰与铁类似,其丰度虽然不如铁,溶解度比铁高,也 是常见的水合金属氧化物。
硅酸的单体 H4SiO4 ,若写成 Si(OH)4 ,则类似于多价金 属,是一种弱酸,过量的硅酸将会生成聚合物褐铁矿:Fe2O3﹒nH2O
水化赤铁矿:2Fe2O3﹒H2O 针铁矿:Fe2O3﹒H2O 水铝石:Al2O3﹒H2O 三水铝石:Al2O3﹒3H2O 二氧化硅凝胶:SiO2﹒nH2O 水锰矿:Mn2O3﹒H2O 所有的金属水合氧化物都能结合水中微量物质,同时其本身 又趋向于结合在矿物微粒和有机物的界面上。 水解 得到具有重要胶体作用的: [Al(OH)3]∞聚合无机高分子 [FeOOH]∞聚合无机高分子 [MnOOH]∞聚合无机高分子 [Si(OH)4]∞聚合无机高分子
O O
OH
OH Al OH OH
Si
O
O
O
O
(2)金属水合氧化物:铝、铁、锰、硅等金属的水合氧化物 在天然水中以无机高分子及溶胶等形态存在,在水环境中发
挥重要的胶体化学作用。
天然水中几种重要的容易形成金属水合氧化物的金属: 铝在岩石和土壤中是大量元素,在天然水中浓度低,不超 过0.1mg/L。铝水解,主要形态AL3+ 、 Al(OH)2+ 、 Al2(OH)24+ 、 Al(OH)2+ 、 Al(OH)3 和 Al(OH)4 - ,随 pH 值变化而改变形态浓度 比例。一定条件下会发生聚合,生成多核配合物或无机高分 子,最终生成[Al(OH)3]n的无定形沉淀物。
(4)水体悬浮沉积物: 天然水体中各种环境胶体物质相互作用结合成聚集体,
即为水中悬浮沉积物,它们可以沉降进入水体底部,也可
重新再悬浮进入水中。 一般悬浮沉积物是以矿物微粒,特别是粘土矿物为核心 骨架,有机物和金属水合氧化物结合在矿物微粒表面上, 成为各微粒间的粘附架桥物质,把若干微粒组合成絮状聚
项目 非专属吸附 专属吸附
发生吸附的表面净电荷的符号 金属离子所起的作用 吸附时所发生的反应 发生吸附时要求体系的pH值 吸附发生的位置
— 反离子 阳离子交换 >零电位点 扩散层
—、0、+ 配位离子 配位体交换 任意值 内层
注:本表摘自陈静生主编,1987。
3、吸附等温线
吸附等温线和等温式:吸附是指溶液中的溶质在界面层浓度升 高的现象。水体中颗粒物对溶质的吸附是一个动态平衡过程, 在固定的温度条件下,当吸附达到平衡时,颗粒物表面上的吸 附量 (G) 与溶液中溶质平衡浓度 (c) 之间的关系,可用吸附等温 线来表达。 水体中常见的吸附等温线有三类: Henry 型、 Freundlich 型、 Langmuir型,简称为H、F、L型。 H型等温线为直线型,其等温式为:G=kC 式中:k—分配系数。该等温式表明溶质在吸附剂与溶液之间按 固定比值分配。 F型等温式为:G=kC1/n 1 lg G lg k lg c 若两侧取对数,则有:
其次是颗粒物的粒度和浓度对重金属吸附量的影响。颗粒物对重金 属的吸附量随粒度增大而减少,并且,当溶质浓度范围固定时,吸附 量随颗粒物浓度增大而减少。 此外,温度变化、几种离子共存时的竞争作用均对吸附产生影响。
4、解吸作用(以沉积物中重金属的释放为例)
重金属从悬浮物或沉积物中重新释放属于二次污染问题,不仅对
专属吸附的另一特点是它在中性表面甚至在与吸附离子 带相同电荷符号的表面也能进行吸附作用。例如,水锰矿 对碱金属 (K 、 Na) 的吸附作用属于离子交换吸附,而对于 Co、Cu、Ni等过渡金属元素离子的吸附则属于专属吸附。 下表列出水合氧化物对重金属离子的专属吸附机理与交 换吸附的区别。
水合氧化物对金属离子的专属吸附与非专属吸附的区别
无定型氢氧化铁[Fe(OH)3]∞=300m2/g左右。
(2)离子交换吸附:是一种物理化学吸附,主要是胶体对各种
介质离子的吸附,曾有人称之为“极性吸附”。
一般情况下,环境中大部分胶体(包括粘土矿物、有机胶体、
含水氧化物等)带负电荷,容易吸附各种阳离子,在吸附过程 中,胶体每吸附一部分阳离子,同时也放出等量的其他阳离子, 因此把这种吸附称为离子交换吸附,它属于物理化学吸附。 需要说明的是,这种负电荷一部分是永久负电荷,主要是由
(3)腐殖质:最早由土壤学研究者所发现,主要就是腐殖酸, 例如富里酸、胡敏酸等。
属于芳香族化合物,有机弱酸性,分子量从700-20 0000不 等; 带负电的高分子弱电解质,其形态构型与官能团(羧基、 羰基、羟基)的离解程度有关。 在 pH 较高的碱性溶液中或离子强度低的条件下,溶液中的 OH- 将腐殖质理解出的 H+ 中和掉,因而分子间的负电性增强, 排斥力增加,亲水性强,趋于溶解。 在pH较低的酸性溶液(H+多,正电荷多),或有较高浓度的 金属阳离子存在时,各官能团难于离解而电荷减少,高分子 趋于卷缩成团,亲水性弱,因而趋于沉淀或凝聚。
能进行交换吸附。
离子交换吸附对于从概念上解释胶体颗粒表面对水合金
属离子的吸附是有用的,但是对于那些在吸附过程中表
面电荷改变符号,甚至可使离子化合物吸附在同号电荷 的表面上的现象无法解释。因此,近年来有学者提出了 专属吸附作用。
( 3 )专属吸附:是指吸附过程中,除了化学键的作用外, 尚有加强的憎水键和范德华力或氢键在起作用。专属吸附 作用不但可使表面电荷改变符号,而且可使离子化合物吸 附在同号电荷的表面上。
粘土矿物:天然水中常见为云母、蒙脱石、高 岭石,层状结构,易于碎裂,颗粒较细,具有粘 结性,可以生成稳定的聚集体。
其中的粘土矿物是天然水中最重要、最复杂的
无机胶体,是天然水中具有显著胶体化学特性的 微粒。主要成分为铝或镁的硅酸盐,具有片状晶 体结构;
粘土矿物的层状晶体基本由两种原子层构成,一种是硅氧四 面体(硅氧片),另一种是铝氢氧原子层(水铝片),其间主 要靠氢键连接,因此易于断裂开来。
(cm2/g)
子受力不均匀(因为表面分子周围的分子数量不相等),因而产生了所谓的
表面能。 计算实例:某湖泊底泥ρ=2.65g/cm3,10%为直径D=1um(10-4cm)的颗 粒物,求面积S=100m2,深度h=0.2m的底泥中,所有直径D=1um(10-4cm)的 颗粒物比表面积?
解:先计算单位比表面积(ρ为密度)
变化,发生的关键是胶体颗粒具有巨大的比表面积,因此
胶体具有巨大的表面能。
单位比表面积(ρ为密度)=面积(球)/重量=
表面能(又称为表面吸附能):任何分子之间均存在引力,在物体内部,
某分子受到各方面作用力相等,因而处于平衡状态,但是在胶体表面上,分
4r 2 4 3 = r 3
3 r
=面积(球)/重量=
4r 2 4 3 r 3
=
3 0.5 10 4 2.65
=2.264×104(cm2/g)
其次计算总体积=100m2×0.2m×10%=2m3=2×106cm3
所以总重量=总体积×比重=2×106cm3×2.65g/cm3=5.3×106g
所以总比表面积=5.3×106g×2.264×104(cm2/g)=12×1010cm3=12万m3
铁是广泛分布元素,水解反应和形态与铝类似。在不
同 pH 值 下 , Fe(Ⅲ) 的 存 在 形 态 是 Fe3+ 、 Fe(OH)2+ 、 Fe(OH)2+ 、 Fe2(OH)24+ 和 Fe(OH)3 。 固 体 沉 淀 物 可 转 化 为 FeOOH的不同晶形物。同样,它也可以聚合成为无机高分 子和溶胶。
