高考化学练习题
高考复习(化学)专项练习:非选择题专项练【含答案及解析】(三)
非选择题专项练(三)1.硼及其化合物在材料制造、有机合成等方面用途非常广泛。
请回答下列问题。
(1)氨硼烷(H3NBH3)是目前最具潜力的储氢材料之一。
①氨硼烷能溶于水,其原因是。
②氨硼烷电池放电时的总反应为H3NBH3+3H2O2NH4BO2+4H2O。
写出负极的电极反应式:。
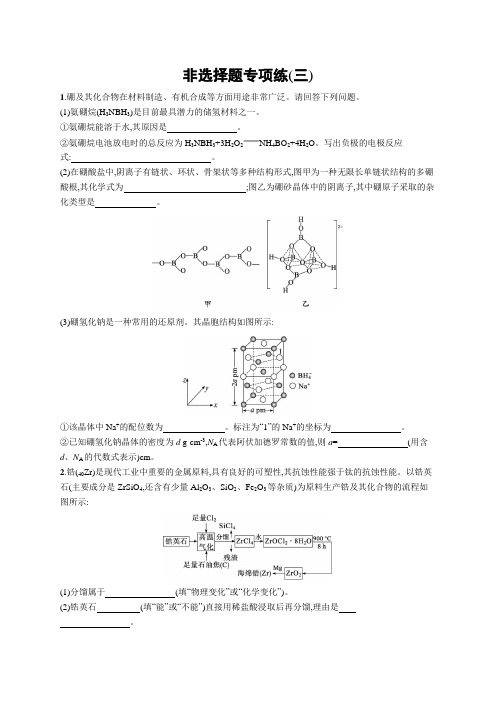
(2)在硼酸盐中,阴离子有链状、环状、骨架状等多种结构形式,图甲为一种无限长单链状结构的多硼酸根,其化学式为;图乙为硼砂晶体中的阴离子,其中硼原子采取的杂化类型是。
(3)硼氢化钠是一种常用的还原剂。
其晶胞结构如图所示:①该晶体中Na+的配位数为。
标注为“1”的Na+的坐标为。
②已知硼氢化钠晶体的密度为d g·cm-3,N A代表阿伏加德罗常数的值,则a=(用含d、N A的代数式表示)cm。
2.锆(40Zr)是现代工业中重要的金属原料,具有良好的可塑性,其抗蚀性能强于钛的抗蚀性能。
以锆英石(主要成分是ZrSiO4,还含有少量Al2O3、SiO2、Fe2O3等杂质)为原料生产锆及其化合物的流程如图所示:(1)分馏属于(填“物理变化”或“化学变化”)。
(2)锆英石(填“能”或“不能”)直接用稀盐酸浸取后再分馏,理由是。
(3)“高温气化”中ZrSiO4发生反应得到ZrCl4的反应的化学方程式为。
(4)流程中ZrCl4与水反应后经过滤、洗涤、干燥等操作可获得ZrOCl2·8H2O,检验该物质是否洗涤干净的实验操作为。
(5)工业上使用惰性电极电解K2ZrF6与KCl组成的熔融盐来制取金属锆。
阳极上的电极反应式为;每转移0.4 mol e-,理论上阴极增加的质量为。
3.FeCl2是重要的媒染剂和污水处理剂。
某校化学探究团队查阅有关资料,在实验室中用氯苯消氯法制备无水FeCl2,原理为C6H5Cl+2FeCl32FeCl2+C6H4Cl2+HCl↑,装置如图所示(夹持装置已略去)。
已知:Ⅰ.FeCl2、FeCl3不溶于氯苯、二氯苯;Ⅱ.C6H5Cl、C6H4Cl2两者互溶,不溶于水;沸点分别为132 ℃、173 ℃。
高考复习(化学)专项练习:非选择题专项练【含答案及解析】(一)

非选择题专项练(一)1.过渡金属及其化合物在化工、医药、材料等领域有着广泛的应用。
(1)基态钛原子的价层电子轨道表示式为;与钛同周期的过渡元素中,基态原子的成对电子数与钛相同的有种;金属钛是一种新兴的结构材料,其硬度比金属镁和铝大的原因是。
(2)在浓的TiCl3的盐酸中加入乙醚,并通入HCl至饱和,可得到配位数为6、组成为TiCl3·6H2O的晶体,该晶体中两种配体的物质的量之比为2∶4,则由该配合离子组成的晶体化学式还可以写为。
(3)航母螺旋桨主要用铜合金制造。
含铜废液可以利用铜萃取剂M,通过如下反应实现铜离子的富集,进行回收。
①M所含元素的第一电离能最大的是(用元素符号表示)。
②X化合物中中心原子铜的配位数是,上述反应中断裂和形成的化学键有。
(4)金红石(TiO2)是含钛的主要矿物之一,其晶胞结构(晶胞中相同位置的原子相同)如图所示。
①A、B、C、D 4种粒子,其中钛原子是(填字母)。
②若A、B、C的原子坐标参数分别为A(0,0,0)、B(0.69,0.69,1)、C(1,1,1),则D的原子坐标参数为D(0.19,,);该化合物的密度为 g·cm-3(用含a、c、N A的代数式表示)。
2.钛铁矿(FeTiO3)中往往含有Fe2O3、MgO、CaO、Al2O3、SiO2等杂质。
一种硫酸法制取白色颜料钛白粉(TiO2)的生产工艺如图所示:已知:Ⅰ.酸浸后,钛主要以TiOSO4形式存在。
Ⅱ.强电解质TiOSO4在溶液中仅能电离出S O42-和一种阳离子。
Ⅲ.H2TiO3不溶于水和稀酸。
(1)为提高酸浸速率,一般采取的措施是。
(写两条)(2)滤渣①的主要成分是。
(3)酸浸过程中,写出含钛化合物发生反应的化学方程式:。
(4)加入铁粉的目的是还原体系中的Fe3+。
为探究最佳反应条件,某实验室做如下尝试。
图1图2①在其他条件不变的情况下,体系中Fe(Ⅲ)含量随pH的变化如图1所示,试分析在pH介于4~6之间时,Fe(Ⅲ)含量基本保持不变的原因:。
高考化学选择题专练 有答案

高考化学选择题专练有答案一、单选题1. 下列物质中不属于非金属元素的是:A.碳B.氧C.铜D.磷答案:C解析:碳、氧、磷均为非金属元素,铜为金属元素。
2. 关于固体的熔点和沸点,下列说法不正确的是:A.固体的熔点等于液体的凝固点B.固体的沸点等于液体的汽化点C.固体的熔点低于液体的沸点D.固体的沸点高于液体的熔点答案:B解析:固体的熔点等于液体的凝固点,固体的沸点高于液体的熔点,固体的熔点低于液体的沸点。
3. 电子亲和能越大的元素,越容易:A.失去电子B.吸收电子C.释放电子D.共用电子答案:B解析:电子亲和能表示元素接受电子的能力大小,越大表示越容易吸收电子。
4. 下列有机物中哪一种物质可以用于检验有机物中是否含有醇官能团?A.酞菁蓝B.铁盐C.碘D.红磷答案:B解析:醇官能团可以与铁盐反应生成酞菁蓝色产物,可以用于检验有机物中是否含有醇官能团。
5. 一种含有A、B两种元素的化合物的质量分数为30%。
若这种化合物中A、B两种元素的原子量比为1:2,则这种化合物的摩尔质量是:A.40g/molB.60g/molC.80g/molD.120g/mol答案:C解析:设化合物的摩尔质量为x,则A元素的质量分数为4x/5,B元素的质量分数为x/5,根据元素的质量分数和原子量比可以列出方程组:4x/5 = 0.3,x/5x =1/2,解得x = 80g/mol。
二、多选题1. 以下哪些是较为广泛存在于自然界的单质?A.氧B.氢C.氦D.铁E.铜答案:A、B解析:氧、氢都是自然界中广泛存在的单质,而氦只存在于极少聚集的自然气体中,铁、铜只存在于自然界中的矿物中。
2. 下列化学反应中促进反应速度的因素有哪些?I.反应物浓度增加;II.反应温度升高;III.反应物表面积变小。
A. IB. IIC. I、IID. I、IIIE. II、IIIF. I、II、III答案:C解析:反应物浓度的增加和反应温度的升高都可以促进反应速度的加快,而反应物表面积的变小不会影响反应速度。
高考化学习题-金属及其化合物的制备(含答案)

高考化学习题-金属及其化合物的制备(含答案)1.[2022·全国甲卷]硫酸锌(ZnSO4)是制备各种含锌材料的原料,在防腐、电镀、医学上有诸多应用。
硫酸锌可由菱锌矿制备,菱锌矿的主要成分为ZnCO3,杂质为SiO2以及Ca、Mg、Fe、Cu等的化合物。
其制备流程如下:本题中所涉及离子的氢氧化物溶度积常数如下表:回答下列问题:(1)菱锌矿焙烧生成氧化锌的化学方程式为____________________________________。
(2)为了提高锌的浸取效果,可采取的措施有__________________、__________________。
(3)加入物质X调溶液pH=5,最适宜使用的X是________(填标号)。
A.NH3·H2O B.Ca(OH)2C.NaOH滤渣①的主要成分是________、________、________。
(4)向80~90℃的滤液①中分批加入适量KMnO4溶液充分反应后过滤,滤渣②中有MnO2,该步反应的离子方程式为____________________________________________________。
(5)滤液②中加入锌粉的目的是___________________________________________。
(6)滤渣④与浓H2SO4反应可以释放HF并循环利用,同时得到的副产物是____________、______________。
2.[2021·湖南卷]Ce2(CO3)3可用于催化剂载体及功能材料的制备。
天然独居石中,铈(Ce)主要以CePO4形式存在,还含有SiO2、Al2O3、Fe2O3、CaF2等物质。
以独居石为原料制备Ce2·n H2O的工艺流程如下:回答下列问题:(1)铈的某种核素含有58个质子和80个中子,该核素的符号为________;(2)为提高“水浸”效率,可采取的措施有________________________(至少写两条);(3)滤渣Ⅲ的主要成分是________(填化学式);(4)加入絮凝剂的目的是_______________________________________________________;(5)“沉铈”过程中,生成Ce2·n H2O的离子方程式为________________________,常温下加入的NH4HCO3溶液呈________(填“酸性”“碱性”或“中性”)(已知:NH3·H2O的K b=1.75×10-5,H2CO3的K a1=4.4×10-7,K a2=4.7×10-11);(6)滤渣Ⅱ的主要成分为FePO4,在高温条件下,Li2CO3、葡萄糖和FePO4可制备电极材料LiFePO4,同时生成CO和H2O,该反应的化学方程式为______________________________________________________________。
2024届全国高考(统考版)化学复习历年真题好题专项(氧化还原反应基本概念)练习(附答案)

2024届全国高考(统考版)化学复习历年真题好题专项(氧化还原反应基本概念)练习1.[2022ꞏ湖南卷]科学家发现某些生物酶体系可以促进H +和e -转移(如a 、b 和c),能将海洋中的NO -2 转化为N 2进入大气层,反应过程如图所示。
下列说法正确的是( ) A .过程Ⅰ中NO -2 发生氧化反应 B .a 和b 中转移的e -数目相等C .过程Ⅱ中参与反应的n (NO)∶n (NH +4 )=1∶4D .过程 Ⅰ→Ⅲ 的总反应为NO -2 +NH +4 ===N 2↑+2H 2O2.[2022ꞏ上海卷]已知反应:I 2+2KClO 3―→2KIO 3+Cl 2,以下说法正确的是( ) A .氧化产物为Cl 2 B .氧化性:KIO 3>KClO 3 C .还原性:I 2>Cl 2D .若生成0.1 mol Cl 2则转移2 mol 电子3.[2022ꞏ浙江卷1月]关于反应4CO 2+SiH 4=====高温4CO +2H 2O +SiO 2,下列说法正确的是( )A .CO 是氧化产物B .SiH 4发生还原反应C .氧化剂与还原剂的物质的量之比为1∶4D .生成1 mol SiO 2时,转移8 mol 电子4.[2023ꞏ全国乙卷]下列应用中涉及到氧化还原反应的是( ) A .使用明矾对水进行净化 B .雪天道路上撒盐融雪 C .暖贴中的铁粉遇空气放热 D .荧光指示牌被照发光5.[2023ꞏ安徽淮北高三摸底]有关反应14CuSO 4+5FeS 2+12H 2O===7Cu 2S +5FeSO 4+12H 2SO 4,下列说法中错误的是( )A.FeS 2既是氧化剂也是还原剂B.CuSO4在反应中被还原C.被还原的S和被氧化的S的质量之比为3∶7D.14 mol CuSO4氧化了1 mol FeS26.根据如图的转化关系判断下列说法正确的是(反应条件已略去)()A.只有反应①②④属于氧化还原反应B.反应⑤说明该条件下铝可用于制熔点较高的金属C.相同条件下生成等量的O2,反应③和④转移的电子数之比为1∶1D.反应①中氧化剂与还原剂的物质的量之比为1∶47.将磁性氧化铁放入稀硝酸中可发生如下反应:3Fe3O4+28HNO3===9Fe(NO3)x+NO↑+14H2O,下列判断合理的是()A.Fe(NO3)x中x为2B.磁性氧化铁中的铁元素全部被氧化C.稀硝酸在反应中只作氧化剂D.反应中每生成0.4 mol还原产物,就有1.2 mol电子转移8.[2023ꞏ贵州贵阳摸底]下列变化过程中,加入氧化剂才能实现的是()A.Cl2→Cl-B.I-→I2C.SO2→SO2-3D.CuO→Cu9.[2023ꞏ福建上杭暑期检测]SF4是有效的应用广泛的选择性有机氟化剂,工业上制备SF4的反应为3SCl2+4NaF===SF4+S2Cl2+4NaCl。
高考化学平衡移动练习题(含答案)-

化学平衡移动专题练习1.在已经处于化学平衡状态的体系中,假如下列量发生变更,其中肯定能表明平衡移动的是()A.反应混和物的浓度B.反应物的转化率C.正、逆反应速率D.反应混和物的压强2.在下列平衡体系中,保持温度肯定时,变更某物质的浓度,混合气体的颜色会变更;变更压强时,颜色也会变更,但平衡并不移动,这个反应是()A.2NO+O22NO2B.Br2(g)+H22HBr C.N2O42NO2 D.6NO+4NH35N2+3H2O 3.在某温度下,反应ClF(g) + F2(g)ClF3(g)(正反应为放热反应)在密闭容器中达到平衡。
下列说法正确的是()A.温度不变,缩小体积,Cl F的转化率增大B.温度不变,增大体积,Cl F3的产率提高C.上升温度,增大体积,有利于平衡向正反应方向移动D.降低温度,体积不变,F2的转化率降低4.已建立化学平衡的可逆反应,当变更条件使化学反应向正反应方向移动时,下列有关叙述正确的是()①生成物的百分含量肯定增加②生成物的产量肯定增加③反应物转化率肯定增大④反应物浓度肯定降低⑤正反应速率肯定大于逆反应速率⑥运用了合适的催化剂A.①②B.②⑤C.③⑤D.④⑥5.在一密闭容器中,反应aA(g) bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新平衡时,B的浓度是原来的60%,则()A.平衡向逆反应方向移动了B.物质B的质量分数增加了C.物质A的转化率减小了D.a>b6.在一固定容积的密闭容器中充入2mol NO2,肯定温度下建立如下平衡:2NO2(g) N2O4此时平衡混合气体中NO2的体积分数为x%;若再充入1mol N2O4,在温度不变的状况下,达到新平衡时,测得NO2的体积分数为y%,则x和y的大小关系正确的是()A.x>y B.x=y C.x<y D.不能确定7.下列事实中,不能用列夏特列原理说明的是( )A.溴水中有下列平衡:Br2+H2O HBr+HBrO当加入AgNO3溶液后溶液颜色变浅B.对二氧化硫的品红溶液加热可使颜色变深C.反应CO+NO2CO2+NO(正反应放热),上升温度可使平衡向逆反应方向移动D.合成氨反应N2+3H22NH3(正反应放热)中运用催化剂8.在密闭容器中进行H2(g)+Br2(g) 2HBr(g)+Q;反应达到平衡后,欲使颜色加深,应实行的措施是()A.升温B .降温C.减小容器体积D.增大容器体积9.在体积可变的密闭容器中,反应mA(g)+nB(s)pC (g)达到平衡后,压缩容器的体积,发觉A的转化率随之降低。
高考复习(化学)专项练习:选择题专项练【含答案及解析】(四)

选择题专项练(四)一、选择题:本题共10小题,每小题只有一个选项符合题目要求。
1.(2021江西红色七校联考)下列有关仪器的使用方法或实验操作正确的是()A.用碱式滴定管量取13.60 mL酸性高锰酸钾溶液B.测定硫酸铜晶体中结晶水的含量时,加热后的坩埚须在干燥器中冷却,再称量C.蒸馏时,应使温度计的水银球置于蒸馏液体中D.过滤时,先将滤纸湿润,然后再将滤纸放入漏斗中2.(2021山东济南十一校3月联考)下列物质的应用中,不涉及氧化还原反应的是()A.用“84”消毒液(有效成分NaClO)杀灭细菌B.补铁剂(有效成分为Fe2+)与维生素C共服效果更佳C.雷雨肥庄稼——自然固氮D.用石灰乳脱除烟气中的SO23.(2021湖南卷)设N A为阿伏加德罗常数的值。
下列说法正确的是()A.18 g H218O含有的中子数为10N AB.0.1 mol·L-1 HClO4溶液中含有的H+数为0.1N AC.2 mol NO与1 mol O2在密闭容器中充分反应后的分子数为2N AD.11.2 L CH4与22.4 L Cl2(均为标准状况)在光照下充分反应后的分子数为1.5N A4.(2021山东邹城一中三模)在中国古代,雌黄(As2S3)经常被用来修改错字,其结构如图所示。
下列说法不正确的是()A.As、S原子的杂化方式均为sp3B.AsH3沸点比NH3的沸点低C.与As同周期且基态原子核外未成对电子数目相同的元素只有VD.已知As2F2分子中各原子均满足8电子结构,分子中σ键和π键的个数比为3∶15.(2021广东模拟)实验室欲将含有Br2、Na2SO4、AlCl3和NaCl的废液处理后得到NaCl固体。
下列实验方案能达到实验目的的是()6.(2021福建泉州第三次质检)从松节油中提取的β-蒎烯可制取诺蒎酮、诺蒎酸等,反应原理如下:下列说法正确的是()A.β-蒎烯的某种同分异构体可能是芳香烃B.诺蒎酮分子中所有碳原子可能共平面C.诺蒎酸与蒎二醇可用NaHCO3溶液鉴别D.以上四种有机物均易溶于水7.(2021河北石家庄二中调研)在碱性溶液中,Cu2+可以与缩二脲形成紫色配离子,其结构如图所示。
2024届全国高考(新高考)化学复习历年真题好题专项(结构与性质综合应用)练习(附答案)

2024届全国高考(新高考)化学复习历年真题好题专项(结构与性质综合应用)练习1.[2023ꞏ全国甲卷][化学——选修3:物质结构与性质]将酞菁—钴钛菁—三氯化铝复合嵌接在碳纳米管上,制得一种高效催化还原二氧化碳的催化剂。
回答下列问题:(1)图1所示的几种碳单质,它们互为________,其中属于原子晶体的是________,C60间的作用力是________。
(2)酞菁和钴酞菁的分子结构如图2所示。
酞菁分子中所有原子共平面,其中p轨道能提供一对电子的N原子是________(填图2酞菁中N原子的标号)。
钴酞菁分子中,钴离子的化合价为________,氮原子提供孤对电子与钴离子形成________键。
(3)气态AlCl3通常以二聚体Al2Cl6的形式存在,其空间结构如图3a所示,二聚体中Al 的轨道杂化类型为________。
AlF3的熔点为1 090 ℃,远高于AlCl3的192 ℃,由此可以判断铝氟之间的化学键为________键。
AlF3结构属立方晶系,晶胞如图3b所示,F-的配位数为________。
若晶胞参数为a pm,晶体密度ρ=________gꞏcm-3(列出计算式,阿伏加德罗常数的值为N A)。
2.[2022ꞏ湖南卷]铁和硒(Se)都是人体所必需的微量元素,且在医药、催化、材料等领域有广泛应用,回答下列问题:(1)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式如下:①基态Se原子的核外电子排布式为[Ar]________;②该新药分子中有________种不同化学环境的C原子;离子(填“>”“<”或“=”),原因是③比较键角大小:气态SeO3分子________SeO2-3____________________________________。
(2)富马酸亚铁(FeC4H2O4)是一种补铁剂。
富马酸分子的结构模型如图所示:①富马酸分子中σ键与π键的数目比为________;②富马酸亚铁中各元素的电负性由大到小的顺序为________。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
化学练习81.某工厂以重晶石(主要含BaSO4)为原料,生产“电子陶瓷工业支柱”——钛酸钡(BaTiO3)的工艺流程如下:回答下列问题:(1)为提高BaCO3的酸浸速率,可采取的措施为___________________________________________________________(写出一条即可);常温下,TiCl4为液体且易水解,配制一定浓度的TiCl4溶液的方法是_______________________________________________________________________________。
(2)用Na2CO3溶液浸泡重晶石(假设杂质不与Na2CO3反应),能将BaSO4转化为BaCO3,此反应的平衡常数K=________(填写计算结果);若不考虑CO2-3的水解,要使2.33 g BaSO4恰好完全转化为BaCO3,则至少需要浓度为1.0 mol·L-1 Na2CO3溶液________ mL。
[已知:K sp(BaSO4)=1.0×10-10、K sp(BaCO3)=5.0×10-9](3)流程中“混合”溶液的钛元素在不同pH时主要以TiO(OH)+、TiOC2O4、TiO(C2O4)2-2三种形式存在(变化曲线如图所示)。
实际制备工艺中,先用氨水调节混合溶液的pH于 2.8左右,再进行“沉淀”,其反应的离子方程式为_________________________________________________;图中曲线c对应钛的形式为________________(填粒子符号)。
(4)流程中“滤液”的主要成分为________;隔绝空气煅烧草酸氧钛钡晶体得到钛酸钡粉体和气态产物,试写出反应的化学方程式:_____________________________________________________。
2.(2019·江淮十校联考)海洋深处有丰富的软锰矿,以此为主要原料生产MnSO4的工业流程如下:已知:①软锰矿的主要成分是MnO2,此外还含有Fe2O3、Al2O3、CuO、NiO、SiO2等少量杂质。
②几种离子沉淀时数据信息如下:(1)写出酸浸过程中SO22(2)为了探究MnO2与SO2反应情况,某研究小组将含有SO2尾气和一定比例的空气通入MnO2悬浊液中,保持温度不变的情况下,测得溶液中c(Mn2+)和c(SO2-4)随反应时间的变化如图所示。
导致溶液中c(Mn2+)和c(SO2-4)的变化产生明显差异的原因是______________________________________________________________________________。
(3)操作Ⅰ是“除铁铝”,其主要步骤为向滤液Ⅰ中加入软锰矿,调节pH=5.2~6.0左右,使其Fe3+、Al3+沉淀完全,再加入活性炭搅拌、抽滤。
写出滤液Ⅰ中生成Fe2+相关的离子方程式:___________________________________________________________________________________、___________________________________________________________________________________。
(4)操作Ⅱ是“除铜镍”,其主要步骤为向滤液Ⅱ中加入MnS(难溶物),充分搅拌,过滤。
加入MnS能除去滤液Ⅱ中Cu2+和Ni2+的原因是_______________________________________________。
(5)以MnSO4溶液为原料可通过电解法制备超级电容器材料MnO2,其装置如图所示:则电解过程中阳极电极反应式为_______________________________,电解一段时间后,阴极溶液中H+的物质的量__________(填“变大”“减小”或“不变”)。
实际生产过程中__________(填“能”或“不能”)用MnCl2溶液代替MnSO4溶液。
3.黄钾铁矾渣经如下流程可将其转化为锰锌铁氧体:已知:①黄钾铁矾渣中铁主要以Fe2O3形式存在,锌主要以硫酸锌(ZnSO4)、氧化锌(ZnO)、硅酸锌(ZnSiO3)形式存在,黄钾铁矾渣的某些元素成分如下表所示:②NH4F溶液用于沉淀Mg2+和Ca2+③Fe和Cd的金属活动性相近(1)“酸浸”后,滤渣1的主要成分为________(填化学式);为了提高浸出率,可采取的措施有________________________________________________________________ (写出一种即可)。
(2)“还原除杂”工序中,加入铁粉是为了除去溶液中、________等金属杂质离子。
(3)加入(NH4)2S沉淀Cd2+时应避免过量,原因是;若此过程中溶液搅拌时间过长,则会导致Cd2+去除率偏低,原因是________________________________________________________________。
(已知:CdS的溶度积K ap=8×10-27,FeS的溶度积K ap=8×10-19,ZnS的溶度积K ap=8×10-24)(1)“酸浸”后,滤渣1的主要成分为________(填化学式);为了提高浸出率,可采取的措施有________________________________________________________________ (写出一种即可)。
(2)“还原除杂”工序中,加入铁粉是为了除去溶液中、________等金属杂质离子。
(3)加入(NH4)2S沉淀Cd2+时应避免过量,原因是;若此过程中溶液搅拌时间过长,则会导致Cd2+去除率偏低,原因是__________________________________________________________________。
(已知:CdS的溶度积K ap=8×10-27,FeS的溶度积K ap=8×10-19,ZnS的溶度积K ap=8×10-24)(4)写出“共沉淀”工序中生成FeCO3的离子反应方程式为_______________________________。
(5)锰锌铁氧体是种重要的磁性材料。
测定铁氧体中ZnO的实验步骤如下:①写出除锰(Mn2+)步骤中的离子方程式:_____________________________________________。
②准确量取25.00 mL溶液A,掩蔽铁后,用二甲酚橙作指示剂,用0.010 0 mol·L-1的EDTA(Na2H2Y)标准溶液滴定其中的Zn2+(反应原理为Zn2++H2Y2-===ZnY2-+2H+),至滴定终点时消耗EDTA标准溶液20.00 mL。
通过计算确定该铁氧体中ZnO的质量分数为________。
4.(2019·江苏高考)实验室以工业废渣(主要含CaSO4·2H2O,还含少量SiO2、Al2O3、Fe2O3)为原料制取轻质CaCO3和(NH4)2SO4晶体,其实验流程如下:(1)室温下,反应CaSO4(s)+CO2-3(aq)CaCO3(s)+SO2-4(aq)达到平衡,则溶液中c(SO2-4)c(CO2-3)=________[K sp(CaSO4)=4.8×10-5,K sp(CaCO3)=3×10-9]。
(2)将氨水和NH4HCO3溶液混合,可制得(NH4)2CO3溶液,其离子方程式为___________________________________________________;浸取废渣时,向(NH4)2CO3溶液中加入适量浓氨水的目的是____________________________________________。
(3)废渣浸取在如图所示的装置中进行。
控制反应温度在60~70 ℃,搅拌,反应3小时。
温度过高将会导致CaSO4的转化率下降,其原因是____________________________;保持温度、反应时间、反应物和溶剂的量不变,实验中提高CaSO4转化率的操作有________________。
(4)滤渣水洗后,经多步处理得到制备轻质CaCO3所需的CaCl2溶液。
设计以水洗后的滤渣为原料,制取CaCl2溶液的实验方案:_________________________________________________________________________________________________________________________________________________________________________________________[已知pH=5时Fe(OH)3和Al(OH)3沉淀完全;pH=8.5时Al(OH)3开始溶解。
实验中必须使用的试剂:盐酸和Ca(OH)2]。
5.(2019·全国Ⅰ卷大联考)高铁酸钾(K2FeO4)具有高效的消毒作用,为一种新型非氯高效消毒剂。
已知:K2FeO4易溶于水、微溶于浓碱溶液,不溶于乙醇,在0~5 ℃的强碱性溶液中较稳定。
实验室中常用KClO在强碱性介质中与Fe(NO3)3反应制备K2FeO4(夹持装置略去)。
回答下列问题:(1)盛放Fe(NO3)3溶液的仪器名称为________________。
(2)氯气的发生装置可以选择图中的________(用图中大写字母表示);检查装置B气密性是否良好的操作为_______________________________________________________________________________。
________________________________________________________________。
(3)选择上述装置,制备K2FeO4,按气流从左到右的方向,合理的连接顺序为a→__________________(填仪器接口字母,仪器不可重复使用)。
(4)装置D中生成K2FeO4的离子方程式为_____________________________________________;实验过程中若装置D的液面上方出现黄绿色气体后,再滴加Fe(NO3)3溶液会产生大量红褐色沉淀,用必要的文字和离子方程式分析原因:________________________________________________________________________________________________________________________。
