2017—2019年江苏13地市中考化学试题分类考点16 溶解度曲线
中考化学专题复习溶解度曲线(20张)

(如:氢氧化钙)
10
硼酸
中考化学专题复习:溶解度曲线(20页 )-PPT 执教课 件【推 荐】
0 10 20 30 40 50 60 70 80 90 100
温度/℃
中考化学专题复习:溶解度曲线(20页 )-PPT 执教课 件【推 荐】
知识回顾
将等质量硝酸钾、氯化钠的饱和溶液 从90℃降低至10℃,会出现什么现象?
(2)当A中含有少量的B,可采用 升温 选填
“降温”或“蒸发”)结晶的方法提纯A物质.
(3) t3℃ 时,ABC三种物质的溶解度大小为 A>B>C 。
5.如图为A、B、C三种固体物质的溶解度 曲线。据图回答下列问题。
(1)在_t_1 _℃时,A、C两种物质的溶解度相等。
(2)A、B、C三种物质中,溶解度受温度影响最小 的是_ B 。
知识回顾
硝酸钾在不同温度时的溶解度
温度 0 10 20 30 40 50 60 70 80 90 100
/℃
溶解 度/g
13.3 20.9 31.6 45.8 63.9 85.5
110
138
168
202
246
中考化学专题复习:溶解度曲线(20页 )-PPT 执教课 件【推 荐】
纵 坐 标 表 示 溶 解 度
专题复习------
溶解度曲线
复习目标
1.能够通过溶解度曲线获得一些相关信息 如:查阅物质在某一温度时的溶解度 判断物质的溶解度随温度变化的趋势 比较不同温度下,不同物质的溶解度大小
2.能根据溶解度曲线具体分析:饱和溶液与不饱和溶液的 转化方法 3.能准确判断:某温度下物质的饱和溶液,改变温度后, 其溶质质量分数的变化 4. 能够根据溶解度曲线,选择物质的结晶方法
江苏省13地市(2017-2019年)中考化学试题分类汇编 考点2 基本实验操作(含解析)
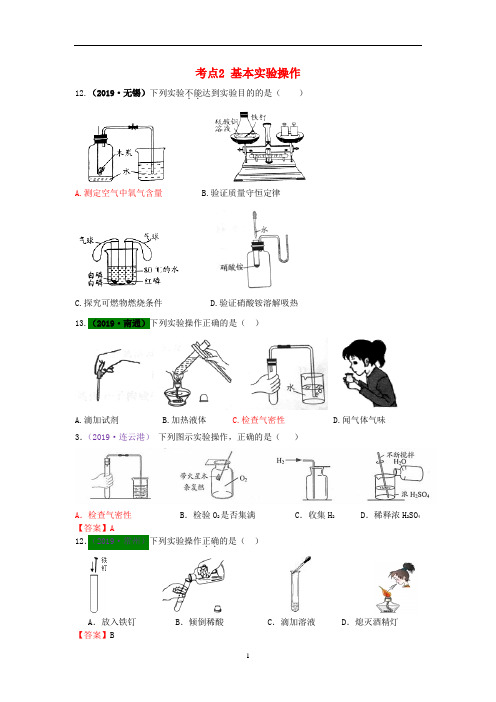
考点2 基本实验操作12.(2019·无锡)下列实验不能..达到实验目的的是()A.测定空气中氧气含量B.验证质量守恒定律C.探究可燃物燃烧条件D.验证硝酸铵溶解吸热13.(2019·南通)下列实验操作正确的是()A.滴加试剂B.加热液体C.检查气密性D.闻气体气味3.(2019·连云港)下列图示实验操作,正确的是()A.检查气密性 B.检验O2是否集满 C.收集H2 D.稀释浓H2SO4【答案】A12.(2019·常州)下列实验操作正确..的是()A.放入铁钉 B.倾倒稀酸 C.滴加溶液 D.熄灭酒精灯【答案】B5.(2019·淮安)下列实验操作符合规范要求的是()A.检查装置的气密性B.点燃酒精灯C.加入块状固体D.读取液体体积【答案】D4.(2019·苏州)下列仪器对应的名称正确的是()A.长颈漏斗B.试管夹C.滴瓶D.蒸发皿【答案】B【解析】A是分液漏斗,而不是长颈漏斗;B是试管夹,用于夹持试管;C是细口瓶,而不是滴瓶;D是研钵,而不是蒸发皿。
11.(2019·苏州)在“粗盐的初步提纯”实验中,下列操作正确的是()A.取用粗盐B.溶解粗盐C.过滤粗盐水D.蒸干滤液【答案】C5.(2019·泰州)下列实验操作正确的是()A.验满氧气B.点燃酒精灯C.检查装置气密性D.滴加液体【答案】C4.(2019·盐城)下列实验操作规范的是()A.量取液体B.引燃酒精灯C.滴加试剂D.稀释浓硫酸【答案】D26.(2018·连云港)下列图示实验操作中,正确的是【答案】A3.(2018·淮安)下列操作正确的是()A.振荡试管B.倾倒液体C.称量药品D.放置洗净的试管【答案】D2.(2018·宿迁)下列实验操作正确的是()A.给液体加热B.稀释浓硫酸C.测溶液酸碱度D.称量固体药品解析:A、给试管中的液体加热时,用酒精灯的外焰加热试管里的液体,且液体体积不能超过试管容积的1/3,图中液体超过试管容积的1/3,图中所示操作错误。
江苏省13地市2017_2019年中考化学试题分类汇编考点16溶解度曲线含解析3

考点16 溶解度曲线17.(2019·镇江)°1T C 时,将等质量的3KNO ,KCl 分别加入到各盛有100.0g 水的两个烧杯中,充分搅拌后恢复到°1T C ,现象如图1、2所示。
下列说法正确的是( )A.甲中加入的固体是3KNOB.甲中溶液可能是该溶质的饱和溶液,乙中上层清液一定是该溶质的饱和溶液C.将甲、乙中的物质混合,充分搅拌,一定有固体剩余D.若将甲、乙的温度从°1T C 升高到o 2T C ,两溶液中的溶质质量分数相等13.(2019·无锡)如图所示是碳酸钠和氯化钠的溶解度曲线,下列叙述错误的是( )A.1t ℃时,NaCl 的溶解度大于23Na CO 的溶解度B.2t ℃时,NaCl 和23Na CO 溶液中所含溶质质量一定相等C.1t ℃时,将NaCl 的饱和溶液加热蒸发,一定有晶体析出D.23Na CO 固体中含有少量的NaCl ,可用降温结晶的方法提纯23Na CO18.(2019·南通)3KNO 、3NaNO 、NaCl 三种物质的溶解曲线如下图所示,下列说法正确的是( )A. 3KNO 的溶解度比NaCl 大B.将3KNO 饱和溶液降温,溶液中3KNO 的质量分数不变C.3KNO 饱和溶液中含少量NaCl ,可通过降温结晶的方法提纯D.将100g 40℃的3NaNO 饱和溶液降温至0℃,析出31g 晶体5.(2019·宿迁) 下图是甲、乙、丙三种物质的溶解度曲线,下列说法正确的是( )A.在t 1℃时,三种物质的溶解度由大到小的顺序是甲>乙>丙B.若甲物质在2℃时的溶解度为12g ,则甲物质属于易溶物质C.丙物质的不饱和溶液升温后溶质质量分数会增大D.在t 2℃时,等质量的甲、乙两物质溶液中所含溶质质量相等【答案】B12.(2019·泰州)如图是甲、乙两种固体物质的溶解度曲线,下列说法正确的是( )A.t 1℃时,甲、乙两物质的溶解度大小关系:甲>乙B. t 2℃时,等质量的甲、乙溶液中,济剂的质量一定相等C. t 3℃时,若将N 点的甲溶液转变为M 点的甲溶液,可采取恒温蒸发溶剂的方法D.将t 1℃时甲、乙的饱和溶液升温至t 3℃,所得甲、乙的溶液仍都是饱和溶液【答案】C11.(2019·连云港) KCl 和KNO 3的溶解度曲线如右图所示。
中考化学考点专训:溶解度及溶解度曲线

1. X 、Y 、Z三种物质的溶解度曲线如图所示。
将t2℃时三种物质的饱和溶液降温至t1℃,溶液中溶质质量分数大小关系正确的是 ( )A.X>Y>ZB.Y>Z>XC.Z>Y>XD.X=Y>Z【答案】B2.我国古代劳动人民常将草木灰(主要成分K2CO3)和生石灰在水中混合,用上层清液漂白丝帛。
清液的主要成分及溶解度如图所示。
(1)t1℃时3种物质的饱和溶液中溶质质量分数由小到大的顺序是。
(2)20 ℃时,向4个盛有50 g水的烧杯中,分别加入一定质量的氢氧化钾并充分溶解。
4组实验数据如下:由上述实验数据可知:①所得溶液是不饱和溶液的是(填序号);②20℃时,将C继续恒温蒸发25 g水,过滤,得到质量为 g的固体。
【答案】(1)Ca(OH)2 KOH K2CO3 (2) ①AB ② 283.下表是Ca(OH)2 和NaOH的溶解度数据。
请回答下列问题:温度/℃0 20 40 60 80 100溶解度/gCa(OH)2 0.19 0.17 0.14 0.12 0.09 0.08NaOH 31 91 111 129 313 336(1)依据上表数据,绘制Ca(OH)2 和NaOH的溶解度曲线,下图中能表示NaOH溶解度曲线的是(填“A”或“B”)。
(2)要想把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,可采取措施有(填序号)。
①蒸发水②升高温度③降低温度④加入水⑤加入氢氧化钙实验序号 A B C D加入氢氧化钾的质量/g7 14 56 70溶液质量/g 57 64 106 106(3)现有60 ℃时含有Ca(OH)2 和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH晶体,应采取的物理方法是。
(4)现有20 ℃时Ca(OH)2的饱和溶液(甲溶液),向其中加入一定量CaO后恢复20 ℃,得到乙溶液,溶液中溶质的质量分数的关系为甲乙(填“>”、“<”或“=”)。
2017—2019年江苏13地市中考化学试题分类考点1变化与性质

1. (2019 •镇江)下列物质的用途主要与其化学性质有关的是(A. 金刚石用于切割玻璃B.高粱常用于酿制白酒C.铜常用来做电线电缆D.干冰可用作人工降雨2. (20佃•无锡)下列物质的用途仅与其物理性质有关的是()A•活性炭作吸附剂B•稀盐酸作除锈剂C. 铁粉作脱氧剂D.生石灰作干燥剂3. (20佃•无锡)下列自然资源的利用过程中,发生了化学变化的是()A•海水晒盐B•粮食酿酒C风力发电 D.空气液化4. (20佃•南通)[下列有关物质的性质与用途具有对应关系的是()A. 铝具有导电性,可用于制炊具B. 活性炭具有吸附性,可用于净化水C盐酸具有挥发性,可用于除铁锈D. 浓硫酸具有腐蚀性,可用作干燥剂5. (2019 •连云港)■下列过程中包含化学变化的是()A. 花香四溢B •海水晒盐C •积雪融化D •粮食酿酒【答案】D【解析】粮食酿酒生成了酒精,是化学变化。
6. (2019 •淮安)■下列变化属于物理变化的是()A. 汽油燃烧B.石蜡融化C.苹果腐烂D.糯米酿酒【答案】B【解析】汽油燃烧、苹果腐烂、糯米酿酒等变化过程中均有新物质生成,都属于化学变化;石蜡融化过程中,物质的状态发生变化,没有新物质生成,属于物理变化。
7. | (2019 •南京)1下列变化中,属于物理变化的是()A. 粮食酿酒B.滤纸折叠C. 红磷燃烧D. 食物腐烂【答案】B【解析】滤纸折叠只有形状发生变化,没有新物质生成,属于物理变化。
& (2019 •泰州)]下列变化属于物理变化的是()A. 浓盐酸挥发B.木柴燃烧C.工业炼铁D.有机肥腐熟【答案】A【解析】浓盐酸挥发只是物质状态由液态变为了气态,没有生成新物质。
9. (2019 •盐城)下列变化属于化学变化的是()A. 蜡烛燃烧B.冰雪融化C.汽油挥发D.氧气液化【答案】A【解析】蜡烛燃烧生成新物质二氧化碳和水,属于化学变化。
10. (2019 •扬州)下列过程涉及化学变化的是()A. 干冰升华B.氧气液化C.氢气燃烧D.矿石粉碎【答案】C【解析】氢气燃烧产生水,有新物质生成。
江苏省13地市2017_2019年中考化学试题分类汇编考点27归纳与推理题含解析

考点27 归纳与推理题7.(2019·宿迁) 下列知识整理的内容中,有错误的一组是( )【答案】C8.(2019·宿迁)推理是学习化学时常用的思维方式,以下推理结果正确的是( )A.用洗洁精洗油污是乳化作用,用汽油洗油污也是乳化作用B.NaOH 溶液能使无色酚酞试液变红色,Cu(OH)2也能使无色酚酞试液变红色C.化合物是由不同种元素组成的纯净物,则只含一种元素的物质一定不是化合物D. 复分解反应有沉淀气体或水生成,有沉淀气体或水生成的反应是复分解反应【答案】C【答案】A12.(2018•无锡)总结、归纳知识,有利于提升学习能力,下列知识归理完全正确的一组是钠,不能再烹调时用工业用盐代替食盐;淡水资源不是取之不尽用之不竭的。
【答案】A16.(2018·镇江)下列说法正确的是( )A .原子通过得失电子形成离子,离子一定不能形成原子B.不饱和溶液转化为饱和溶液,溶质的质量分数一定增大C.中和反应生成盐和水,有盐和水生成的反应一定是中和反应D.某溶液中滴入无色酚酞试液后变红,该溶液一定是碱性溶液【答案】D8.(2017·宿迁)下列归纳总结完全正确的一组是()【答案】A【解析】①老年人缺钙会导致骨质疏松②人体缺乏维生素A会引起夜盲症③要牢记“吸烟有害健康”“毒品万万试不得!”说法都正确,A选项符合题意;天然气不属于新能源;综合利用化石能源提高其利用率,是常用的化工资源,故B选项错误;天然气和海水都含有多种物质,属于混合物;纯碱是碳酸钠,属于盐;尿素属于氮肥,故C选项错误;化肥、农药过量使用易导致环境污染,故D选项错误;大气;生石灰能与水反应生成氢氧化钙,具有强烈的腐蚀性,不能用于补钙剂;不用硫酸钠配置波尔多液,应用硫酸铜。
【答案】A13.(2017·无锡)某同学梳理归纳了以下知识:①硬水通过活性炭吸附后可变为软水②二瓶气体元素组成相同、各元素的质量分数相同,则它们的化学性质一定相同③离子是带电的粒子,所以带电的粒子一定是离子④配制6%的氯化钠溶液,量取水时,俯视量筒刻度会使所配氯化钠溶液质量分数偏高⑤所谓“低碳”就是较低二氧化碳的排放⑥除去铜粉中混有的少量炭粉,可采用在空气中灼烧混合物的方法。
江苏省13地市2017_2019年中考化学试题分类汇编考点31探究题含解析

考点31 探究题14.(2019·宿迁)碳酸氢钠是小苏打的主要成分,在生产和生活中有许多重要的用途,化学课上同学们为了解碳酸氢钠的性质,将一定质量的碳酸氢钠和稀硫酸混合,充分反应后有气体逸出,写出该反应的化学方程式____________,同学们对反应后溶液中溶质的成分进行了探究,认为除一定含有硫酸钠外,可能还含有其他成分,因此进行了猜想并作了如下实验【实验用品】pH试纸、锌片,氧化铜粉末,稀硫酸,氢氧化钠溶液,氯化钡溶液【猜想与假设】反应后溶液中溶质的可能组成成分:猜想一:碳酸钠猜想二:碳酸钠、碳酸氢钠猜想三:硫酸钠、硫酸【实验探究】同学们取反应后的溶液用不同方案进行如下实验,请根据结论完成如表实验现象中的空格:【得出结论】猜想三正确【评价反思】(1)老师对同学们能用多种方案进行探究,并且得出正确的实验结论给予了肯定,同时指出探究中存在一处明显的操作错误_______________,(2)有同学对实验方案B的结论提出了质疑,认为仅凭此现象不能得出猜想三正确,请说明理由______________。
【总结提高】依据所给实验用品设计与上述实验不同的方案确认猜想三是正确的,请你写出你的实验方案________________________________________________________。
【答案】2NaHCO3+H2SO4=Na2SO4+2CO2↑+2H2O 无气泡产生有气泡产生(1)C实验中将pH 试纸直接浸入待测液中(2)氯化钡与碳酸钠也能反应生成白色沉淀取少量氧化铜粉末与试管中,加入足量反应后的溶液,若氧化铜溶解,溶液变蓝,则猜想三正确28.(2019·常州)装品牌苏打饼干的配料和营养成分如下表,研究性学习小组対其成分进分解。
Ⅰ.定性判断饼干中有关成分的确认。
取一小包饼干。
研碎后放入烧杯,加入适量蒸馏水,用玻璃棒搅拌,得到待检液。
【交流讨论】(1)饼干中的________元素可减少人体骨质疏松、畸形、佝偻病的发生,有利于人体健康。
2017—2019年江苏13地市中考化学试题分类考点10微观示意图
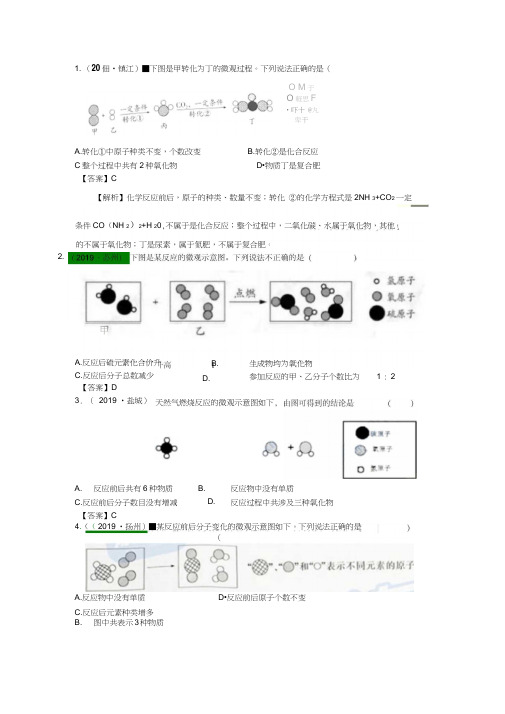
1. (20佃•镇江)■下图是甲转化为丁的微观过程。
下列说法正确的是(A.转化①中原子种类不变,个数改变 C 整个过程中共有2种氧化物 【答案】CA. 反应前后共有6种物质 C.反应前后分子数目没有增减【答案】CA.反应物中没有单质 C.反应后元素种类增多B. 图中共表示3种物质D •反应前后原子个数不变O M 于O 軽思F•吓十 @丸卑干的不属于氧化物;丁是尿素,属于氮肥,不属于复合肥。
甲1 : 2生成物均为氧化物参加反应的甲、乙分子个数比为B. 条件CO (NH 2)2+H 20,不属于是化合反应;整个过程中,二氧化碳、水属于氧化物,其他 【解析】化学反应前后,原子的种类、数量不变;转化 ②的化学方程式是2NH 3+CO 2 一定 2. A.反应后硫元素化合价升C.反应后分子总数减少 【答案】D3. ( 2019 •盐城) D.天然气燃烧反应的微观示意图如下,4.(( 2019 •扬州)■某反应前后分子变化的微观示意图如下。
下列说法正确的是(B.转化②是化合反应 D •物质丁是复合肥B. D.反应物中没有单质反应过程中共涉及三种氧化物【答案】D5. (2019 •无锡)能源的利用与社会可持续发展密切相关。
(1) 煤燃烧时产生NO?、__________ 等气体,这些气体或气体在空气中发生反应后的生成物溶于雨水,会形成酸雨。
(2) 在一定条件下,甲烷( CH4 )和水反应(未配平)的微观示意图如图4所示。
①W表示的物质的化学式是 ________ 。
②该反应中两种生成物Z和W的分子个数比为 _________(3 )实验室可用锌和稀硫酸反应制取氢气。
写出该反应的化学方程式: _____________ 。
目前,氢气作为新能源在生活和生产中还未能广泛应用,其原因是 _____________ 。
(4 )在高温下,工业上以赤铁矿(主要成分是Fe2O3)和一氧化碳反应来炼铁的化学方程式为__________ 。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1.(2019·镇江)°1T C 时,将等质量的3KNO ,KCl 分别加入到各盛有100.0g 水的两个烧杯中,充分搅拌后恢复到°1T C ,现象如图1、2所示。
下列说法正确的是( )A.甲中加入的固体是3KNOB.甲中溶液可能是该溶质的饱和溶液,乙中上层清液一定是该溶质的饱和溶液C.将甲、乙中的物质混合,充分搅拌,一定有固体剩余D.若将甲、乙的温度从°1T C 升高到o 2T C ,两溶液中的溶质质量分数相等2.(2019·无锡)如图所示是碳酸钠和氯化钠的溶解度曲线,下列叙述错误的是( )A.1t ℃时,NaCl 的溶解度大于23Na CO 的溶解度B.2t ℃时,NaCl 和23Na CO 溶液中所含溶质质量一定相等C.1t ℃时,将NaCl 的饱和溶液加热蒸发,一定有晶体析出D.23Na CO 固体中含有少量的NaCl ,可用降温结晶的方法提纯23Na CO3.(2019·南通)3KNO 、3NaNO 、NaCl 三种物质的溶解曲线如下图所示,下列说法正确的是( )A. 3KNO 的溶解度比NaCl 大B.将3KNO 饱和溶液降温,溶液中3KNO 的质量分数不变C.3KNO 饱和溶液中含少量NaCl ,可通过降温结晶的方法提纯D.将100g 40℃的3NaNO 饱和溶液降温至0℃,析出31g 晶体4.(2019·泰州)如图是甲、乙两种固体物质的溶解度曲线,下列说法正确的是( )A.t 1℃时,甲、乙两物质的溶解度大小关系:甲>乙B. t 2℃时,等质量的甲、乙溶液中,济剂的质量一定相等C. t 3℃时,若将N 点的甲溶液转变为M 点的甲溶液,可采取恒温蒸发溶剂的方法D.将t 1℃时甲、乙的饱和溶液升温至t 3℃,所得甲、乙的溶液仍都是饱和溶液【答案】C5.(2019·连云港) KCl 和KNO 3的溶解度曲线如右图所示。
下列说法正确的是( )A .10℃时,KNO 3的溶解度比KCl 的大B .KNO 3的溶解度受温度的影响比KCl 的大C .随着温度的升高,KCl 的溶解度逐渐减小D .40℃时KNO 3的饱和溶液,升温至60℃时仍是饱和溶液(忽略水分挥发)【答案】B6.(2019·盐城) 下表是KCl 、NH 4Cl 、KNO 3三种物质在不同温度时的溶解度:根据表格信息可以推知( )A.3种物质中溶解度最小的是KClB.40℃时,100g克KNO3饱和溶液中含有63.9克KNO3C.3种物质中溶解度受温度变化影响最大的是KNO3D.在0℃~100℃以内的相同温度下,KCl和NH4Cl的溶解度可能相等【答案】C7.(2019·徐州)甲、乙两种均不含结晶水的固体物质(设它们从溶液中析出时也都不含结晶水)的溶解度曲线如右图所示。
下列说法正确的是()A.t1℃时,将甲、乙各17g分别加入到50g水中,所得两溶液的质量相等B.将甲、乙两种溶液由t3℃降温至t2℃,所得两溶液中溶质质量分数一定相等C.若甲中混有少量的乙,可先配制较高温度下甲的饱和溶液,再采用降温结晶的方法提纯甲D.将t3℃时甲的饱和溶液100g降温至t1℃,析出甲的质量是59.4g【答案】C8.(2019·南京)溶液在生活、生产中具有广泛的用途。
(1)在20℃时,将20g氯化钾固体加入50g水中,充分搅拌后,仍有3g氯化钾固体未溶解。
所得溶液中氯化钾的质量分数为 (计算结果保留一位数);20℃时氯化钾的溶解度为。
(2)甲、乙两种不含结晶水的固体物质的溶解度曲线如图。
t1℃时,甲溶液的溶质质量分数与乙溶液的溶质质量分数相比,前者与后者的关系是(填字母)。
A.大于B.小于C.等于D.无法确定(3)如图是实验室稀释浓硫酸的正确和错误操作,请说明不能将水直接倒入浓硫酸中进行稀释的原因。
【答案】(1)25.4% 34g (2)D (3)水的密度比浓硫酸的小,将浓硫酸倒入水中,浓硫酸会浮在水上,且放出大量的热会使表面的水迅速沸腾,导致混有浓硫酸的液滴向外飞溅,发生危险9.(2019·常州)图4是A、B两种物质的溶解度曲线。
(1)0℃时,B的溶解度是________g;t1℃时,A、B的溶解度(S)的大小关系为:S A_______(填“>”“=”或“<”)S B。
(2)现有t2℃的A、B的饱和溶液各100g,同时将两份溶液升度温至t3℃(不考虑水的蒸发),则此时A、B两溶液的溶质质量分数(a)的大小关系为:ωA______(填“>”“<”或“=”)ωB。
(3)现有t2℃的B的溶液100g将其蒸发掉10g水,再将温度恢复到t2℃时,析出3gB。
若继续蒸发掉10g水,仍将温度恢复到t2℃,此时析出B的质量_______3g(填“>”“=”或“≥”)。
(4)当A中混有少量的B时,提纯A采用的方法是_________(填“蒸发结晶”或“降温结晶”)。
(5)现将经提纯的A用于配制一定溶质质量分数的溶液,实验中用到的仪器除了托盘天平(含砝码)、纸片、药匙、烧杯、玻璃棒、试剂瓶、标签外,还需用到的仪器有_________。
【答案】(1)36.0 = (2)>(3)>(4)降温结晶(5)量筒、胶头滴管10.(2019·淮安)如图是几种固体物质的溶解度曲线。
(1)80℃时,KCl、NH4Cl与NaNO3的溶解度由大到小的顺序为______。
(2)20℃时,50g水中加入20gNaCl充分搅拌后形成_____(填“饱和”或“不饱和”)溶液。
(3)60℃时,分别将相同质量的NaCl、NH4Cl与KNO3饱和溶液降温至20℃,析出晶体质量最大的是________。
(4)60℃时,配制KNO3溶液,其溶质质量分数最高不会超过_______(精确到0.1%)。
【答案】(1)NaNO3>NH4Cl>KCl (2)饱和(3)KNO3(4)52.4%11.(2019·苏州)硝酸钾的溶解度曲线如图所示。
(1)30℃时,硝酸钾的溶解度是__________。
(2)60℃时,在200g水中加入120g硝酸钾固体,充分搅拌。
①所得溶液是________(填“饱和”或”不饱和”)溶液。
②将上述溶液降温至30℃,可析出硝酸钾晶体____________g,此时溶液的溶质质量分数_________(填“>”“<”或“=”)45.8%。
【答案】(1)45.8 g(2)①不饱和②28.4 <12.(2018•徐州)甲、乙、丙三种固体物质的溶解度曲线如图所示,从中获取的信息正确的是()A.蒸发溶剂可使丙的饱和溶液变为不饱和溶液B.t2℃时,100g甲的饱和溶液降温至t1℃,析出甲的质量为15gC.t1℃时,甲、乙、丙三种溶液所含溶质的质量可能相同D.t2℃时,甲、乙、丙的饱和溶液降温至t1℃,所得溶液的溶质质量分数大小顺序为乙>甲=丙【解析】蒸发溶剂后,丙的饱和溶液仍为饱和溶液;t2℃时,甲物质的溶解度是25g,所以125g甲的饱和溶液降温至t1℃,析出甲的质量为15g;t1℃时,乙物质的溶解度最大,甲、丙物质的溶解度相等,降低温度,甲、乙物质的溶解度减小,丙物质的溶解度增大,应该按照t2℃时的溶解度计算,所以t2℃时,甲、乙、丙的饱和溶液降温至t1℃,所得溶液的溶质质量分数大小顺序为乙>甲>丙,。
【答案】C13.(2018·连云港)甲、乙、丙三种固体物质的溶解度曲线如右图所示。
下列说法不正确的是A.T2℃时,取等质量的甲、乙分别配制成饱和溶液,所需水的质量:甲>乙B.T2℃时,将甲、乙的饱和溶液均降温到T1℃,得到的溶液仍饱和C.若甲中混有少量的丙,可采用降温结晶的方法提纯甲D. T2℃时,甲、乙各30g分别加入100g水中,均形成饱和溶液【答案】A14.(2018·淮安)如图是甲、乙两固体物质(不含结晶水)的溶解度曲线,下列说法不正确的是()A.t1℃时,向50g水中加入10g甲,所得溶液可以达到饱和状态B.采用升高温度的方法,可使乙的饱和溶液变为乙的不饱和溶液C.甲中混有少量乙,可以采用冷却热的饱和溶液的方法提纯甲D.t2℃时,将甲、乙两溶液蒸发等质量的水,析出的晶体质量一定相等【答案】D15.(2018·宿迁)下图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线,下列说法正确的是A.甲的溶解度大于乙的溶解度B.降温可使接近饱和的丙溶液变为饱和溶液C.将t2°C甲、乙、丙的饱和溶液降温至t1℃,所得溶液的溶质质量分数:乙>甲=丙D.P点表示t1℃时甲、丙两种物质的溶解度都是25g【答案】D16.(2018·扬州)KNO3与KCl的溶解度曲线如图所示。
下列说法正确的是A. KNO3的溶解度比KCl的溶解度大B. t1温度下的KCl的饱和溶液升温至t2,有晶体析出C. A点所表示的KCl饱和溶液溶质的质量分数为29%D. 冷却热的KNO3饱和溶液可获得KNO3晶体【答案】D17.(2018·盐城)甲、乙两种固体物质(不含结晶水)的溶解度曲线如右图所示,下列说法正确的是A.t1℃时,甲、乙的溶液中所含溶质质量相等B.t2℃时,将50g甲加入5Og水中,可得到100g溶液C.甲中含有少量乙时,可用降温结晶法提纯甲D.t1℃时分别将甲、乙的饱和溶液升温至t2℃时,所得溶液的溶质质量分数甲>乙【答案】C18.(2018•无锡)如图是甲、乙两种固体物质的溶解度曲线。
下列说法正确的是()A.15℃时,甲和乙的饱和溶液中溶质质量相等B.35℃时,30g甲加入50g水中,得到80g甲溶液C.从乙溶液中获得乙晶体,常用蒸发结晶的方法D.降低温度,甲溶液中溶质的质量分数一定减小【解析】5℃时,甲、乙物质的溶解度相等,甲和乙的饱和溶液的质量不能确定,所以饱和溶液中溶质质量也不能确定;35℃时,甲物质的溶解度是40g,所以30g甲加入50g水中,得到70g甲溶液;乙物质的溶解度受温度变化影响较小,所以从乙溶液中获得乙晶体,常用蒸发结晶的方法;降低温度,甲溶液的状态不能确定,所以溶液中溶质的质量分数不一定减小。
【答案】C19.(2018•常州)如图是3种物质的溶解度曲线。
下列叙述正确的是()A.0℃时,NaCl的溶解度小干NH4Cl的溶解度B.40℃时,饱和Na2 CO3溶液的溶质质量分数为49%C.将饱和Na2 CO3溶液由80℃冷却至40℃时,有固体析出D.80℃时,分别将等质量的NH4Cl和NaCl固体溶于适量的水,恰好均配成饱和溶液,所得溶液的质量前者小于后者【解析】0℃时,NaCl的溶解度大于NH4Cl的溶解度;40℃时,碳酸钠的溶解度是49g,饱和Na2CO3溶液的溶质度量分数为49g/149g×100%≠49%;将饱和Na2CO3溶液由80℃冷却至40℃时,溶解度增大,不会有固体析出;80℃时,氯化铵的溶解度大于氯化钠的溶解度,分别将等质量的NH4C1和NaCl固体溶于适量的水,恰好均配成饱和溶液,所得溶液的质量前者小于后者,D正确。
