QC-7129B鲎试剂灵敏度复核操作规程
细菌内毒素测定技术—鲎试剂灵敏度复核和方法验证试验

知识点:鲎试剂灵敏度复核试验
二、鲎试剂灵敏度的复核 在本检查法规定的条件下,使鲎试剂产生凝集的内毒素的最低
知识点:鲎试剂灵敏度复核试验
当λc在0.5λ~2λ(包括0.5λ和2λ)时,方可用于内毒素 检查。但是注意要以标示灵敏度λ为该批鲎试剂的灵敏度。
知识点:干扰试验
一、干扰试验 是为了确定供试品在多大的稀释倍数或 浓度下对内毒素和鲎试剂的反应不存在干扰作用,为产 品能否用细菌内毒素检查法提供依据,并且验证供试品 的配方和工艺有变化,鲎试剂来源改变或供试品阳性对 照结果呈阴性时,供试品是否存在干扰作用。
编号
内毒素浓度
被加入内毒素的溶液 平行管数
A
无
供试品溶液
至少2
标准曲线的中点(或附近点
B
)的浓度(设为λm)
C
至少3个浓度 (最低一点设定为λ)
供试品溶液 检查用水
至少2 每一浓度至少2
D
无
检查用水
至少2
A 为稀释倍数不超过MVD 的供试品溶液。B 为加入了标准曲线中点或 靠近中点的一个已知浓度内毒素的,且与溶液A 有相同稀释倍数的供 试品溶液。C 为如“标准曲线的可靠性试验”项下描述的,用于制备 标准曲线的标准内毒素溶液。D 为阴性对照。
浓度即为鲎试剂的标示灵敏度,用EU/ml 表示。当使用新批号的 鲎试剂或试验条件发生了任何可能影响检验结果的改变时,应进 行鲎试剂灵敏度复核试验。
复核的目的不仅是考察鲎试剂的灵敏度是否准确,也是考察检 验人员操作方法是否正确及试验条件是否符合规定。
鲎试剂灵敏度复核记录
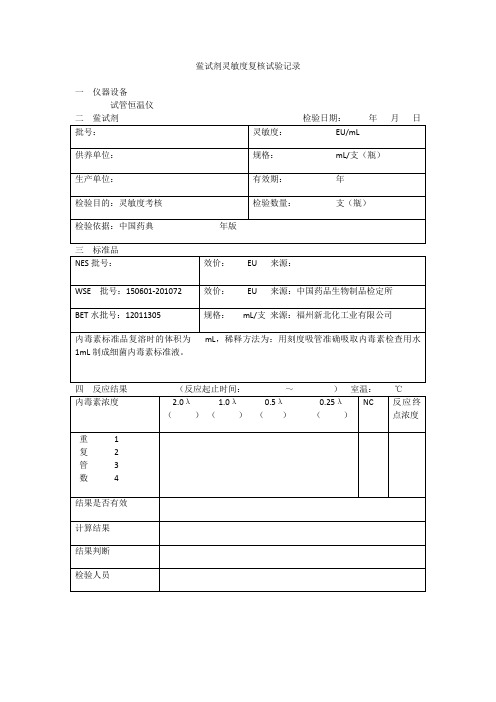
结果是否有效
计算结果
结果判断
检验人员
BET水批号:12011305
规格:mL/支来源:福州新北化工业有限公司
内毒素标准品复溶时的体积为mL,稀释方法为:用刻度吸管准确吸取内毒素检查用水1mL制成细菌内毒素标准液0λ1.0λ0.5λ0.25λ
()()()()
NC
反应终点浓度
重1
复2
管3
鲎试剂灵敏度复核试验记录
一仪器设备
试管恒温仪
二鲎试剂检验日期:年月日
批号:
灵敏度:EU/mL
供养单位:
规格:mL/支(瓶)
生产单位:
有效期:年
检验目的:灵敏度考核
检验数量:支(瓶)
检验依据:中国药典年版
三标准品
NES批号:
效价:EU来源:
WSE批号:150601-201072
效价:EU来源:中国药品生物制品检定所
美国USP鲎试剂检测方法

USP这一章节的部分内容已与欧洲药典和日本药典协调一致,不一致的部分以符号*标出。
本章阐述了关于检查和定量供试品内毒素的方法。
本法利用鲎(Limuluspolyhemus或 Tachypleus tridentatus)血细胞提取物制备的用于内毒素检测的鲎试剂(LAL)检定内毒素。
*1该检查包括两种方法:一为凝胶法,系利用鲎试剂与内毒素产生凝集反应的原理;另一种为光度测定法,该法利用鲎试剂与内毒素反应过程中的光学变化来实现内毒素的测定,这种方法又可分为浊度法(基于形成凝胶的过程中,溶菌液的浊度变化)和显色法(得到的肽-呈色基团复合物断裂后,检测反应混合物的色度)。
检测时,可用其中任一种方法进行试验。
当测定结果可疑或有争议时,除非各论中另有规定,以凝胶法测定结果为准。
直接比较供试品溶液与标准内毒素溶液,判断凝胶法的反应终点。
内毒素含量以USP内毒素单位(USP-EU)表示。
[注-1USP EU相当于1个内毒素单位。
]LAL试剂专用于浊度检查法或显色法,因此,使用这两种方法进行检定时,必须符合它们各自的要求。
两种检查法都要求建立标准曲线,以检定供试品的内毒素含量。
主要的实验步骤有:在预定的时间内将内毒素和对照品分别与LAL试剂保温培养;读取相应波长处的吸光度等。
使用终点浊度法时,应在孵育时间结束时马上读数;对终点显色法,则要在孵育终止时添加酶反应-终止制剂,反应停止后,方可读数。
动态浊度法和动态显色法分析整个反应时间内吸光度的变化,并通过这些读数计算比值。
仪器所有玻璃器皿及由其他耐热材料制成的器皿需用已验证的工艺在热烘箱内进行去热原处理。
*2去热原时,常用的最小时间和温度设置分别为30分钟和250℃。
若使用塑料器械,如微孔板和微量进样器配套的吸头等,它们必须标明无内毒素并确对试验无干扰。
[注-本章内,“管”也包括任何其他反应容器,如微孔板的孔等。
]内毒素储备标准溶液和内毒素标准溶液的制备USP内毒素RS的效价规定为10000 USP内毒素单位(EU)/西林瓶。
鲎试验检查细菌内毒素应注意的问题

鲎试验检查细菌内毒素应注意的问题鲎试验检查细菌内毒素应注意的问题发布时间02年09月05日 09时18分方法:通过对干扰鲎试验准确性干扰因素的分析(包括鲎试剂本身、操作条件、配制原料等),提出了鲎试验中应注意的问题。
结果:只要克服了检查中的干扰因素,鲎法具有比家兔法更简便、快速、灵敏度高、重现性好等优点。
鲎试验是利用鲎的变形细胞与微量内毒素产生凝集反应的现象,作为判断供试品中细菌内毒素限量是否符合规定的一种方法[1]。
它具有比家兔法更简便、快速、灵敏度高、重现性好等优点。
中国药典1995年版已收载细菌内毒素检查法(简称鲎试验),但只用于几种输液的检查。
根据现有的实验证明,凡不干扰细菌内毒素检查或虽有干扰,但可以克服的药品注射剂,将能够全部以鲎法代替家兔热原检查法。
但是该法受到许多因素的影响,故在做鲎试验检查时,应注意下列问题。
1鲎试剂本身1.1鲎试剂灵敏度 为了保证检查细菌内毒素结果的准确性,用于试验的鲎试剂应首先核对灵敏度。
因为在我们的实际工作中,发现鲎试剂均符合药典规定标准前提下,由于生产厂家不同,部分鲎试剂的实测灵敏度与标示值有差异而导致检测同一检品时,用相同标示值的鲎试剂,出现不同结果。
因而先核对灵敏度可避免因鲎试剂本身造成的判断失误。
建议法定部门和生产单位应注意鲎试剂的质量检查。
1.2供试品稀释 在取样品时,一定要熟悉中国药典的内容,不能直接取大输液原液0.1ml进行检查,这是排除干扰因素的简单有效的方法。
因药典已明确规定试验中鲎试剂的灵敏度不超过0.5EU/ml,根据供试品的稀释公式: 供试品稀释倍数= L/λυL :供试品的内毒素限量(1EU/ml)λυ:鲎试剂灵敏度的标示值(EU/ml)故检测大输液均应稀释后才能进行试验,如选用更高灵敏度的鲎试剂,则应增加样品的稀释倍数。
稀释用的细菌内毒素检查用水药典作了规定。
在4h内不得与鲎试剂产生凝集反应。
如果直接用供试品原液试验,就会使供试品的内毒素提高到0.5EU/ml或0.5EU/ml以下,这样,根据目前大输液的生产和贮藏条件,有些就会达不到,鲎法检出的阳性率会提高,兔法复核的机遇也将增多,势必会浪费人力物力。
sop细菌内毒素检查操作规程
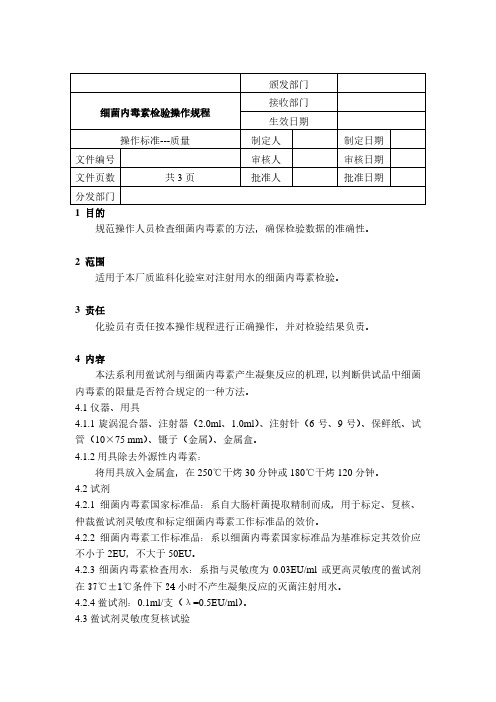
1 目的规范操作人员检查细菌内毒素的方法,确保检验数据的准确性。
2 范围适用于本厂质监科化验室对注射用水的细菌内毒素检验。
3 责任化验员有责任按本操作规程进行正确操作,并对检验结果负责。
4 内容本法系利用鲎试剂与细菌内毒素产生凝集反应的机理,以判断供试品中细菌内毒素的限量是否符合规定的一种方法。
4.1仪器、用具4.1.1旋涡混合器、注射器(2.0ml、1.0ml)、注射针(6号、9号)、保鲜纸、试管(10×75 mm)、镊子(金属)、金属盒。
4.1.2用具除去外源性内毒素:将用具放入金属盒,在250℃干烤30分钟或180℃干烤120分钟。
4.2试剂4.2.1细菌内毒素国家标准品:系自大肠杆菌提取精制而成,用于标定、复核、仲裁鲎试剂灵敏度和标定细菌内毒素工作标准品的效价。
4.2.2细菌内毒素工作标准品:系以细菌内毒素国家标准品为基准标定其效价应不小于2EU,不大于50EU。
4.2.3细菌内毒素检查用水:系指与灵敏度为0.03EU/ml或更高灵敏度的鲎试剂在37℃±1℃条件下24小时不产生凝集反应的灭菌注射用水。
4.2.4鲎试剂:0.1ml/支(λ=0.5EU/ml)。
4.3鲎试剂灵敏度复核试验鲎试剂灵敏度的标示值(λ,此处λ=0.5EU/ml),将细菌内毒素国家标准品用细菌内毒素检查用水溶解,在旋涡混合器混合15分钟,然后制备成合适的稀释浓度,1EU/ml、0.5EU/ml、0.25EU/ml、0.125EU/ml,每稀释一步均应在旋涡混合器上混合30秒钟。
按检查法项下试验,每一浓度平行做4支,同时用细菌内毒素检查用水做2支阴性对照管,如最大浓度管均为阳性,最低浓度管均为阴性,阴性对照管均为阴性,按下式计算鲎试剂灵敏度的测定值λc。
λc=lg-1(∑X/4)式中X为反应终点浓度的对数值(lg)。
反应终点浓度是系列浓度递减的内毒素溶液中最后一个呈阳性结果的浓度。
当λc在0.5λ~2.0λ(包括0.5λ和2.0λ)时,方可用于细菌内毒素检查,并以λ为该批鲎试剂的灵敏度。
鲎试剂灵敏度复核SOP

鲎试剂灵敏度复核SOP1.目的为规范鲎试剂标示灵敏度复核的操作,确保鲎试剂试验的准确性,特制定此操作规程。
2.范围本标准操作规程适用于新批号鲎试剂使用前对标示灵敏度的复核以及试验条件发生任何可能影响检验结果的改变时,对鲎试剂标示灵敏度的复核。
3.定义无4.职责4.1QC负责本规程的起草、修订、培训及执行。
4.2QA、QC组长、质量管理部经理负责本规程的审核。
4.3质量总监负责批准本规程。
4.4QA负责本规程执行的监督。
5.引用标准《中华人民共和国药典》2020年版二部6.材料见8.程序。
7.流程图无8.程序8.1试剂:细菌内毒素工作标准品、鲎试剂溶解水、待复核灵敏度的鲎试剂。
8.2仪器与设备:恒温水浴箱、烤箱、小试管、中管、半中管。
8.3操作步骤8.3.1试验前准备试验用吸管、小管等玻璃器皿应在试验前1~2天内包好,经200℃干烤2小时除内毒素备用。
8.3.2鲎试剂灵敏度复核根据鲎试剂灵敏度的标示值(λ),将细菌内毒素国家标准品或细菌内毒素工作标准品用细菌内毒素检查用水溶解,在漩涡混合器上混匀15分钟,然后制成2λ、λ、0.5λ和0.25λ四个浓度的内毒素标准溶液,每稀释一步均应在漩涡混合器上混匀30秒钟;取分装有0.1ml鲎试剂溶液的10mm×100mm试管18支,其中16管分别加入0.1ml不同浓度的内毒素标准溶液,每一个内毒素浓度平行做4管;另外2管加入0.1ml细菌内毒素检查用水作为阴性对照;将试管中溶液轻轻混匀后,封闭管口,垂直放入37℃±1℃的恒温器中,保温60分钟±2分钟。
8.4结果判定8.4.1将试管从恒温器中轻轻取出,缓缓倒转180°,若管内形成凝胶,并且凝胶不变形、不从管壁滑脱者为阳性;未形成凝胶或形成的凝胶不坚实、变形并从管壁滑脱者为阴性。
保温和拿取试管过程应避免受到振动造成假阴性结果。
8.4.2当最大浓度2λ管均为阳性,最低浓度0.25λ管均为阴性,阴性对照管为阴性,试验方为有效。
中国药典2020版鲎试剂细菌内毒素检查预试验SOP

1目的建立细菌内毒素预试验操作规程,以指导检验人员的正确规范操作,为保证细菌内毒素检查凝胶法的准确性提供依据。
2适用范围适用于细菌内毒素检查法的“鲎试剂灵敏度复核试验”和“干扰试验”。
本规程参照《中国药典》2020年版四部-1143细菌内毒素检查法制定。
3职责进行细菌内毒素检查的操作人员严格按本规程进行操作。
4内容4.1基本原理4.1.1本法采用凝胶法,系通过鲎试剂与内毒素产生凝集反应的原理进行限度检测或半定量检测内毒素的方法。
4.1.2鲎试剂灵敏度复核试验:当使用新批号的鲎试剂或试验条件发生了任何可能影响检验结果的改变时,应进行鲎试剂灵敏度复核试验。
4.1.3干扰试验:当进行新药的内毒素检查试验前,或无内毒素检查项目的品种建立内毒素检查法时,须进行干扰试验;当鲎试剂、供试品的处方、生产工艺改变或试验环境中发生了任何有可能影响试验结果的变化时,须重新进行干扰试验。
4.1.4本试验操作过程应防止内毒素的污染。
4.1.5EU:内毒素单位,1EU与1个内毒素国际单位(IU)相当。
4.1.6λ:鲎试剂的标示灵敏度,单位:EU/ml。
4.1.7MVD:最大有效稀释倍数,指在试验中供试品溶液被允许达到稀释的最大倍数。
4.2材料准备4.2.1细菌内毒素工作标准品:应经细菌内毒素国家标准品为基准标定效价;4.2.2鲎试剂:当使用新批号前,按《细菌内毒素预试验SOP》进行灵敏度检查;4.2.3细菌内毒素检查用水(BET水):内毒素含量应<0.015EU/ml,且对内毒素试验无干扰作用;4.2.4供试品溶液:pH宜在6.0~8.0范围内,否则用已去除内毒素和干扰因子的酸、碱溶液或缓冲液调节。
4.3器具准备4.3.1移液枪、一次性除热源枪头(1000μL、200μL);4.3.2剪刀、砂轮片、试管架、除热源试管、医用胶布;4.3.3恒温培养箱(37℃±1℃)、旋涡混合器、洁净工作台。
4.4鲎试剂灵敏度复核试验4.4.1试验过程:4.4.1.1根据当批鲎试剂的标示灵敏度(λ),把细菌内毒素工作标准品用适量BET水充分溶解,避免产生气泡,在旋涡混合器上混匀15分钟。
G试验和鲎实验操作技术

五、血样检测过程
7、葡聚糖参考标准: 100.5pg/ml为正常值; 100.5~151.5pg/ml之间,为病变期 ,应连续检测; 151.5pg/ml以上,为念珠菌或曲霉菌 深部感染。 灵敏度:最小有效检出值10pg/ml 特异性:对小于或等于1.0EU/ml,脂多糖不反 应 标准曲线范围:10~500pg/ml
3
一、前期的准备工作
8、反应试管(储备量是两倍左右) 9、高低试管架各两个 10、采血管(看院方情况,可用BD 管,可用我们的采血管) 11、工作服两套 12、一次性塑料手套、一次性乳胶 手套各一盒
一、前期的准备工作
。
三、仪器(装机):
1、动态试管器有两线线,一条接 电脑,一条接电源,另外电脑也 接上电源线; 2、先把仪器提前接上,以便让温 度快速达到37°C,再把恒温仪接 上电源,以便让温度快速到达 75°C。
6
五、血样检测过程
临床操作规程:B-G检测 1、采血2ml --离心(1500转/10分钟;3000 转/分钟) --样品稀释液0.9ml+0.1血浆(稀释10倍) --放在漩涡器上混匀,3秒 --避光转移到恒温仪加热(75度,10分钟) --冷却(冷却区2~8度或常温冷却,10 分钟);
注意:桌子要平稳、水平,不能摇晃
五、血样检测过程
8、LPG参考标准: 10pg/ml以下,为健康人群; 10~20pg/ml之间,为病变观察期,应连续检测; 20pg/ml以上,为深部真菌感染症状,需对症治疗。 灵敏度:最小有效检出值5pg/ml 精密度:批间 CV≤10% 准确性:回收率平均75-125%
Hale Waihona Puke 127五、血样检测过程
2、试剂干粉0.25+试剂复溶剂 0.25ml(不能用漩涡混合机, 自动沉清1分钟; 3、打开反应试管(每一个样品 取两根,只能用手指夹试管 中间,头部避免污染,底部 怕影响透光度,影响结果)
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
正文
规范鲎试剂灵敏度复核的操作过程和要求,确保鲎试剂灵敏度复核结果的可靠性。
适用于质监处药理室对鲎试剂灵敏度的复核。
质监处药理室分析人员负责本规程的实施和完成相关记录。
USP版附录85;
CP版附录Ⅺ E 。
细菌内毒素检查法:本法系利用从鲎的变形细胞中提取的试剂来检测或量化由革兰阴性菌产生的细菌内毒素,以判断供试品中细菌内毒素的含量是否符合规定的一种方法。
细菌内毒素的量用内毒素单位(EU)表示。
鲎试剂:是鲎变形细胞的溶出物经提取而成。
鲎试剂灵敏度:在本检查法规定的条件下能检测出内毒素标准溶液或供试品溶液中的最低内毒素浓度,用EU/ml表示。
细菌内毒素检查用水(BET水):系指与灵敏度为0.03EU/ml 或更高灵敏度的鲎试剂在37 1 C 条件下24小时不产生凝集反应的灭菌注射用水。
细菌内毒素标准品:USP细菌内毒素参考标准品(RSE)或已标定的细菌内毒素工作标准品(CSE)。
反应终点浓度:是指系列递减的内毒素浓度中最后一个呈现阳性结果的浓度。
一、试剂、材料与仪器设备
试剂:
鲎试剂批号、灵敏度、规格、生产商。
细菌内毒素检查用水(BET水) 批号、规格、生产商。
细菌内毒素标准品批号、效价、生产商。
材料及仪器设备:
电热恒温水箱型号、设备编号。
电热鼓风干燥箱型号、设备编号。
漩涡混合器型号。
无热原试管规格:1075mm。
正文
无热原玻璃瓶规格:25ml。
无热原玻璃吸管规格:1ml、2ml、5ml、10ml。
试管架、无热原封口膜、洗耳球、酒精棉球、砂轮片。
二、试验准备
试验所用的容器、用具都必须经过处理,250C以上干烤至少1小时,以去除外源性内毒素。
试验操作过程应避免微生物的污染。
三、内毒素溶液配制
细菌内毒素标准品系列溶液配制取RSE或CSE 1瓶,按照使用说明书加入规定量的细菌内毒素检查用水使溶,并用漩涡混合器间歇混匀30分钟,然后用细菌内毒素检查用水进一步稀释至2.0、、 0.5、 0.25四个浓度的内毒素标准溶液,每一步稀释应混匀至少30秒钟。
四、试验过程
取被复核的鲎试剂原安瓿18支,分别用0.1ml细菌内毒素检查用水复溶。
其中16支加入0.1ml细菌内毒素系列标准溶液,每浓度溶液平行做4支;另外2支加入0.1ml 细菌内毒素检查用水作为阴性对照。
将安瓿中的溶液轻轻混匀后,用封口膜封闭管口,垂直放入371℃电热恒温水箱中,保温602分钟。
反应结果记录在鲎试剂灵敏度复核记录中。
五、试验结果观察和有效性
结果观察将安瓿从电热恒温水箱中轻轻取出,缓缓倒转180°时,管内凝胶不变形,不从管壁滑脱者为阳性,记录为(+);凝胶不能保持完整并从管壁滑脱者为阴性,记录为(–)。
保温和拿取安瓿过程应避免受到振动造成假阴性结果。
有效性对于细菌内毒素标准品系列溶液,如果最大浓度2.0管均为阳性,最低浓度0.25管均为阴性,阴性对照管均为阴性,试验方为有效。
六、灵敏度复核结果的计算
计算公式为:
c=lg-1(Σe/4)
正文
式中e为细菌内毒素标准品反应终点浓度的对数值。
合格标准当0.5≤c<1.3时,方可用于细菌内毒素检查,并以标示灵敏度为该批鲎试剂的灵敏度。
鲎试剂有效期按厂家规定执行。
鲎试剂应在2~10℃条件下保存。
当鲎试剂的批号改变时需进行鲎试剂灵敏度的复核。
.。
