有机化学实验习题、思考题与解答
大学大二学期有机化学实验思考题答案

大学大二学期有机化学实验思考题答案篇一:大学有机化学二课后题第二章饱和脂肪烃2.1 用系统命名法(如果可能的话,同时用普通命名法)命名下列化合物,并指出(c)和(d) 中各碳原子的级数。
a.CH3(CH2)32)3CH3C(CH3)22CH(CH3)2CH3d.CH3CH2CH2b.HHHHHHHHHHc.CH322CH3)2CH231HH。
CH3CH3e.3H3CH3f.(CH3)4Cg.CH32CH32H52CH2CH3h.(CH3)2CHCH2CH2CH(C2H5)2答案:a. 2,4,4-三甲基-5-正丁基壬烷5-butyl-2,4,4-trimethylnonaneb. 正己烷hexanec. 3,3-二乙基戊烷3,3-diethylpentaned. 3-甲基-5-异丙基辛烷5-isopropyl-3-methyloctanee. 2-甲基丙烷(异丁烷)2-methylpropane (iso-butane)f. 2,2-二甲基丙烷(新戊烷) 2,2-dimethylpropane (neopentane)g. 3-甲基戊烷3-methylpentaneh. 2-甲基-5-乙基庚烷5-ethyl-2-methylheptane2.2 下列各结构式共代表几种化合物?用系统命名法命名。
CH3a.CH32CHCH3CH3d.CH32CHCH3H3CCH3e.CHCH33CH3CH3CHCH2CHCH3CH33f.b.CH3CHCH3CH2CH33CH3CH33CH33CH3CH3c.CH3CH3CH33CH3CH3答案:a =b = d = e为2,3,5-三甲基己烷c = f 为2,3,4,5-四甲基己烷2.3 写出下列各化合物的结构式,假如某个名称违反系统命名原则,予以更正。
a. 3,3-二甲基丁烷b. 2,4-二甲基-5-异丙基壬烷 c. 2,4,5,5-四甲基-4-乙基庚烷 d. 3,4-二甲基-5-乙基癸烷e.2,2,3-三甲基戊烷 f. 2,3-二甲基-2-乙基丁烷g. 2-异丙基-4-甲基己烷h. 4-乙基-5,5-二甲基辛烷答案:a.错,应为2,2-二甲基丁烷b.c.d.e.f.错,应为2,3,3-三甲基戊烷g.错,应为2,3,5-三甲基庚烷h.2.5将下列化合物按沸点由高到低排列(不要查表)。
有机实验思考题答案

基本操作实验一常压蒸馏和沸点的测定1、在有机化学实验中经常使用的玻璃冷凝管有哪些?它们各用在什么地方?答:学生实验中经常使用的冷凝管有:直形冷凝管,球形冷凝管,空气冷凝管及刺形分馏柱等。
直形冷凝管一般用于沸点低于140℃的液体有机化合物的沸点测定和蒸馏操作中;沸点大于140℃的有机化合物的蒸馏可用空气冷凝管。
球形冷凝管一般用于回流反应即有机化合物的合成装置中(因其冷凝面积较大,冷凝效果较好);刺形分馏柱用于精馏操作中,即用于沸点差别不太大的液体混合物的分离操作中。
2、蒸馏的原理是什么?写出蒸馏装置中仪器的名称。
答:纯的液态物质在一定的压力下具有确定的沸点,不同的物质具有的不同的沸点。
蒸馏操作就是利用不同物质的沸点差异对液态混合物进行分离和纯化。
把一个液体化合物加热,其蒸汽压升高,当与外界大气压相等时,液体沸腾为蒸汽,再通过冷凝使蒸汽变为液体的过程。
蒸馏适用于沸点相差30℃以上的混合物的分离。
如果组分沸点差异不大,就需要采用分馏操作对液体混合物进行分离和纯化。
蒸馏装置主要由圆底烧瓶、蒸馏头、温度计、直形冷凝管、尾接管(又叫接液管)和接受瓶组成。
3、纯净化合物的沸点是固定的,所以具有恒定沸点的液体就一定是纯净物,对不对,为什么?答:在一定压力下,纯净化合物的饿沸点是固定的。
但是,具有恒定沸点的液体就不一定是纯净物。
因为两个或两个以上的化合物形成的共沸混合物也具有一定的沸点。
4、冷凝管通水方向是由下而上,反过来行吗?为什么?答:冷凝管通水是由下而上,反过来不行。
因为这样冷凝管不能充满水,由此可能带来两个后果:其一,气体的冷凝效果不好。
其二,冷凝管的内管可能炸裂。
5、蒸馏时加热的快慢,对实验结果有何影响?为什么?答:蒸馏时加热过猛,火焰太大,易造成蒸馏瓶局部过热现象,使实验数据不准确,而且馏份纯度也不高。
加热太慢,蒸气达不到支口处,不仅蒸馏进行得太慢,而且因温度计水银球不能被蒸气包围或瞬间蒸气中断,使得温度计的读数不规则,读数偏低。
王全瑞主编《有机化学》习题及思考题答案
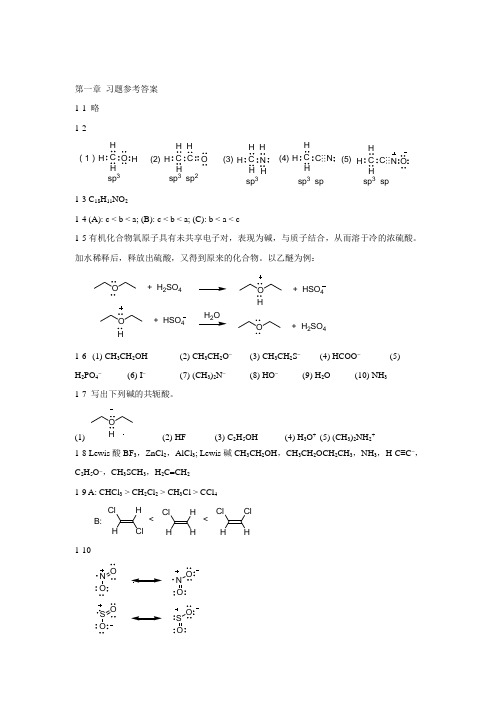
第一章 习题参考答案 1-1 略 1-2C O H H H C C OH H (1)(2)H(3)sp 3sp 3 sp 2C NH H H H C C H H H ⋯⋯N (4)(5)C C HHH ⋯⋯N O sp 3 sp 3sp sp 3 sp1-3 C 18H 11NO 21-4 (A): c < b < a; (B): c < b < a; (C): b < a < c1-5有机化合物氧原子具有未共享电子对,表现为碱,与质子结合,从而溶于冷的浓硫酸。
加水稀释后,释放出硫酸,又得到原来的化合物。
以乙醚为例:O+ H 2SO 4O + HSO 4H+ HSO 4HH OO+ H 2SO 41-6 (1) CH 3CH 2OH (2) CH 3CH 2O - (3) CH 3CH 2S - (4) HCOO -(5)H 2PO 4-(6) I -(7) (CH 3)2N -(8) HO -(9) H 2O (10) NH 31-7 写出下列碱的共轭酸。
(1) O H(2) HF (3) C 2H 5OH (4) H 3O + (5) (CH 3)2NH 2+1-8 Lewis 酸BF 3,ZnCl 2,AlCl 3; Lewis 碱CH 3CH 2OH ,CH 3CH 2OCH 2CH 3,NH 3,H-C ≡C -,C 2H 5O -,CH 3SCH 3,H 2C =CH 2 1-9 A: CHCl 3 > CH 2Cl 2 > CH 3Cl > CCl 4HCl H HHCl Cl H HCl HCl B:<<1-10N ON OS S ON OON OON OO第二章 习题参考答案 2-1(1)3-甲基-4-乙基庚烷;(2)2-甲基-4-异丙基己烷;(3)新壬烷;(4)2-甲基-5-乙基庚烷 (5)2-甲基-3-丙基己烷;(6)4-叔丁基辛烷;2-2 (1)(2)CH 3CHCHCH 3H 3CCH 3C CH 2CH 3CH 3CH 3H 3C (3)CH 3CHCH2CH 2CH 3CH32-3(1)庚烷(2)2-甲基己烷(3)(4)(5)(6)(7)(8)(9)3-甲基己烷2, 2-二甲基戊烷3, 3-二甲基戊烷2, 3-二甲基戊烷2, 4-二甲基戊烷3-乙基戊烷2, 2, 3-三甲基丁烷2-4CH 3—C —CH 2—CH —CH 2—CH 3CH 3CH 3CH 31°2°3°2°4°1°1°1°1°2-5 该化合物分子式为C 8H 18,结构式 命名为:2,2,3,3-四甲基丁烷 2-6 化合物沸点依次降低顺序:(4)>(2)>(3)>(5)>(1)H 3CH 3CC C CH 3CH 3H3CCH 3(7) (CH 3)2CHCH 2CH 3(8) (CH 3)2CHCHCH 2CH 2 CCH 2CH 3CH 2CH 3CH 3CH 2CH 3(9)(10)2-7 熔点:(1)>(2);沸点:(1)<(2) 2-8 稳定性大小:(1)>(3)>(2)>(4)2-9 1,2-二溴乙烷的四种典型构象式(从左到右稳定性依次降低)H HBr H H BrH H H HBrH H H HHHBr HBrH BrBr对位交叉式邻位交叉式 部分重叠式 全重叠式3, 4-二甲基己烷的优势构象为:2-10链引发:Cl 22Cl •链增长:Cl •+Cl•+ HCl•+ Cl 2Cl •+链终止:Cl •Cl •+Cl 2•Cl •+Cl•+•2-11 主要的原因是:甲基环己烷分子结构中有1个3º H ,10个2º H ,3个1º H ,进行溴代CH 3Br25反应时,不同类型氢原子的反应活性大小是3º H ∶2º H ∶1º H = 1600∶82∶1,可以初步计算出3º H 被溴取代后的产物所占百分比例大约是66%,因此反应主要得到 2-13 该化合物为: Cl 2++ HClC C H 3C H 3C H 3C CH 3CH 3CH 3C C H 3C H 3C H 3C CH 3CH 3CH 2Cl第三章 习题参考答案 3-1(1)甲基环戊烷 (2)1-甲基-4-乙基环己烷 (3)2-甲基-3-环丙基-6-环丁基辛烷 (4)反-1-甲基-2-异丙基环丁烷 (5)1-甲基-3-环戊基环己烷 (6)2-甲基-8-乙基螺[4.5]癸烷 (7)2, 7, 7-三甲基二环[4.1.0]庚烷 (8)二环[3.3.3]十一烷(9)1-甲基二环[2.2.2]辛烷(10) (11) (12) (13)3-2 该烃分子可能为下列化合物之一:甲基环己烷 乙基环戊烷 丙基环丁烷 丁基环丙烷 3-3(1)2) H 2OBrBr CH 2BrOHC C H 3C H 3C H 3C CH 3CH 3CH 3(2)HBrBr3-4顺-1-甲基-4-丙基环己烷的椅式构象式 反-1-甲基-4-丙基环己烷的椅式构象式CH 3C(CH 3)3H 3CC(CH 3)3CH 3C(CH 3)3C(CH 3)3CH 3最优势构象 3-5(1)CH 3H 3CC(CH 3)3(2) CH 3C 2H 5CH 3(3)CH 3(4) C(CH 3)3C 2H 5(5)C 2H 5C 2H 5H 5C 23-6 3, 4-二溴-1-叔丁基环己烷可能的构象异构体如下:C(CH 3)3C(CH 3)3Br BrC(CH 3)3BrBr C(CH 3)3BrBrC(CH 3)3Br BrBrBr C(CH 3)3BrBrC(CH 3)3BrBrC(CH 3)3BrBr3-7 化合物A 是: 化合物B 是: Br反应式:溴水褪色BrCH2BrBr3-8溴 水褪 色褪 色无变化无变化褪 色3-9 反-1,2-二甲基环己烷采用ee 构象时,亚甲基和甲基是处在对位交叉式,分子内能较小;而在aa 构象中,亚甲基和甲基是处在邻位交叉式,分子扭转张力相对比较大,同时由于1,3-竖键作用,空间张力大。
有机实验思考题答案知识讲解

从茶叶中提取咖啡因1、提取咖啡因时用到生石灰,它起什么作用?答:放置生石灰可以中和茶叶中的单宁酸,此外还可以吸收水分。
2、从茶叶中提取出的粗咖啡因有绿色光泽,为什么?答:茶叶中除了含有咖啡因,还含有棕色的黄酮类色素、叶绿素和丹宁等。
带有绿色光泽是因为产品不纯,含有叶绿素。
萘的重结晶1、重结晶的主要操作过程及各步骤的目的(1)热饱和溶液的制备。
溶剂充分分散产物和杂质,以利于分离提纯。
(2)脱色。
吸附色素和树脂状杂质。
(3)热过滤。
除去不溶物质。
(4)冷却结晶。
进一步与可溶性杂质分离。
(5)过滤。
晶体从留在母液中的杂质彻底分离。
2、加活性炭脱色应注意哪些问题?答:活性炭的加入量为粗产品的1—5%,活性碳要在固体物质全部溶解后加入。
先加少量,视脱色情况再考虑是否增加加入量;活性炭需在热饱和溶液的制备好后稍冷时加入,防止暴沸;加入后继续加热搅拌使溶液沸腾至完全脱色。
3、如何选择重结晶溶剂?答:溶剂的筛选:1. 与被提纯的有机物不起化学反应。
2. 对被提纯的有机物应易溶于热溶剂中,而在冷溶剂中几乎不溶。
3. 对杂质的溶解度应很大(杂质留在母液中不随被提纯物的晶体析出,以便分离)或很小(趁热过滤除去杂质)。
4. 能得到较好的结晶。
5. 溶剂的沸点适中。
6. 价廉易得,毒性低,回收率高,操作安全。
4、如何鉴定重结晶纯化后产物的纯度?答:测定重结晶物质的熔点,接近或相等于纯净物质的熔点,这可认为重结晶物质纯度高。
乙酸乙酯的合成1、酯化反应有什么特点?本实验如何创造条件促使酯化反应尽量向生成物方向进行?答:酯化反应特点:属于可逆反应,一般情况下反应进行不彻底,依照反应平衡原理,要提高酯的产量,需要用从产物分离出一种成分或使反应物其中一种成分过量的方法使反应正方向进行。
2、本实验可能有哪些副反应?答:浓H₂SO₄CH₃CH₂OH ------→CH₂=CH₂↑+ H₂O170℃浓H₂SO₄2CH₃CH₂OH ------→CH₃CH₂OCH₂CH₃+ H₂O140℃3、在酯化反应中,用作催化剂的硫酸量,一般只需醇质量的3%就够了,本实验方法(Ⅰ)为何用了6mL,方法(Ⅱ)中用了4mL?答:因为过量的硫酸还有他用,在反应物中加入的硫酸不仅仅有催化剂的作用还为反应提供了酸,增大了反应平衡常数同时也吸收了生成的部分水分,促使反应向生成乙酸乙酯的方向发生。
有机化学实验思考题答案

实验一乙酰苯胺的制备(苯胺5ml、冰醋酸7.5ml,生成苯-NHCOCH3+、水,韦氏分馏柱、温度计蒸馏头尾接管等、布氏漏斗抽滤)1.制备乙酰苯胺为什么选用乙酸做酰基化试剂?(乙酰氯、乙酸酐反应过于激烈。
)答:冰醋酸与苯胺反应最慢,但反应平稳、易于控制,且醋酸价格较便宜。
2.为什么要控制分馏柱上端温度在100到110之间,若温度过高有什么不好?答:主要由原料CH3COOH和生成物水的沸点所决定。
控制在100到110度之间,这样既可以保证原料CH3COOH 充分反应而不被蒸出,又可以使生成的水立即移走,促使反应向生成物方向移动,有于提高产率。
3.本实验中采用了那些措施来提高乙酰苯胺的产率?答:加入过量冰醋酸,分馏时加入少量锌粉,控制分馏时温度,不断除去生成的水。
4.常用的乙酰化试剂有哪些?哪一种较经济?哪一种反应最好?答:常用的乙酰化试剂有乙酸、乙酸酐和乙酰氯。
乙酸较经济。
乙酰氯反应速度最快,但易吸潮水解。
因此应在无水条件下进行反应。
实验二重结晶(乙酰苯胺,加热溶解、稍冷却、加活性炭、继续加热、热过滤、冷却结晶、抽滤)1.重结晶一般包括哪几个操作步骤?各步操作的目的是什么?答:重结晶一般包括:溶解、脱色、热过滤、冷却结晶、抽滤、干燥等操作步骤。
各步操作的目的如下:熔解:配制接近饱和的热溶液;脱色:使样品中的有色杂质吸附于活炭上,便于在热过滤时将其分离;热过滤:除去样品中的不溶性杂质;冷却结晶:使样品结晶析出,而可溶性杂质仍留在溶液中;抽滤:使样品可溶性杂质与样品分离。
干燥:使样品结晶表面的溶剂挥发。
2.在什么情况下需要加活性炭?应当怎样加活性炭?答:样品颜色较深时,需要加入活性炭进行脱色。
为了防止爆沸,加活性炭时应将热溶液取下稍冷后再加。
3.为什么热过滤时要用折叠滤纸?答:增大过滤面积,加快过滤速度。
4.为什么利用重结晶只能提纯杂质含量低于5%的固体有机物?答:如果样品中杂质含量大于5%,则可能在样品结晶析出时,杂质亦析出,经抽滤后仍有少量杂质混入样品,使重结晶后的样品纯度仍达不到要求。
(完整版)大学大二学期有机化学实验思考题答案

一、熔点的测定1.测定熔点时, 遇到下列情况将产生什么结果?(1 熔点管壁太厚;(2熔点管底部未完全封闭, 尚有一针孔。
(3)熔点管不洁净;(4样品未完全干燥或含有杂质;(5样品研得不细或装的不紧密。
(6加热太快。
答: (1 熔点管壁太厚, 影响传热, 其结果是测得的初熔温度偏高。
(2 熔点偏低(3 熔点管不洁净, 相当于在试料中掺入杂质, 其结果将导致测得的熔点偏低。
(4 熔点偏低(5 样品研得不细或装的不紧密, 这样试料颗粒之间空隙较大, 其空隙之间为空气所占据, 而空气导热系数较小, 结果导致熔距加大, 测得的熔点数值偏高。
(6 加热太快, 则热浴体温度大于热量转移到待测样品中的转移能力, 而导致测得的熔点偏高, 熔距加大。
2、是否可以使用第一次测定熔点时已经熔化了的有机化合物再作第二次测定呢?为什么?答:不可以。
因为有时某些物质会发生部分分解, 有些物质则可能转变为具有不同熔点的其它结晶体。
二、重结晶提纯有机物1.重结晶一般包括哪几个步骤?各步骤的主要目的是什么?答: 重结晶一般包括下列几个步骤:(1)选择适宜溶剂, 目的在于获得最大回收率的精制品。
(2)制成热的饱和溶液。
目的是脱色。
(3)热过滤, 目的是为了除去不溶性杂质(包括活性炭)。
(4)晶体的析出, 目的是为了形成整齐的晶体。
(5)晶体的收集和洗涤, 除去易溶的杂质, 除去存在于晶体表面的母液。
(6)晶体的干燥, 除去附着于晶体表面的母液和溶剂。
2.重结晶时, 溶剂的用量为什么不能过量太多, 也不能过少?正确的应该如何?答: 过量太多, 不能形成热饱和溶液, 冷却时析不出结晶或结晶太少。
过少, 有部分待结晶的物质热溶时未溶解, 热过滤时和不溶性杂质一起留在滤纸上, 造成损失。
考虑到热过滤时, 有部分溶剂被蒸发损失掉, 使部分晶体析出留在波纸上或漏斗颈中造成结晶损失, 所以适宜用量是制成热的饱和溶液后, 再多加20%左右。
3、用活性炭脱色为什么要在固体物质完全溶解后才加入?为什么不能在溶液沸腾时加入?答:说法一、若固体物质未完全溶解就加入活性炭, 就无法观察到晶体是否溶解, 即无法判断所加溶剂量是否合适。
有机化学实验习题思考题与解答
其缺点是除原料价格昂贵外,该法不适用于钝化的胺(如邻或对硝
基苯胺)。
(3)用醋酸作乙酰化剂,其优点是价格便宜;缺点是反应时间长。
在肉桂酸制备实验中,能否在水蒸汽蒸馏前用氢氧化钠代替碳
酸钠来中和水溶液?
答:不能。因为苯甲醛在强碱存在下可发生Cannizzaro反应。
浓 O H
2 C 6 H 5 C H O
在正溴丁烷制备实验中,硫酸浓度太高或太低会带来什么结果?
答:硫酸浓度太高:(1)会使NaBr氧化成Br2,而Br2不是亲核试剂。 2 NaBr + 3 H2SO4(浓) →Br2 + SO2 + 2 H2O +2 NaHSO4
(2)加热回流时可能有大量HBr气体从冷凝管顶端逸出形成酸雾。硫酸浓度 太低:生成的HBr量不足,使反应难以进行。
51 如果液体具有恒定的沸点,能否认为它是单纯物质?为什么?
答:如果液体具有恒定的沸点,不能认为它是单纯物质。因为
有些液体能与其它组份化合物形成二元或三元恒沸物,它们也有恒
定的沸点,但确是混合物,而不是单纯物质。
52
21
管,空气冷凝管及刺形分馏柱等。直形冷凝管一般用于沸点低于 140℃的液体有机化合物的沸点测定和蒸馏操作中;沸点大于140℃ 的有机化合物的蒸馏可用空气冷凝管。球形冷凝管一般用于回流反 应即有机化合物的合成装置中(因其冷凝面积较大,冷凝效果较好); 刺形分馏柱用于精馏操作中,即用于沸点差别不太大的液体混合物 的分离操作中。
7
在蒸馏装置中,温度计水银球的位置不符合要求会带来什么结
果?
答:如果温度计水银球位于支管口之上,蒸气还未达到温度计
水银球就已从支管流出,测定沸点时,将使数值偏低。若按规定的
有机实验思考题
有机实验思考题P45(1)为什么在拉制玻璃管及毛细管等时,玻璃管必须均匀转动加热?答:1、保证玻璃管受热均匀,从而保障拉管和弯管的效果,否则极易变形且不具有较好的对称性。
2、均匀转动,以免玻管在受热转动过程中绞曲。
(2)在强热玻璃管(棒)之前,应先用小火加热。
在加工完毕后,又需经小火“退火”,这是为什么?答:强热之前,先用小火烘,再加大火焰,以防止玻璃管破裂。
加工后,若直接从火焰中拿出玻璃管,它会因急速冷却,内部产生很大的压力,即使不立即开裂,过后也有破裂的可能。
若经小火退火,可使温度逐渐降低,不致出现上述结果。
P61(1)三个瓶子中分别装有A、B、C三种白色结晶的有机固体每一种都在149—150熔化。
一种50:50的A与B的混合物在130-139℃熔化;50:50的A与C的混合物在149-150℃熔化,那么50:50的B与C的混合物在什么样的温度范围内熔化呢?你能说明A,B,C是同一种物质?应采取什么方法鉴别样品?答:通过熔点判定化合物纯度有一个经验规则:混合物熔点低于任何一个组分,即两两混合,如果熔点不下降,那就表示是同种物质。
A和B是不同种物质,A和C是同种物质,那B和C就与A和B是一样的,在130-139℃熔化。
(2)测熔点时,若有下列情况,将产生什么结果?(a)熔点管不洁净。
答:等于样品中有杂质致使测得熔点偏低熔程加大。
( b ) 熔点管底部未完全封闭,尚有一针孔。
答:空气会进入,加热时,可看到有气泡从溶液中跑出,接着溶液进入,结晶很快熔化,也测不准,偏低。
( c ) 熔点管壁太厚。
答:受热不均匀,熔点测不准,熔点数据易偏高,熔程大。
( d ) 样品未完全干燥或含有杂质。
答:内有水分和其它溶剂,加热,溶剂气化,使样品松动熔化,也使所测熔点数据偏低,熔程加大,样品含有杂质的话情况同上。
(e)加热太快。
答:升温太快,会使所测熔点数据偏高,熔程大,所以加热不能太快。
这一方面是为了保证有充分的时间让热量由管外传至管内,以使固体熔化。
有机化学实验思考题全
正丁醚的制备[思考题]1、反应物冷却后为什么要倒入50mL 水中?各步的洗涤目的何在?答:反应物冷却后倒入50mL 水中,是为了分出有机层,除去沸石和绝大部分溶于水的物质。
水洗,除去有机层中的大部分醇;碱洗,中和有机层中的酸;10mL水洗,除去碱和中和产物;15mL 饱和氯化钙溶液,除去有机层中的大部分水和醇类。
2、能否用本实验方法由乙醇和2-丁醇制备乙基仲丁基醚?你认为用什么方法比较好?答:不能,会产生很多副产物。
应该用Williamson 合成法。
用氯乙烷钠和2- 甲基-1-丙醇钠正溴丁烷的制备[思考题]1、什么时候用气体吸收装置?如何选择吸收剂?答:反应中生成的有毒和刺激性气体(如卤化氢、二氧化硫)或反应时通入反应体系而没有完全转化的有毒气体(如氯气),进入空气中会污染环境,此时要用气体吸收装置吸收有害气体。
选择吸收剂要根据被吸收气体的物理、化学性质来决定。
可以用物理吸收剂,如用水吸收卤化氢;也可以用化学吸收剂,如用氢氧化钠溶液吸收氯和其它酸性气体。
2、在正溴丁烷的合成实验中,蒸馏出的馏出液中正溴丁烷通常应在下层,但有时可能出现在上层,为什么?若遇此现象如何处理?答:若未反应的正丁醇较多,或因蒸镏过久而蒸出一些氢溴酸恒沸液,则液层的相对密度发生变化,正溴丁烷就可能悬浮或变为上层。
遇此现象可加清水稀释,使油层(正溴丁烷)下沉。
3、粗产品正溴丁烷经水洗后油层呈红棕色是什么原因?应如何处理?答:油层若呈红棕色,说明含有游离的溴。
可用少量亚硫酸氢钠水溶液洗涤以除去游离溴。
反应方程式为Br + NaHSO + H O →2HBr + NaHSO2 3 2 4己二酸的制备[思考题]1、加料时,量过环己醇的量筒能否直接用来量取50% HNO ?答:量过环己醇的量筒不可直接用来量取50% NHO 。
因为50% NHO 与残留的环己醇会剧烈反应,同时放出大量的热,这样一来,量取50% NHO3 的量不准,而且容易发生意外事故。
有机化学实验思考题答案【精选】
实验一乙酰苯胺的制备(苯胺5ml、冰醋酸7.5ml,生成苯-NHCOCH3+、水,韦氏分馏柱、温度计蒸馏头尾接管等、布氏漏斗抽滤)1.制备乙酰苯胺为什么选用乙酸做酰基化试剂?(乙酰氯、乙酸酐反应过于激烈。
)答:冰醋酸与苯胺反应最慢,但反应平稳、易于控制,且醋酸价格较便宜。
2.为什么要控制分馏柱上端温度在100到110之间,若温度过高有什么不好?答:主要由原料CH3COOH和生成物水的沸点所决定。
控制在100到110度之间,这样既可以保证原料CH3COOH 充分反应而不被蒸出,又可以使生成的水立即移走,促使反应向生成物方向移动,有于提高产率。
3.本实验中采用了那些措施来提高乙酰苯胺的产率?答:加入过量冰醋酸,分馏时加入少量锌粉,控制分馏时温度,不断除去生成的水。
4.常用的乙酰化试剂有哪些?哪一种较经济?哪一种反应最好?答:常用的乙酰化试剂有乙酸、乙酸酐和乙酰氯。
乙酸较经济。
乙酰氯反应速度最快,但易吸潮水解。
因此应在无水条件下进行反应。
实验二重结晶(乙酰苯胺,加热溶解、稍冷却、加活性炭、继续加热、热过滤、冷却结晶、抽滤)1.重结晶一般包括哪几个操作步骤?各步操作的目的是什么?答:重结晶一般包括:溶解、脱色、热过滤、冷却结晶、抽滤、干燥等操作步骤。
各步操作的目的如下:熔解:配制接近饱和的热溶液;脱色:使样品中的有色杂质吸附于活炭上,便于在热过滤时将其分离;热过滤:除去样品中的不溶性杂质;冷却结晶:使样品结晶析出,而可溶性杂质仍留在溶液中;抽滤:使样品可溶性杂质与样品分离。
干燥:使样品结晶表面的溶剂挥发。
2.在什么情况下需要加活性炭?应当怎样加活性炭?答:样品颜色较深时,需要加入活性炭进行脱色。
为了防止爆沸,加活性炭时应将热溶液取下稍冷后再加。
3.为什么热过滤时要用折叠滤纸?答:增大过滤面积,加快过滤速度。
4.为什么利用重结晶只能提纯杂质含量低于5%的固体有机物?答:如果样品中杂质含量大于5%,则可能在样品结晶析出时,杂质亦析出,经抽滤后仍有少量杂质混入样品,使重结晶后的样品纯度仍达不到要求。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
空隙中,再加热已不能产生细小的空气流而失效,必须重新补加沸
石。
8
5 冷凝管通水方向是由下而上,反过来行吗?为什么? 答:冷凝管通水是由下而上,反过来不行。因为这样冷凝管不
能充满水,由此可能带来两个后果:其一,气体的冷凝效果不好。 其二,冷凝管的内管可能炸裂。 6
蒸馏时加热的快慢,对实验结果有何影响?为什么? 答:蒸馏时加热过猛,火焰太大,易造成蒸馏瓶局部过热现象, 使实验数据不准确,而且馏份纯度也不高。加热太慢,蒸气达不到 支口处,不仅蒸馏进行得太慢,而且因温度计水银球不能被蒸气包 围或瞬间蒸气中断,使得温度计的读数不规则,读数偏短,致使最后蒸馏是前馏份增 多而影响产率。
10 在环己烯制备实验中,为什么要控制分馏柱顶温度不超过73℃? 答:因为反应中环己烯与水形成共沸混合物(沸点70.8℃,含水
10 %);环己醇与环己烯形成共沸混合物(沸点64.9℃,含环己醇 30.5 %);环己醇与水形成共沸混合物(沸点97.8℃,含水80 %),因 此,在加热时温度不可过高,蒸馏速度不易过快,以减少未反应的 环己醇的蒸出。
刺激性气体SO2放出。 9
如果你的实验产率太低,试分析主要在哪些操作步骤中造成损 失?
答:(1)环己醇的粘度较大,尤其室温低时,量筒内的环己醇很 难倒净而影响产率。
(2)磷酸和环己醇混合不均,加热时产生碳化。 (3)反应温度过高、馏出速度过快,使未反应的环己醇因于水形 成共沸混合物或产物环己烯与水形成共沸混合物而影响产率。
移能力,而导致测得的熔点偏高,熔距加大。
(5) 若连续测几次时,当第一次完成后需将溶液冷却至原熔点
温度的二分之一以下,才可测第二次,不冷却马上做第二次测量,
测得的熔点偏高。
(6) 齐列熔点测定的缺点就是温度分布不均匀,若温度计歪斜
或熔点管与温度计不附贴,这样所测数值会有不同程度的偏差。
2
是否可以使用第一次测定熔点时已经熔化了的试料使其固化后
如果温度计的水银球位于支管口之下或液面之上,测定沸点时,
数值将偏高。但若按规定的温度范围集取馏份时,则按此温度计位
置集取的馏份比要求的温度偏低,并且将有一定量的该收集的馏份
误认为后馏份而损失。
10
8 用磷酸做脱水剂比用浓硫酸做脱水剂有什么优点? 答:(1)磷酸的氧化性小于浓硫酸,不易使反应物碳化;(2)无
做第二次测定?
6
答:不可以。因为有时某些物质会发生部分分解,有些物质则 可能转变为具有不同熔点的其它结晶体。 3
测得A、B两种样品的熔点相同,将它们研细,并以等量混合(1) 测得混合物的熔点有下降现象且熔程增宽;(2)测得混合物的熔点与 纯A、纯B的熔点均相同。试分析以上情况各说明什么?
答:(1)说明A、B两个样品不是同一种物质,一种物质在此充 当了另一种物质的杂质,故混合物的熔点降低,熔程增宽。
(2)除少数情况(如形成固熔体)外,一般可认为这两个样品为 同一化合物。 4
沸石(即止暴剂或助沸剂)为什么能止暴?如果加热后才发现7 没
加沸石怎么办?由于某种原因中途停止加热,再重新开始蒸馏时,
是否需要补加沸石?为什么?
答:(1)沸石为多孔性物质,它在溶液中受热时会产生一股稳
定而细小的空气泡流,这一泡流以及随之而产生的湍动,能使液体
为便于学习,我们在制作了有机化学实验的网上预习 课件的同时,又制作了有机化学实验习题及解答课件,以
2
全面提高有机化学实验课的教学质量。 本课件将有机化学实验的习题分为以下五类:
思考题(SK) 实验操作(CZ) 实验装置(ZZ) 判断题(PD) 填空题(TK) 试题难度系数分为三级:N 1为容易题;N 2为较难题; N 3为难题。 试题编码为:题类—序号—难度。如:
有机化学实验习题、思考题与解答
有机化学实验习题及解答
有机化学实验教学经长期发展,已形成了独立的教学 体系。实验课的任务不仅是验证、巩固和加深课堂所学的 理论知识,更重要的是培养学生实验操作能力、综合分析 和解决问题的能力,养成严肃认真、实事求是的科学态度 和严谨的工作作风;培养学生积极思维,勇于实践,敢于 动手,不怕挫折,逐步掌握科学研究方法的创新能力,以 提高学生的综合素质。
TK — 5 — N 3 ↑↑↑ 题类 序号 难度
3
(SK)
4
思考题
1 测定熔点时,遇到下列情况将产生什么结果? (1) 熔点管壁太厚;(2) 熔点管不洁净;(3) 试料研的不细或装得
不实;(4)加热太快;(5) 第一次熔点测定后,热浴液不冷却立即做 第二次;(6)温度计歪斜或熔点管与温度计不附贴。
11 在乙酸正丁酯的制备实验中,粗产品中除乙酸正丁酯外,还有
哪些副产物?怎样减少副产物的生成?
12
答:主要副产物有:1-丁烯和正丁醚。 回流时要用小火加热,保持微沸状态,以减少副反应的发生。
12 在正溴丁烷制备实验中,硫酸浓度太高或太低会带来什么结果? 答:硫酸浓度太高:(1)会使NaBr氧化成Br2,而Br2不是亲核
中的大气泡破裂,成为液体分子的气化中心,从而使液体平稳地沸
腾,防止了液体因过热而产生的暴沸。
(2)如果加热后才发现没加沸石,应立即停止加热,待液体冷却
后再补加,切忌在加热过程中补加,否则会引起剧烈的暴沸,甚至
使部分液体冲出瓶外,有时会引起着火。
(3)中途停止蒸馏,再重新开始蒸馏时,因液体已被吸入沸石的
答:(1) 熔点管壁太厚,影响传热,其结果是测得的初熔温度 偏高。
(2) 熔点管不洁净,相当于在试料中掺入杂质,其结果将导致 测得的熔点偏低。
(3) 试料研得不细或装得不实,这样试料颗粒之间空隙较大,
5
其空隙之间为空气所占据,而空气导热系数较小,结果导致熔距加
大,测得的熔点数值偏高。
(4) 加热太快,则热浴体温度大于热量转移到待测样品中的转
9
7
在蒸馏装置中,温度计水银球的位置不符合要求会带来什么结
果?
答:如果温度计水银球位于支管口之上,蒸气还未达到温度计
水银球就已从支管流出,测定沸点时,将使数值偏低。若按规定的
温度范围集取馏份,则按此温度计位置集取的馏份比规定的温度偏
高,并且将有一定量的该收集的馏份误作为前馏份而损失,使收集
量偏少。
