15 第十四章 羧酸衍生物
第十四章 羧酸衍生物 酰基碳上的亲核取代反应
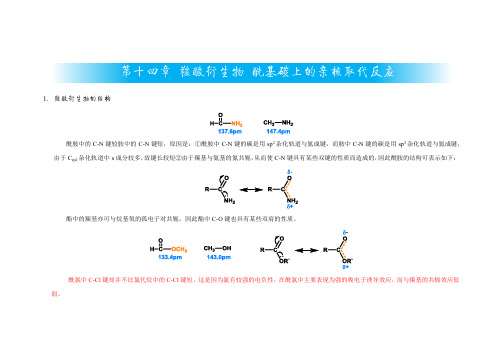
第十四章羧酸衍生物酰基碳上的亲核取代反应1.羧酸衍生物的结构酰胺中的C-N键较胺中的C-N键短,原因是:①酰胺中C-N键的碳是用sp2杂化轨道与氮成键,而胺中C-N键的碳是用sp3杂化轨道与氮成键,由于C sp2杂化轨道中s成分较多,故键长较短②由于羰基与氨基的氮共轭,从而使C-N键具有某些双键的性质而造成的,因此酰胺的结构可表示如下:酯中的羰基亦可与烷基氧的孤电子对共轭,因此酯中C-O键也具有某些双肩的性质。
酰氯中C-Cl键却并不比氯代烷中的C-Cl键短,这是因为氯有较强的电负性,在酰氯中主要表现为强的吸电子诱导效应,而与羰基的共轭效应很弱。
酰胺、酯、酰氯的共振式如下:在酰胺中具有相反电荷的偶系结构是主要的,酯中次之,而在酰氯中这种偶极结构很少。
2.羧酸衍生物的物理性质低级酰氯与酸酐是有刺激气味的液体。
高级的为固体。
低级酯具有芳香的气味,存在于水果中,可用作香料。
十四碳以下的甲酯/乙酯均为液体。
酰胺除甲酰胺外,均是固体,只是因为分子中形成氢键,如果氮上的氢逐个被取代,则氢键缔合减少,因此脂肪族的N-取代酰胺常为液体。
酰氯和酯的沸点因分子中没有缔合,比相应的羧酸低,酸酐与酰胺的沸点,比相应的羧酸高。
(乙酰氯bp:51℃乙酸酐bp:140℃乙酸乙酯bp:77℃乙酰胺bp:222℃)酰氯和酸酐不溶于水,低级的遇水分解;酯在水中的溶解度很小;低级的酰胺可溶于水,N,N-二甲基甲酰胺和N,N-二甲基乙酰胺是很好的非质子性溶剂,可与水以任何比例混合。
乙酸乙酯是很好的有机溶剂,大量用于油漆工业。
3.羧酸衍生物的反应1)酰基碳上的亲核取代反应①酰基碳上的亲核取代反应概述基团离去能力的次序是:I- > Br- > Cl- > -OCOOR > -OR > -OH > -NH2(氨基的碱性比氢氧根强)不管是酸催化还是碱催化的机理,羧酸衍生物亲核取代反应性顺序都是:卤酐醛酮(活泼)酯酸胺腈(较稳定)②羧酸衍生物的水解——形成羧酸a)酰卤的水解在羧酸衍生物中,酰卤的水解速率很快,低分子酰卤水解很猛烈,如乙酰氯在湿空气中会发烟,这是因为乙酰氯水解产生盐酸。
羧酸衍生物知识点

羧酸衍生物知识点羧酸衍生物是一类化合物,它们在化学反应和有机合成中有着广泛的应用。
羧酸衍生物的结构中包含一个羧酸基团,它们的化学性质也与羧酸有关。
本文将从羧酸衍生物的性质、合成和应用三个方面进行阐述。
一、羧酸衍生物的性质羧酸衍生物中含有一个羧酸基团(-COOH),这个基团可以参与许多化学反应。
例如,在碱性条件下,羧酸基团会失去一个质子,形成相应的负离子,即羧酸盐,这种反应叫做羧化反应。
除此之外,羧酸衍生物还能与醇、胺等反应,生成相应的酯、酰胺等衍生物。
二、羧酸衍生物的合成羧酸衍生物的合成方法非常多,下面介绍两种常用的方法:1.羧化反应羧化反应是一种重要的合成羧酸衍生物的方法。
在这种反应中,通常使用羧酸和一定量的碱反应,生成相应的羧酸盐。
羧酸盐再与酸反应,失去一个水分子,形成相应的酯。
这种反应常用的催化剂有酸性离子交换树脂、三氧化硫等。
2.加成反应加成反应是另一种合成羧酸衍生物的方法。
在这种反应中,羧酸衍生物的反应物通常是烯烃或炔烃。
它们与羧酸在催化剂的存在下发生加成反应,生成相应的羧酸衍生物。
加成反应的催化剂有酸性离子交换树脂、钯等。
三、羧酸衍生物的应用羧酸衍生物在有机合成、材料科学、生物化学等领域有着广泛的应用。
1.有机合成羧酸衍生物是有机合成中常用的反应物和中间体。
它们可以通过羧化反应、加成反应等多种方法进行合成。
羧酸衍生物可以与醇、胺等反应,生成相应的酯、酰胺等衍生物。
2.材料科学羧酸衍生物可以与金属离子、聚合物等反应,形成新的材料。
例如,聚丙烯酸可以与铁离子反应,生成Fe3O4/聚丙烯酸复合材料。
这种材料具有磁性,可以应用于磁性材料、制备催化剂等领域。
3.生物化学羧酸衍生物在生物化学中也有着重要的应用。
例如,羧酸基团是许多生物分子的一部分,例如脂肪酸、氨基酸等。
羧酸衍生物还可以用于制备生物活性分子,例如药物、抗生素等。
羧酸衍生物是一类重要的化合物,在化学反应和有机合成中有着广泛的应用。
通过羧化反应、加成反应等方法可以合成羧酸衍生物。
第十四章 羧酸衍生物

R—C—X 酰卤
(腈由于与羧酸关系密切故被纳入羧酸衍生物)
2
★命名
1. 酰卤和酰胺根据相应的酰基来命名
O R—C—OH - —OH O R—C— [酰基]
羧酸去掉-OH后剩下的部分叫酰基
O CH3C Cl 乙酰氯
O HCN(CH3)2 N,N-二甲基甲酰胺 (DMF)
O C Br 苯甲酰溴
O
O CH2 CH
化合成的酯,也可将一个低沸点醇的酯转为高沸
点醇的酯。
12
★3. 酰氯、酸酐、酯和酰胺酸解
酰氯、酸酐、酯和酰胺与另一羧酸一起加热, 都得到平衡混合物。
O R C Cl
O O
O C R'
O R' C
O
Cl
O
R C O C R
'R C O C R
O
O R C OR'
O R C NH2
+ HO
O 'R C O OR'
酯水解反应机理: 碱催化(B) 酸催化(A)
H
+
或-OH
O RCOH + HOR´
酰氧断裂(Ac)
烷氧断裂(Al)
单分子 双分子
碱性水解
酸性水解
BAc2:碱性双分子酰氧断裂 AAc2:酸性双分子酰氧断裂
AAc1:酸性单分子酰氧断裂
注意:酯的碱性水解 是不可逆的;碱既是 BAl2: 碱性双分子烷氧断裂 催化剂又是试剂。
O
X
O
HX
O R C NR2'' +
HO O R'
R C O C R' + H NR2''
(二) 羧酸衍生物

Nu-:进攻的亲核试剂,即H2O、ROH、NH3、RNH2或R2NH等。
L-:离去基团,即X、-OOCR 、-OR、-NH2、-NHR或-NR2
总的反应速度和两步反应的速度都有关系,但第一步更为重要。酰基中羰基碳原子是sp2杂化,三个σ键是平面形分布。羰基碳上如果连有吸电子基团,将增加羰基碳的正电性,有利于亲核试剂的进攻;反之,如果连有供电子基团,将不利于亲核试剂的进攻。亲核加成生成的中间体,其碳原子为sp3杂化,即四面体结构。如果原来羰基碳原子上连接的基团过于庞大,在四面体结构中就显得过于拥挤而不利于反应进行。上述电子效应和空间效应都将对第一步的反应速度有所影响。第二步反应易否进行,取决于离去基团L-的碱性,碱性越弱,越易离去。羧酸衍生物各离去基团离去的难易次序为:
在有机合成中酯的还原是使羧酸间接转变为伯醇的重要方法,因为羧酸的还原比酯困难。
14.8.3 α-氢化反应
羧酸衍生物分子中的α-氢由于受羰基影响(σ-π超共轭和吸电诱导效应),比较活泼,与醛酮相似,在一些碱性试剂催化下可以发生缩合反应。在有机合成中酯缩合反应应用较多。
由于酯的α-H酸性小于醛酮,也小于酰氯(但大于酰胺),所以酯缩合用的碱是醇钠或其他碱性催化剂(如氨基钠)而不是氢氧化钠的水溶液。酯在强碱作用下发生分子间的缩合反应,称为(Claisen)酯缩合反应,在制备β-二羰基化合物时很有用。
一般克莱森酯缩合反应是在两个相同的酯之间进行。虽然我们可以进行混合酯的交叉缩合反应,即采用两种不同的酯,但产物太复杂,没有实用价值,除非一个酯有α-氢,一个酯没有α-氢,才有制备意义。例如草酸乙酯、苯甲酸酯、甲酸酯等都是不含α-氢的酯,可用于交叉酯缩合反应。这时产物比较纯。
己二酸酯和庚二酸酯在醇钠作用下主要是发生分子内的酯缩合反应,称为狄克曼(Dieckmann) 缩合反应,生成环状的β-酮酸酯。
第14章__羧酸衍生物

第二节 羧酸衍生物的物性
低级的酰氯和酸酐是有刺鼻气味的液体,高级的为固体; 低级的酯具有芳香的气味,可作为香料;十四碳酸以下 的甲酯和乙酯均为液体; 酰胺除甲酰胺外,由于分子内形成氢键,均是固体; 而当酰胺的氮上有取代基时为液体; 羧酸衍生物可溶于有机溶剂; 酰氯和酸酐不溶于水,低级的遇水分解; 酯在水中溶解度很小; 低级酰胺可溶于水。
碱性水解的讨论
1. 碱性水解速率与 [-OH]成正比。 2. 羰基活性越大,-C空阻越小,酯基空阻越小, 反应速率越快。
CH3COOCMe3 Me3CCOOEt CH3COOEt ClCH2COOEt
V相对
0.002
0.01
1
296
3. 形成的四面体中间体能量越低,反应速度越快。 (能分散负电荷的取代基对反应是有利的) 4. 酯的碱性水解是不可逆的。 5. 碱的用量要超过催化量。
3. 酯的酸性水解和酯化反应互为逆反应,平衡的 移动取决于反应的条件。体系中有大量水存在, 发生酯的水解。若有大量醇存在,并采取去水 措施,则有利于酯化反应。
4. 在RCOOR1中, R对速率的影响是: 一级 > 二级 > 三级 R1对速率的影响是: 三级 > 一级 > 二级 CH3COOR1在盐酸中,于25OC时水解的相对速率v的 实验数据如下: R1: v: CH3 1 C2H5 0.97 CH(CH3)2 0.53 C(CH3)3 1.15(机理不同)
问: 反应条件为什么会各有不同?
亚硝酸在酰胺制酸中的作用 ---空阻大的酰胺水解的方法
O CH3CNH2
O
HNO2
CHCH + N2 3-C-OH 2 + 3COOH
羧酸的衍生物

羧酸的衍生物
工业上,在合成纤维“涤纶”的生产中就利用了酯交换反应。 通过酯交换反应可以从廉价的低级醇来制备高级醇。例如: 酰胺的醇解反应是可逆的,需要过量的醇才能生成酯并释放出氨。
羧酸的衍生物
3. 溶解性
所有羧酸衍生物均能溶于乙醚、氯仿、丙酮、苯等有机 溶剂。酰卤和酸酐遇水就分解,酯在水中的溶解性很低,但 低级的酰胺(如N,N-二甲基甲酰胺)能与水混溶,是优良的 非质子极性溶剂。
部分羧酸衍生物的物理常数列于表11-4。
羧酸的衍生物
表11-4 部分羧酸衍生物的物理常数
羧酸的衍生物
羧酸的衍生物
(2)酸酐的命名
酸酐的名称是由两个羧酸的名称加上“酐”字来命名。相 同羧酸形成的酸酐称为单酐;不同羧酸形成的酸酐称为混酐。 混酐命名时,通常将简单的羧酸写在前面,复杂的羧酸写在 后面。例如:
羧酸的衍生物
(3)酯的命名
酯的名称是由相应的羧酸和醇中的烃基名称组合后加“酯” 字来命名的。例如:
羧酸的衍生物
4. 还原反应
(1)催化加氢
羧酸衍生物在催化加氢条件下都可以被还原,但一般具有制备意 义的是酰卤的选择性还原和酯的还原。
酰卤选择性加氢的催化体系是Pd/BaSO4-硫-喹啉(或硫脲),此 催化体系可使酰卤的加氢反应停止在生成醛的阶段,称为罗森门德 (Rosenmund)反应,这是一种制备醛的方法。
的杂原子(X、O、N)上都具有未共用电子对,它们所占据的p轨道
与羰基的π轨道形成p-π共轭体系,未共用电子对向羰基离域,使C-L
键具有部分双键的性质。因此,羧酸衍生物的C-L键较典型的单键C-L
羧酸衍生物习题

OOIIIICH3CCH2COC2H5第十四章羧酸衍生物练习题OHOIIICH3C=CHCOC2H5与325是什么异构体?一、选择题1.2分(0179)2.3.4. (A)碳干异构(B)位置异构(C)官能团异构(D)互变异构2分(0846)(A)酸2分(4033)有强大爆炸力的三硝基甘油属于下列哪类物质:(B)碱(C)脂(D)酯用⑴CH3CH2MgBr(2)也0处理乙酰乙酸乙酯得到的是:(A)CH3COCH(C2H5)COOEt(C)CH3CH2C(OH)(CH3)CH2COOEt(B)CH3COCH(C2H5)C(OH)(C2H5)2(D)CH3COCH2COOEt2分(0284)尼龙-66是一种聚酰胺,其单体为:(A)己内酰胺(B)己二酸己二胺盐(c)己二酸+尿素(D)丁二酰亚胺5.2分(4101)下列试剂分别同“三乙”作用,哪个作用后,只回收到乙酰乙酸乙酯?(A)Br2(C)①C2H5ONa②CH£H2Br (B)NH2OH(D)①RMgX②电0+6.7.8. 、填空题分(5740)写出下列反应的主要有机产物或所需之原料、试剂(有立体化学请注明)/OOEtCH2+2HOCH2CH2C^—2NaOE^COOEt分(5729)写出下列反应的主要有机产物或所需之原料、试剂(有立体化学请注明)OCOOH电叫?分(5019)写出下列反应的主要有机产物,如有立体化学问题也应注明CH2(COOC2H5)2**?2⑵BrCH2CH2CH2CH2CH2Br'⑶H3+O,,_CO329.2 10. 11. 4分(8254)给出反应的主要产物:12. (5712)写出下列反应的主要产物或所需之试剂(如有立体化学问题请注明)。
OO (CH 3C)2O +HCOH ^?CH 3OH13.(1466) O化合物Cl C Cl 的俗名称是: 14. (5757) 写出下列反应的主要有机产物或所需之原料、试剂(有立体化学请注明HNO /H SO 4 15.(5120) 写出下列反应的主要有机产物,如有立体化学问题,也应注明。
《羧酸衍生物 》课件

羧酸衍生物可以与醇反应,生成酯类物质,常用于酯化反应的有机合成。
3 加成反应
羧酸衍生物可通过加成反应与其他有机物发生化学反应,生成功能化的有机化合物。
羧酸衍生物的应用领域
1
染料领域
2
羧酸衍生物在染料的合成和染色工艺中
起到重要的作用,用于改善染料的染色
性能和稳定性。
3
食品工业
4
羧酸衍生物在食品工业中可以作为调味 剂、增酸剂和防腐剂等添加剂。
医药领域
羧酸衍生物广泛应用于药物研发领域, 用于合成医药品、制药工艺中的反应催 化剂等。
聚合物领域
羧酸衍生物可作为聚合物的功能单体, 用于合成具有特定性能的聚合物材料。
羧酸衍生物的市场前景
市场需求增长 技术创新推动 环境友好性
羧酸衍生物的应用领域广泛,市场需求稳步增长, 尤其是在医药、染料和聚合物等领域。
酯化反应是将羧酸与醇反应生成酯类产物的方法, 常用酯化剂包括酸、酸酐等。
羰基化反应
羰基化反应是将羧酸与羰基化试剂反应生成酮类产 物的方法,常用羰基化试剂包括酰氯、酸酐等。
特殊制备方法
特定的有机化学反应可用于制备特定的羧酸衍生物, 例如将邻羟基苯甲酸酰化得到苯甲酸。
羧酸衍生物的化学性质
1 酸性性质
羧酸衍生物具有酸性,可以与碱发生中和反应,生成相应的盐和水。
随着科学技术的进步,对羧酸衍生物性能的研究 和改良不断推动着羧酸衍生物市场的发展。
羧酸衍生物具有较好的环境友好性,符合环保趋 势,因此在绿色化学领域具有广阔的市场前景。
总结
通过本课件的学习,我们了解了羧酸衍生物的定义、结构特点、制备方法、 化学性质、应用领域以及市场前景。希望这些知识能够对大家有所启发。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
+ H O C R'
O 'R C
O 'R C NH2
+
OR'
30
用途:① 酰氯在吡啶存在下酸解可以制备单酐
O
O
例:Cl
CCl
+ Cl
C5H5N
COH
O Cl C 2 O
+
HCl
96%~98%
酰氯和羧酸盐反应可以制备混合酐:
O R C Cl
O O
+
R'COONa
R C O C R'
O R O R'
13
碱性水解: BAc2:碱性双分子酰氧断裂
O R
O R C 'RO OH
OR'
+
OH
慢
R
O C 'RO OH
快
R
O
+
OH
OR'
O
+
R OH
OR'
快
O
+
R O
HOR'
注意:酯的碱性水解是不可逆的;碱既是催化剂又是试剂。
14
酸性水解:
AAc2:酸性双分子酰氧断裂
O
+
R OR'
OH R
OH R C OR' OH2
H
快
OH R OR'
OH R C OR' OH2
+ H2O
慢
OR'
快
R OH
C OR' + OH
H
15
OH R C OR' OH
+
H
快
R
OH
H C OR'
OH
O H R C OR' H OH
OH R OH
快
R
OH
+
OH
O
HOR'
快
R
+
OH
H
酸在反应中有两个的作用:
① 活化酯中的羰基 羊 盐而更易离去 ② 使OR形成 钅
R'OMgX
O (H)R C R''
O MgX
R''MgX
OH
H2O
(H)R C R'' R''
(H)R C R'' R''
37
O
例:
C OC2H5
1. 2CH3MgI 2. H2O
OH
OH C CH3 CH3
例:
O
1. 2CH3MgI
O
2. H2O
CH3 C CH2CH2CH2OH CH3
38
O
第十五章 羧酸衍生物
第
十
五
章
羧 酸 衍 生 物
一. 羧酸衍生物的结构和命名 二. 羧酸衍生物的反应
三. 其它羧酸衍生物
四. 乙酰乙酸乙酯 五. 丙二酸二乙酯
2
O R OH
羧酸
O O O R'
O
O R OR'
羧 酸 衍 生 物
R
X
R
酰卤
O R NR'R''(H) 酰胺
酸酐
酯
R C N
腈
3
一. 结构和命名 结构:
41
CH2COCl CH2COOCH3
+ H2
O
Pd / BaSO4
CH2CHO CH2COOCH3
Pd / BaSO4
硫脲
O
CH3O C CH2CH2 C Cl + H2
O CH3O C CH2CH2 O
S
C H
喹啉
COCl
H2 , Pd/BaSO4 硫 喹啉
Cl
CHO
Cl
42
O
O
酐: R C O C R'
CH3(CH 2)3CN
Br(CH 2)5CN
乙腈
戊腈
6–溴己腈
11
二. 羧酸衍生物的反应 1. 水解
O R
O R O
HX
X
O R'
O
+ H OH
R
OH
+
O HO R'
O R
O R NR'R ''
OR'
HOR'
HNRR'
12
O
R C N
+ H OH
H2O
NH2
O R OH
R
注意:只有酯和腈的水解用于羧酸的制备。 水解速度:酰卤>酸酐>酯>酰胺 酯的水解反应机理
+ HOCH2CH2OH
O C O COCH2CH2O n
Zn(OAc)2 , Sb2S3
涤纶
22
O CH2 C OCH3
练习: 由 解:
HOOCCH2CH2COOH
制备
CH2
O
C O O
HOOCCH2CH2COOH
O CH2 C OCH3 CH2 C OH O
P2O5
O O
CH3OH
回流
O
三氟乙酐
Mg , 干Et2O
CO2
H2O
CH3CH2CHCH3
H
SOCl2
COOH
NH3
CH3CHCH2CH3 CONH2
29
4. 酸解 酰氯、酐、酯和酰胺与另一羧酸一起加热,都得到平衡
混合物。
O R C Cl
O O R C O C R
O 'R C Cl
O
O
O R C OH
O
'R C O C R
O R C OR'
O
+ CH3 C OH
环酐的氨(胺)解可以得到酰胺酸:
O
O
CH3NH2
O
O C N CH3 C O
27
例:
C C O
C NHCH 3 C OH O
练习1:完成反应
O 1. (CH3)2CCH2CH2COCH3 NH2 CH3OH
O N H
2. O
O + C2H5OH
H
HO(CH2)3COOC2H5
HN(CH3)2
O HO(CH2)3CN(CH3)2
28
练习2:用指定原料及必要的试剂合成
O
1. 从苯合成
CH2CH2CNHCH3
2. 从两个碳化合物合成 CH3CHCH2CH3
CONH2
解: CH3CHO
1. CH3CH2MgBr , 干Et2O
CH3CH2CHCH3
HBr
OH
2. H2O , H
O
CH3
+
CH3
3O2 (空气)
V2O5 400 ℃
O O
③酯
羧酸与醇在酸催化作用下直接酯化 酰卤的醇解
④ 酰胺 酰氯、酸酐的氨(胺)解制备酰胺 铵盐加热失水
34
水解、醇解、氨(胺)解反应机理: 羰基上亲核加成-消去
O
O R C Y+ B 加 成
R
C B
Y
O 消 去
B:亲核试剂
R
C
B+Y
H2O、 ROH、 NH3、 RNH2 、RR’NH
OH
CH2 C OCH3 CH2 C O O
23
Br
练习:实现下列转变
CH2CHCOOC2H5 CH2CH2COOC2H5
CH2CH2COOH CH2CH2COOH
O O
解:
KMnO4, H
(CH3CO)2O CH2CH2C
CH2CH2C O
CH3CH2OH CH2CH2COOC2H5
SOCl2
CH2CH2COOC2H5 CH2CH2COCl
O H N(CH3)2
乙酰胺
甲酰胺
N, N–二甲基甲酰胺 DMF
8
O NH
CH3 CH3CHCH 2
O NHCH 3
己内酰胺
N, 3–二甲基丁酰胺
酸酐: 单酐:在羧酸的名称后加酐字。
混酐: 将简单的酸放前面,复杂的酸放后面,去掉酸
字, 再加酐字。
O CH3 O O CH3
CH3 O O O CH2CH3
反应机理:一般为亲核加成-消除机理
25
用途: ① 酰氯氨(胺)解可以制备酰胺 例:
O C6H5 C Cl
NaOH , H 2O
O C6H5 C N
+
HN
+ HCl
87%~91%
26
② 酸酐的胺解用于胺的酰化
O
例: CH3 C O + H2N
2
CH(CH3)2
O CH3 C HN CH(CH3)2
③ 酯的醇解:生成新的酯和醇,称为酯交换反应,是可
逆
反应。
C11H23 C11H23 C11H23 CO2 CH2 CO2 CH CO2 CH2 + 3CH3OH HO CH2 HO CH + 3C11H23CO2H HO CH2
21
例: 酯交换反应用于工业生产中制备涤纶:
O CH3OC O COCH3
O
1. LiAlH4 2. H2O
RCH 2OH + R'CH2OH
酯: R C OR'
O R C OR'
1. LiAlH4 2. H2O
Na, EtOH
