2018版高考化学大一轮(人教版)复习(课时训练)第三章
2018版高考化学大一轮专题复习课时作业:高考理综(化学)模拟试卷 Word版含答案

2018年高考理综(化学)模拟试卷(一)(时间:50分钟,满分:100分)可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 Al-27 Si-28 S-32 Fe-56 Cu-64第Ⅰ卷一、选择题(本大题共7小题,每小题6分,共42分。
在每小题给出的四个选项中,只有一个选项符合题目要求。
)1.在环境保护、资源利用等与社会可持续发展密切相关的领域,化学发挥着积极作用。
下列做法与此理念相违背的是( )。
A.食品中大量添加苯甲酸钠等防腐剂,可有效延长其保质期B.“地沟油”可以制成肥皂,提高资源的利用率C.加快开发高效洁净能源转换技术,缓解能源危机D.“APEC蓝”是2014年新的网络词汇,形容2014年APEC会议期间北京蓝蓝的天空,说明京津冀实施道路限行和污染企业停工等措施,对减轻雾霾、保证空气质量是有效的2.下列说法正确的是( )。
①标准状况下,6.02×1023个分子所占的体积约是22.4 L②0.5 mol H2所占体积为11.2 L③2 L 0.5 mol·L-1亚硫酸溶液中含有的H+离子数为2N A④标准状况下,28 g CO与N2的混合气体的体积约为22.4 L⑤各种气体的气体摩尔体积都约为22.4 L·mol-1⑥标准状况下,体积相同的气体的分子数相同A.④⑥ B.①③⑤ C.③④⑥ D.①④⑥3.刺囊酸具有滋肝补血、凉血止血功能,其结构如右图所示。
下列关于刺囊酸的说法不正确...的是( )。
A.和氧气催化氧化后产物中含有醛基B.能和NaHCO3溶液反应生成CO2C.能使酸性高锰酸钾溶液褪色D.能发生取代、氧化、加成等反应4.短周期元素X、Y、Z、W、U原子序数依次增大。
X与W位于同一主族,Y、Z形成的氧化物是常见的耐火材料,W原子的最外层电子数是次外层电子数的一半,Z、W、U原子的最外层电子数之和为13。
下列说法正确的是( )。
2018新高考人教版高考化学三轮训练大题练一 Word版含答案

押题练一(时间:30分钟 分值:43分)1.(14分)某研究性学习小组为合成1-丁醇,查阅资料得知一条合成路线:CH 3CH===CH 2+CO +H 2―→CH 3CH 2CH 2CHO ――→H2Ni ,△CH 3CH 2CH 2CH 2OHCO 的制备原理:HCOOH ――→浓硫酸△CO↑+H 2O ,并设计出原料气的制备装置(如图)。
请填写下列空白:(1)实验室现有锌粒、稀硝酸、稀盐酸、浓硫酸、2-丙醇,从中选择合适的试剂制备氢气、丙烯。
写出化学方程式:______________________________________________。
(2)若用以上装置制备干燥纯净的CO ,装置中a 和b 的作用分别是________、________;c 和d 中盛装的试剂分别是________、________。
(3)制丙烯时,还产生少量SO 2、CO 2及水蒸气,该小组用以下试剂检验这四种气体,混合气体通过试剂的顺序是________(填序号)。
①饱和Na 2SO 3溶液 ②酸性KMnO 4溶液 ③石灰水④无水CuSO 4⑤品红溶液(4)合成正丁醛的反应为正向放热的可逆反应,为增大反应速率和提高原料气的转化率,你认为应该采用的适宜反应条件是________。
a .低温、高压、催化剂b .适当的温度、高压、催化剂c .常温、常压、催化剂d .适当的温度、常压、催化剂(5)正丁醛经催化加氢得到含少量正丁醛的1-丁醇粗品,为纯化1-丁醇,该小组查阅文献得知:①R —CHO +NaHSO 3(饱和)―→RCH(OH)SO 3Na↓;②沸点:乙醚 34 ℃,1-丁醇 118 ℃,并设计出如下提纯路线:粗品――→试剂1操作1滤液――→乙醚操作2、分液有机层――→干燥剂过滤1-丁醇、乙醚――→操作3纯品 试剂1为________,操作1为________,操作2为________,操作3为________。
2018版金版教程高考化学一轮总复习学案课件3a课时作业

10
高考一轮总复习 ·化学 (创新版)
解析 溶质的质量分数 w=ρaV×100%,A 错误;氨水 中的溶质是 NH3,而不是 NH3·H2O,将 w=ρaV×100%代入 公式 c=100M0ρw,化简可得 c=11070V0a mol·L-1,B 错误;氨 水中含有的阳离子为 H+和 NH+ 4 ,含有的阴离子只有 OH-, 根据电荷守恒可知 C 正确;由于氨水的密度小于水的密度, 与水等体积混合所得稀氨水的质量大于原氨水质量的 2 倍, 故其质量分数小于 0.5w,D 错误。
4
高考一轮总复习 ·化学 (创新版)
2.在硫酸钠和硫酸铝的混合溶液中,Al3+的物质的量
浓度为 0.2 mol·L-1,SO24-为 0.4 mol·L-1,溶液中 Na+的物
质的量浓度为( )
A.0.1 mol·L-1 B.0.2 mol·L-1
C.0.3 mol·L-1 D.0.4 mol·L-1
解析
由电荷守恒
c(Na+
)+
3c(Al3+
)=
2c(SO
2- 4
),
则
c(Na+)+3×0.2 mol·L-1=2×0.4 mol·L-1,得 c(Na+)=0.2
mol·L-1,故选 B。
5
高考一轮总复习 ·化学 (创新版)
3.4 ℃时,在 100 mL 水中溶解 22.4 L HCl 气体(标准 状况下)形轮总复习 ·化学 (创新版)
【步步高】2018届新人教课标Ⅰ高三化学一轮总复习资料word版:第三章 大题冲关滚动练之二

大题冲关滚动练之二——无机化工流程题1.活性氧化锌用作橡胶硫化的活性剂、补强剂。
以氧化锌粗品为原料制备活性氧化锌的生产工艺流程如下:一些阳离子以氢氧化物形式完全沉淀时溶液的pH见下表:Fe(OH>3(1>“溶解的是____________________________。
(2>“溶解”后得到的酸性溶液中含有Zn2+、SO错误!,另含有Fe2+、Cu2+等杂质。
先加入__________(填“Na2CO3”或“H2SO4”>调节溶液的pH至5.4,然后加入适量KMnO4,Fe2+转化为Fe(OH>3,同时KMnO4转化为MnO2。
经检测溶液中Fe2+的浓度为0.009mol·L-1,则每升溶液中至少应加入________molKMnO4。
(3>杂质Cu2+可利用置换反应除去,应选择的试剂是____________________________。
(4>“沉淀”得到ZnCO3·2Zn(OH>2·H2O,“煅烧”在450~500℃下进行,“煅烧”反应的化学方程式为___________________________________________________。
答案(1>增大固液接触面积,加快溶解时的反应速率(2>Na2CO30.003(3>锌粉(4>ZnCO3·2Zn(OH>2·H2O错误!3ZnO+CO2↑+3H2O↑2.以下是用硫铁矿烧渣(主要成分为Fe2O3、Fe3O4、FeO、SiO2>为原料制备高纯氧化铁的生产流程示意图:回答下列问题:(1>酸浸、过滤后滤液A中的金属阳离子是_________________________________。
(2>煅烧FeCO3生成产品Ⅰ的化学反应方程式为_____________________________。
2018版高考化学一轮总复习(限时训练):第一章第3讲限时训练含解析

限时训练[选题细目表]一、选择题(本题包括7个小题,每小题6分,共42分,每小题仅有一个选项符合题意)1.下列有关摩尔质量的描述或应用中,正确的是( )A.OH-的摩尔质量是17 g·mol-1B.CO2的摩尔质量是44 gC.铁原子的摩尔质量等于铁原子的相对原子质量D.一个钠原子的质量约等于错误!答案:A2.(2016·泉州一模)某气体的摩尔质量为M g·mol-1,N A表示阿伏加德罗常数的值,在一定的温度和压强下,体积为V L的该气体所含有的分子数为X。
则错误!表示的是( )A.V L该气体的质量(以g为单位)B.1 L该气体的密度C.1 mol该气体的体积(以L为单位)D.1 L该气体中所含的分子数解析:错误!是该气体的物质的量,与M相乘是该气体的质量,质量除以V(体积)得气体的密度.答案:B3.(2016·周口模拟)下列叙述不正确的是( )A.CO2的摩尔质量是44 g·mol-1,表示1 mol CO2的质量为44 gB.H2SO4溶液的物质的量浓度为1 mol·L-1,表示1 L溶液中含有1 mol H2SO4C.气体摩尔体积V m≈22。
4 L·mol-1,表示1 mol任何气体的体积都约为22.4 LD.阿伏加德罗常数N A≈6。
02×1023 mol-1,表示1 mol任何粒子集体所含的粒子数约为6.02×1023解析:在标准状况下,1 mol任何气体的体积都约为22。
4 L,故C错误。
答案:C4.(2017·洛阳调研)工业上将氨气和空气的混合气体通过铂—铑合金网发生氨氧化反应,若有标准状况下V L氨气完全反应,并转移n个电子,则阿伏加德罗常数(N A)可表示为()A.11.2n5V B.5V11。
2nC.错误!D。
错误!解析:根据反应4NH3+5O2错误!4NO+6H2O,当有标准状况下V L NH3完全反应时,NH3的物质的量为错误!mol,转移电子的物质的量为错误!mol,已知在此反应中转移电子数为n,则n=错误!×N A,所以,N A=错误!。
【步步高】2018届新人教课标Ⅰ高三化学一轮总复习资料word版:第三章 排查落实练五
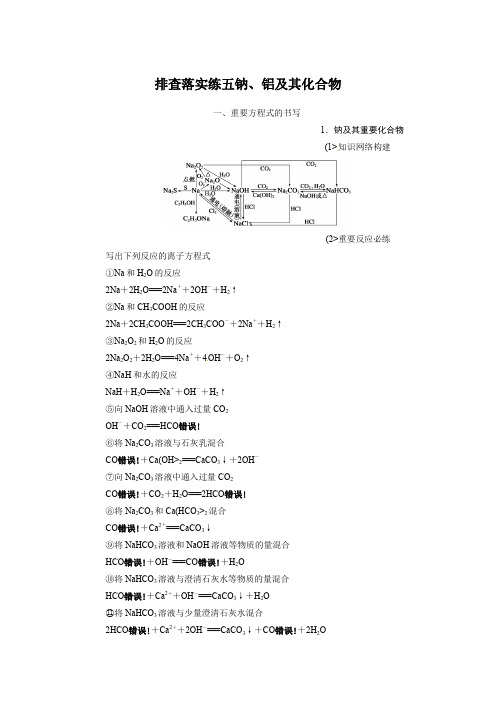
排查落实练五钠、铝及其化合物一、重要方程式的书写1.钠及其重要化合物(1>知识网络构建(2>重要反应必练写出下列反应的离子方程式①Na和H2O的反应2Na+2H2O===2Na++2OH-+H2↑②Na和CH3COOH的反应2Na+2CH3COOH===2CH3COO-+2Na++H2↑③Na2O2和H2O的反应2Na2O2+2H2O===4Na++4OH-+O2↑④NaH和水的反应NaH+H2O===Na++OH-+H2↑⑤向NaOH溶液中通入过量CO2OH-+CO2===HCO错误!⑥将Na2CO3溶液与石灰乳混合CO错误!+Ca(OH>2===CaCO3↓+2OH-⑦向Na2CO3溶液中通入过量CO2CO错误!+CO2+H2O===2HCO错误!⑧将Na2CO3和Ca(HCO3>2混合CO错误!+Ca2+===CaCO3↓⑨将NaHCO3溶液和NaOH溶液等物质的量混合HCO错误!+OH-===CO错误!+H2O⑩将NaHCO3溶液与澄清石灰水等物质的量混合HCO错误!+Ca2++OH-===CaCO3↓+H2O⑪将NaHCO3溶液与少量澄清石灰水混合2HCO错误!+Ca2++2OH-===CaCO3↓+CO错误!+2H2O⑫向饱和Na2CO3溶液中通入过量CO2气体2Na++CO错误!+CO2+H2O===2NaHCO3↓2.铝及其重要化合物(1>知识网络构建(2>重要反应必练写出下列反应的离子方程式①Al和NaOH溶液的反应2Al+2OH-+2H2O===2AlO错误!+3H2↑②Al(OH>3和NaOH溶液的反应Al(OH>3+OH-===AlO错误!+2H2O③Al(OH>3和盐酸的反应Al(OH>3+3H+===Al3++3H2O④Al2O3和NaOH的反应Al2O3+2OH-===2AlO错误!+H2O⑤Al2O3和盐酸的反应Al2O3+6H+===2Al3++3H2O⑥NaAlO2和过量盐酸的反应AlO错误!+4H+===Al3++2H2O⑦向NaAlO2溶液中通入过量CO2气体AlO错误!+CO2+2H2O===Al(OH>3↓+HCO错误!⑧将NaAlO2与NaHCO3混合AlO错误!+HCO错误!+H2O===Al(OH>3↓+CO错误!⑨将NaAlO2与AlCl3溶液混合3AlO错误!+Al3++6H2O===4Al(OH>3↓⑩向AlCl3溶液中加入过量NaOH溶液Al3++4OH-===AlO错误!+2H2O⑪向AlCl3溶液加入过量氨水Al3++3NH3·H2O===Al(OH>3↓+3NH错误!⑫将AlCl3溶液与NaHCO3溶液混合Al3++3HCO错误!===Al(OH>3↓+3CO2↑二、值得强化记忆的实验现象1.Na和水反应的实验现象答案Na浮在水面上,四处游动,发出“嘶嘶”的响声,并熔化成光亮的小球,最后小球完全消失,滴入酚酞试液,立即变红。
2018届高考化学一轮复习考情分析检测:第3章 金属及其化合物3-4 含解析

时间:45分钟满分:100分一、选择题(每题6分,共66分)1.[2017·山东潍坊高三联考]我国晋代《抱朴子》中描述了大量的化学反应,其中有:①“丹砂(HgS)烧之成水银,积变又还成丹砂”;②“以曾青涂铁,铁赤色如铜”。
下列有关叙述正确的是 ( )A .①中描述的化学反应是可逆反应B .“曾青”是含有Cu 2+的溶液,如硫酸铜溶液C .“积变又还成丹砂”中的“还”可理解为“被还原”D .水银能跟曾青发生置换反应生成单质铜 答案 B解析 ①中描述的化学反应为HgS=====△Hg +S 、Hg +S===HgS ,两个反应的反应条件不同,不是可逆反应,A 项错误;“铁赤色如铜”,说明铁置换出铜,故“曾青”应为可溶性铜盐的水溶液,B 项正确;“积变又还成丹砂”,发生的反应是Hg +S===HgS ,Hg 发生了氧化反应,“还”是指恢复原来的状态,C 项错误;Hg 的活动性比Cu 弱,因此水银不能与曾青发生置换反应生成单质铜,D 项错误。
2.[2016·石家庄模拟]下列关于金属的冶炼方法叙述不正确的是( )解析 用电解熔融NaCl 来制取金属钠,电解饱和NaCl 溶液得到的是NaOH、H2和Cl2。
3.[2017·兰州一中高三月考]如图所示的反应均是在高温引燃后进行,选项中的物质表示A和B,不合理的是( )A.MgO Al B.CO2MgC.Fe3O4Al D.CuO H2答案 A解析Mg的活泼性强于Al,若A为MgO,B为Al,二者不能发生铝热反应,A项错误;CO2与Mg反应生成C(即C)和MgO(即D),Mg 与O2反应生成MgO,C与足量O2反应生成CO2,B项正确;Fe3O4与Al 能发生铝热反应,生成Fe(即C)和Al2O3(即D),C项正确;H2还原CuO 生成Cu(即C)和H2O(即D),D项正确。
4.[2017·大连二十四中测试]人们习惯上把金、银、铜、铁、锡五种金属统称为“五金”。
全程复习构想2018高考化学一轮复习 第三章 金属及其化合物 3 铁及其化合物课时作业 新人教版

铁及其化合物[基础题组]1.(2017·北京模拟)下列说法正确的是( )A.铁是位于第四周期ⅦB族元素,是一种重要的过渡元素B.四氧化三铁是氧化铁和氧化亚铁组成的混合物C.14 g铁粉和7 g硫粉混合后高温下充分反应能生成21 g硫化亚铁D.铁在溴蒸气中点燃可生成FeBr3答案:D2.(2017·西安调研)一定条件下,下列物质可通过化合反应制得的共有( )①小苏打②硫酸铝③氯化亚铁④磁性氧化铁⑤氢氧化铜⑥氢氧化铁A.3种B.4种C.5种 D.6种解析:①Na2CO3+H2O+CO2===2NaHCO3,属于化合反应;③2FeCl3+Fe===3FeCl2,属于化合反应;④Fe与O2在点燃条件下生成Fe3O4,是化合反应;⑥4Fe(OH)2+O2+2H2O===4Fe(OH)3,是化合反应。
答案:B3.下列叙述正确的是( )A.Fe与稀HNO3、稀H2SO4反应均有气泡产生,说明Fe与两种酸均发生置换反应B.足量的Fe在Cl2中燃烧生成FeCl2和FeCl3C.Fe和Fe2O3等物质的量混合物溶于稀盐酸时无气体放出D.在FeCl3溶液中加入KHCO3溶液,会有CO2产生,但无Fe(OH)3沉淀生成解析:HNO3具有强氧化性,与Fe反应产生的气体为NO,A项错;铁与Cl2反应无论量的多少产物都是FeCl3,B项错;C项中Fe2O3溶解产生Fe3+恰好将铁单质氧化,因而不能置换出H2,正确;Fe3+与HCO-3会发生水解相互促进反应,有CO2和Fe(OH)3沉淀生成,D项错。
答案:C4.(2017·扬州模拟)下列关于Fe3+、Fe2+性质实验的说法错误的是( )A.用如图装置可以制备沉淀Fe(OH)2B.配制FeCl3溶液时,先将氯化铁晶体溶于较浓的盐酸中,再加水稀释到所需要的浓度C.向某溶液中滴加KSCN溶液,溶液不变色,滴加氯水后溶液显红色,此现象不能确定溶液中含有Fe2+D.向FeCl2溶液中加入少量铁粉是为了防止Fe2+被氧化解析:A、C、D三项中的氧化剂虽均能使Fe2+氧化为Fe3+,但同时会引入新的杂质,故此三项不符合题意;双氧水具有氧化性,能氧化亚铁离子为铁离子,还原产物为水,不引入新杂质,故选B。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
课时2 镁、铝及其重要化合物课时跟踪训练一、选择题1.(基础题)下列说法正确的是()A.铝罐可久盛食醋B.焰火的五彩缤纷是某些金属元素化学性质的展现C.氧化铝熔点很高,可作耐火材料D.明矾作净水剂,可以除去废水中的铜离子解析铝罐的主要成分铝可与醋酸反应,故铝罐不能久盛食醋,A项错误;焰火的五彩缤纷是因为某些金属元素的焰色反应,焰色反应是金属元素的物理性质,B项错误;氧化铝熔点很高,可用于制耐火砖、耐火坩埚、耐火管、耐高温实验仪器,C项正确;明矾净水利用的是Al(OH)3胶体的吸附性,其可吸附水中不溶于水的杂质形成沉淀,从而起到净水的作用,D项错误。
答案 C2.(2017·厦门模拟)镁铝性质相似,下表中对两者的对比不正确的是()3.多年前,世界卫生组织把铝确定为食品的污染源之一而加以控制使用。
铝在下列应用中应加以控制的是()①制铝合金②制电线③制炊具④制银色漆颜料⑤用明矾净水⑥用明矾与苏打作食品膨松剂⑦制易拉罐⑧用氢氧化铝凝胶制胃舒平药品⑨包装糖果和食品A.③⑤⑧⑨B.②⑥⑧⑨C.③④⑤⑨D.③⑤⑥⑦⑧⑨解析解答本题时,要抓住题中的“把铝确定为食品的污染源之一”与“控制使用”。
D项符合题意。
答案 D4.易拉罐的主要成分为铝合金,其中以铝铁合金和铝镁合金最为常见。
现取几小块易拉罐碎片进行下列实验,其中实验方案与现象、结论正确的是()金属的结论,A错误;铝、铁、镁三种金属中只有铝能与NaOH溶液反应产生无色气体,B错误;氢氧化镁与氢氧化铝均为白色沉淀,C错误;用盐酸溶解后生成的亚铁离子在空气中易被氧化成Fe3+,加入KSCN溶液呈红色,D正确。
答案 D5.下列叙述正确的是()A.向氯化铝溶液中加入过量氨水反应的实质是Al3++3NH3·3H2O=== Al(OH)3↓+3NH+4B.存在于污水中的重金属离子,常用加入明矾等电解质的方法进行处理C.镁铝合金既可完全溶于过量盐酸又可完全溶于过量NaOH溶液D.依据铝热反应原理,能发生反应2Al+3MgO高温,3Mg+Al2O3解析B项中明矾只能使污水中的悬浮物沉降,不能除去重金属离子;C项中Mg不能溶于NaOH溶液;D项中Mg的金属性比Al强,故Al与MgO不能发生铝热反应。
答案 A6.下列由实验现象得出正确结论的是()是与碱反应,故A 错误;没有脱落表明氧化铝的熔点高,故B 错误;氯化铵溶液显酸性,与铝反应时放出氢气,故C 错误;氯化铝和氢氧化钠溶液反应先生成氢氧化铝白色沉淀,氢氧化铝再和氢氧化钠溶液反应生成可溶性的偏铝酸钠,故D 正确。
答案 D7.(2017·广西调研)某工厂用提取粗盐后的盐卤(主要成分为MgCl 2)制备金属镁,其工艺流程如下。
盐卤――→足量的石灰浆操作①Mg (OH )2――→适量盐酸MgCl 2溶液――→ 操作②MgCl 2·6H 2O ――→HCl 气流操作③MgCl 2――→电解操作④Mg 下列说法错误的是( )A .在实验室实施操作①需要的玻璃仪器是漏斗、烧杯、玻璃棒B .Mg(OH)2―→MgCl 2的离子方程式为:Mg(OH)2+2H +===Mg 2++2H 2OC .操作②是将MgCl 2溶液蒸干后冷却结晶D .操作④阴极和阳极产物的质量比是24∶71解析 操作①为过滤,A 项正确;Mg(OH)2→MgCl 2为中和反应,B 项正确;由MgCl 2溶液获得氯化镁晶体不能用加热蒸干的方法,因为加热促进Mg 2+水解,生成的盐酸易挥发,导致水解彻底,蒸干后不能得到氯化镁晶体,C 项错误;操作④为电解熔融的氯化镁,阳极得到Cl 2,阴极得到金属Mg ,D 项正确。
答案 C8.(2017·北京海淀区期末)铝自然形成的氧化膜易脱落。
以硫酸为电解液,分别以石墨和铝材作阴、阳极材料,经过电解处理形成氧化铝膜,抗蚀能力强。
其制备的简要流程如图所示。
下列用来解释流程中反应的方程式不正确的是( )A.碱洗目的是除去铝材表面的自然氧化膜:2OH-+Al2O3===2AlO-2+H2O B.碱洗时铝材表面会出现气泡:2Al+2OH-+2H2O===2AlO-2+3H2↑C.获得耐蚀铝材的电极反应:4Al-12e-+3O2===2Al2O3D.用稀氨水洗去耐蚀铝材表面的酸:NH3·H2O+H+===NH+4+H2O解析A.氧化铝能够溶于氢氧化钠,离子方程式为2OH-+Al2O3===2AlO-2+H2O,正确;B.铝能够与氢氧化钠反应放出氢气,离子方程式为:2Al+2OH-+2H2O===2AlO-2+3H2↑,正确;C.电极反应方程式也要满足电荷守恒,4Al-12e -+3O2===2Al2O3,电荷不守恒,错误;D.氨水是弱电解质,用化学式表示,离子方程式为NH3·H2O+H+===NH+4+H2O,D正确;故选C。
答案 C9.某校化学兴趣小组用如图所示过程除去AlCl3溶液中含有的Mg2+、K+杂质离子并尽可能减少AlCl3的损失。
下列说法正确的是()A.NaOH溶液可以用氨水来代替B.溶液a中含有Al3+、K+、Cl-、Na+、OH-C.溶液b中只含有NaClD.向溶液a中滴加盐酸需控制溶液的pH解析A项,氨水也沉淀Al3+,不能代替NaOH溶液;B项,a中不含Al3+;C 项,b也含有KCl。
答案 D10.现有Al、Cl2、Al2O3、HCl(aq)、Al(OH)3、NaOH(aq)六种物质,它们之间有如图所示转化关系,图中每条线两端的物质之间都可以发生反应,下列推断中不合理的是()A .N 一定是HCl(aq)B .X 可能为Al 或Cl 2C .Y 一定为NaOH(aq)D .Q 、Z 中的一种必定为Al 2O 3解析 在Al 、Cl 2、Al 2O 3、HCl(aq)、Al(OH)3、NaOH(aq)中,只有NaOH(aq)能与Al 、Cl 2、Al 2O 3、HCl(aq)、Al(OH)3五种物质反应,对照图示转化关系,可知Y 为NaOH(aq)。
只有HCl(aq)能与Al 、Al 2O 3、Al(OH)3、NaOH(aq)四种物质反应,对照图示转化关系可知N 为HCl(aq),故选项A 、C 正确;选项B ,若X 为Al ,Al 能与Cl 2、HCl(aq)、NaOH(aq)三种物质反应,而图示给出的是与两种物质反应,所以X 不可能是Al ,但可能是Cl 2;选项D ,Al 2O 3既能与HCl(aq)反应,也能与NaOH(aq)反应,故Q 、Z 中的一种必定为Al 2O 3。
答案 B11.铝土矿的主要成分中含有氧化铝、氧化铁和二氧化硅等,工业上经过下列工艺可以冶炼金属铝。
下列说法错误的是( ) 铝土矿――→盐酸①a ――→过量NaOH ②b ――→③c ――→④d ――→电解Al A .①中还需要进行过滤操作,滤渣为二氧化硅B .a 、b 中铝元素的存在形式不同C .③中需要通入过量的氨气D .④进行的操作是加热,而且d 一定是氧化铝解析 铝土矿加盐酸生成Al 3+和Fe 3+,二氧化硅不溶于盐酸,所以要过滤、分离出二氧化硅;滤液中加过量NaOH ,Al 3+转化为AlO -2、Fe 3+转化为Fe(OH)3沉淀,过滤除去Fe(OH)3沉淀,向滤液中通入过量的二氧化碳,生成Al(OH)3沉淀,Al(OH)3分解生成Al 2O 3,最后电解熔融的Al 2O 3生成Al 。
由以上分析可知①、②中除加试剂外,还需要进行过滤操作,故A 正确;a 中为Al 3+,b 中为AlO -2,故B 正确;③中需要把AlO -2转化为Al(OH)3沉淀,要通入过量的二氧化碳,AlO -2+CO 2+2H 2O===Al(OH)3↓+HCO -3,故C 错误;根据上面分析可知④是Al(OH)3受热分解生成Al 2O 3,故D 正确。
答案 C12.向等物质的量浓度的HCl 、AlCl 3、NH 4Cl 、MgCl 2混合溶液中逐滴加入1 mol·L-1的NaOH 溶液,生成沉淀的物质的量与加入NaOH 溶液的体积关系如图所示。
下列有关说法正确的是( )A.在0~a段加入的NaOH溶液与NH4Cl反应B.在b~c段加入NaOH溶液发生反应的离子方程式为Al3++3OH-===Al(OH)3↓C.在d~e段加入NaOH溶液发生反应的离子方程式为Al3++4OH-===AlO-2+2H2OD.在滴加NaOH溶液全过程中主要粒子参与反应的先后顺序是H+、Al3+、Mg2+、NH+4、Al(OH)3解析A项错误,加入的NaOH溶液应先与H+反应;B项错误,由图像中耗用NaOH溶液的体积可知,在b~c段加入NaOH溶液发生反应的离子方程式为Mg2++2OH-===Mg(OH)2↓;C项错误,在d~e段加入NaOH溶液发生反应的离子方程式为Al(OH)3+OH-===AlO-2+2H2O;D项正确。
答案 D二、填空题13.利用铝灰(主要成分为Al、Al2O3、AlN、FeO等)制备铝鞣剂[主要成分为Al(OH)2Cl]的一种工艺如下:(1)气体A能使湿润的红色石蕊试纸变蓝。
铝灰在90 ℃水解生成A的化学方程式为_________________________________________。
“水解”采用90 ℃而不在室温下进行的原因是______________________________________________________________________________。
(2)“酸溶”时,Al2O3发生反应的离子方程式为__________________________________________________________________________________。
(3)“氧化”时,发生反应的离子方程式为____________________________________________________________________________________。
(4)“废渣”成分为________(填化学式)。
(5)采用喷雾干燥而不用蒸发的原因是____________________________________________________________________________________。
答案 (1)AlN +3H 2O=====90 ℃Al(OH)3+NH 3↑ 加快AlN 水解反应速率;降低NH 3在水中的溶解度,促使NH 3逸出(2)Al 2O 3+6H +===2Al 3++3H 2O(3)2Fe 2++2H ++ClO -===2Fe 3++Cl -+H 2O(4)Fe(OH)3(5)防止Al(OH)2Cl 水解生成Al(OH)314.氯化铝融盐电解法是以氯化铝为原料,以碱金属或碱土金属氯化物(含少量MgCl 2、KCl 、CaCl 2)为电解质进行电解制取铝的方法。
