高考化学复习1989年
1989年上海市高考化学试题和参考答案

1989年上海市高考化学试题可能用到的数据原子量H 1 He 4 Li 7 C 12 N 14 O 16 F 19Ne20 Na 23 Mg 24 Al 27 P 31 S 32 Cl 35.5K 39 Ca 40 Fe 56 Cu Ag 108对数值lg2=0.301 lg3=0.477 lg5=0.699一、选择题(本题共52 分)将正确答案的序号填入题后的括号内,第1~16 小题只有一个正确答案,第17~26 小题各有一个或两个正确答案。
只有一个正确答案的,多选不给分。
有两个正确答案的,选对一个给2 分,选错一个倒扣1 分,但每小题不出现负分。
1.芒硝的分子式是()A、NaNO3B、Na2SO4·10H2OC、Na2CO3·10H2OD、Na2SO42.用石灰软化含Mg(HCO3)2的硬水时,产生的沉淀是()A. CaCO3B. MgCO3C. MgCO3和CaCO3D. Mg(OH)2和CaCO33.下列离子或分子中,不能与金属镁反应的是()A.H+B.OH-C.N2D.CO24.下列物质中,含有非极性共价键的离子化合物是()A. Na2O2B. NaOHC. H2O2D. NH3·H2O 5.某原子最外电子排布是ns2,该元素()A.是ⅡA 族元素B.是金属C.是非金属D.无法确定属哪一类6.下列四个反应:①氨气与氯化氢混合产生白烟;②硫化氢与二氧化硫混合生成黄色固体;③乙醇和乙酸反应生成乙酸乙酯;④CH3COO-和H+结合成CH3COOH,其中属于化合反应的是()A. ①B. ①②C. ①②③D. ①④7.下列各组物质混合后能发生反应,但无明显现象的是()A. Na2SO4溶液与盐酸B. 过量CO2与石灰水C. NaOH 溶液与NaAlO2溶液D. NaOH 溶液与NaHCO3溶液8.下列各组离子中,因发生氧化还原反应而不能大量共存的是()A. H+、Na+、S2O32 、Cl-B. Fe3+、Fe2+、SO42-、NO3-C. Na+、OH-、SO42-、HPO42-D.D. Cu2+、Na+、S2-、SO42-9.下列叙述正确的是()A.相同质量的甲醛和乙烷,在任何条件下含有的分子个数一定相同B.等物质量的不同物质,在同温同压下占有相同的体积C.甲气体的相对分子质量比乙气体的相对分子质量大,则甲气体的密度也一定比乙气体的密度大D.等体积、等物质的量浓度的酸溶液,其c(H+)必然相同10. V mL Al2 (SO4)3溶液中含Al3+ a g,取V mL 溶液稀释到4V mL,则稀释后溶液中SO42-物质的量浓度为()A. 125a9Vmol/L B.125a18Vmol/L C.125a36Vmol/L D.125a54V11.有甲、乙、丙三瓶等体积等物质的量浓度的NaOH 溶液,若将甲蒸发一半水,在乙中通入少量CO2,丙不变。
高考化学复习资料大全

高中化学必背知识点归纳与总结一、俗名无机部分:纯碱、苏打Na2CO3、天然碱、口碱:Na2CO3小苏打:NaHCO3大苏打:Na2S2O3石膏(生石膏):CaSO4.2H2O 熟石膏:2CaSO4·.H2O 莹石:CaF2重晶石:BaSO4(无毒)碳铵:NH4HCO3 石灰石、大理石:CaCO3生石灰:CaO 食盐:NaCl 熟石灰、消石灰:Ca(OH)2芒硝:Na2SO4·7H2O (缓泻剂) 烧碱、火碱、苛性钠:NaOH 绿矾:FaSO4·7H2O 干冰:CO2明矾:KAl (SO4)2·12H2O 漂白粉:Ca (ClO)2、CaCl2(混和物)泻盐:MgSO4·7H2O 胆矾、蓝矾:CuSO4·5H2O 双氧水:H2O2皓矾:ZnSO4·7H2O 硅石、石英:SiO2刚玉:Al2O3 水玻璃、泡花碱、矿物胶:Na2SiO3铁红、铁矿:Fe2O3磁铁矿:Fe3O4黄铁矿、硫铁矿:FeS2铜绿、孔雀石:Cu2 (OH)2CO3菱铁矿:FeCO3赤铜矿:Cu2O 波尔多液:Ca (OH)2和CuSO4石硫合剂:Ca (OH)2和S 玻璃的主要成分:Na2SiO3、CaSiO3、SiO2过磷酸钙(主要成分):Ca (H2PO4)2和CaSO4重过磷酸钙(主要成分):Ca (H2PO4)2天然气、沼气、坑气(主要成分):CH4水煤气:CO和H2硫酸亚铁铵(淡蓝绿色):Fe (NH4)2 (SO4)2溶于水后呈淡绿色光化学烟雾:NO2在光照下产生的一种有毒气体王水:浓HNO3:浓HCl按体积比1:3混合而成。
铝热剂:Al + Fe2O3或其它氧化物。
尿素:CO(NH2) 2有机部分:氯仿:CHCl3电石:CaC2电石气:C2H2 (乙炔) TNT:三硝基甲苯氟氯烃:是良好的制冷剂,有毒,但破坏O3层。
酒精、乙醇:C2H5OH裂解气成分(石油裂化):烯烃、烷烃、炔烃、H2S、CO2、CO等。
1989年高考化学试题和参考答案

1989年高考化学试题和参考答案可能用到的数据原子量 H 1 He 4 C 12 N 14 O 16 Na 23Mg 24 Al 27 P 31 S 32 Cl 35.5 Ar 40Cu 63.5 Ag 108一、二、三题都是选择题,每题各有一个或两个正确答案。
试将每题正确答案的编号(A 、B 、C 、D)填入括号内.如果试题只有一个正确答案,选多个者不给分;如果试题有两个正确答案,只选一个答案或选了一个正确答案和一个错误答案或选了多于两个答案者,都不给分.一、选择题(每题1分,共12分)1、下列物质中,属于高分子化合物的是( )(A)淀粉 (B)油脂 (C)棉花 (D)蔗糖2、下列盛放物质的方法,错误的是( )(A)把汽油放在带橡皮塞的玻璃瓶中 (B)把硝酸银溶液放在棕色玻璃瓶中(C)把氢氧化钠溶液放在带橡皮塞的玻璃瓶中 (D)把氢氟酸放在玻璃瓶中3、只能用排水集气法收集的气体是( )(A)H 2 (B)NO (C)CH 4 (D)C 3H 84、现有5种气体:①H 2、②NO 2、③SO 2、④CO 2、⑤H 2S,在实验室里能用启普发生器来制取的是( )(A)①、④、⑤ (B)②、④、⑤ (C)①、②、④ (D)①、③、⑤5、在允许加热的条件下,只用一种试剂就可以鉴别硫酸铵、氯化钾、氯化镁、硫酸铝和硫酸铁溶液,这种试剂是( )(A)AgNO 3 (B)BaCl 2 (C)NaOH (D)NH 3·H 2O6、等摩尔的氢气和氦气在同温同压下具有相同的( )(A)原子数 (B)体积 (C)质子数 (D)质量7、下列溶液中的[Cl -]与50毫升1摩尔/升氯化铝溶液中的[Cl -]相等的是( )(A)150毫升1摩尔/升氯化钠(B)75毫升2摩尔/升氯化铵 (C)150毫升3摩尔/升氯化钾 (D)75毫升1摩尔/升氯化铝8、X 和Y 两元素的阳离子具有相同的电子层结构,X 元素的阳离子半径大于Y 元素的阳离子半径;Z 和Y 两元素的原子核外电子层数相同,Z 元素的原子半径小于Y 元素的原子半径.X 、Y 、Z 三种元素原子序数的关系是( )(A)X>Y>Z (B)Y>X>Z (C)Z>X>Y (D)Z>Y>X9、与OH -具有相同质子数和电子数的微粒是( ) (A )F - (B)Cl - (C)NH 3 (D)NH 2-10、90℃时水的离子积K W =3.8×10-13,该温度时纯水的pH 值( )(A)等于7 (B)小于7 (C)大于7 (D)无法确定11、下列说法正确的是( )(A)二氧化硅溶于水显酸性(B)二氧化碳通入水玻璃可以得到原硅酸(C)因为高温时二氧化硅与碳酸钠反应放出二氧化碳,所以硅酸的酸性比碳酸强(D)二氧化硅是酸性氧化物,它不溶于任何酸12、下列说法错误的是( )(A)石油中含有C 5—C 11的烷烃,可以通过石油的分馏得到汽油(B)含C18以上烷烃的重油经过催化裂化可以得到汽油(C)煤是由有机物和无机物组成的复杂的混和物(D)煤中含有苯和甲苯,可以用先干馏后分馏的方法把它们分离出来参考答案:1.A、C2.A、D3.B4.A5.C6.B、C7.C、D8.D9.A、D 10.B 11.B 12.D二、选择题(每题2分,共28分)13、下列反应中,气体反应物只能作还原剂的是()(A)氯气通入石灰水(B)二氧化碳通入苯酚钠的水溶液(C)一氧化氮与硝酸反应生成三氧化二氮和水(D)二氧化氮与水反应14、pH值和体积都相同的醋酸和硫酸,分别跟足量的碳酸钠溶液反应,在相同条件下,放出二氧化碳气体的体积是()(A)一样多(B)醋酸比硫酸多(C)硫酸比醋酸多(D)无法比较15、在100毫升0.1摩尔/升醋酸溶液中,欲使醋酸的电离度和溶液的pH值都增大,可以采用的方法是()(A)加少量1摩尔/升氢氧化钠溶液(B)加少量1摩尔/升盐酸(C)加100毫升水(D)加热16、已知下列两个热化学方程式2H2(气)+O2(气)=2H2O(液)+571.6千焦C3H8(气)+5O2(气)=3CO2(气)+4H2O(液)+2220.0千焦实验测得氢气和丙烷和混和气体共5摩尔完全燃烧时放热3847千焦,则混和气体中氢气与丙烷的体积比是()(A)1:3 (B)3:1 (C)1:4 (D)1:117、99毫升0.5摩尔/升硫酸跟101毫升/升氢氧钠化溶液混和后,溶液的pH值为()(A)0.4 (B)2 (C)12 (D)13.618、下列数量的各物质所含原子个数按由大到小的顺序排列的是()①0.5摩尔氨气②标准状况下22.4升氦③4℃时9毫升水④0.2摩尔磷酸钠(A)①④②③(B)④③②①(C)②③④①(D)①④②③19、在强酸性溶液中能大量共存、并且溶液为无色透明的离子组是()20、某离子X2+的最外层电了排布是5s2.当把固体XCl2溶于水配制成溶液时,需加入少量的单质X和盐酸.由此判断下列说法正确的是(A)X元素常见的化合价是+2和+4 (B)X(OH)2是强碱(C)XCl2溶液显酸性(D)X元素的最高价氧化物的水化物显强酸性21、下列事实中不能应用勒沙特列原理来解释的是()(A)往硫化氢水溶液中加碱有利于S2-的增多(B)加入催化剂有利于氨氧化的反应(C)高压有利于合成氨的反应(D)500℃左右比室温更有利于合成氨的反应22、下图容器中盛有海水,铁在其中被腐蚀时由快到慢的顺序是( )(A)4>2>1>3 (B)2>1>3>4 (C)4>2>3>1 (D)3>2>4>123、下列离子方程式正确的是( )24、乙烯的丙烯按1:1(摩尔)聚合时,生成聚合物乙丙树脂,该聚合物的结构式可能是( )25、下列有机反应的化学方程式正确的是( )(A)CH 3CH 2OH ()−−−−→−C140浓硫酸CH 2=CH 2+H 2O (B)CH 3CH 2Br+CH 3CH 2OH+NaOH →CH 3CH 2OCH 2CH 3+NaBr+H 2O(C)CH 2=CHCH=CH 2+Br 2→BrCH 2CHBrCHBrCH 2和BrCH 2CHBr=CHCHBr(即两种物质都有)(D)CH 3CH 2COOH+CH 3CH 2CH 2OH −−→−NaOH CH 3CH 2COOCH 2CH 2CH 3+H 2O26、X 、Y 、Z 三种元素的原子,其最外电子层排布分别为ns 1、3s 23p 1和2s 22p 4,由这三种元素组成的化合物的分子式可能是( )(A)XYZ 2 (B)XYZ 3 (C)X 2YZ 2 (D)X 3YZ 3参考答案:13.C14.B 15.A 、C 16.B 17.C 18.A19.A 20.A 、C 21.B 、D 22.A 23.D 24.A 、B25.C26.A 、D 三、选择题(每题3分,共15分) 27、体积为V 毫升、密度为d 克/厘米3的溶液,含有分子量为M 的溶质m 克,其摩尔浓度为C 摩尔/升,质量百分比浓度为W%.下列表示式中正确的是( )28、在273℃和1.01×105帕斯卡条件下, 将1.40克氮气、1.60克氧气和4.00克氩气混和,该混和气体的体积是( )(A)3.36升 (B)6.72升 (C)8.96升 (D)4.48升29、具有如下电子层结构的原子,其相应元素一定属于同一主族的是( )(A)3p 亚层上有2个未成对电子的原子和4p 亚层上有2个未成对电子的原子(B)3p 亚层上只有1个空轨道的原子和4p 亚层上只有1个空轨道的原子(C)最外层电子排布为1S 2的原子和最外层电子排 布为2S 2P 6的原子(D)最外层电子排布为1S 2的原子和最外层电子排 布为2S 2的原子30、右图表示外界条件(温度、压力)的变化对下列反应的影响L(固)+G(气) 2R(气)-热在图中,Y 轴是指( )(A)平衡混和气中R 的百分含量 (B)平衡混和气中G 的百分含量(C)G 的转化率 (D)L 的转化率31、一定条件下,将等体积NO 和O 2 的混和气体置于试管中,并将试管倒立于水槽中,充分反应后剩余气体的体积约为原总体积的( ) (A)41(B)43(C)81(D)83参考答案:27.B 、D 28.C 29.B 、C 30.B 31.C四、(本题共14分)32、下列有机化合物中,有的有多个官能团:(1)可以看作醇类的是(填入编号) ;(2)可以看作酚类的是 ;(3)可以看出羧酸类的是 ;(4)可以看出酯类的是 .33、一氯丁烯(C 4H 7Cl)的同分异构体只有8种,某学生却写了如下10种:其中,两两等同的式子是和, 和。
最好的高考化学复习资料

最好的高考化学复习资料1、SO2能作漂白剂。
SO2虽然能漂白一般的有机物,但不能漂白指示剂如石蕊试液。
SO2使品红褪色是因为漂白作用,SO2使溴水、高锰酸钾褪色是因为还原性,SO2使含酚酞的NaOH溶液褪色是因为溶于不生成酸。
2、SO2与Cl2通入水中虽然都有漂白性,但将二者以等物质的量混合后再通入水中则会失去漂白性3、往某溶液中逐滴加入稀盐酸,出现浑浊的物质:第一种可能为与Cl- 生成难溶物。
包括:①AgNO3 第二种可能为与H+反应生成难溶物。
包括:① 可溶性硅酸盐SiO32-,离子方程式为:SiO32-+2H+=H2SiO3↓② 苯酚钠溶液加盐酸生成苯酚浑浊液。
③ S2O32- 离子方程式:S2O32- +2H+=S↓+SO2↑+H2O④ 一些胶体如FeOH3先是由于FeOH3的胶粒带负电荷与加入的H+发生电荷中和使胶体凝聚,当然,若继续滴加盐酸至过量,该沉淀则会溶解。
若加HI溶液,最终会氧化得到I2。
⑤ AlO2- 离子方程式:AlO2- +H+ +H2O==AlOH3当然,若继续滴加盐酸至过量,该沉淀则会溶解。
4、浓硫酸的作用:①浓硫酸与Cu反应——强氧化性、酸性②实验室制取乙烯——催化性、脱水性③实验室制取硝基苯——催化剂、吸水剂④酯化反应——催化剂、吸水剂⑤蔗糖中倒入浓硫酸——脱水性、强氧化性、吸水性⑥胆矾中加浓硫酸——吸水性5、能发生银镜反应的有机物不一定是醛.可能是:①醛;②甲酸;③甲酸盐;④甲酸酯;⑤葡萄糖;⑥麦芽糖均在碱性环境下进行6、既能与酸又能与碱反应的物质① 显两性的物质:Al、Al2O3、AlOH3② 弱酸的铵盐:NH42CO3、NH42SO3、NH42S 等。
③ 弱酸的酸式盐:NaHS、NaHCO3、NaHSO3等。
④ 氨基酸。
⑤ 若题目不指定强碱是NaOH,则用BaOH2, Na2CO3、Na2SO3也可以。
7、有毒的气体:F2、HF、Cl2、H2S、SO2、CO、NO2、NO、Br2g、HCN。
历年高考化学学习方法

历年高考化学学习方法历年高考化学学习方法1Ⅰ、基本概念与基础理论:一、阿伏加德罗定律1.内容:在同温同压下,同体积的气体含有相同的分子数。
即“三同”定“一同”。
2.推论(1)同温同压下,V1/V2=n1/n2 (2)同温同体积时,p1/p2=n1/n2=N1/N2(3)同温同压等质量时,V1/V2=M2/M1 (4)同温同压同体积时,M1/M2=ρ1/ρ2注意:①阿伏加德罗定律也适用于不反应的混合气体。
②使用气态方程PV=nRT 有助于理解上述推论。
3、阿伏加德罗常这类题的解法:①状况条件:考查气体时经常给非标准状况如常温常压下,1.01×105Pa、25℃时等。
②物质状态:考查气体摩尔体积时,常用在标准状况下非气态的物质来迷惑考生,如H2O、SO3、已烷、辛烷、CHCl3等。
③物质结构和晶体结构:考查一定物质的量的物质中含有多少微粒(分子、原子、电子、质子、中子等)时常涉及希有气体He、Ne等为单原子组成和胶体粒子,Cl2、N2、O2、H2为双原子分子等。
晶体结构:P4、金刚石、石墨、二氧化硅等结构。
二、离子共存1.由于发生复分解反应,离子不能大量共存。
(1)有气体产生。
如CO32-、SO32-、S2-、HCO3-、HSO3-、HS-等易挥发的弱酸的酸根与H+不能大量共存。
(2)有沉淀生成。
如Ba2+、Ca2+、Mg2+、Ag+等不能与SO42-、CO32-等大量共存;Mg2+、Fe2+、Ag+、Al3+、Zn2+、Cu2+、Fe3+等不能与OH-大量共存;Pb2+与Cl-,Fe2+与S2-、Ca2+与PO43-、Ag+与I-不能大量共存。
(3)有弱电解质生成。
如OH-、CH3COO-、PO43-、HPO42-、H2PO4-、F-、ClO-、AlO2-、SiO32-、CN-、C17H35COO-、等与H+不能大量共存;一些酸式弱酸根如HCO3-、HPO42-、HS-、H2PO4-、HSO3-不能与OH-大量共存;NH4+与OH-不能大量共存。
1989年高考化学试题和参考答案

1989年高考化学试题和参考答案LT1989年高考化学试题和参考答案可能用到的数据原子量 H 1 He 4 C 12 N 14 O 16 N a 23 Mg 24 A l 27 P31 S32 C l 35.5 Ar 40Cu 63.5 Ag 108一、二、三题都是选择题,每题各有一个或两个正确答案。
试将每题正确答案的编号(A、B、C、D)填入括号内.如果试题只有一个正确答案,选多个者不给分;如果试题有两个正确答案,只选一个答案或选了一个正确答案和一个错误答案或选了多于两个答案者,都不给分.一、选择题(每题1分,共12分)1、下列物质中,属于高分子化合物的是()(A)淀粉(B)油脂(C)棉花(D)蔗糖2、下列盛放物质的方法,错误的是()(A)把汽油放在带橡皮塞的玻璃瓶中(B)把硝酸银溶液放在棕色玻璃瓶中(C)把氢氧化钠溶液放在带橡皮塞的玻璃瓶中(D)把氢氟酸放在玻璃瓶中3、只能用排水集气法收集的气体是()(A)H2(B)NO (C)CH4(D)C3H84、现有5种气体:①H2、②NO2、③SO2、④CO2、⑤H2S,在实验室里能用启普发生器来制取的是()(A)①、④、⑤(B)②、④、⑤(C)①、②、④(D)①、③、⑤5、在允许加热的条件下,只用一种试剂就可以鉴别硫酸铵、氯化钾、氯化镁、硫酸铝和硫酸铁溶液,这种试剂是()(A)AgNO3(B)BaCl2 (C)NaOH(D)NH3·H2O6、等摩尔的氢气和氦气在同温同压下具有相同的()(A)原子数(B)体积(C)质子数(D)质量7、下列溶液中的[Cl-]与50毫升1摩尔/升氯化铝溶液中的[Cl-]相等的是()(A)150毫升1摩尔/升氯化钠(B)75毫升2摩尔/升氯化铵(C)150毫升3摩尔/升氯化钾(D)75毫升1摩尔/升氯化铝8、X和Y两元素的阳离子具有相同的电子层结构,X元素的阳离子半径大于Y元素的阳离子半径;Z和Y两元素的原子核外电子层数相同,Z元素的原子半径小于Y元素的原子半径.X、Y、Z三种元素原子序数的关系是()(A)X>Y>Z (B)Y>X>Z (C)Z>X>Y(D)Z>Y>X9、与OH-具有相同质子数和电子数的微粒是()(A)F-(B)Cl-(C)NH3(D)NH2-10、90℃时水的离子积K W=3.8×10-13,该温度时纯水的pH值()(A)等于7 (B)小于7 (C)大于7(D)无法确定11、下列说法正确的是()(A)二氧化硅溶于水显酸性(B)二氧化碳通入水玻璃可以得到原硅酸(C)因为高温时二氧化硅与碳酸钠反应放出二氧化碳,所以硅酸的酸性比碳酸强(D)二氧化硅是酸性氧化物,它不溶于任何酸12、下列说法错误的是()(A)石油中含有C5—C11的烷烃,可以通过石油的分馏得到汽油(B)含C18以上烷烃的重油经过催化裂化可以得到汽油(C)煤是由有机物和无机物组成的复杂的混和物(D)煤中含有苯和甲苯,可以用先干馏后分馏的方法把它们分离出来参考答案:1.A、C2.A、D3.B4.A5.C6.B、C7.C、D 8.D 9.A、D 10.B 11.B 12.D二、选择题(每题2分,共28分)13、下列反应中,气体反应物只能作还原剂的是()(A)氯气通入石灰水(B)二氧化碳通入苯酚钠的水溶液(C)一氧化氮与硝酸反应生成三氧化二氮和水(D)二氧化氮与水反应14、pH值和体积都相同的醋酸和硫酸,分别跟足量的碳酸钠溶液反应,在相同条件下,放出二氧化碳气体的体积是()(A)一样多(B)醋酸比硫酸多(C)硫酸比醋酸多(D)无法比较15、在100毫升0.1摩尔/升醋酸溶液中,欲使醋酸的电离度和溶液的pH值都增大,可以采用的方法是()(A)加少量1摩尔/升氢氧化钠溶液(B)加少量1摩尔/升盐酸(C)加100毫升水(D)加热16、已知下列两个热化学方程式2H2(气)+O2(气)=2H2O(液)+571.6千焦C3H8(气)+5O2(气)=3CO2(气)+4H2O(液) +2220.0千焦实验测得氢气和丙烷和混和气体共5摩尔完全燃烧时放热3847千焦,则混和气体中氢气与丙烷的体积比是()(A)1:3 (B)3:1 (C)1:4 (D)1:117、99毫升0.5摩尔/升硫酸跟101毫升/升氢氧钠化溶液混和后,溶液的pH值为()(A)0.4 (B)2 (C)12 (D)13.618、下列数量的各物质所含原子个数按由大到小的顺序排列的是()①0.5摩尔氨气②标准状况下22.4升氦③4℃时9毫升水④0.2摩尔磷酸钠(A)①④②③(B)④③②①(C)②③④①(D)①④②③19、在强酸性溶液中能大量共存、并且溶液为无色透明的离子组是()20、某离子X2+的最外层电了排布是5s2.当把固体XCl2溶于水配制成溶液时,需加入少量的单质X和盐酸.由此判断下列说法正确的是(A)X元素常见的化合价是+2和+4(B)X(OH)2是强碱(C)XCl2溶液显酸性(D)X元素的最高价氧化物的水化物显强酸性21、下列事实中不能应用勒沙特列原理来解释的是()(A)往硫化氢水溶液中加碱有利于S2-的增多(B)加入催化剂有利于氨氧化的反应(C)高压有利于合成氨的反应(D)500℃左右比室温更有利于合成氨的反应22、下图容器中盛有海水,铁在其中被腐蚀时由快到慢的顺序是()(A)4>2>1>3 (B)2>1>3>4(C)4>2>3>1 (D)3>2>4>123、下列离子方程式正确的是()24、乙烯的丙烯按1:1(摩尔)聚合时,生成聚合物乙丙树脂,该聚合物的结构式可能是()25、下列有机反应的化学方程式正确的是()(A)CH3CH2OH()−−浓硫酸CH2=CH2+H2O−C 140−→−(B)CH3CH2Br+CH3CH2OH+NaOH→CH3CH2OCH2CH3+NaBr+H2O(C)CH2=CHCH=CH2+Br2→BrCH2CHBrCHBrCH2和BrCH2CHBr=CHCHBr(即两种物质都有)(D)CH3CH2COOH+CH3CH2CH2OH−−→−NaOH CH3CH2COOCH2CH2CH3+H2O26、X、Y、Z三种元素的原子,其最外电子层排布分别为ns1、3s23p1和2s22p4,由这三种元素组成的化合物的分子式可能是()(A)XYZ2(B)XYZ3(C)X2YZ2(D)X3YZ3参考答案:13.C 14.B 15.A、C 16.B 17.C 18.A 19.A 20.A、C 21.B、D22.A 23.D 24.A、B 25.C 26.A、D三、选择题(每题3分,共15分)27、体积为V毫升、密度为d克/厘米3的溶液,含有分子量为M的溶质m克,其摩尔浓度为C摩尔/升,质量百分比浓度为W%.下列表示式中正确的是()28、在273℃和1.01×105帕斯卡条件下, 将1.40克氮气、1.60克氧气和4.00克氩气混和,该混和气体的体积是()(A)3.36升(B)6.72升(C)8.96升(D)4.48升29、具有如下电子层结构的原子,其相应元素一定属于同一主族的是()(A)3p亚层上有2个未成对电子的原子和4p 亚层上有2个未成对电子的原子(B)3p亚层上只有1个空轨道的原子和4p亚层上只有1个空轨道的原子(C)最外层电子排布为1S2的原子和最外层电子排布为2S2P6的原子(D)最外层电子排布为1S2的原子和最外层电子排布为2S2的原子30、右图表示外界条件(温度、压力)的变化对下列反应的影响L(固)+G(气) 2R(气)-热在图中,Y轴是指()(A)平衡混和气中R的百分含量(B)平衡混和气中G的百分含量(C)G 的转化率 (D)L 的转化率31、一定条件下,将等体积NO 和O 2 的混和气体置于试管中,并将试管倒立于水槽中,充分反应后剩余气体的体积约为原总体积的( ) (A)41 (B)43 (C)81 (D)83 参考答案:27.B 、D 28.C 29.B 、C 30.B31.C四、(本题共14分)32、下列有机化合物中,有的有多个官能团:(1)可以看作醇类的是(填入编号) ;(2)可以看作酚类的是 ; (3)可以看出羧酸类的是 ;(4)可以看出酯类的是 .33、一氯丁烯(C 4H 7Cl)的同分异构体只有8种,某学生却写了如下10种:其中,两两等同的式子是和, 和。
高考化学 有机高分子化合物知识精讲
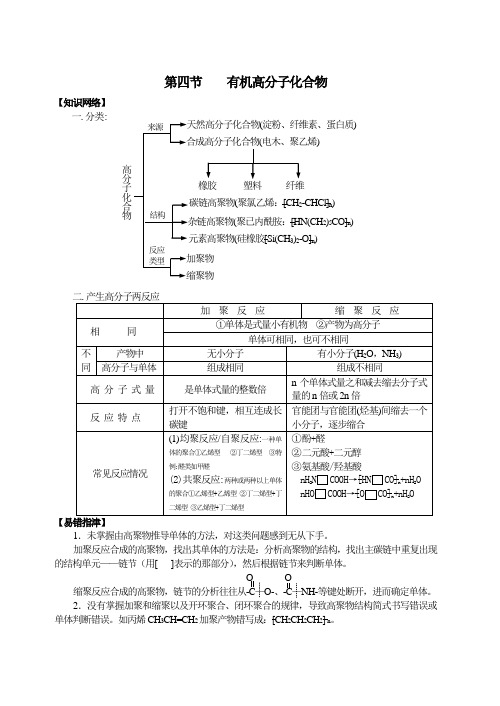
第四节有机高分子化合物【知识网络】一.分类【1.未掌握由高聚物推导单体的方法,对这类问题感到无从下手。
加聚反应合成的高聚物,找出其单体的方法是:分析高聚物的结构,找出主碳链中重复出现的结构单元——链节(用[ ]表示的那部分),然后根据链节来判断单体。
O O缩聚反应合成的高聚物,链节的分析往往从—O-、-C—NH-等键处断开,进而确定单体。
2.没有掌握加聚和缩聚以及开环聚合、闭环聚合的规律,导致高聚物结构简式书写错误或单体判断错误。
如丙烯CH3CH=CH2加聚产物错写成:[CH2CH2CH2] n。
3.若给出高分子化合物的碳碳结构,要确定其组成的单体,则必须按照加聚或缩聚的原理,由高分子的链节,采用逆向思维,反推单体结构,确定规律如下:(1)如果高分子化合物中含有醚键(-O-)、酯基(-COO-)、肽键(-CONH-)等官能团,则一定为缩聚产物。
缩聚产物的单体判断,只要从官能团处补充消去的小分子(一般为水),即可得到相应的单体。
醚键水解(补充消去的水分子),得两种醇,它的单体是两个含有羟基的化合物;酯基水解,得一种含羧基的化合物和一种含羟基的化合物,如;[OC-C6H5-COOCH2CH2-O]n的单体是HOOC-C6H5-COOH和HO-CH2CH2-OH;肽键水解得到一种含羧基的化合物,一种含氨基的化合物。
可见,缩聚反应的单体中都至少有两个官能团。
(2)如果高分子化合物中没有官能团,则一定为加聚产物。
加聚产物的单体判断,一般是将主链上的碳原子两个两个地断开,然后在这两个碳原子间写上双键(如果主链上有取代基,则取代基随主链上的碳原子一起移向单体中),但当主链上有双键时,则为丁二烯结构的1,4-加成产物,单体中有丁二烯结构。
【典型例题评析】例1 下列物质中,属于高分子化合物的是(1989年全国高考题)A.淀粉B.油脂C.棉花D.蔗糖思路分析:油脂是油和脂肪的总称,它是高级脂肪酸甘油酯,蔗糖是二糖,分子式为C12H22O11,油脂和蔗糖的相对分子质量均较小,两者均不属于高分子化合物;棉花的主要成分是纤维素,淀粉和纤维素都是天然高分子化合物。
高考化学复习1998年普通高等学校招生全国统一考试化学试卷

高中化学学习材料(灿若寒星**整理制作)1998年全国普通高等学校招生考试化学试题可能用到的原子量:H-1 C-12 N-14 O-16 Na-23 Mg-24 Al-27 S-32 Cl-35.5 K-39Fe-56 Zn-65一、选择题(本题包括5小题,每小题3分,共15分。
每小题只有一个选项符合题意)1、1998年山西朔州发生假酒案,假酒中严重超标的有毒成份主要是A、HOCH2CHOHCH2OHB、CH3OHC、CH3COOCH2CH3D、CH3COOH2、向下列溶液滴加稀硫酸,生成白色沉淀,继续滴加稀硫酸,沉淀又溶解的是A、Na2SiO3B、BaCl2C、FeCl3D、NaAlO23、按下列实验方法制备气体,合理又实用的是A、锌粒与稀硝酸反应制备氢气B、向饱和氯化钠溶液中滴加浓硫酸制备HClC、亚硫酸钠与浓硫酸反应制备SO2D、大理石与浓硫酸反应制备CO24、起固定氮作用的化学反应是A、氮气与氢气在一定条件下反应生成氨气B、一氧化氮与氧气反应生成二氧化氮C、氨气经催化氧化生成一氧化氮D、由氨气制碳酸氢铵和硫酸铵5、300毫升某浓度的NaOH溶液中含有60克溶质。
现欲配制1摩/升NaOH溶液,应取原溶液与蒸馏水的体积比约为A、1:4B、1:5C、2:1D、2:3二、选择题(本题包括12小题,每小题3分,共36分。
每小题有一个或两个选项符合题意,多选时,该题为0分,若正确答案包括两个选项,只选一个且正确的给1分,选两个且都正确的给3分,但只要选错一个,该小题就为0分) 6、氯化碘(ICl )的化学性质跟氯气相似,预计它跟水反应的最初生成物是 A 、HI 和HClO B 、HCl 和HIO C 、HClO 3和HIOD 、HClO 和HIO7、X 和Y 属短周期元素,X 原子的最外层电子数是次外层电子数的一半,Y 位于X 的前一周期,且最外层只有一个电子,则X 和Y 形成的化合物的化学式可表示为A 、XYB 、XY 2C 、XY 3D 、X 2Y 38、反应4NH 3(气)+5O 2(气) 4NO(气)+6H 2O(气)在2升的密闭容器中进行,1 分钟后,NH 3减少了0.12摩尔,则平均每秒钟浓度变化正确的是A 、NO :0.001摩/升B 、H 2O :0.002摩/升C 、NH 3:0.002摩/升D 、O 2:0.00125摩/升9、用水稀释0.1摩/升氨水时,溶液中随着水量的增加而减小的是A 、][][23O H NH OH ⋅-B 、][][23-⋅OH O H NH C 、[H +]和[OH -]的乘积D 、OH -的物质的量10、下列关于铜电极的叙述 正确的是 A 、铜锌原电池中铜是正极B 、用电解法精炼粗铜时铜作阳极C 、在镀件上电镀铜时可用金属铜作阳极D 、电解稀硫酸制H 2、O 2时铜作阳极 11、等体积等浓度的MOH 强碱溶液和HA 弱酸溶液混和后,混和液中有关离子的浓度应满足的关系是A 、[M +]>[OH -]>[A -]>[H +]B 、[M +]>[A -]>[H +]>[OH -]C 、[M +]>[A -]>[OH -]>[H +]D 、[M +]>[H +] =[OH -]+[A -] 12、下列分子中所有原子都满足最外层8电子结构的是A 、光气(COCl 2)B 、六氟化硫C 、二氟化氙D 、三氟化硼13、下列叙述正确的是A 、同主族金属的原子半径越大熔点越高B 、稀有气体原子序数越大沸点越高C 、分子间作用力越弱分子晶体的熔点越低D 、同周期元素的原子半径越小越易失去电子14、将铁屑溶于过量盐酸后,再加入下列物质,会有三价铁生成的是 A 、硫酸B 、氯水C 、硝酸锌D 、氯化铜15、有五瓶溶液分别是①10毫升0.60摩/升NaOH 水溶液 ②20毫升0.50摩/升硫酸水溶液 ③30毫升0.40摩/升HCl 溶液 ④40毫升0.30摩/升HAc 水溶液 ⑤50毫升0.20摩/升蔗糖水溶液。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
高中化学学习材料(灿若寒星**整理制作)1989年普通高等学校招生全国统一考试化学试题及评分标准可能用到的数据原子量H1He4C12N14O16Na23Mg24Al27P31S32Cl35.5A r40Cu63.5Ag108答案的编号(A、B、C、D)填入括号内.如果试题只有一个正确答案,选多个者不给分;如果试题有两个正确答案,只选一个答案或选了一个正确答案和一个错误答案或选了多于两个答案者,都不给分.一、选择题(每题1分,共12分)1.下列物质中,属于高分子化合物的是(A)淀粉(B)油脂(C)棉花(D)蔗糖答〔〕2.下列盛放物质的方法,错误的是(A)把汽油放在带橡皮塞的玻璃瓶中(B)把硝酸银溶液放在棕色玻璃瓶中(C)把氢氧化钠溶液放在带橡皮塞的玻璃瓶中(D)把氢氟酸放在玻璃瓶中答〔〕3.只能用排水集气法收集的气体是(A)H2(B)NO(C)CH4(D)C3H8答〔〕4.现有5种气体:①H2、②NO2、③SO2、④CO2、⑤H2S,在实验室里能用启普发生器来制取的是(A)①、④、⑤(B)②、④、⑤(C)①、②、④(D)①、③、⑤答〔〕5.在允许加热的条件下,只用一种试剂就可以鉴别硫酸铵、氯化钾、氯化镁、硫酸铝和硫酸铁溶液,这种试剂是(A)AgNO3(B)BaCl2(C)NaOH(D)NH3·H2O 答〔〕6.等摩尔的氢气和氦气在同温同压下具有相同的(A)原子数(B)体积(C)质子数(D)质量答〔〕7.下列溶液中的[Cl-]与50毫升1摩尔/升氯化铝溶液中的[Cl-]相等的是(A)150毫升1摩尔/升氯化钠(B)75毫升2摩尔/升氯化铵(C)150毫升3摩尔/升氯化钾(D)75毫升1摩尔/升氯化铝答〔〕8.X和Y两元素的阳离子具有相同的电子层结构,X元素的阳离子半径大于Y元素的阳离子半径;Z和Y两元素的原子核外电子层数相同,Z元素的原子半径小于Y元素的原子半径.X、Y、Z三种元素原子序数的关系是(A)X>Y>Z(B)Y>X>Z (C)Z>X>Y(D)Z>Y>X 答〔〕9.与OH-具有相同质子数和电子数的微粒是答〔〕10.90℃时水的离子积K W=3.8×10-13,该温度时纯水的pH值(A)等于7(B)小于7(C)大于7(D)无法确定答〔〕11.下列说法正确的是(A)二氧化硅溶于水显酸性(B)二氧化碳通入水玻璃可以得到原硅酸(C)因为高温时二氧化硅与碳酸钠反应放出二氧化碳,所以硅酸的酸性比碳酸强(D)二氧化硅是酸性氧化物,它不溶于任何酸答〔〕12.下列说法错误的是(A)石油中含有C5—C11的烷烃,可以通过石油的分馏得到汽油(B)含C18以上烷烃的重油经过催化裂化可以得到汽油(C)煤是由有机物和无机物组成的复杂的混和物(D)煤中含有苯和甲苯,可以用先干馏后分馏的方法把它们分离出来答〔〕二、选择题(每题2分,共28分)13.下列反应中,气体反应物只能作还原剂的是(A)氯气通入石灰水(B)二氧化碳通入苯酚钠的水溶液(C)一氧化氮与硝酸反应生成三氧化二氮和水(D)二氧化氮与水反应答〔〕14.pH值和体积都相同的醋酸和硫酸,分别跟足量的碳酸钠溶液反应,在相同条件下,放出二氧化碳气体的体积是(A)一样多(B)醋酸比硫酸多(C)硫酸比醋酸多(D)无法比较答〔〕15.在100毫升0.1摩尔/升醋酸溶液中,欲使醋酸的电离度和溶液的pH值都增大,可以采用的方法是(A)加少量1摩尔/升氢氧化钠溶液(B)加少量1摩尔/升盐酸(C)加100毫升水(D)加热答〔〕16.已知下列两个热化学方程式2H2(气)+O2(气)=2H2O(液)+571.6千焦C3H8(气)+5O2(气)=3CO2(气)+4H2O(液)+2220.0千焦实验测得氢气和丙烷和混和气体共5摩尔完全燃烧时放热3847千焦,则混和气体中氢气与丙烷的体积比是(A)1:3 (B)3:1(C)1:4 (D)1:1 答〔〕17.99毫升0.5摩尔/升硫酸跟101毫升/升氢氧钠化溶液混和后,溶液的pH值为(A)0.4 (B)2(C)12 (D)13.6 答〔〕18.下列数量的各物质所含原子个数按由大到小的顺序排列的是①0.5摩尔氨气②标准状况下22.4升氦③4℃时9毫升水④0.2摩尔磷酸钠(A)①④②③(B)④③②①(C)②③④①(D)①④②③答〔〕19.在强酸性溶液中能大量共存、并且溶液为无色透明的离子组是答〔〕20.某离子X2+的最外层电了排布是5s2.当把固体XCl2溶于水配制成溶液时,需加入少量的单质X和盐酸.由此判断下列说法正确的是(A)X元素常见的化合价是+2和+4(B)X(OH)2是强碱(C)XCl2溶液显酸性(D)X元素的最高价氧化物的水化物显强酸性答〔〕(A)往硫化氢水溶液中加碱有利于S2-的增多(B)加入催化剂有利于氨氧化的反应(C)高压有利于合成氨的反应(D)500℃左右比室温更有利于合成氨的反应答〔〕22.下图容器中盛有海水,铁在其中被腐蚀时由快到慢的顺序是(A)4>2>1>3(B)2>1>3>4(C)4>2>3>1(D)3>2>4>1答〔〕23.下列离子方程式正确的是答〔〕24.乙烯的丙烯按1:1(摩尔)聚合时,生成聚合物乙丙树脂,该聚合物的结构式可能是答〔〕25.下列有机反应的化学方程式正确的是(A)CH 3CH 2OH ()−−−−→−C140浓硫酸CH 2=CH 2+H 2O (B)CH 3CH 2Br+CH 3CH 2OH+NaOH →CH 3CH 2OCH 2CH 3+NaBr+H 2O (C)CH 2=CHCH=CH 2+Br 2→BrCH 2CHBrCHBrCH 2和BrCH 2CHBr=CHCHBr(即两种物质都有) (D)CH 3CH 2COOH+CH 3CH 2CH 2OH −−→−NaOH CH 3CH 2COOCH 2CH 2CH 3+H 2O 答〔 〕26.X 、Y 、Z 三种元素的原子,其最外电子层排布分别为ns 1、3s 23p 1和2s 22p 4,由这三种元素组成的化合物的分子式可能是(A)XYZ 2 (B)XYZ 3 (C)X 2YZ 2 (D)X 3YZ 3 答〔 〕三、选择题(每题3分,共15分)27.体积为V 毫升、密度为d 克/厘米3的溶液,含有分子量为M 的溶质m 克,其摩尔浓度为C 摩尔/升,质量百分比浓度为W%.下列表示式中正确的是答〔 〕28.在273℃和1.01×105帕斯卡条件下, 将1.40克氮气、1.60克氧气和4.00克氩气混和,该混和气体的体积是(A)3.36升 (B)6.72升(C)8.96升 (D)4.48升 答〔 〕29.具有如下电子层结构的原子,其相应元素一定属于同一主族的是(A)3p 亚层上有2个未成对电子的原子和4p 亚层上有2个未成对电子的原子 (B)3p 亚层上只有1个空轨道的原子和4p 亚层上只有1个空轨道的原子 (C)最外层电子排布为1S 2的原子和最外层电子排 布为2S 2P 6的原子 (D)最外层电子排布为1S 2的原子和最外层电子排 布为2S 2的原子答〔 〕30.右图表示外界条件(温度、压力)的变化对下列反应的影响L(固)+G(气) 2R(气)-热在图中,Y 轴是指(A)平衡混和气中R 的百分含量 (B)平衡混和气中G 的百分含量 (C)G 的转化率 (D)L 的转化率 答〔 〕31.一定条件下,将等体积NO 和O 2 的混和气体置于试管中,并将试管倒立于水槽中,充分反应后剩余气体的体积约为原总体积的(A)41 (B)43 (C)81 (D)83答〔 〕四、(本题共14分)32.下列有机化合物中,有的有多个官能团:(1)可以看作醇类的是(填入编号) ;(2)可以看作酚类的是;(3)可以看出羧酸类的是;(4)可以看出酯类的是.33.一氯丁烯(C4H7Cl)的同分异构体只有8种,某学生却写了如下10种:其中,两两等同的式子是和, 和。
34.有4种钠的化合物W、X、Y、Z,根据以下反应式判断W、X、Y、Z的分子式.W−→−∆X+CO2↑+H2O Z+CO2→X+O2Z+H2O→Y+O2↑X+Ca(OH)2→Y+CaCO3↓W是,X是,Y是,Z是.35.在适当的温度和压力下,4体积某气态化合物完全分解后产生1体积磷蒸气和6体积氢气,由此可推断该气态化合物的分子式为,该分解反应的化学方程式为.36.某温度时,在2升容器中X、Y、Z三种物质的物质的量随时间的变化线如下图所示.由图中数据分析,该反应的化学方程式为;反应开始至2分钟,Z的平均反应速度为.37.将等体积的0.4摩尔/升CH3COONa溶液与0.2摩尔/升HNO3溶液相混和,混和液中各离子浓度按由大到小的顺序排列为.38.配平下列化学方程式,将系数填在括号内.[ ]Cu2S+[ ]HNO3=[ ]Cu(NO3)2+[ ]H2SO4+[ ]H2O五、(本题共8分)实验室里用下列仪器和药品来制取纯净的无水氯化铜:序号(1)(2)(3)(4)(5)(6)仪器及装置图图中A、B、C、D、E、F的虚线部分表示玻璃管接口,接口的弯曲和伸长等部分未画出.根据要求填写下列各小题空白.39.如果所制气体从左向右流向时,上述各仪器装置的正确连接顺序是(填各装置的序号)( )接( )接( )接( )接( )接( );其中,(2)与(4)装置相连时,玻璃管接口(用装置中字母表示)应是接.40.装置(2)的作用是;装置(4)的作用是;装置(6)中发生反应的化学方程式是.41.实验开始时,应首先检难装置的;实验结束时,应先熄灭处的酒精灯.42.在装置(5)的烧瓶中,发生反应的化学方程式为43.待充分反应后,装置(1)的玻离管中剩余物呈色.冷却后,将制得的产物配成饱和溶液,溶液呈色.六、(本题共11分)44.固体A、B都由两种相同的元素组成.在A、B中两种元素的原子个数比分别为1:1和1:2.将A 和B在高温时煅烧,产物都是C(固体)和D(气体).由D最终可制得E(酸),E和另一种酸组成混和酸,常用于制取有机炸药.E的稀溶液和A反应时,生成G(气体)和F(溶液),G通入D的水溶液,有浅黄色沉淀生成.在F中滴入溴水后,加入氢氧化钾溶液,有红褐色沉淀生成,该沉淀加热时又能转变为C.根据上述事实回答:(1)A的分了式是,B的分子式是.(2)写出下列反应的化学方程式①B煅烧生成C和D②G通入D溶液中③在F中滴入溴水(3)写出A和E反应的离子方程式45.在红磷存在时,羧酸跟溴起反应,可以在连接羧基的碳原子上导入溴原子.例如:把下列各步变化中指定分子式的有机产物的结构式填入空格内:七、(本题共12分)46.氢气和氧气的混和气体,在120℃和一定压强下体积为a升,点燃后发生反应.待气体恢复至原来温度和压强时,测得其体积为b升。
