产品信息传递反馈单
药品质量信息反馈单

反馈部门:编号:
品名ቤተ መጻሕፍቲ ባይዱ
规格
单位
数量
批号
有效期
批准文号
生产企业
质量情况:
反馈人:日期:
药店负责人意见:
负责人:日期:
质量负责人意见:
经办人:日期:
主管领导意见:
签字:日期:
处理结果追踪:
质管部:日期:
质量信息传递反馈处理单
信
息
输
出
信息发出日期
信息发出部门
信息发出人
信息级别
A B C
信息内容及要求:
信
息
接
收
传入日期:
反馈日期:
接收人员:
处理人:
信息处理情况:
质量管理员意见
负责人:日期:
处理结果追踪:
经办人:日期:
1、信息类别按“质量信息管理制度”规定划分一级为重要信息,报经理及有关部门;二级为较重要信息,报质管部及有关部门;三级为一般信息,报本部门领导。2、本信息单根据需要一式2份,如需要处理后1份返回传递发出部门。
《出厂产品退货返修及三包管理规定》

出厂产品退货返修及三包管理规定企管字(2013)第188号一、定义(一)出厂产品退货是指业务部、外贸部、业务部已经开票销售的产品,或未开票结算但已经办理发出商品手续发出的产品,因公司产品质量原因、市场发生变化、用户原因、货款回收原因或销售部门将产品退回公司的产品。
(二)出厂产品招回是指公司产品销售或发出后,公司技术部或品管部发现公司产品存在某种技术或质量缺陷,为避免给用户造成不必要的伤害,或减轻对公司形象的负面影响,经公司研究决定,让业务部门通知用户,将有缺陷的产品进行招回处理。
二、适用范围本规定适用于XXX有限公司生产的产品及相关零部件。
三、职责1、销售部、业务室负责退货、招回产品的的分类统计。
内容包括产品型号、机器编号、退货原因。
2、业务部负责市场销售的零部件退货及三包的分类统计。
内容包括产品型号、零部件名称、销售数量、退货数量、退货原因。
3、品管部、技术部负责退货原因分析、责任的界定、返修方案的制定。
4、生产一部负责整机产品的返修,生产二部、生产三部负责市场销售零部件的返工和返修。
5、财务部负责返修、退货质量成本的统计和分析、考核。
四、产品退货的条件1、产品及零部件存在明显质量问题,影响销售或使用的;2、客户拒不履行付款义务时间一年以上的;3、客户因经营不善,存在破产风险,给公司造成潜在损失的。
五、退货的批准程序产品及零部件退货前,当事部门及其经办人员要书面申请需要退回(招回)产品的品名、规格型号、数量以及产品退回(招回)的原因,经部门负责人审核,报总经理批准后实施产品退回(招回)。
六、业务处理程序(一)销售(发出)产品退回1、没有质量问题的销售(发出)产品退回:销售经办人员按照批准程序,经批准后,依据批准报告向业务室办理退库手续,已经开出发票的,要将原发票收回或提供对方税务机关出具的退货证明(下同)。
退库的产品应保持出库时的完好状态;业务室接到退回产品后,形成退货明细并及时通知品管部进行检验,品管部在进行检验过程中,退回产品如不能达到公司规定产品入库质量要求的,比如:有缺件或个别零件损坏等,由品管部提报“返修生产通知单”交业务室,由业务室向计划部下达返修计划,生产一部负责修复完好,经品管部检查员检查合格后,由生产一部办理入库,生产一部根据返修计划,提报该计划维修资料明细,由财务部进行核算,报企管部进行处理,费用由销售部具体责任人承担。
质量信息管理程序
1 目的本标准规定了质量信息管理的职责、内容、要求及质量信息收集、贮存、传递、处理和利用。
确保产品质量信息管理满足顾客的需要。
目的是建立质量信息管理系统,充分利用质量信息资源,提供质量管理体系正常运行和产品符合要求的证明,不断改进质量管理体系,满足顾客需求。
2 范围本标准适用于公司内、外部质量信息的收集、处理、保存和传递等的管理。
3 职责3.1 品质管理部负责质量信息的归口管理,按照医疗器械标淮,结合本公司工作特点,组织医疗器械研制生产过程中的质量信息的采集、保存、处理和传递等工作,并按要求向顾客报送质量信息。
3.2 各部门负责与其开展的质量活动有关的信息的收集、保存(归档前)和传递,确保信息的安全性和保密性。
4 程序4.1 信息的范围与产品质量、工作质量和管理质量有关的信息、质量记录、报表、电子邮件、电话记录等的项目与要求(格式见附录A)。
4.2 信息的收集各类质量信息按程序文件、作业指导书等规定,由责任人负责收集、记录(录入)。
4.3 信息的传递4.3.1 各种报表、记录资料和文件承载信息通过文件的收发,按程序文件规定的文件、记录传递要求,完成信息的传递。
4.3.2 医疗器械在研制、生产、试验和使用过程中发生的质量问题按《故障报告、分析和纠正措施程序》实行质量问题信息快报制度。
4.3.3 属于无章可循、职责不明等管理问题,发现部门应按《文件控制程序》要求使用《文件更改申请单》提出管理文件的更改意见和建议。
4.3.4 生产车间若需要反映产品质量问题或潜在的产品缺陷的,应使用《质量信息反馈单》。
其使用方法如下:a) 生产车间应及时填写《质量信息反馈单》,报品质管理部;b) 品质管理部接到信息单后应建账登记,同时将《质量信息反馈单》送给相关部门负责人;c) 相关部门负责人接到信息单后,应明确处理要求、处理责任人,传递给处理部门;d) 处理责任人按信息单内容要求应及时处理,处理完填妥返回给品质管理部;e) 相关部门负责人对处理效果验证认可后,分别给处理责任人,报送品质管理部和返回信息发出部门;f) 信息发出部门在填写质量信息单同时,须在《质量信息反馈登记表》登记,以便汇总、统计分类、跟踪实行闭环管理。
信息报送范文10篇

信息报送范文10篇信息报送是一种信息传递方式,它可以传递各种各样的信息。
在日常工作之中,我们会经常需要进行信息报送。
而如何写好信息报送,就成为了我们必须要解决的问题。
下面,我将为大家提供10篇信息报送范文,以便大家参考和借鉴。
第一篇:请假报告尊敬的领导:本人因为身体原因,需要请病假一天,从明天开始请假,预计到下周一返回工作岗位。
关于工作安排,本人已经和您的工作助理做了沟通,并得到了同意。
在此向您报告并请求批准,请假期间,我会保持电话和网络畅通,以便及时与你联系和协调工作。
敬礼!XXX第二篇:汇报工作尊敬的领导:根据您的要求,XXX项目已进入了关键阶段,本人特将项目的最新进展情况汇报如下:经过团队的共同努力,目前项目已完成70%的工作量,关键节点已顺利通过并顺利继续推进。
目前,我们的分工明确,各部分任务有序推进。
同时,我们在项目过程中遇到了一些困难,但我们已经采取措施积极解决。
预计在下周二,项目能够按时交付。
如有疑虑,敬请及时与本人联系。
敬礼!XXX第三篇:邀请函尊敬的XXX:本人公司即将在X月X日举办一次庆祝活动,特邀请您出席。
活动时间:XX:XX-XX:XX。
届时,我们将提供精美的餐点和丰富多彩的节目环节。
这是我们公司与合作伙伴共同取得的一项重大进展,并致力于与大家一同分享喜悦。
恳请您能抽出宝贵的时间前来参加此次活动,您的到来将为我们增添无限光彩。
敬礼!XXX第四篇:感谢信尊敬的XXX:谨向您表示最诚挚的感谢。
感谢您长期以来对我公司的关心和支持。
正是由于您的多年支持和关爱,我公司才能够乘风破浪,不断前行。
同时,我也要感谢您对我个人的支持和指导。
近年来,我在您的帮助下得到了很大的提升和提高。
我将倍加珍惜您的支持和指导,继续努力工作,回报您的重托和期许。
再次感谢您的帮助和付出。
敬礼!XXX第五篇:通知公告各位同事:根据公司年度工作安排,XXX项目已进入了重要阶段。
为确保项目安全高效的推进,特告知如下:1.请大家密切关注项目进展情况,及时报告问题,并定期参加项目汇报会,听取项目的最新进展情况。
质量信息反馈制度范文(二篇)

质量信息反馈制度范文一、概述我们公司致力于提供高质量的产品和服务,为了确保客户的满意度,我们建立了质量信息反馈制度,以便及时收集、处理和解决客户的质量问题。
该制度旨在促进公司的持续改进,保证产品和服务的质量和可靠性。
二、反馈渠道为了方便客户反馈质量问题,我们提供以下几种渠道:1. 电话反馈:客户可以通过拨打我们提供的客服热线,将质量问题告知我们的客服代表。
2. 邮件反馈:客户可以将质量问题以邮件形式发送至我们指定的邮箱,我们将在收到邮件后尽快跟进处理。
3. 在线反馈:客户可以登录我们的官方网站,在反馈页面填写相关信息并描述质量问题,我们将在收到反馈后尽快处理。
4. 实体反馈:客户可以将质量问题以书面形式寄送至我们公司的地址,我们将在收到反馈后尽快处理。
三、质量信息收集与处理1. 收集流程:a) 我们的客服人员将负责接收来自不同渠道的客户质量反馈,并详细记录下反馈的问题描述、时间、地点等。
b) 客服人员将及时整理并转交给质量部门进行进一步处理。
2. 处理流程:a) 质量部门将负责对收集到的信息进行初步评估,并将问题分类和分级。
b) 质量部门将与相关部门进行沟通,协调解决质量问题。
c) 质量部门将对解决方案进行评估和验证,并将结果反馈给客户。
四、问题解决与改进1. 问题解决:a) 我们将尽快处理收到的质量反馈,并与客户保持及时的沟通。
b) 对于紧急问题,我们将采取紧急措施,以确保问题能够及时解决。
c) 在解决问题的过程中,我们将充分调动各部门的资源,确保问题的彻底解决。
2. 改进措施:a) 我们将不断总结提出质量问题的原因,分析并找出解决问题的根本办法。
b) 我们将建立并完善质量管理体系,加强相关业务人员的培训,提高质量意识和技能水平。
c) 我们将定期组织质量管理会议,对质量改进工作进行评估和调整,确保质量改进的持续性和可持续发展。
五、保密与保护我们承诺对客户的质量信息进行保密,除非得到客户的明确许可,否则不会向任何第三方透露。
质量信息传递反馈表

质量信息传递反馈表
编号:MLH-ZD-005 【5-1(18】
信息名称:总局关于39批次药品不合格的通告(2017年第193号)
信息来源:国家食品药品监督管理局
收集时间:2017年12月04日
收 集 人:***
信息等级:B类
信息主体:经中国食品药品检定研究院等11家药品检验机构检验,标示为吉林省力胜制药有限公司等19家企业生产的39批次药品不合格。现将相关情况通告如下:
一、不合格产品的标示生产企业、药品品名和生产批号为:
吉林省力胜制药有限公司生产的批号为20160902、20160903、20161002、20161102的安胃片,甘肃佛仁制药科技有限公司生产的批号为150902、151101、160301、170201的安胃片,山西云鹏制药有限公司生产的批号为D150501、D150502、D160201、D160602的安胃片,山西汾河制药有限公司生产的批号为170202的吡拉西坦片,山东仁和堂药业有限公司生产的批号为160601的吡拉西坦片,大同市云岗制药有限公司生产的批号为161214的硫酸庆大霉素颗粒,丹东宏业制药有限公司生产的批号为20160404、20160702的硫酸庆大霉素碳酸铋胶囊,上海全宇生物科技确山制药有限公司生产的批号为1605051的硫酸庆大霉素碳酸铋胶囊,太极集团重庆桐君阁药厂有限公司生产的批号为17030008的龙胆泻肝片,山东齐都药业有限公司生产的批号为1C16120305的羟乙基淀粉130/0.4氯化钠注射液,山东华鲁制药有限公司生产的批号为D17021802、D17012504、D17021601、D16102201、D17012402的羟乙基淀粉130/0.4氯化钠注射液,焦作联盟医用材料股份有限公司生产的批号为20160501的曲安奈德新霉素贴膏,上海金不换兰考制药有限公司生产的批号为20160506的曲克芦丁片,六安华源制药有限公司生产的批号为161120022-A的替硝唑氯化钠注射液,天津儿童药业有限公司生产的批号为20160502的头孢克洛颗粒,焦作市银河药业有限公司生产的批号为20160310、20160405、20160407、20160409、20160506的头孢拉定颗粒,广西邦琪药业集团有限公司生产的批号为160327、160525的头孢拉定颗粒,辽宁丹生生物制药有限公司生产的批号为20160801的胰酶肠溶片,陕西中医学院制药厂生产的批号为160701、17A01的银翘解毒合剂。不合格项目包括含量测定、脆碎度、装量差异、溶出度、微生物限度、可见异物、效价测定、性状等(详见附件)。
2022新版gsp质量管理制度(零售)

2022新版gsp质量管理制度(零售)某某某某某大药房质量管理文件1、目的:加强药品购进环节的质量管理,确保购进药品的质量和合法性。
2、依据:《药品经营质量管理规范》3、适用范围:适用于本药房药品购进的质量管理。
4、责任:采购员和质量管理人员对本制度的实施负责。
5、内容:5.1确定供货单位的合法资格,把质量作为选择药品和供货单位条件的首位,从具有合法证照的供货单位进货,严格执行“按需购进、择优选购,质量第一”的原则购进药品,并在购进药品时签订质量保证协议。
5.2确定所购入药品的合法性,严格执行《药品购进程序》,认真审查供货单位的法定资格、经营范围和质量信誉等,确保从合法的药房购进符合规定要求和质量可靠的药品。
5.3核实供货单位销售人员的合法资格,购进药品应签订有明确规定质量条款的购货合同。
如购货合同不是以书面形式确立时,应与供货单位签订质量保证协议书,协议书应明确有效期限。
5.4严格执行《首营药房和采购品种审核制度》,做好首营药房和采5.5购进药品应有合法票据,做好真实完整的购进记录,并做到票、帐、货相符。
药品购进记录和购进票据应保存至超过药品有效期一年,但不得少于两年。
5.6药品购进记录应包括:购货日期、药品通用名称(商品名)、剂型、规格、生产厂家、供货单位、购进数量、价格、有效期、批号、采购员、备注等内容,中药饮片还应标明产地。
某某某某某大药房质量管理文件1、目的:把好购进药品质量关,保证药品数量准确,外观性状和包装质量符合规定要求,防止不合格药品进入本药房。
2、依据:《药品经营质量管理规范》3、适用范围:适用于药房所购进药品的验收。
4、责任:验收员对本制度的实施负责。
5、内容:5.1验收药品应在待验区内按规定比例抽取样品进行检查,并在规定时限内完成。
5.2药品验收必须执行制定的《药品质量检查验收程序》,由验收人员依照药品的法定标准、购进合同所规定的质量条款以及购进凭证等,对所购进药品进行逐批验收。
药品质量信息传递、处理、反馈单
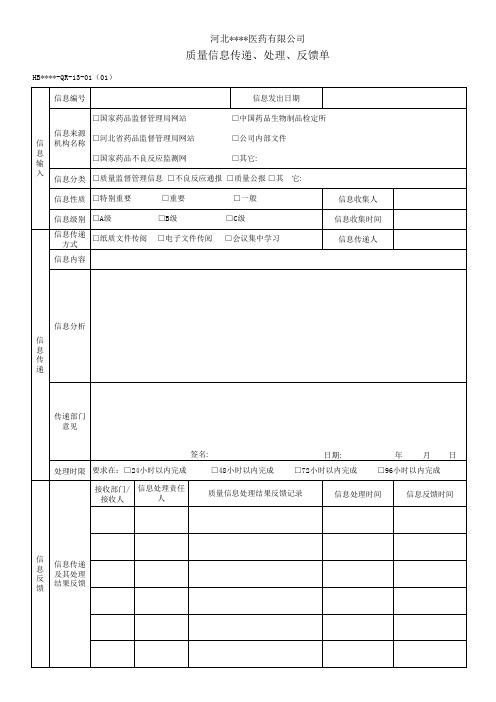
质量信息传递、处理、反馈单
HB****-QR-13-01(01)
信息编号
信息发出日期
□国家药品监督管理局网站
□中国药品生物制品检定所
信
信息来源 机构名称
□河北省药品监督管理局网站
□公司内部文件
息 输
□国家药品不良反应监测网
□其它:
入 信息分类 □质量监督管理信息 □不良反应通报 □质量公报 □其 它:
接收部门/ 信息处理结果反馈记录
信息处理时间
信息反馈时间
信 息 反 馈
信息传递 及其处理 结果反馈
信息性质 □特别重要
□重要
□一般
信息收集人
信息级别 □A级
信息传递 方式
□纸质文件传阅
信息内容
□B级 □电子文件传阅
□C级 □会议集中学习
信息收集时间 信息传递人
信息分析
信 息 传 递
传递部门 意见
签名:
处理时限 要求在:□24小时以内完成
□48小时以内完成
日期: □72小时以内完成
年
月日
□96小时以内完成
