PH值检测数据记录表
水质检测实验报告

水质检测实验报告本次实验旨在了解水质检测的基本原理和方法,以及掌握现代化的水质检测技术,为水环境保护和管理提供基础数据。
实验采集水样来自附近的自来水厂,我们分别对PH值、溶解氧、高锰酸钾指数、总磷、总氮进行测定,下面将分别介绍实验过程和结果。
PH值测定PH值在水环境中是一个十分重要的指标,是反映水体酸碱情况的重要指标。
我们采用了玻璃电极PH计、试纸法、酚酞法三种测定方法,最终结果如下:测定方法 PH值玻璃电极PH计法 7.48试纸法 7.5酚酞法 7.4通过对比三种测定方法,可以看出三种方法测定的PH值结果基本一致,其中玻璃电极PH计法结果最为精确。
相比试纸法和酚酞法,玻璃电极PH计法操作简便、准确性高,是目前水质检测常用的PH值测定方法。
溶解氧测定溶解氧是水体中生物生长和呼吸的必需气体,它对于水体生态系统的稳定起着至关重要的作用。
我们采用了电极法和试剂盒法,最终结果如下:测定方法溶解氧(mg/L)电极法 6.99试剂盒法 6.78通过对比两种方法结果,发现两种方法结果接近。
但是电极法操作繁琐,对工作人员技术要求较高,而试剂盒法则准确度稍逊于电极法,但是采样方便、易操作,因此谨慎选择合适的测定方法才能提高检测数据的准确性和可靠性。
高锰酸钾指数测定高锰酸钾指数是水污染程度的一个重要指标,是反映有机物氧化性能的普遍指标。
这一指标可以反映水污染的严重程度。
实验室我们采用了显色滴定法和紫外分光光度法,最终结果如下:测定方法高锰酸钾指数显色滴定法 6.04紫外分光光度法 6.01两种方法所得结果基本一致,但以紫外分光光度法更能准确确定高锰酸钾指数,在实际水质检测工作量较大时显色滴定法效率相对较低。
总磷测定总磷是动植物体内一种重要的生物元素,是表征水体富营养化程度的关键指标。
我们采用了纳斯塔技术,最终结果如下:测定方法总磷含量纳斯塔技术 0.040 mg/L总氮测定总氮包括无机氮和有机氮,这些物质是影响水生态稳定的重要因素。
水质分析成果台账

水质分析成果台账一、项目描述该项目是对水体的水质状况进行全面分析和评估,以确保水质符合相应的环保要求和安全标准。
本项目主要包括采样、实验室测试、数据分析和结果汇报等环节。
二、采样过程1.采样时间:2024年5月1日至5月5日,每日上午8时至下午5时进行。
2.采样点位:共设立10个采样点,包括山塘、河流、湖泊等不同类型水体。
3.采样工具:采用无菌玻璃瓶作为采样容器,每个采样点位采集2L 水样。
4.采样方法:每个采样点位进行5次独立采样,随机选取5个不同位置,保证样品的代表性。
5.采样记录:每次采样时记录采样点位、采样时间、天气情况、采样深度等信息,并编号标识。
三、实验室测试1.pH值测定:使用PHS-3C电极仪进行检测,采用标准曲线法计算pH 值。
2.溶解氧测定:采用WP6880型溶解氧仪进行检测,测量值以毫克/升为单位。
3. 氨氮测定:使用Nessler法进行测定,结果以毫克/升为单位。
4.总硬度测定:采用EDTA络合滴定法进行测定,结果以毫克/升为单位。
5.总大肠菌群测定:采用多管最概胜法进行测定,结果以最概胜值(MPN)为单位。
6.COD测定:采用高锰酸钾法进行测定,结果以毫克/升为单位。
7.浊度测定:使用NTU浊度计进行测定,结果以浊度单位(NTU)表示。
四、数据分析1.统计分析:对每个指标的测定结果进行统计分析,包括平均值、标准差、最大值和最小值等。
2.对比分析:将测定结果与相关限值进行对比分析,判断是否符合环保要求和安全标准。
3.趋势分析:根据历史数据和测定结果,分析水质状况的变化趋势。
五、结果汇报在本次水质分析中,共采集到50个独立样品,并进行了全面的实验室测试。
下表为各指标的测定结果和分析汇总:采样点位, pH值,溶解氧(mg/L),氨氮(mg/L),总硬度(mg/L),总大肠菌群(MPN), COD(mg/L),浊度(NTU)-,-,-,-,-,-,-,-采样点1,7.2,6.5,0.8,120,300,15,5采样点2,6.8,7.2,1.2,150,500,20,8采样点3,7.5,5.6,0.5,100,200,12,4采样点4,7.0,6.0,1.0,130,400,18,10采样点5,7.4,6.8,0.7,140,250,14,6采样点6,7.1,6.4,0.9,125,350,16,7采样点7,7.3,5.8,0.6,110,150,10,3采样点8,7.6,7.0,1.1,160,450,22,9采样点9,7.0,6.2,0.9,130,400,18,8分析结果显示,各指标测定值均在正常范围内,并且没有超过环保要求和安全标准。
新方法验证报告(pH 便携式pH计法 《水和废水监测分析方法》)

XXXX有限公司新项目方法验证能力确认报告pH 便携式pH计法《水和废水监测分析方法》(第四版项目名称:增补版)国家环境保护总局(2002年)负责人:审核人:日期:pH 便携式pH计法《水和废水监测分析方法》(第四版增补版)国家环境保护总局(2002年)方法验证能力确认报告1、方法依据及适用范围本方法依据是pH 便携式pH计法《水和废水监测分析方法》(第四版增补版)国家环境保护总局(2002年)本方法能力验证应随标准更新而更新。
本方法还用于水质pH值的测定。
2、方法原理以玻璃电极为指示电极,以Ag/AgCl等为参比电极合在一起组成pH复合电极,利用pH复合电极电动势随似离了活度变化而发生偏移来测定水样的pH值,复合电极pH计均有温度补偿装置,用以校正温度对地极的影响,用于常规水样监测可准确至0.1pH单位。
较精密仪器可准确到0.01pH单位,为了提高测定的准确度,校准仪器时选用的标准缓冲溶液的pH值应与水样的pH值接近。
3、主要仪器、设备及试剂除非另有说明,分析时均使用符合国家标准的分析纯试剂。
3.1试剂和材料3.1.1配制标准溶液所用的蒸馏水应符合下列要求:煮沸并冷却、电导率小于2×10-6S/cm的蒸馏水,其pH 以6.7~7.3之间为宜。
3.1.2测量pH时,按水样呈酸性,中性和碱性三种可能,常配制以下三种标准溶液:1)pH标准溶液(pH4.008 25℃):c(C8H5KO4)=0.05mol/L,标准证书编号:XXXXXXXX,有效期限:XXXX年XX月XX日。
2)pH标准溶液(pH6.865 25℃):c(KH2PO4)=0.025mol/L,标准证书编号:XXXXXXXX,有效期限:XXXX年XX月XX日。
3)pH标准溶液(pH9.180 25℃):c(Na2B4O7)=0.01mol/L,标准证书编号:XXXXXXXX,有效期限:XXXX年XX月XX日。
3.1.3标准溶浓的保存:标准溶液要在聚乙稀瓶中密闭保存,在室温条件下标准溶浓一般以保存1~2个月为宜,当发现有浑浊、发霉或沉淀现象时,不能继续使用。
纯水机水质监测记录
纯水机水质监测记录
纯水机水质监测记录
一、概述
本记录用于记录纯水机水质监测的数据和分析结果。
纯水机是一种用于制备纯净水的设备,其水质直接关系到人们的健康和生产安全。
因此,对纯水机水质进行定期监测和记录至关重要。
二、监测项目
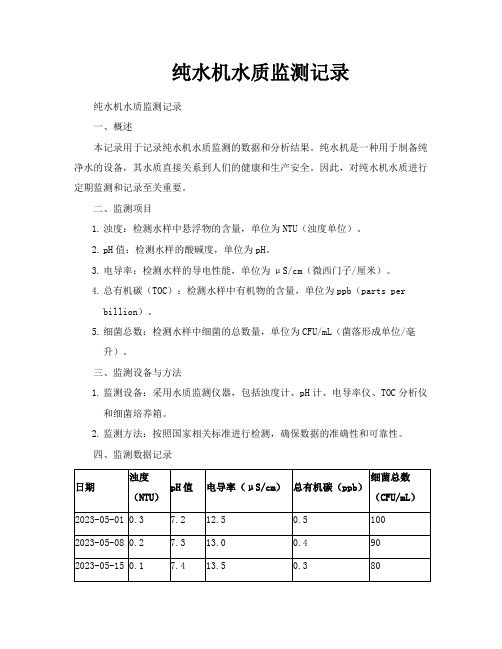
1.浊度:检测水样中悬浮物的含量,单位为NTU(浊度单位)。
2.pH值:检测水样的酸碱度,单位为pH。
3.电导率:检测水样的导电性能,单位为μS/cm(微西门子/厘米)。
4.总有机碳(TOC):检测水样中有机物的含量,单位为ppb(parts per
billion)。
5.细菌总数:检测水样中细菌的总数量,单位为CFU/mL(菌落形成单位/毫
升)。
三、监测设备与方法
1.监测设备:采用水质监测仪器,包括浊度计、pH计、电导率仪、TOC分析仪
和细菌培养箱。
2.监测方法:按照国家相关标准进行检测,确保数据的准确性和可靠性。
四、监测数据记录
通过对监测数据的分析,我们可以得出以下结论:
1.水质浊度、pH值、电导率和总有机碳含量均符合国家相关标准,说明水质
良好,符合生产和生活用水的要求。
2.水质细菌总数控制在较低水平,说明纯水机在制备过程中有效地抑制了细菌
的生长和繁殖,保障了饮用水的安全性。
电位法测定水溶液的pH值

实验1 电位法测定水溶液的pH值一、实验目的1.掌握用玻璃电极测量溶液pH值的基本原理和测量技术;2.学会怎样测定玻璃电极的响应斜率,进一步加深对玻璃电极响应特性的了解。
二、方法原理以玻璃电极作指示电极,饱和甘汞电极作参比电极,用电位法测量溶液的pH值,组成测量电池的图解表示式为:电池的电动势等于各相界电位的代数和。
即,其中为试液与饱和氯化钾溶液之间的液接电位E j,于是当测量体系确定后,式中E(电池)、E(Ag,AgCl)及E j均为常数,而合并常数项,电动势可表示为:其中0.059为玻璃电极在25℃的理论响应斜率。
由于玻璃电极常数项,或说电池的“常数”电位值无法准确确定,故实际中测量pH值的方法是采用相对方法。
即选用pH值已经确定的标准缓冲溶液进行比较而得到欲测溶液的pH值。
为此,pH值通常被定义为其溶液所测电动势与标准溶液的电动势差有关的函数,其关系式是: (1)式中pH x和pH s分别为欲测溶液和标准溶液的pH值,E x和E s分别为其相应电动势。
该式常称为pH值的实用定义。
测定pH用的仪器-pH电位计是按上述原理设计制成的。
例如在25℃时,pH计设计为单位pH变化58mV。
若玻璃电极在实际测量中响应斜率不符合58mV的理论值,这时仍用一个标准pH缓冲溶液校准pH计,就会因电极响应斜率与仪器不一致引入测量误差。
为了提高测量的准确度,需用双标准pH缓冲溶液法将pH计的单位pH的电位变化与电极的电位变化校为一致。
当用双标准pH缓冲溶液法时,电位计的单位pH变化率S可校定为: (2)式中pH(s,1)和pH(s,2)分别为标准pH缓冲溶液1和2的pH值,E(s,1)和E(s,2)分别为其电动势。
代入(1)式,得:从而消除了电极响应斜率与仪器原设计值不一致引入的误差。
显然,标准缓冲溶液的pH值是否准确可靠,是准确测量pH值的关键。
目前,我国所建立的pH标准溶液体系有7个缓冲溶液,它们在0~95℃的标准pH值可查阅相关文献。
探究盐溶液的酸碱性试验记录 (2)

02
实验原理
盐的水解原理
盐的水解是指盐溶液中的盐离子 或阴、阳离子与水电离出的氢离 子或氢氧根离子结合,生成弱电
解质的过程。
盐的水解反应通常为可逆反应, 受溶液的酸碱度和温度等因素影
学习使用酸碱指示剂
酸碱指示剂是一种用于指示溶液酸碱性的化学试剂。通过实 验,可以学习如何正确使用酸碱指示剂,了解其在不同酸碱 度下的颜色变化。
在实验过程中,需要注意指示剂的浓度和滴定方法,以确保 实验结果的准确性。
掌握pH值的测定方法
pH值是衡量溶液酸碱性的一个重要指标。通过实验,可以掌握使用pH试纸或pH 计测定溶液pH值的方法。
使用滴管分别取适量的不同种类的盐溶液,滴在pH试纸上 。
观察试纸的颜色变化,与标准比色卡进行对比,记录盐溶 液的pH值。
记录实验数据和现象
记录每种盐溶液的浓度、体积以及测得的pH值。
记录实验过程中观察到的现象,如是否有沉淀生成、颜色变化等。
通过以上实验步骤,我们可以探究不同种类的盐溶液的酸碱性,并记录实验数据和现象。在实验过程中, 需要注意安全事项,如避免试剂接触皮肤和眼睛,以及正确使用实验器材等。
通过实验,我学会了使用酸碱指示剂 和pH试纸测定溶液的酸碱性,以及如 何正确操作滴定管等实验器材。
通过实验观察、记录和分析数据,我 学会了科学探究的方法,提高了分析 和解决问题的能力。
加深对盐类水解的理解
实验让我更加深入地理解了盐类水解 的原理及其在日常生活中的应用,如 食盐、小苏打等。
实验不足与改进建议
04
实验结果与分析
实验数据汇总
ph值测定作业指导书

ph值测定作业指导书一、实验目的本实验旨在通过测定溶液的酸碱度,了解PH值的概念和测定方法,并掌握PH试纸和PH计的使用技巧。
二、实验原理PH值是衡量溶液酸碱度的指标,其数值范围为0-14。
PH值小于7的溶液为酸性,大于7的溶液为碱性,等于7的溶液为中性。
本实验使用两种常见的PH测定方法:PH试纸法和PH计法。
1. PH试纸法PH试纸是一种简便易行的测定方法。
试纸上涂有一种酸碱指示剂,当试纸浸入溶液中时,指示剂会根据溶液的酸碱度发生颜色变化,通过对照试纸颜色与标准色卡,可以确定溶液的PH值范围。
2. PH计法PH计是一种精确测定PH值的仪器。
PH计通过测量溶液中的氢离子浓度来确定PH值。
PH计的电极浸入溶液中,根据溶液中的氢离子浓度与电极的电位差来计算PH值。
三、实验步骤1. PH试纸法(1)准备工作:将试纸取出并摊开,确保试纸表面没有受到任何污染。
(2)将试纸浸入待测溶液中,稍微晃动试纸,使其充分浸润。
(3)将试纸取出,并在光线充足的地方与标准色卡进行对照,确定溶液的PH 值范围。
2. PH计法(1)准备工作:校准PH计,按照仪器说明书进行操作。
(2)将PH计电极浸入待测溶液中,等待数秒,直到PH计稳定显示数值。
(3)记录PH计显示的数值,即为溶液的PH值。
四、实验注意事项1. 实验过程中要保持实验台面整洁,避免试纸受到污染。
2. PH试纸使用后要及时封好,防止受潮。
3. PH计使用前要进行校准,确保测量结果准确可靠。
4. 在使用PH计时,要注意电极的清洁和保养,避免损坏。
五、实验数据记录与处理根据实验步骤记录所测得的溶液PH值,并进行数据处理。
可以绘制PH值与时间的曲线图,分析溶液的酸碱性变化趋势。
六、实验结果分析根据实验数据和曲线图,分析溶液的酸碱性变化情况。
可以比较不同溶液的PH值,了解它们的酸碱度差异。
七、实验总结通过本实验,我们学习了PH值的概念和测定方法。
PH试纸法简便易行,适合于普通的PH值测定;PH计法准确可靠,适合于精确测定和实验研究。
纯化水检查记录表

纯化水检查记录表1. 介绍纯化水是指通过各种物理、化学和生物方法处理获得的除去大部分杂质和离子的水。
在实验室、制药、电子、化妆品等行业中,纯化水是一种重要的原料。
为了确保纯化水的质量符合需要,需要进行定期的检查和记录。
本文档将介绍纯化水检查记录表的使用方法以及填写要求。
2. 纯化水检查记录表使用方法下面是纯化水检查记录表的使用方法:2.1. 填写日期在记录表的顶部,有一个日期的填写位置,请在每次进行检查时填写当天的日期。
2.2. 填写负责人在记录表中,有一个负责人的填写位置,请填写进行检查的负责人的姓名。
2.3. 填写检查项目在表格的左侧列中,列出常见的纯化水检查项目,如水温、电导率、溶解氧、pH值等等。
根据实际需求,可以在列表中增加或删除项目。
2.4. 填写检查结果在表格的右侧列中,填写每个检查项目的具体数值或结果。
对于数值型的数据,可以直接填写测量的数值;对于结果型的数据,可以填写合格或不合格。
2.5. 填写备注在表格的最后一列,填写与每个检查项目相关的备注信息。
例如,检查中发现异常情况,可以在备注中说明具体原因,并记录下后续处理的情况。
2.6. 签字确认在记录表底部,有一个签字确认的位置,请填写进行检查的人员的签名和日期。
3. 纯化水检查记录表样例日期负责人水温(℃)电导率(μS/cm)溶解氧(mg/L)pH值备注2022-01-01 张三25.5 10 6.5 7.02022-01-02 李四26.0 12 7.0 7.22022-01-03 王五24.5 8 6.8 6.8 pH值偏低,进行调整处理4. 纯化水检查记录表填写要求为了保证纯化水检查记录的准确性和可读性,有以下填写要求:•日期的填写要正确无误,使用YYYY-MM-DD的格式。
•负责人的姓名填写清晰,确保负责人可以被准确识别。
•检查项目的填写要准确无误,确保所有重要的检查项目都被包括。
•每个检查项目的结果填写要清晰明确,使用数值或合格/不合格等方式表示。
