酸碱调节加药量计算
水处理调节ph值加药量计算

以NaOH控制PH值
参数
7.00
7.00
40 g/mol
1.00E-07 mol/l 1.00E-07 mol/l PH=
7.00
10.00%
0.0000 g/l
需反应的离子量
【H】 【H】加入 浓度 加药量
1.00E-07 mol/l 0.00E+00 mol/l PH=
5.00% 0.0000 g/l
PH(原始) PH(要求) H2SO4 【H】 【OH】 浓度 加药量
以H2SO4控制PH值
参数
7.00
7.00
98 g/mol
1.00E-07 mol/l 1.00E-07 mol/l PH=
7.00 需反应的离子量
5.00%
0.0001 g/l
PH(原始) PH(要求)
NaOH 【H】 【OH】 浓度 加药量
参数 7.00
7.00
36.5 g/mol 1.00E-07 mol/l 1.00E-07 mol/l PH= 7.00 需反应的离子量
10.00% 0.0000 g/l
合计加药量
PH(原始) PH(要求) CaOH 【H】 【OH】 浓度 加药量
0.0000 g/l PH由 7.00 到 7.00 的加药量 以Ca(OH)2控制PH值
参数 7.00
7.00
74 g/mol 1.00E-07 mol/l 1.00E-07 mol/l PH= 7.00 需反应的离子量
10.00% 0.0000 g/l
【H】 【H】加入 浓度 加药量
1.00E-07 mol/l 0.00E+00 mol/l PH=
10.00% 0.0000 g/l
盐酸调节ph的用量计算

盐酸调节ph的用量计算盐酸是一种常用的强酸,可以用于调节溶液的酸碱度,即pH值。
调节pH值是实验室和工业生产中常见的操作,下面我们来详细讨论一下如何计算盐酸的用量来调节pH。
首先,我们需要明确盐酸的浓度和目标pH值。
浓度通常以摩尔浓度来表示,单位为mol/L。
而pH值则表示溶液的酸碱性,数值范围从0到14,其中7为中性。
如果目标是调节酸性溶液的pH值较低,那么我们会选择添加盐酸来降低pH值;如果目标是调节碱性溶液的pH值较高,那么我们会选择添加盐酸来提高pH值。
接下来,我们需要使用两种酸碱反应的基本原理来计算盐酸的用量。
对于碱性溶液而言,比如氢氧化钠(NaOH)溶液,它可以被盐酸中的氢离子(H+)中和,形成水(H2O)和氯离子(Cl-)。
反应方程式可以表示为:NaOH+HCl→H2O+NaCl。
根据这个反应方程式,我们可以使用化学计量法来计算所需的盐酸用量。
首先,获取溶液的体积(单位为升)和浓度(单位为摩尔/升)。
假设我们需要调节的溶液体积为V1升,浓度为C1摩尔/升,目标pH值为pH2。
根据反应方程式,酸和碱的摩尔比为1:1,因此,我们可以得到下面的化学计量关系:C1V1=C2V2,其中C2是盐酸的浓度,V2是盐酸的体积。
然后,我们可以通过下面的公式计算所需的盐酸体积:V2=(C1V1)/C2。
最后,根据所得的盐酸体积和浓度,可以准确地计算出盐酸的用量。
需要注意的是,为了保证实验的准确性和安全性,应该根据具体实验情况进行必要的调整。
此外,还应掌握好盐酸的性质和操作要点,合理控制操作条件(比如温度、搅拌等)。
在实际操作中,我们可以使用称量法、滴定法等方法来控制盐酸的用量。
重要的是,我们需要不断调整实验条件和观察实验结果,以达到预期的pH值。
总而言之,盐酸调节pH的用量计算是一项重要的操作,在实验和工业生产中有着广泛的应用。
通过了解盐酸的性质和针对目标pH值的化学计量方法,我们可以准确地计算盐酸的用量,并进行相应的实验调节。
酸碱中和计算方式

碱性废水加盐酸调PH值,原水PH值是A,出水PH值是B,当B>7时,需要添加的盐酸量为:V×10A-14-10B-14×36.5kg/h,当B<7时,需要添加的盐酸量为:V×10B-14+10-A×36.5kg/hV:废水的流速m3/h;例如进水流速为45m3/h,PH为11,出水为8,PH用31%的盐酸来调节,则需要盐酸量为:45×10-3-10-6×÷31%=5.3kg/h进水流速为45m3/h,PH为8,出水为,PH用10%的盐酸来调节,则需要盐酸量为:45×10-6+×÷10%=1.64kg/h两溶液等积混合求溶液pH的规则的内容可叙述如下:两种强酸溶液,或两种强碱溶液,或一种强酸溶液与一种强碱溶液等体积混合,当两溶液的pH值之和为14时,混合液pH=7;当两溶液的pH值之和小于13时,混合液的pH值为原pH值小的加上;当两溶液的pH值之和大于15时,混合液的pH值为原pH值大的减去;若用pHA、pHB、pHC分别表示两种溶液及混合液的pH值,且pHA<pHB,当pHA+pHB=14时,pHC=7;当pHA+pHB<13时,则pHC=pHA+;当pHA+pHB>15时,则pHC=pHB-;规则的意义是弱者仅对强者起一个稀释作用,或者说,弱者是强者的陪衬;由于溶液的体积增加一倍,溶液的H+或OH-除2,实际上是lg2的值;因此,pH=2的盐酸与pH=6的盐酸等体积混合,或与pH =10的NaOH溶液等体积混合,以及用水稀释一倍,其结果都一样,pH 值都是;规则是一个近似规则;因为两种强酸或两种强碱溶液等体积混合时,若pH值相差1,混合液的pH值应是±;强酸、强碱混合,pH 值与pOH值相差1即pH值之合为13或15,应是±;若以上相差值小于1,误差就更大;另外,这一规律只适用于强酸、强碱,不适用于弱酸合弱碱;是等体积混合,而非不等体积混合;。
乙酸钠加药量计算12024

乙酸钠加药量计算引言概述:乙酸钠是一种常用的化工原料,广泛应用于制药、化妆品、染料等领域。
在实际生产过程中,乙酸钠的加药量计算是一个重要的环节,直接影响产品质量和生产效益。
本文将从化学反应原理、计算方法以及实际操作中的注意事项等方面,详细阐述乙酸钠加药量计算的相关知识。
正文内容:1.化学反应原理乙酸钠是由乙酸和钠离子反应的化合物。
乙酸和钠离子在水溶液中发生酸碱中和反应,乙酸钠和水,化学方程式如下:CH3COOH+Na+→CH3COONa+H2O根据化学方程式,可以得知乙酸钠的摩尔比为1:1。
2.计算方法乙酸钠加药量的计算可以根据所需的乙酸的摩尔数来确定。
需要知道所需乙酸的摩尔质量和目标乙酸浓度。
根据所需乙酸的摩尔数和酸碱中和反应的化学方程式,可以推算出所需乙酸钠的摩尔数。
通过乙酸钠的摩尔质量,计算出对应的质量或体积加药量。
3.实际操作中的注意事项a.定量加药:根据计算得出的乙酸钠加药量,需要准确地称取或分装,避免过量或不足。
b.溶解度限制:乙酸钠在水中的溶解度有限,加药量过大可能导致残留固体。
c.液相反应:乙酸钠加入反应体系后,需要充分搅拌溶解,确保反应均匀进行。
d.溶液浓度监控:实际操作中,可通过浓度计等设备对乙酸钠溶液进行实时监测,确保加药量的准确性。
4.乙酸钠加药量计算中的常见问题a.批量大小:乙酸钠加药量的计算应考虑批量大小的影响,即根据不同批量大小计算出相应的加药量。
b.偏差分析:在实际操作中,可能会存在一些因素导致计算结果与实际情况存在偏差。
因此,需要对加药量的准确性进行偏差分析,找出导致偏差的原因并予以调整。
c.设备选择:乙酸钠的加药量计算需要考虑使用的设备,不同设备的操作方法和测量误差可能会对计算结果产生影响。
5.乙酸钠加药量计算的实际应用乙酸钠加药量计算在生产实际中具有重要的应用价值。
它可以帮助生产单位根据所需乙酸的摩尔数,计算出相应的乙酸钠加药量,从而控制产品质量。
在药物制剂中,乙酸钠加药量计算也起着关键的作用,影响着药物的溶解性和稳定性。
酸碱中和计算方式

碱性废水加盐酸调PH值,原水PH值是A,出水PH值是B,当B>7时,需要添加的盐酸量为:V×(10A-14-10B-14)×36.5kg/h,当B<7时,需要添加的盐酸量为:V×(10B-14+10-A) ×36.5kg/h V:废水的流速m3/h;例如进水流速为45m3/h,PH为11,出水为8,PH用31%的盐酸来调节,则需要盐酸量为:45×(10-3-10-6)×36.5÷31%=5.3kg/h 进水流速为45m3/h,PH为8,出水为6.5,PH用10%的盐酸来调节,则需要盐酸量为:45×(10-6+10-6.5)×36.5÷10%=1.64kg/h两溶液等积混合求溶液pH的0.3规则的内容可叙述如下:两种强酸溶液,或两种强碱溶液,或一种强酸溶液与一种强碱溶液等体积混合,当两溶液的pH值之和为14时,混合液pH=7;当两溶液的pH值之和小于13时,混合液的pH值为原pH 值小的加上0.3;当两溶液的pH值之和大于15时,混合液的pH值为原pH 值大的减去0.3。
若用pHA、pHB、pHC分别表示两种溶液及混合液的pH值,且pHA<pHB,当pHA+pHB=14时,pHC=7;当pHA+pHB<13时,则pHC=pHA+0.3;当pHA+pHB>15时,则pHC=pHB-0.3。
0.3规则的意义是弱者仅对强者起一个稀释作用,或者说,弱者是强者的陪衬。
由于溶液的体积增加一倍,溶液的[H+]或[OH-]除2,0.3实际上是lg2的值。
因此,pH=2的盐酸与pH=6的盐酸等体积混合,或与pH=10的NaOH溶液等体积混合,以及用水稀释一倍,其结果都一样,pH值都是2.3。
0.3规则是一个近似规则。
因为两种强酸或两种强碱溶液等体积混合时,若pH值相差1,混合液的pH值应是±0.26;强酸、强碱混合,pH值与pOH值相差1(即pH值之合为13或15),应是±0.35;若以上相差值小于1,误差就更大。
PH值调节酸碱量计算方法

PH值调节酸碱量计算方法
PH值调节酸碱量根据pH计算出液体中H+的浓度(OH-的浓度也可以得出)根据液体的体积,可以计算出H+的物质的量(同样OH-的物质的量也可以得出)再根据你要调节到的pH时的H+浓度,就可以计算需要用酸或碱的量,前提是你要知道你用的酸或碱的浓度。例如:你测得一样品的pH为1,体积为1L。需要将其调节到pH=2时,问理论上需要1mol/L的NaO H多少毫升?计算时:pH=1,则C(H+)=0.1mol/L。体积为1L,则H+的物质的量为0. 1mol。pH=2时,C (H+)=0.01mol/L。设需要1mol/L的NaOH体积为XL,列式(0.1 mol-1mol/L*X)/(1+X)=0.01mol/L 解得,X=0.089L 即需要1mol/L 的NaOH89mL。
加药计算方式

各种加药计算1. 浓联氨的需用量的计算:N2H4= c*d*v*1000/w (kg)式中:c——欲配溶液的百分比浓度d——所配制溶液的比重(稀联氨溶液可取1.0g/m3)v——所配稀联氨溶液体积m3w——浓联氨的百分比浓度(一般为40%)2.一般是程序控制,连续加入.1. 氢氧化钠和碳酸钠加药量的计算(1) 空锅上水时给水所需加碱量X1=(YD-JD +JD+ JDGMV式中:X1 一一空锅上水时, 需加NaOH 或Na2C03 的量,g;YD 一一给水总硬度,mmol/L;JD 一一给水总碱度,mmol/L;JDG 一一锅水需维持的碱度,mmol/L;V 一一锅炉水容量,m3;M 一一碱性药剂摩尔质量; 用NaOH 为40 g/mol, 用Na2C03 为53g/mol 。
(2) 锅炉运行时给水所需加碱量1) 对于非碱性水可按下式计算X2=(YD-JD +JDGP)M式中:X2 一一每吨给水中需加NaOH 或Na2C03 的量,g/t;PL 一锅炉排污率,10-2;其余符号同上式。
如果NaOH 和NazC03 同时使用时, 则在上述各公式中应分别乘以其各自所占的质量分数, 如NaOH 的用量占总碱量的η×10-2, 则Na2C03 占(1-η)×10-2 , 两者的比例应根据给水水质而定。
一般对于高硬度水、碳酸盐硬度高或续硬度高的水质宜多用NaOH, 而对于以非碳酸盐硬度为主的水质, 应以Na2C03 为主, 少加或不加NaOH 。
2) 对于碱性水, 也可按上式计算, 但如果当JDG 以标准允许的最高值代入后, 计算结果出现负值, 则说明原水钠钾碱度较高, 将会引起锅水碱度超标, 宜采用偏酸性药剂, 如Na2HP04 、NaHJ04 等。
2. 磷酸三纳(Na3P04 ·12H20) 用量计算磷酸三纳在锅内处理软水剂中, 一般用来作水渣调解剂和消除残余硬度用。
当单独采用锅内水处理时, 加药量是按经验用量计算。
污水pH值调节药剂计算公式
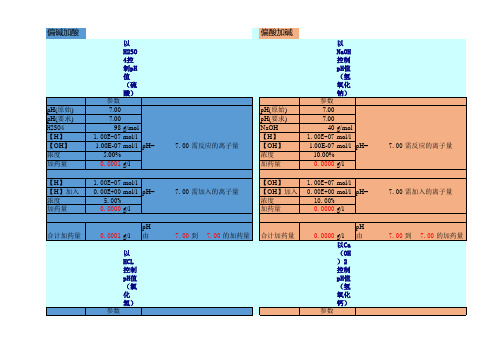
以 H2SO 4控 制pH 值 (硫 酸) 参数
7.00
7.00
98 g/mol 1.00E-07 mol/l
1.00E-07 mol/l pH=
5.00% 0.0001 g/l
【H】 【H】加入 浓度 加药量
1.00E-07 mol/l 0.00E+00 mol/l pH=
以Ca (OH )2 控制 pH值 (氢 氧化 钙) 参数
7.00 需反应的离子量 7.00 需加入的离子量 7.00 到 7.00 的加药量
pH(原始) pH(要求)
HCL 【H】 【OH】 浓度 加药量
7.00 7.00 36.5 g/mol 1.00E-07 mol/l 1.00E-07 mol/l pH= 10.00% 0.0000 g/l
10.00% 0.0000 g/l
7.00 需加入的离子量 7.00 到 7.00 的加药量
【OH】 【0H】加入 浓度 加药量
合计加药量
1.00E-07 mol/l 0.00E+00 mol/l pH=
10.00% 0.0000 g/l
pH 0.00004 g/l 由
7.00 需反应的离子量 7.00 需加入的离子量 7.00 到 7.00 的加药量
【H】 【H】加入 浓度 加药量
合计加药量
1.00E-07 mol/l 0.00E+00 mol/l pH=
10.00% 0.0000 g/l
pH 0.00004 g/l 由
7.00 需反应的离子量
pH(原始) pH(要求)
CaOH 【H】 【OH】 浓度 加药量
7.00 7.00
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
加药量计算
1、加碱量计算
一级反渗透产水按PH=5计算,需加碱将PH值调到9;
PH=5时,POH=14-5=9,OH-浓度为10-9mol/L;
PH=9时,POH=14-9=5,OH-浓度为10-5mol/L;
30%NaOH摩尔浓度约为10mol/L。
一级反渗透单套进水量按20m³/h计算,则每小时加药量为
(10-5mol/L-10-9mol/L)×20m³/h×1000
10mol/L
=0.02L/H。
稀释10倍则为0.2L/H。
加药泵选型为P056,流量为0-3.8L/H。
两套系统加药量为0.4L/H,按24小时,7天的用量计算,则药箱容积为:0.4×24×7=67.2L。
2、加氨量计算
EDI产水按PH=6计算,需加氨将PH值调到10;
PH=6时,POH=14-6=8,OH-浓度为10-8mol/L;
PH=10时,POH=14-10=4,OH-浓度为10-4mol/L;
28%液氨摩尔浓度约为15mol/L。
除盐水量按30m³/h计算,则每小时加药量为
(10-4mol/L-10-8mol/L)×30m³/h×1000
15mol/L
=0.2L/H。
稀释10倍则为2L/H。
加药泵选型为P056,流量为0-3.8L/H。
按24小时,7天的用量计算,则药箱容积为:2×24×7=336L。
