高中有机化学方程式总结 (1)
高中有机化学方程式总结(绝对全)

光照 光照 光照 光照 催化剂 催化剂 △ 催化剂 △浓硫酸 △催化剂 △ △NO 2 NO 2 O 2NCH 3 CH 3催化剂 H 2O 浓硫酸 140℃ OH BrBr Br OH 一、取代反应1. CH 4 + Cl 2 CH 3Cl + HCl2. CH 3Cl + Cl 2 CH 2Cl 2 + HCl3. CH 2Cl + Cl 2 CHCl 3 + HCl4. CHCl 3 + Cl 2 CCl 4+ HCl22. + HO -NO 2 NO 2 +H 2O 23. + HO -SO 3H SO 3H+H 2O25. +3HO -NO 2 +3H 2O28. CH 3CH 2Br + NaOH CH 3CH 2OH + NaBr33.C 2H 5OH+C 2H 5OH C 2H 5OC 2H 5+H 2O 37. +3Br 2 ↓ +3HBr二、加成反应8. CH 2 = CH 2 + Br 2 CH 2Br —CH 2Br9. CH 2 = CH 2 + H 2O CH 3CH 2OH10. CH 2 = CH 2 + HBr CH 3—CH 2Br 11. CH 2 = CH 2 + H 2 CH 3—CH 3 15. CH ≡CH + Br 2 CHBr = CHBr16. CHBr = CHBr+ Br 2 CHBr 2-CHBr 217. CH ≡CH + HCl H 2C = CHCl催化剂 催化剂醇 △催化剂 △催化剂 △ 浓硫酸 170℃ 催化剂 △△△ 催化剂 △24.+ 3H 238. CH 3CHO + H 2 CH 3CH 2OH三、加聚反应12. nCH 2 = CH 2 [ CH 2—CH 2 ] n13. nCH 2=CH-CH=CH 2 [CH 2-CH=CH-CH 2] n18. nCH 2 = CH [ CH 2-CH ] nCl Cl四、消去反应29. CH 3CH 2Br+ NaOH CH 2 = CH 2 ↑+ NaBr +H 2O32. CH 3CH 2OH CH 2 = CH 2↑+ H 2O五、置换反应30. 2CH 3CH 2OH+2Na 2CH 3CH 2ONa + H 2↑42. 2CH 3COOH+2Na 2CH 3COONa+H 2↑六、氧化反应39. 2CH 3CHO + O 2 2CH 3COOH40. CH 3CHO+2Ag(NH 3)2OH CH 3COONH 4+2Ag ↓+3NH 3+H 2O41CH 3CHO+2Cu(OH)2 CH 3COOH+Cu 2O ↓+2H 2O31. 2CH 3CH 2OH+O 2 2CH 3CHO + 2H 2O浓硫酸 △ 七、复分解反应34. OH+NaOH ONa+H 2O36. ONa+H 2O+CO 2 OH+ NaHCO 343.2CH 3COOH+Na 2CO 3 2CH 3COONa+H 2O+CO 2↑44. CH 3COOH+NaHCO 3 CH 3COONa+H 2O+CO 2↑45. CH 3COOH + NaOH CH 3COONa + H 2O46. 2CH 3COOH + Cu(OH)2 (CH 3COO)2Cu + 2H 2O八、酯化反应47.CH 3COOH+CH 3CH 2OH CH 3COOCH 2CH 3 +H 2O 九、水解反应48. CH 3COOCH 2CH 3+NaOH CH 3COONa+CH 3CH 2OH十、缩聚反应49. nOHCH 2CH 2COO H → [ OCH 2CH 2C ] n +H 2O高中有机化学知识点总结1.需水浴加热的反应有:(1)、银镜反应(2)、乙酸乙酯的水解(3)苯的硝化(4)糖的水解(5)、酚醛树脂的制取(6)固体溶解度的测定凡是在不高于100℃的条件下反应,均可用水浴加热,其优点:温度变化平稳,不会大起大落,有利于反应的进行。
高中化学方程式(烃、卤代烃、醇、苯、醛)

有机化学方程式总结一、烃1.甲烷烷烃通式:(1)氧化反应甲烷的燃烧:。
甲烷不可使酸性高锰酸钾溶液及溴水褪色。
(2)取代反应一氯甲烷:CH4+Cl2。
二氯甲烷:CH3Cl+Cl2。
三氯甲烷:CH2Cl2+Cl2。
四氯化碳:CHCl3+Cl2。
2.乙烯乙烯的制取:。
烯烃通式:(1)氧化反应乙烯的燃烧:乙烯可以使酸性高锰酸钾溶液褪色,发生氧化反应。
(2)加成反应(3)聚合反应乙烯加聚,生成聚乙烯:。
3.乙炔乙炔的制取:。
炔烃的通式:。
(1)氧化反应乙炔的燃烧:。
乙炔可以使酸性高锰酸钾溶液褪色,发生氧化反应。
(2)加成反应图1 乙烯的制取图2 乙炔的制取与溴水加成:HC CH+Br 2CHBr=CHBr+Br 2与氢气加成:与氯化氢加成:(3)聚合反应氯乙烯加聚,得到聚氯乙烯: 。
乙炔加聚,得到聚乙炔: 。
4.苯苯的同系物通式:(1)氧化反应苯的燃烧: 。
苯不能使溴水和酸性高锰酸钾溶液褪色。
(2)取代反应①苯与溴反应②硝化反应(3)加成反应5.甲苯(1)氧化反应甲苯的燃烧: 。
甲苯不能使溴水褪色,但可以使酸性高锰酸钾溶液褪色。
(2)取代反应(与HNO 3)甲苯硝化反应生成2,4,6-三硝基甲苯,简称 ,又叫 ,是一种 色晶体,不溶于水。
它是一种 ,广泛用于 。
注意:甲苯在光照条件下发生侧链的取代,而在催化剂条件下发生苯环上的取代。
注意:制取乙烯、乙炔均用排水法收集;乙烯、乙炔的加成反应(3)加成反应二、烃的衍生物6.溴乙烷纯净的溴乙烷是 ,沸点 ,密度比水 。
(1)取代反应溴乙烷的水解: 。
(2)消去反应:。
7.乙醇(1)取代反应:①与钠反应 。
②与HBr 反应 。
(2)氧化反应①催化剂催化氧化:②燃烧(3)消去反应C 2H 5OHC 2H 5-OH + OH-C 2H 58.苯酚苯酚是 ,露置在空气中会因 。
苯酚具有 气味,水中溶解度 ,易溶于 。
苯酚有 ,是一种重要的化工原料。
如果苯酚沾到皮肤上,应该用 处理。
高中有机化学方程式汇总(全)(已免费)

光照 光照 光照 光照 高温 CaO△ 催化剂加热、加压 催化剂催化剂△ 催化剂 △ 催化剂 催化剂催化剂 催化剂△ 催化剂催化剂浓硫酸△ △CH 3 NO 2O 2N CH 3催化剂△高中有機化學方程式匯總1. CH 4 + Cl 2 CH 3Cl + HCl2. CH 3Cl + Cl 2 CH 2Cl 2 + HCl3. CH 2Cl + Cl 2 CHCl 3 + HCl4. CHCl 3 + Cl 2 CCl 4+ HCl5. CH 4 C +2H 26. C 16H 34 C 8H 18 + C 8H 167. CH 3COONa + NaOH CH 4↑+ Na 2CO 38. CH 2 = CH 2 + Br 2 CH 2Br —CH 2Br9. CH 2 = CH 2 + H 2O CH 3CH 2OH10. CH 2 = CH 2 + HBr CH 3—CH 2Br11. CH 2 = CH 2 + H 2 CH 3—CH 312. nCH 2 = CH 2 [ CH 2—CH 2 ] n13. nCH 2=CH-CH=CH 2 [CH 2-CH=CH-CH 2] n14. 2CH 2 = CH 2 + O 2 2CH 3CHO15. CH ≡CH + Br 2 CHBr = CHBr16. CHBr = CHBr+ Br 2 CHBr 2-CHBr 217. CH ≡CH + HCl H 2C = CHCl18. nCH 2 = CH [ CH 2-CH ] nCl Cl19. CH ≡CH + H 2O CH 3CHO20. CaC 2 + 2H 2O CH ≡CH ↑+ Ca(OH)221. + Br 2 Br + HBr22. + HO -NO 2 NO 2 +H 2O23. + HO -SO 3H SO 3H+H 2O24. + 3H 2催化剂NaOH H 2O 醇△ 催化剂 △ 浓硫酸 170℃ 浓硫酸140℃OH Br Br OH 催化剂 △ 催化剂△△ △ 浓硫酸△ Br25. +3HO -NO 2 +3H 2O26. 3CH ≡CH →27. CH 3CH 2Br + H 2O CH 3CH 2OH + HBr28. CH 3CH 2Br + NaOH CH 3CH 2OH + NaBr29. CH 3CH 2Br+ NaOH CH 2 = CH 2 + NaBr +H 2O30. 2CH 3CH 2OH+2Na 2CH 3CH 2ONa + H 2↑31. 2CH 3CH 2OH+O 2 2CH 3CHO + 2H 2O 32. CH 3CH 2OH CH 2 = CH 2↑+ H 2O 33.C 2H 5OH+C 2H 5OH C 2H 5OC 2H 5+H 2O 34. OH+NaOH ONa+H 2O35. OH+H 2O O -+H 3O +36. ONa+H 2O+CO 2 OH+ NaHCO 337. +3Br 2 ↓ +3HBr 38. CH 3CHO + H 2 CH 3CH 2OH39. 2CH 3CHO + O 2 2CH 3COOH 40. CH 3CHO+2Ag(NH 3)2OH CH 3COONH 4+2Ag ↓+3NH 3+H 2O41CH 3CHO+2Cu(OH)2 CH 3COOH+Cu 2O ↓+2H 2O 42. 2CH 3COOH+2Na 2CH 3COONa+H 2↑43.2CH 3COOH+Na 2CO 3 2CH 3COONa+H 2O+CO 2↑44. CH 3COOH+NaHCO 3 CH 3COONa+H 2O+CO 2↑45. CH 3COOH + NaOH CH 3COONa + H 2O46. 2CH 3COOH + Cu(OH)2 (CH 3COO)2Cu + 2H 2O47.CH 3COOH+CH 3CH 2OH CH 3COOCH 2CH 3 +H 2O 48. CH 3COOCH 2CH 3+NaOH CH 3COONa+CH 3CH 2OH催化剂催化剂催化剂催化剂催化剂△催化剂加热、加压+ 浓硫酸△+ 2H2O O OC — CO OCH2-CH249. nOHCH2CH2COOH→ [ OCH2CH2C ] n +H2O50. C6H12O6 (s)+ 6O2 (g)6CO2 (g)+ 6H2O(l)51. C6H12O62CH3CH2OH + 2CO252. C12H22O11+H2O C6H12O6+ C6H12O6蔗糖葡萄糖果糖53. C12H22O11+ H2O2C6H12O6麦芽唐葡萄糖54. (C6H10O5)n+ nH2O n C6H12O6淀粉葡萄糖55. (C6H10O5)n+ nH2O n C6H12O6纤维素葡萄糖56.C17H33COO-CH2 C17H35COO-CH2C17H33COO-CH +3H2 C17H35COO-CHC17H33COO-CH2 C17H35COO-CH2 57. C17H35COO-CH2 CH2-OH C17H35COO-CH +3NaOH 3C17H35COONa+ CH-OHC17H35COO-CH2 CH2-OH 58. CH2OH COOHCH2OH COOH1.HClClCHClCH+−→−+324光2.3.4.5.6.7.8.9.10.11.12.13.14.15.16.17.18.19.20.21.高中有机化学知识点总结1.需水浴加热的反应有:(1)、银镜反应(2)、乙酸乙酯的水解(3)苯的硝化(4)糖的水解(5)、酚醛树脂的制取(6)固体溶解度的测定凡是在不高于100℃的条件下反应,均可用水浴加热,其优点:温度变化平稳,不会大起大落,有利于反应的进行。
高中有机化学方程式总结(绝对全)

高中有机化学方程式总结(绝对全)高中有机化学方程式总结(肯定全)1.CH4+Cl2光照CH3Cl+HCl2.CH3Cl+Cl2CH2Cl2+HCl3.CH2Cl+Cl2CHCl3+HCl4.CHCl3+Cl2CC l4+HCl5.CH4高温C+2H26.C16H34C8H18+C8H16加热、加压催化剂光照光照光照7.CH3COONa+NaOHCaOCH4↑+Na2CO3△8.CH2=CH2+Br2CH2BrCH2Br9.CH2=CH2+H2OCH3CH2OHCHCHBr10.CH2=CH2+HBr催化剂32△催化剂11.CH2=CH2+H2催化剂CH3CH3△催化剂12.nCH2=CH2[CH2CH2]n13.nCH2=CH-CH=CH2[CH2-CH=CH-CH2]n14.2CH2=CH2+O22CH3CHO15.CH≡CH+Br2CHBr=CHBr16.CHBr=CHBr+Br2CHBr2-CHBr217.CH≡CH+HCl催化剂△H2C=CHCl18.nCH2=CH[CH2-CH]nClCl19.CH≡CH+H2O催化剂CH3CHO20.CaC2+2H2OCH≡CH↑+Ca(OH)221.+Br2Br+HBr22.+HO-NO2浓硫酸NO2+H2O△催化剂催化剂催化剂23.+HO-SO3HSO3H+H2O24.CH3O2N+3H2催化剂△CH3NO2NO2△25.+3HO-NO2催化剂+3H2O26.3CH≡CH→27.CH3CH2Br+H2OCH3CH2OH+HBr28.CH3CH2Br+NaOHCH3CH2OH+NaBr29.CH3 CH2Br+NaOH醇CH2=CH2+NaBr+H2O△H2ONaOH30.2CH3CH2OH+2Na2CH3CH2ONa+H2↑31.2CH3CH2OH+O2催化剂2CH3CHO+2H2O△32.CH3CH2OH浓硫酸CH2=CH2↑+H2O170℃浓硫酸33.C2H5OH+C2H5OHC2H5OC2H5+H2O140℃34.OH+NaOHONa+H2O35.OH+H2OO-+H3O+36.ONa+H2O+CO2OH+NaHCO3OHOHBr37.+3Br2Br↓+3HBrBr38.CH3CHO+H2催化剂CH3CH2OH△39.2CH3CHO+O2催化剂2CH3COOH △40.CH3CHO+2Ag(NH3)2OHCH3COONH4+2Ag↓+3NH3+H2O41CH3CHO+2Cu(OH)2△CH3COOH+Cu2O↓+2H2O△42.2CH3COOH+2Na2CH3COONa+H2↑43.2CH3COOH+Na2CO32CH3COONa+H2O+CO2↑44.CH3COOH+NaHCO3CH3COONa+H2O+CO2↑45.CH3COOH+NaOHCH3COONa+H2O46.2CH3COOH+Cu(OH)2(CH3COO)2Cu+2H2O浓硫酸△47.CH3COOH+CH3CH2OHCH3COOCH2CH3+H2O48.CH3COOCH2CH3+NaOHCH3COONa+CH3CH2OH49.nOHCH2CH2COOH→[OCH2CH2C]n+H2O50.C6H12O6(s)+6O2(g)6CO2(g)+6H2O(l)51.C6H12O6催化剂2CH3CH2OH+2CO252.C12H22O11+H2O催化剂C6H12O6+C6H12O6蔗糖葡萄糖果糖53.C12H22O11+H2O催化剂2C6H12O6麦芽唐葡萄糖54.(C6H10O5)n+nH2O催化剂nC6H12O6淀粉葡萄糖55.(C6H10O5)n+nH2O催化剂nC6H12O6△纤维素葡萄糖56.C17H33COO-CH2C17H35COO-CH2催化剂C17H33COO-CH+3H2C17H35COO-CH加热、加压C17H33COO-CH2C17H35COO-CH257.C17H35COO-CH2CH2-OHC17H35COO-CH+3N aOH3C17H35COONa+CH-OHC17H35COO-CH2OCH2-OHO58.CH2OHCOOH浓硫酸+ CH2OHCOOH△CCOO+2H2OCH2-CH21.CH4Cl2CH3ClHCl光CH3ClCl2CH2Cl2HCl光2.3.4.5.6.7.8.CH2CHCHCH2Br29.10.11.12.13.14.15.16.17.HOCH2(CHOH)4CHO2Ag(NH3)2OHHOCH2(CHOH)4COONH42Ag3NH3H2O18.19.20.21.高中有机化学学问点总结1.需水浴加热的反应有:(1)、银镜反应(2)、乙酸乙酯的水解(3)苯的硝化(4)糖的水解(5)、酚醛树脂的制取(6)固体溶解度的测定凡是在不高于100℃的条件下反应,均可用水浴加热,其优点:温度变化平稳,不会大起大落,有利于反应的进行。
(完美版)高中有机化学方程式总结

高中有机化学方程式总结一、烃1.甲烷烷烃通式:C n H 2n -2(1)氧化反应 甲烷的燃烧:CH 4+2O 2 CO 2+2H 2O 甲烷不可使酸性高锰酸钾溶液及溴水褪色。
(2)取代反应 一氯甲烷:CH 4+Cl 2 CH 3Cl+HCl 二氯甲烷:CH 3Cl+Cl 2CH 2Cl 2+HCl 三氯甲烷:CH 2Cl 2+Cl 2 CHCl 3+HCl (CHCl 3又叫氯仿) 四氯化碳:CHCl 3+Cl 2 CCl 4+HClCH4 C +2H 2(3)裂化反应C 16H 34 C 8H 18 + C 8H 162.乙烯 乙烯的制取:CH 3CH 2OH H 2C=CH 2↑+H 2O 烯烃通式:C n H 2n(1)氧化反应 乙烯的燃烧:H 2C=CH 2+3O 2 2CO 2+2H 2O乙烯可以使酸性高锰酸钾溶液褪色,发生氧化反应。
(2)加成反应 与溴水加成:H 2C=CH 2+Br 2 CH 2Br —CH 2Br 与氢气加成:H 2C=CH 2+H 2 CH 3CH 3 与氯化氢加成: H 2C=CH 2+HCl CH 3CH 2Cl 与水加成:H 2C=CH 2+H 2O CH 3CH 2OH (3)聚合反应 乙烯加聚,生成聚乙烯:n H 2C=CH n(氢加氢多)丙烯的加成CH 2=CH -CH 3+HBrCH 2-CH -CH 3 主要产物| |H BrCH 2-CH -CH 3| |Br H点燃 光 光 光 光 浓硫酸 170℃高温 催化剂 △ 2-CH 2 图1 乙烯的制取 图2 乙炔的制取高温 高温 催化剂加热3.乙炔乙炔的制取:CaC 2+2H 2O ≡CH ↑+Ca(OH)2(1)氧化反应 乙炔的燃烧:HC ≡CH+5O 24CO 2+2H 2O乙炔可以使酸性高锰酸钾溶液褪色,发生氧化反应。
(2)加成反应与溴水加成:HC ≡CH+Br 2 HC=CHCHBr=CHBr+Br 2CHBr 2—CHBr 2与氢气加成:HC ≡CH+H 2 H 2C=CH 2与氯化氢加成:HC ≡CH+HCl CH 2=CHCl(3)聚合反应 氯乙烯加聚,得到聚氯乙烯:n CH 2n乙炔加聚,得到聚乙炔:n HC ≡ n4.苯 苯的同系物通式:C n H 2n-6(1)氧化反应苯的燃烧:2C 6H 6+15O 2 12CO 2+6H 2O 苯不能使溴水和酸性高锰酸钾溶液褪色。
高中有机化学方程式总结(默写版)

高中有机化学方程式总结(默写版) 高中有机化学方程式默写一、烃1.甲烷烷烃通式:1) 氧化反应甲烷燃烧产生二氧化碳和水:CH4 + 2O2 -。
CO2 + 2H2O甲烷不能使酸性高锰酸钾溶液和溴水褪色。
2) 取代反应一氯甲烷:CH3Cl二氯甲烷:CH2Cl2三氯甲烷:CHCl3四氯化碳:CCl42.乙烯烯烃通式:乙烯的制取:1) 氧化反应乙烯燃烧产生二氧化碳和水:C2H4 + 3O2 -。
2CO2 + 2H2O乙烯能使酸性高锰酸钾溶液褪色。
2) 加成反应与溴水加成:C2H4 + Br2 -。
C2H4Br2 与氢气加成:C2H4 + H2 -。
C2H6与氯化氢加成:C2H4 + HCl -。
C2H5Cl 与水加成:C2H4 + H2O -。
C2H5OH 3) 聚合反应乙烯加聚,生成聚乙烯。
3.乙炔乙炔的制取:1) 氧化反应乙炔燃烧产生二氧化碳和水:C2H2 + 5/2O2 -。
2CO2 + H2O乙炔不能使酸性高锰酸钾溶液褪色。
2) 加成反应与溴水加成:C2H2 + Br2 -。
C2H2Br2与氢气加成:C2H2 + H2 -。
C2H4与氯化氢加成:C2H2 + HCl -。
C2H3Cl3) 聚合反应氯乙烯加聚,得到聚氯乙烯。
乙炔加聚,得到聚乙炔。
4.苯苯的同系物通式:1) 氧化反应苯燃烧产生二氧化碳和水:2C6H6 + 15O2 -。
12CO2 + 6H2O苯能使溴水和酸性高锰酸钾溶液褪色。
2) 取代反应①苯与溴反应②硝化反应3) 加成反应5.甲苯1) 氧化反应甲苯燃烧产生二氧化碳和水:C7H8 + 9O2 -。
7CO2 + 4H2O甲苯能使溴水褪色和酸性高锰酸钾溶液褪色。
2) 取代反应甲苯硝化反应生成2,4,6-三硝基甲苯,简称三硝基甲苯(TNT)。
二、烃的衍生物烃的衍生物的重要类别和主要化学性质:类别通式代表性物质分子结构特点主要化学性质卤代烃 R—X 溴乙烷 C-X键有极性,易断裂 1.取代反应 2.消去反应醇 R—OH 乙醇有C-O键和O-H键,有极性;-OH与链烃基直接相连 1.与钠反应,生成醇钠并放出氢气 2.氧化反应:生成乙醛 3.脱水反应:乙醚、乙烯 4.酯化反应酚 -OH 苯酚 -OH直接与苯环相连取代反应醛 O || CH3-C-H C=O双键有极性,具有不饱和性氧化反应:生成酮羧酸 COOH 乙酸有C=O双键和C-OH单键,有极性 1.与碱反应,生成盐 2.酯化反应酯 R-COOR' 乙酸乙酯 C=O双键和O-C单键,有极性 1.水解反应:生成醇和羧酸 2.酸催化下的加成反应注:删除了明显有问题的段落,对每段话进行了小幅度的改写。
高中有机化学反应方程式总结(较全)

高中有机化学反应方程式总结(较全)
简介
这份文档总结了高中有机化学中常见的反应方程式,旨在帮助学生更好地理解和记忆有机化学反应。
以下是一些常见的有机化学反应类型及其方程式。
1. 烷烃类反应
1.1 烷烃燃烧反应
烷烃 + 氧气→ 二氧化碳 + 水
例如:甲烷 + 氧气→ 二氧化碳 + 水
1.2 烷烃与卤素反应
烷烃 + 卤素→ 卤代烷 + 氢卤酸
例如:甲烷 + 溴→ 溴代甲烷 + 氢溴酸2. 烯烃类反应
2.1 烯烃与卤素反应
烯烃 + 卤素→ 二卤代烷
例如:乙烯 + 光→ 过氧化氢 + 氯乙烷3. 醇类反应
3.1 醇脱水反应
醇→ 烯烃 + 水
例如:乙醇→ 乙烯 + 水
3.2 醇氧化反应
醇 + 氧气→ 酮/醛 + 水
例如:乙醇 + 氧气→ 乙酸 + 水
4. 酮类反应
4.1 酮的高温还原反应
酮 + 还原剂→ 伯胺
例如:丙酮+ NaBH4 → 正丙胺
5. 羧酸类反应
5.1 羧酸与醇酸酐化反应
羧酸 + 醇酸酐→ 酯 + 水
例如:乙酸 + 乙酸酐→ 乙酸乙酯 + 水
5.2 羧酸与碱反应
羧酸 + 碱→ 盐 + 水
例如:乙酸 + 氢氧化钠→ 乙酸钠 + 水
6. 醛类反应
6.1 醛还原反应
醛 + 还原剂→ 一级醇
例如:乙醛+ NaBH4 → 乙醇
以上是高中有机化学反应方程式的一些简单总结。
更详细的反应方程式及反应条件请参考有机化学教材或咨询化学老师。
注意:文档中的所有反应方程式仅供参考,请在实验操作时遵循正确的操作规程和安全注意事项。
(完整版)高中有机化学方程式归纳
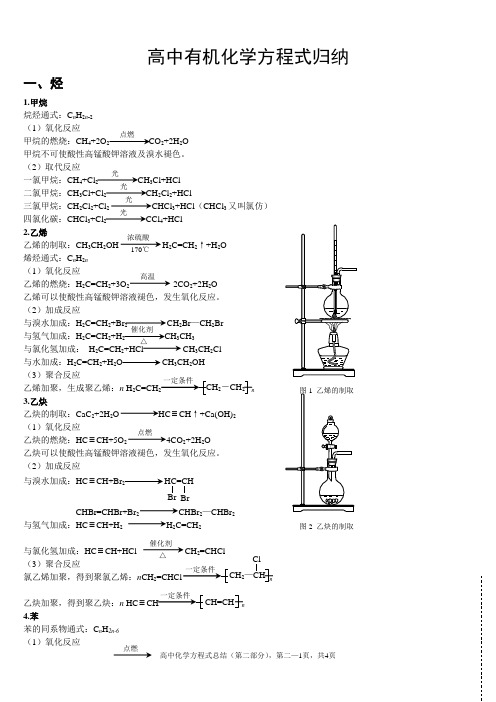
高中有机化学方程式归纳一、烃1.甲烷烷烃通式:C n H 2n -2 (1)氧化反应甲烷的燃烧:CH 4+2O 2 CO 2+2H 2O甲烷不可使酸性高锰酸钾溶液及溴水褪色。
(2)取代反应一氯甲烷:CH 4+Cl 2 CH 3Cl+HCl二氯甲烷:CH 3Cl+Cl 2CH 2Cl 2+HCl三氯甲烷:CH 2Cl 2+Cl 2 CHCl 3+HCl (CHCl 3又叫氯仿)四氯化碳:CHCl 3+Cl 2 CCl 4+HCl2.乙烯乙烯的制取:CH 3CH 2OH H 2C=CH 2↑+H 2O 烯烃通式:C n H 2n (1)氧化反应乙烯的燃烧:H 2C=CH 2+3O 2 2CO 2+2H 2O 乙烯可以使酸性高锰酸钾溶液褪色,发生氧化反应。
(2)加成反应与溴水加成:H 2C=CH 2+Br 2 CH 2Br —CH 2Br与氢气加成:H 2C=CH 2+H 2 CH 3CH 3与氯化氢加成: H 2C=CH 2+HCl CH 3CH 2Cl 与水加成:H 2C=CH 2+H 2O CH 3CH 2OH(3)聚合反应乙烯加聚,生成聚乙烯:n H 2C=CH n 3.乙炔乙炔的制取:CaC 2+2H 2O ≡CH ↑+Ca(OH)2 (1)氧化反应乙炔的燃烧:HC ≡CH+5O 2 4CO 2+2H 2O 乙炔可以使酸性高锰酸钾溶液褪色,发生氧化反应。
(2)加成反应与溴水加成:HC ≡CH+Br2HC=CHCHBr=CHBr+Br 2 CHBr 2—CHBr 2与氢气加成:HC ≡CH+H 2 H 2C=CH 2与氯化氢加成:HC ≡CH+HCl CH 2=CHCl(3)聚合反应氯乙烯加聚,得到聚氯乙烯:n CH 2 n乙炔加聚,得到聚乙炔:n HC ≡ n4.苯苯的同系物通式:C n H 2n-6 (1)氧化反应点燃光光光光浓硫酸170℃ 高温催化剂 △2-CH 2点燃图2 乙炔的制取催化剂△Br 2—CHClCH=CH苯的燃烧:2C 6H 6+15O 2 12CO 2+6H 2O 苯不能使溴水和酸性高锰酸钾溶液褪色。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
高中有机化学方程式总结 烷烃
C n H 2n+2+21
3n +O 2−−→−点燃nCO 2+(n+1)H 2O (n≥1) CH 4 + Cl 2−−→−光照CH 3Cl + HCl
CH 3Cl + Cl 2 −−→−光照CH 2Cl 2 + HCl
CH 2Cl + Cl 2−−→−光照CHCl 3 + HCl
CHCl 3 + Cl 2−−→−光照CCl 4+ HCl
CH 4−−→−︒C 1000 C +2H 2
CH 3COONa + NaOH −−−→−,△O C a CH 4↑+ Na 2CO 3(甲烷实验室制法)
烯烃
C n H 2n +23n
O 2−−→−点燃
nCO 2+nH 2O (烯烃,n≥2;环烷烃,n≥3) 2CH 2=CH 2 + O 2−−→−催化剂2CH 3CHO
CH 2=CH 2 + Br 2→CH 2BrCH 2Br
CH 2=CH 2 + H 2O −−→−催化剂CH 3CH 2OH
CH 2=CH 2 + HX −−−→−催化剂,△CH 3CH 2X
CH 2=CH 2 + H 2−−−→−催化剂,△CH 3CH 3
CH 3CH=CH 2+HCl −−−→−催化剂,△CH 2-CHCl-CH 3(马氏规则) CH 2=CH-CH=CH 2+H 2−−−→−催化剂,△CH 3-CH=CH-CH 3(1,4加成,主要) CH 2=CH-CH=CH 2+H 2−−−→−催化剂,△CH 3-CH 2-CH=CH 3(1,2加成,次要) nCH 2=CH 2−−→−催化剂-[CH 2-CH 2]- n
nCH 2=CH-CH=CH 2−−→−催化剂-[CH 2-CH=CH-CH 2]- n
CH 3CH 2OH −−−−→−︒C SO H 1704
2,浓CH 2=CH 2↑+ H 2O (乙烯实验室制法)
炔烃
C n H 2n-2+21
3n -O 2−−→−点燃nCO 2+(n-1)H 2O (炔烃,n≥2;二烯烃,n≥3) HC≡CH +Br 2→CHBr=CHBr ,CHBr=CHBr+Br 2→CBr 2CBr 2 CH≡CH + H 2−−→−催化剂CH 3CH 3
CH≡CH + H X −−−→−催化剂,△CH 2=CHX
CH≡CH + H 2O −−→−催化剂CH 3CHO
CH≡CH −−−−→−溶液酸性4
n O KM CO 2+H 2O n CH≡CH −−→−催化剂-[CH 2=CH 2]- n
CaC 2 + 2H 2O →CH≡CH↑+ Ca(OH)2(乙炔实验室制法)
苯及其同系物
C n H 2n-6+2
33n -O 2−
−→−点燃
nCO 2+(n-3)H 2O (
n≥6
) +Br 2−−−→
−3/FeBr Fe + HBr
+HO-NO 224H SO −−−−→浓+ H 2O (硝化)
+HO-SO 3H −−→
△+ H 2O (磺化) +3H 2−−−→−催化剂,△
+3H 2−−−→−催化剂,△
+3HO-NO 224H SO −−−−→浓+ 3H 2O
−−−−→−溶液酸性4n O KM (α-C 连有H )
卤代烃
CH 3CH 2Br + H 2O −−−→NaOH CH 3CH 2OH + HBr (卤代烃的水解)
CH 3CH 2Br + NaOH 2
H O −−−→CH 3CH 2OH + NaBr CH 3CH 2Br+ NaOH 32
−−−−−→CH CH OH ,△CH 2=CH 2↑ + NaBr +H 2O CH 3CH 2CHBrCH 3+NaOH 32
−−−−−→CH CH OH ,△CH 3CH=CHCH 3+NaBr+H 2O (扎依采夫规则)
醇
C n H 2n+2O+23n
O 2−−→−点燃
nCO 2+(n+1)H 2O (饱和一元醇、醚,n≥1)2CH 3CH 2OH+O 2−−−→−,△Ag Cu /2CH 3CHO + 2H 2O
2CH 3CHOHCH 3+O 2−−−→−,△Ag Cu /2 + 2H 2O
2CH 3CH 2OH+2Na→2CH 3CH 2ONa + H 2↑
CH 3CH 2ONa+ H 2O→C H 3CH 2OH+ NaOH (醇钠的水解)
CH 3CH 2OH −−−−→−︒C SO H 1704
2,浓CH 2=CH 2↑+ H 2O (分子内脱水,β-H ) 2CH 3CH 2OH −−−−→−︒C SO H 1404
2,浓CH 3CH 2-O-CH 2CH 3+ H 2O (分子间脱水) CH 3CH 2CHOHCH 3 −−−−→−,△浓4
2SO H CH 3CH=CHCH 3+H 2O (扎依采夫规则) ROH+HX −→−△RX+H 2O
CH 3COOH+ CH 3CH 2OH CH 3COOCH 2CH 3+H 2O
(三硝酸甘油酯,硝化甘油)酚
2+2Na→2+H2↑
+Na2CO3→+NaHCO3
+HCl→+NaCl
−
−
−→
−催化剂,△
(酚醛树脂)
醛、酮
C n H2n O+3n-1
2O2−
−→
−点燃nCO2+nH2O(饱和一元脂肪醛,n≥1;饱和一元脂肪
酮,n≥3;烯醇,环氧某烷)RCHO + H2−
−
−→
−催化剂,△RCH2OH
+ H2−
−
−→
−催化剂,△
2CH3CHO + O2−
−→
−催化剂,△2CH3COOH
−
CH3CHO+2Ag(NH3)2OH−→
−△CH3COONH4+2Ag↓+3NH3+H2O(银镜反应)
CH3CHO+2Cu(OH)2−→
−△CH3COOH+Cu2O↓+2H2O
HCHO+4Ag(NH3)2OH−→
−△(NH4)2CO3+4Ag↓+6NH3+2H2O
HCHO+4Cu(OH)2−→
−△H2CO3+2Cu2O↓+4H2O
羧酸、酯
2CH3COOH+2Na→2CH3COONa+H2↑
CH3COOH + NaOH→CH3COONa + H2O
2CH3COOH+Na2CO3→2CH3COONa+H2O+CO2↑
CH3COOH+NaHCO3→CH3COONa+H2O+CO2↑
CH3COOH+ CH3CH2OH CH3COOCH2CH3+H2O
CH3COOCH2CH3+NaOH−→
−△CH3COONa+CH3CH2OH
RCOOCH2
RCOOCH
2+3NaOH→3RCOONa +(皂化反应)
糖类
C6H12O6 + 6O2→6CO2 + 6H2
O
C6H12O6−−−→
酒化酶2CH3CH2OH + 2CO2。
