原子吸收光谱法
原子吸收光谱法

原子吸收光谱法1、原子吸收光谱的基本原理是什么,为什么采用锐线光源?答:原子吸收法是基于物质所产生的原子蒸气对特征谱线的吸收作用来进行定量分析的一种方法。
任何元素的原子都是由原子核和绕核运动的电子组成,原子核外电子按其能量的高低分层分布而形成不同的能级,因此,一个原子核可以具有多种能级状态。
能量最低的能级状态称为基态能级(E0=0),其余能级称为激发态能级,而能最低的激发态则称为第一激发态。
正常情况下,原子处于基态,核外电子在各自能量最低的轨道上运动。
如果将一定外界能量如光能提供给该基态原子,当外界光能量E恰好等于该基态原子中基态和某一较高能级之间的能级差ΔE时,该原子将吸收这一特征波长的光,外层电子由基态跃迁到相应的激发态,而产生原子吸收光谱。
核外电子从基态跃迁至第一激发态所吸收的谱线称为共振吸收线,简称共振线。
由于基态与第一激发态之间的能级差最小,电子跃迁几率最大,故共振吸收线最易产生。
对多数元素来讲,它是所有吸收线中最灵敏的,在原子吸收光谱分析中通常以共振线为吸收线。
若测定溶液中某金属的量,需先将金属离子化合物在高温下解离成原子蒸气,两种形态间存在定量关系。
光源发射出的特征波长光辐射通过原子蒸气时,原子中的外层电子吸收能量,使得特征谱线的光强度减弱。
光强度的变化符合朗伯-比耳定律,在此基础上再进行定量分析。
与分子光谱的带状光谱不同,原子吸收光谱理论上是线状光谱,但由于自然宽度、多普勒宽度、压力变宽、自吸变宽、场致变宽等,使得谱线具有一定的宽度。
从理论上来说,可以通过计算在吸收线轮廓内,吸收系数的积分称为积分吸收系数,简称为积分吸收,它表示吸收的全部能量。
但实际上,测定该值需要分辨率非常高的色散仪器,很难实现。
1955年澳大利亚学者沃尔森(Walsh) 提出,在温度不太高的稳定火焰条件下,峰值吸收系数与火焰中被测元素的原子浓度也正比。
因此,目前一般采用测量峰值吸收系数的方法代替测量积分吸收系数的方法。
原子吸收光谱

8
第三阶段 电热原子吸收光谱仪器的产生 1959年,苏联里沃夫发表了电热原子化技术的第一篇论 文。电热原子吸收光谱法的绝对灵敏度可达到10-12-10-14g, 使原子吸收光谱法向前发展了一步。近年来,塞曼效应和自 吸效应扣除背景技术的发展,使在很高的的背景下亦可顺利 地实现原子吸收测定。
(3) 压力变宽(Pressure effect) 又称为碰撞(Collisional broadening)变宽。它是由于碰撞使激发 态寿命变短所致。外加压力越大,浓度越大,变宽越显著。可分为
a) Lorentz 变宽:待测原子与其它原子之间的碰撞。变宽在10-3nm。
劳伦兹变宽用Δν表示,可表达为 :
单色光谱线很窄才有明显吸收! 若 103 nm 则 I / I 0 1, A 0 无法分析
23
对于分子的紫外-可见吸收光谱的测量,入射光是由单 色器色散的光束中用狭缝截取一段波长宽度为0.xnm至1.xnm 的光,这样宽度的光对于宽度为几十nm甚至上百nm的分子带 状光谱来说,是近乎单色了,它们对吸收的测量几乎没有影 响,当然入射光的单色性更差时,就会引起吸收定律的偏离。 而对于原子吸收光谱是宽度很窄的线状光谱来说,如果 还是采用类似分子吸收的方法测量,入射光的波长宽度将比 吸收光的宽度大得许多,原子吸收的光能量只作入射光总能 量的极小部分。这样测量误差所引起的对分析结果影响就很 大。这种关系如下图所示。
33
若吸收线轮廓单纯取决于多普勒变宽,则:
原子吸收光谱法
15:35
(2)谱线的热变宽 又称多普勒( Doppler )变宽,它是由于原子在空间 作热运动而引起的。
从物理学原理可知,从一个运动的原子发出的光,如果运动方 向离开观察者,则在观察者看来,其频率要比静止原子所发出 的光频率低,反之,如果原子向着观察者运动,则其频率要比 静止原子发出的光的频率高,这就是多普勒效应。 原子吸收分析法中,气体中的原子是处于无规则热运动中,有 的向着检测器方向运动,使光能增大,波长变短一点。有的背 向检测器运动,光能减弱,波长变长一点,一长一短,使谱线 变宽。这种频率分布和气体中原子的热运动的速度分布相符。
§5-1概述
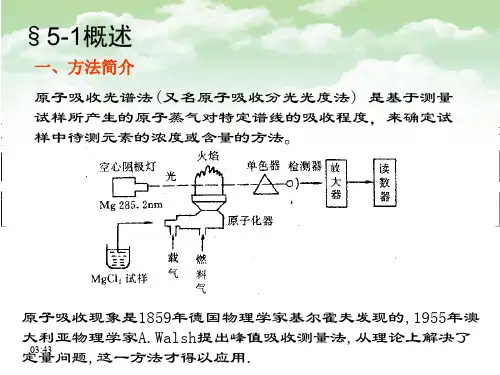
一、方法简介 原子吸收光谱法 (又名原子吸收分光光度法 ) 是基于测量 试样所产生的原子蒸气对特定谱线的吸收程度,来确定试 样中待测元素的浓度或含量的方法。
原子吸收现象是1859年德国物理学家基尔霍夫发现的,1955年澳 大利亚物理学家A.Walsh提出峰值吸收测量法,从理论上解决了 15:35 定量问题,这一方法才得以应用.
1.14 10 4
从以上计算可以看出,与基态原子数相比,激发态原子数可忽 略不计。
即 N0≈N总
由此我们可以得到结论: (1)基态原子数等于总原子数。
15:35 ( 2)原子吸收法受温度影响不大。
二、吸收轮廓及变宽原因 1.吸收轮廓 从能级跃迁的观点看,吸收线与发射线应是一条严格的几何线, 但实际上是有一定宽度的。我们把吸收线或发射线的强度按频 率的分布叫谱线轮廓。如图5-2所示。 图中最大吸收对应的 频率 ν 0 称为峰值吸收
15:35
§5-2 原子吸收法的基本原理 一、基态原子数与火焰温度的关系 根据热力学原理,在一定温度下达到热力学平衡状态时,基态 和激发态的原子数之比与热力学温度的关系,可以用玻尔茨曼公 式描述: E j E0
原子吸收光谱法(atomic absorption spectrometry,简称AAS)

双光束型:来自光源的光束被分 成两束,一束作测量光束,通过 火焰;另一束作参比光束;交替 进入单色器到达光电倍增管检测 比较
– 特点:消除因光源波动造成的影响,
但不能抵消因火焰波动造成的影响
完整版ppt
16
四、定量分析方法
1、标准曲线法:吸光度—浓度标准曲线
– 方法:
配制一组含有不同浓度被测元素的标准溶液 在与试样测定完全相同的条件下,按浓度由低到高的顺序测定吸 光度值 绘制吸光度对浓度的校准曲线。 测定试样的吸光度 查校准曲线上用内插法求出被测元素的含量。
完整版ppt
12
火焰原子化器和石墨炉原子化器可测定的元素
H Li Be Na Mg
火焰 火焰 & 石墨炉
He B C N O F Ne Al Si P S Cl Ar
K Ca Sc Ti V Cr Mn Fe Co Zn Cu Zn Ga Ge As Se Br Kr
Rb Sr Y Zr Nb Mo Tc Ru Rh Pd Ag Cd In Sn Sb Te I Xe
e- e-
e-
Dynode (9-13)
Quartz Window
*100 Million Amplification of Signal
Photomultiplier Tube Operation
三、原子吸收分光光度计
单光束型:空白溶液调透光率T 到100%。测试剂溶液的透射比
– 特点:仪器结构简单,不能消除因 光源波动造成的影响,基线漂移
完整版ppt
6
完整版ppt
7
原子化器
原子化:将试样转变为原子蒸汽的过程
原子化器的功能:提供能量使试样干燥、蒸 发和原子化。同时入射光束在这里被基态原 子吸收,因此也可把它视为“吸收池”。
原子吸收光谱法(AAS)

局限性:测不同的元素需不同的元 素灯,不能同时测多元素,难熔元 素、非金属元素测定困难。
原子吸收光谱法基本原理
1.原子的能级与跃迁
基态第一激发态,吸收一定频率的辐射能量。 产生共振吸收线(简称共振线) 吸收光谱 激发态基态,发射出一定频率的辐射。 产生共振吸收线(也简称共振线) 发射光谱
原子吸收光谱法基本原理
A kc
原子吸收分光度计
原子吸收分光度计
原子吸收分光度计
光源
原子化器
单色器
检测系统
思考:光学系统(单色器)为什么在原子化器和检 测系统之间?
光 源
提供待测元素的特征光谱。获得较高的 灵敏度和准确度。 光源应满足如下要求; (1)能发射待测元素的共振线; (2)能发射锐线; (3)辐射光强度大,稳定性好。
2.元素的特征谱线
(1)各种元素的原子结构和外层电子排布不同 基态第一激发态:
跃迁吸收能量不同——具有特征性。
(2)各种元素的基态第一激发态
最易发生,吸收最强,最灵敏线。特征谱线。
(3)利用原子蒸气对特征谱线的吸收可以进行定量分析
原子吸收光谱法基本原理
从光源发射出具有待测元素特征 谱线的光,通过试样蒸气时,被蒸气 中待测元素的基态原子所吸收,吸收 的程度与被测元素的含量成正比。故 可根据测得的吸光度,求得试样中被 测元素的含量。
将待测试样在专门的氢化物生成器中产生氢
化物,送入原子化器中检测。
单色器
•作用:将待测元素的吸收线与邻近线分开
•组件:色散元件 ( 棱镜、光栅 ) ,凹凸镜、 狭缝等
检测系统
•作用: 将待测元素光信号转换为电信号, 经放大数据处理显示结果。 •组件: 检测器、放大器、对数变换器、显 示记录装置。
第七章原子吸收光谱分析法

原子吸收光谱法(也称原子吸收分光光法 )与可 见、紫外分光光度法基本原理相同,都是基于物质 对光选择吸收而建立起来的光学分析法。
2010年1月25日1时53分
组成:阳极(吸气金属)、空心圆筒形(使待测原子集中)阴极(W+ 待测元素)、低压惰性气体(谱线简单、背景小)。
工作过程:高压直流电(300V)---阴极电子---撞击隋性原子---电离(二 次电子维持放电)---正离子---轰击阴极---待测原子溅射----聚集空 心阴极内被激发----待测元素特征共振发射线。
? 自然宽度(约在10-5nm数量级)。
?
?2.多普勒变宽(热变宽):
? 由于多普勒效应而导致的谱线 变宽。由于原子热运动引起的。 其宽度约为 10-3nm数量级。
?3.压力变宽:由于同类原子或 与其它粒子(分子、原子、离子、 电子等)相互碰撞而造成的吸收 谱线变宽。其宽度也约为 10-3nm 数量级。
区别:在可见、紫外分光光度法中,吸光物质 是溶液中被测物质的分子或离子对光的选择吸收, 原子吸收光谱法吸光物质是待测元素的基态原子对 光的选择吸收,这种光是由待测元素制成的空心阴 极灯(称元素灯)作光源。
原子吸收光谱分析的过程:
A元素含量测定----- A元素的空心阴极灯发射特征辐射 --------试样在原子化器中变为气态的基态原子-------吸收空心 阴极灯发射特征辐射---------空心阴极灯发射特征辐射减弱-----产生吸光度------元素定量分析
钨丝灯光源和氘灯,经分光后,光谱通带0.2nm。而原子吸收线
原子吸收光谱法
半宽度受原子性质和 外界因素的影响
原子吸收光谱轮廓图
基本原理
Basic principle
谱线变宽因素
自然宽度
Doppler变宽
压力变宽 自吸效应 场致变宽
基本原理
Basic principle 自然宽度(△nN) :无外界因素影响时谱线具有的宽度,与激
发态原子的平均寿命有关,平均寿命越长,谱线宽度越窄。根据量子力 学的测不准原理,粒子能级能量和跃迁时刻不可能同时测准,其能量的 不确定度△E和其跃迁时刻的不确定度△t间有如下关系
其中Kv为吸收系数
基本原理
Basic principle
• 吸收线轮廓
In I0
中心频率n0最大吸收系数 所对应的频率或波长,由 原子能级决定
不同元素原子吸收不同频率的 光,由图可见,在频率为v0处
透过光强度最小,也就是吸收
最大。原子群从基态跃迁到激
发态所吸收的谱线并不是绝对
单色,而是具有一定的宽度,
第七章 原子吸收分光光度法
Atomic Absorption Spectrometry
( AAS)
专业:环境工程 姓名:韩朝丽
原子吸收光谱法
Atomic Absorption Spectrometry
概 述 基本原理
本章内容
仪 器
干扰及其 消除办法
分析应用
原子吸收光谱法概述
Atomic Absorption Spectrometry
原子吸收光谱法——仪器
(Atomic Absorption Spectrometry)
原子吸收分 光光度计
光源
原子化系统
光学系统
检测系统
仪器分析 第七章 原子吸收光谱法
第七章原子吸收光谱法1.原子吸收光谱的历史2.原子吸收光谱的特点3.原子吸收光谱与紫外可见吸收光谱的区别4.原子吸收光谱分析过程第一节概述1. 原子吸收光谱的历史◆1802年,沃拉斯顿(Wollaston)在研究太阳连续光谱时,首次发现太阳连续光谱中出现暗线。
◆1817年,夫琅和费(Fraunhofer)研究太阳连续光谱时再次发现这些暗线,但无法解释暗线产生的原因。
2/1363/1361825年,法国著名哲学家孔德在哲学讲义中说“恒星的化学组成是人类绝对不能得到的知识”◆1859年,本生、基尔霍夫研究碱金属和碱土金属火焰光谱时,发现钠蒸气发出的光通过温度较低的钠蒸气时,会引起钠光的吸收,并且钠在光谱中位置相同。
发射线与暗线D◆太阳光谱暗线:太阳外围大气圈中钠原子对太阳光谱中钠辐射特征波长光进行吸收的结果。
4/1365/136太阳中含有94种稳定和放射性元素:氢(71%)、氮(27%)、氧、碳、氖、硅、铁等。
◆1955年,澳大利亚物理学家Walsh(沃尔什)发表了著名论文《原子吸收光谱法在分析化学中的应用》,奠定了原子吸收光谱法的基础。
◆1960年以后,原子吸收光谱法得到迅速发展,成为微量、痕量金属元素的可靠分析方法。
6/1362. 原子吸收光谱法的特点✓检出限低:10-10~10-14g。
✓准确度高:1%~5%。
✓选择性好:一般情况下共存元素无干扰。
✓应用范围广:可测定70多种元素。
✗缺点:难熔元素、非金属元素测定困难,不能实现多元素同时分析。
7/1363. 原子吸收与紫外可见吸收的区别✓相同点:利用物质对辐射的吸收进行分析。
✗不同点:◆吸收机理不同:紫外可见为溶液中分子或离子宽带吸收,带宽为几纳米至几十纳米;原子吸收为气态基态原子的窄带吸收,带宽仅为10-3nm。
◆光源不同。
◆试样处理、实验方法及对仪器的要求不同。
8/1364. 原子吸收光谱分析过程◆确定待测元素。
◆选择该元素相应锐线光源,发射出特征谱线。
仪器分析第五章原子吸收光谱法
仪器分析第五章原⼦吸收光谱法第五章原⼦吸收光谱法Chapter FiveAtomic Absorption SpectrumFor Short:AAS第⼀节基本原理⼀、原⼦吸收光谱分析概述1、原⼦吸收光谱的起源18世纪初,⼈们便开始观察和研究原⼦吸收光谱-----太阳光谱中的暗线。
1955年,澳⼤利亚物理学家⽡尔西发表了著名论⽂“原⼦吸收光谱在化学分析中的应⽤”,奠定了原⼦吸收光谱分析法的理论基础。
1955年,原⼦吸收光谱作为⼀种分析⽅法开始应⽤。
并在60年代得到迅速发展和普及。
2、什么是原⼦吸收光谱?溶液中的⾦属离⼦化合物在⾼温下能够解离成原⼦蒸⽓,两种形态间存在定量关系。
当光源发射出的特征波长光辐射通过原⼦蒸⽓时,原⼦中的外层电⼦吸收能量,特征谱线的光强度减弱。
光强度的变化符合朗伯-⽐⽿定律,进⾏定量分析。
它是基于物质所产⽣的原⼦蒸⽓对特征谱线的吸收作⽤来进⾏定量分析的⼀种⽅法。
原⼦与分⼦⼀样,吸收特定能量后,产⽣基态→激发态跃迁;产⽣原⼦吸收光谱,即共振吸收。
原⼦由基态→第⼀激发态的跃迁,最易发⽣。
每种原⼦的核外电⼦能级分布不同,当产⽣由基态→第⼀激发态的跃迁时,吸收特定频率的辐射能量。
⼆、共振线:共振吸收线——电⼦从基态跃迁⾄第⼀激发态所产⽣的吸收谱线称为共振吸收线(简称共振线)。
共振发射线——电⼦从第⼀激发态再跃回基态时,则发射出同样频率的辐射,对应的谱线称为共振发射线(也简称共振线)。
原⼦的共振线的吸收共振线称为元素的特征谱线,因为:各种元素的原⼦结构和外层电⼦排布不同。
所以不同元素的原⼦从基态激发成第⼀激发态(或由第⼀激发态跃回基态)时,吸收(或发射)的能量不同,因此各种元素的共振线各有其特征性。
共振线⼜称为元素的灵敏线,因为:这种从基态到第⼀激发态的跃迁最容易发⽣,因此对⼤多数元素来说,共振线是指元素所有谱线中最灵敏的谱线。
在原⼦吸收光度法中,就是利⽤处于基态的待测原⼦蒸⽓对从光源发射的共振发射线的吸收来进⾏分析的。
第十章 原子吸收光谱法
二、原子化系统
作用是将试样中待测元素转变成原子蒸气。 1.火焰原子化法 (1)雾化器:作用是将试样溶液雾化。当助
燃气高速通过时,在毛细管外壁与喷嘴口构 成的环形间隙中,形成负压区,将试样溶液 吸入,并被高速气流分散成气溶胶,在出口 与撞击球碰撞,进一步分散成微米级的细雾。 (2)混合室:作用是将未被细微化的较大雾 滴在混合室内凝结为液珠,沿室壁流入泄漏 管排走;并让气溶胶在室内与燃气充分混匀。
第十章 原子吸收光谱法
§10-1 §10-2 §10-3 §10-4 §10-5 §10-6
试题
概述 原子吸收法的基本原理 原子吸收分光光度计 定量分析方法 干扰及其抑制方法 灵敏度与检出限
1
§10-1 概述
一、 原子吸收光谱法
原子吸收光谱是利用待测元素的原子蒸 气中基态原子对特征电磁辐射(共振线)的吸 收来测定的。
式中ν0为谱线中心频率;M 为吸光原子的相对 原子质量;T 为绝对温度。 ΔνD约10-3数量
级,是谱线变宽的主要原因。 3.碰撞变宽(压力变宽) 由于原子相互碰撞使能量发生轻微变化。
劳伦兹变宽ΔνL :待测原子和其他原子碰撞引
起的谱线变宽。
ΔνL约10-3数量级,是碰撞变宽的主要因素。
10
赫鲁兹马克变宽ΔνH :同种原子碰撞引起的
29
二、标准加入法
取若干份体积相同的试液(cX),依次按比 例加入不同量的待测物的标准溶液(cO), 定容后浓度依次为:cX、cX+cO、cX+2cO、 cX+3cO、cX+4cO,分别测得吸光度为:A0、 A1、A2、A3、A4。以A对浓度c做图得一直 线,图中cX点即待测溶液浓度。
30
注意: 1.本法只能消除基体效应带来的干扰,不能消
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
发射线
吸收线
K
0
1、光源的能量能被原子充分吸收,测定的灵敏度较高。 如果用连续光源,则吸收的光的强度只占入射光强度的极小部分 ,使测定的灵敏度极差:如图所示
2、在锐线光源半宽度范围内,可以认为原子的吸收系数为常数, 并等于中心波长处的吸收系数。
宽。其宽度约为10-3nm数量级。 待测原子相对原子质量越小,温度越高,多普勒变宽越严重。
3.劳仑兹变宽(碰撞变宽):由于同类原子或与其它粒子(分子、原子、 离子、电子等)相互碰撞而造成的吸收谱线变宽。其宽度也约为10-3nm 数量级。
三、热激发时基态原子和激发态原子的分布
原子吸收测量的是基态原子对共振线的吸收,而在热激发时不可能全 部都是基态原子,必有一部分是激发态的原子。
⁗共振发射线
⁗特征谱线:不同元素原子结构和外层电子排布不同,其原子跃迁 时吸收和发射的能量不同,因此共振线各有其特征
⁗在原子吸收光谱法中,就是利用待测元素原子蒸汽中基态原子 对光源所发射出的共振线的吸收来进行分析的。
二.原子吸收线的形状(或轮廓)
由于物质的原子对不同频率入射光的吸收具有选择性,所以透过
原子的吸收光谱线具有一定宽度的原因有以下几个: 1.谱线的自然宽度( △λN ):
无外界条件影响时的谱线宽度。其大小与激发态的原子寿命有关, 激发态的原子寿命越长,吸收线的自然宽度越窄。
一般来讲△λN 约为10-6--10-5nm,和其他因素引起的谱线宽度相
比可忽略不计。
2.多普勒变宽(热变宽△γD): 由于原子在空间做无规则的热运动产生多普勒效应而导致的谱线变
当在正负电极上施加适当电压(一般 为200~500伏)时,在正负电极之间便 开始放电,这时,电子从阴极内壁射出, 经电场加速后向阳极运动。
电子在由阴极射向阳极的过程中,与载气 (惰性气体)原子碰撞使其电离成为阳离子。 带正电荷的惰性气体离子在电场加速下,以 很快的速度轰击阴极表面,使阴极内壁的待 测元素的原子溅射出来,在阴极腔内形成待 测元素的原子蒸气云。
log
I I0
0.434K l
A
其中k 为一定频率的光吸收系数。 注意: K 不是常数,而是与谱线频率或波长有关。由于任何谱线并非
都是无宽度的几何线,而是有一定频率或波长宽度的,即谱线
是有轮廓的!因此将 K 作为常数而使用此式将带来偏差!
⁗共振吸收线:电子从基态跃迁到能量最低的激发态为共振吸跃迁, 所产生的谱线称共振吸收线。
总数N ,但求积分吸收十分困难,因为原子吸收线很窄,约0.002nm。
尽管原子吸收现象早在18世纪就被发现,但一直未用于分析。
1955,瓦尔什提出用峰值吸收系数K0来代替积分吸收
2、峰值吸收与原子浓度的关系: 在一定条件下:
K0 kN
为了测定K0值,使用的光源必须是锐线光源
(一)锐线光源: 光源发射线的中心频率与吸收线的中心频率一致,而且发射线的
所以,吸光度与试液中待测元素的C也成正比,可用下式表示: A=KC
K包含了所有的常数。此式就是原子吸收光谱法进行定量分析的理论 基础。
§10—3 原子吸收分光光度计 • 原子分光光度计由光源、原子化系统、
分光系统及检测显示系统四个部分构成。
光源
原子化器 切光器
单色器
燃气
助燃气 雾化器 废液 样品液
不足: 多元素同时测定有困难; 对非金属及难熔元素的测定尚有困难; 对复杂样品分析干扰也较严重; 石墨炉原子吸收分析的重现性较差。
10.1基本理论
一、共振线和吸收线
以频率为,强度为 I0 的光通过原子蒸汽,其中一部分光被吸收,
使该入射光的光强降低为 I :
h
I0
原ห้องสมุดไป่ตู้蒸汽
I
l
据吸收定律,得
I I0e( k l)
心
阴极灯发射特征辐射---------空心阴极灯发射特征辐射减弱--
---产生吸光度------元素定量分析
AAS特点:
1)灵敏度高:火焰原子法,ppm 级,有时可达 ppb 级;石
墨炉可达10-9--10-14(ppt 级或更低).
2)准确度高:FAAS 的 RSD 可达1~3%。 3)干扰小,选择性极好; 4)测定范围广,可测70 种元素。
第十章 原子吸收光谱法( AAS)
原子吸收光谱法是基于被测元素基态原子在蒸 气状态对其原子共振辐射的吸收进行元素定量分析
的方法。
1802年,发现原子吸收现象;1955年, Australia 物理学家Walsh A建立将该现象应用于 分析;60年代中期发展最快。
原子吸收光谱分析的过程:
A元素含量测定----- A元素的空心阴极灯发射特征辐射 --------试样在原子化器中变为气态的基态原子-------吸收空
检测显 示系统
原子化系统
一.光源: 1.光源应满足的条件: 1)能发射出待测元素的共振线,其半宽度比吸 收线半宽度窄得多; 2)辐射的强度应足够大。 3)辐射光的强度要稳定,且背景小。
2.空心阴极灯:
空心阴极灯是一种气体放电管,其结构 如图:
钨棒构成的阳极和一个圆柱形的空心阴 极,空心阴极是由待测元素的纯金属或合 金构成,或者由空穴内衬有待测元素的其 它金属构成。
光的强度和吸收系数K会随着入射光的频率而变化。
若将吸收系数对频率作图,所得曲线为吸收线轮廓。
K0
K0/2
K
0
K~ (谱线轮廓)
K为吸收系数,表示单位体积内原子对光的吸收值;γ为频率;吸收 最大处所对应的频率叫中心频率;最大吸收值叫峰值吸收;最大吸收值 的一半处所对应的宽度叫半宽度,用△γ表示,它定量的描述吸收曲线 的轮廓。
(二)原子吸收的测量: 在使用锐线光源的条件下原子蒸气的吸光度与峰值吸收有如
下关系: A=lgI0/I=0.4343K0L
式中A为中心频率处的吸光度;L为原子蒸气的厚度;
由此式可知,只要测定吸光度并固定L,就可求得K0,而K0与原子 蒸气中原子的浓度成正比。并且在稳定的测定条件下,被测定试液 中待测元素的浓度与原子蒸气中的原子浓度也成正比。
服从玻尔兹曼分布定律,基态原子数可以代表待测元素的原子总数。
四.原子的吸收法的定量基础: 1、积分吸收与原子浓度的关系:
某一频率的吸收不能代表所有原子的总吸收,因此要准确测定原子 吸收值,必须测定原子蒸汽所吸收的全部能量即吸收曲线和横坐标轴 所包围的总面积。用积分吸收表示:
K d kN
积分吸收与被测原子总数成正比,只要求得积分吸收,就能确定原子
