有机化学第十一章酚和醌
第十一章酚和醌

O CH2COOH Cl Cl
2,4-二氯苯氧乙酸(2,4-D) 酚醚化学性质比酚稳定,不易氧化,而且与HI作 用,分解为酚,此反应可用来保护酚羟基。
OCH3 OH
+
2015/11/28
HI
+
习题13
CH3I
23
克莱森重排
定义:烯丙基芳基醚在高温下可以重排为邻烯 丙基酚或对烯丙基酚,这称为克莱森重排。
X
X
亲核性比醇弱
O O CH3
成酯:
OH + CH3COOH + CH3COCl + (CH3CO)2O
OH + CH3COOH
O
98%H2SO4 4h/55%
O C CH3
乙酸苯酯
2015/11/28
25
在酸催化下,酚与羧酸作用也能生成酯,但比醇 难。通常采用酰氯或酸酐与酚反应。例如:
O C Cl + HO
14
OCH2CH=CH2
OH
200oC
14
OH
CH2CH=CH2
200oC
14
O
CH2CH CH2
190-220C 6h
OH CH2CH CH2
CH2CH=CH2
O H3C
CH2CH CH2 CH3 H3C
OH CH3
CH2CH CH2
2015/11/28
24
(3)酯的生成
难
OH + HX
对 10.00 10.26 10.21 9.81 9.38 9.26 9.20 7.15
徐寿昌《有机化学》(第2版)配套题库【名校考研真题】(下册)-第1~20章【圣才出品】

第一部分名校考研真题第11章酚和醌一、选择题1.下列化合物碱性最强的是()。
[中国科学院-中国科学技术大学2001研]【答案】(A)【解析】酚的碱性与酚羟基上氧的孤对电子有关,氧原子上的电子云密度越大,碱性越强。
氰基、溴原子都为吸电子基,使氧原子上电子云密度降低。
2.下列化合物中,酸性最强的是()。
[天津大学2000研]【答案】(D)【解析】硝基为吸电子基,使邻、对位的电子云密度降低,使酚羟基的酸性增强。
3.下列物种作为离去基团时最易离去的是()。
[大连理工大学2004研]【答案】(A)【解析】硝基为吸电子基,使负电荷得以分散,故(A)最稳定,作为离去基团,最易离去。
二、简答题1.为什么?[上海大学2004研]答:甲氧基的给电子共轭效应使对位电子云密度增大,从而使对位酚羟基的酸性减弱,而间位甲氧基只有吸电子的诱导效应而无给电子的共轭效应,故间甲氧基苯酚的酸性比对甲氧基苯酚强。
2.从反应机理说明为什么烷芳混合醚(ArOR)在与氢碘酸共热时,只得到RI和ArOH,而不是ArI和ROH。
[南京大学2002研]答:醚与氢碘酸共热时先生成烊盐,然后发生碳氧键的断裂,生成醇和碘代烷。
对于混合醚,碳氧键断裂的顺序为:三级烷基>二级烷基>一级烷基>芳基,芳基与氧的孤对电子共轭,因此烷芳混合醚与氢碘酸共热时,芳基与氧相连的碳氧键没有断裂,烷基与氧相连的碳氧键断裂,产物为酚和碘代烷。
3.化合物(A)和(B)中哪个酸性较强?(C)和(D)相比较呢?简述理由。
[华东理工大学2003研]答:硝基的吸电子共轭效应,使邻、对位电子云密度降低,酚羟基的酸性增强,故酸性(B)>(A);甲基的立体效应使(C)中硝基的π-π共轭效应减弱。
化合物(A)和(B)中酸性(B)>(A);化合物(C)和(D)中酸性(D)>(C)。
甲基的立体效应使(C)中硝基的共轭效应减弱。
4.以苯以及必要的有机、无机试剂为原料合成3,4,5-三溴苯酚。
[武汉大学2002研]答:酚羟基为邻对位定位基,若先合成苯酚,再溴化将得到2,4,6一三溴苯酚,而题目要求合成3,4,5一三溴苯酚,故必须借助氨基的定位效应来定位,然后通过重氮化来完成目标产物的合成。
有机化学-酚

O2N
NO2 OH NO2
0.25
(CH3)3CCH2
CH2C(CH3)3 CH2C(CH3)3
酸性极弱
pka
2,与三氯化铁的显色反应 , 多数酚能与三氯化铁溶液反应生成紫, 多数酚能与三氯化铁溶液反应生成紫,蓝,绿,棕 等颜色的化合物. 此反应可用于酚类的鉴定) 等颜色的化合物.(此反应可用于酚类的鉴定) 苯酚与三氯化铁溶液作用显紫色. 苯酚与三氯化铁溶液作用显紫色. 与三氯化铁溶液的显色反应并不限于酚,凡 与三氯化铁溶液的显色反应并不限于酚, 具有烯醇式结构的化合物( 具有烯醇式结构的化合物(—C=C—)也有此反 ) 应. OH
(1)卤代反应
酚在中性或碱性溶液中卤化,得到2,4,6酚在中性或碱性溶液中卤化,得到2,4,6-三卤苯酚 2,4,6
Br
OH + Br2Br BrOH白色(2)硝化反应 )
OH
OH
+ HNO3(20%)
-H2O 室温
NO2
+ HO
OH OH O2N NO2 NO2
NO2
+ HNO3
浓H2SO4
+ H2O
OH
O
+ H+
pKa≈10
OH + NaOH
ONa
+H2O
苯酚的酸性比碳酸弱, 苯酚的酸性比碳酸弱,它不能溶于碳酸氢钠 溶液;在苯酚钠的溶液中通入 溶液;在苯酚钠的溶液中通入CO2,可使苯酚游 离析出. 离析出.
ONa + CO + H O 2 2 OH
+NaHCO3
苯环上的取代基对酚酸性强弱的影响
OH OH
4-甲基苯酚
CH3 SO3H
有机化学第十一章

羰基化合物的活性次序(电子效应和空间效应): 羰基化合物的活性次序(电子效应和空间效应):
HCHO > CH3CHO > ArCHO > CH3COCH3 > CH3COR> CH3COAr > RCOR' > ArCOAr'
O 2N CHO > CHO
>
H 3C
CHO
1、与HCN的加成 、 的加成
维纶
4、与金属有机试剂的加成 、
(1)格氏试剂 )格氏试剂: H2CO +
MgCl 无水 乙醚
CH2OH 64-96%
H2O CH2OMgCl H SO 2 4
CH3 无水 乙醚 CH3COPh + PhCH2MgCl PhCH2 C OMgCl Ph CH3 H2O PhCH2 C OH NH4Cl Ph 92% Grignard: 1912 Nobel Prize
异 丙 醇 铝 ,丙 酮 丙 苯,回流
80%
CHCH CCH CH2 CH3
CH3 C CH CHCH CCH CH2 CH3 O
Oppenauer氧化: 异丙醇铝是催化剂 反应中双键不受影响。 氧化: 异丙醇铝是催化剂, 反应中双键不受影响。 氧化
脱氢:醇在适当的催化剂条件下脱去一分子氢 生成醛酮。 脱氢:醇在适当的催化剂条件下脱去一分子氢,生成醛酮。
CH3OH 浓H2SO4
COOCH3
CH2 C COOCH3 CH3 90%
过氧化苯甲酰
CH2 C CH3
n
甲基丙烯酸甲酯
聚甲基丙烯酸甲酯 (有机玻璃) 有机玻璃)
2、与NaHSO3的加成 、
加成生成a-羟基磺酸钠 羟基磺酸钠: 醛和甲基酮与饱和的NaHSO3加成生成 羟基磺酸钠: 醛和甲基酮与饱和的
徐寿昌《有机化学》(第2版)配套题库【章节题库】(下册)-第11~14章【圣才出品】

第三部分章节题库第11章酚和醌一、选择题1.下列化合物发生溴化反应,反应速率最快的是()。
A.苯B.苯甲酸C.苯酚【答案】C【解析】羧基是钝化苯环的,难发生亲电取代反应;羟基是活化苯环的,易发生亲电取代反应。
二、简答题1.写出下列化合物的名称。
答:(1)间-苯二酚(1,3-苯二酚)(2)4-硝基-1,3-苯二酚(3)2-硝基-5-羟基苯甲酸(4)2-甲基-6-羟基-1,4-萘二磺酸(5)7-氨基-3-氯-1-萘酚2.有毒常春藤和栎木中具有刺激气味的物质叫漆酚,根据如下实验报告,写出漆酚A 的结构和反应中间体B~I的结构。
答:3.。
答:4.2,4,6-三叔丁基苯酚在醋酸溶液中与溴反应,生产化合物A(C18H29BrO),产率差不多是定量的。
A的红外光谱图中在1630cm-1和1650cm-1处有吸收峰,1HNMR 谱图中有3个单峰δH=1.19、1.26和6.90,其面积比为9:18:2。
试推测A的结构。
答:A.5.完成下列合成反应,可用其他任何必要的试剂。
(1)由均三甲苯(1,3,5-三甲苯)合成2,4,6-三甲基苯酚;(2)由苯酚合成对叔丁基苯酚;(3)由苯酚合成2-溴乙基苯基醚;(4)由间甲苯酚合成2,6-二硝基-4-叔丁基-3-甲基茴香醚。
答:6.用化学方法把下列混合物分离成单一组分。
(1)苯酚和环己醇混合物;(2)2,4,6-三硝基苯酚和2,4,6-三硝基甲苯混合物。
答:7.按酸性由大到小的顺序排列下列各组中的化合物。
(1)苯甲酸,环己醇,苯酚,碳酸,硫酸,水;(2)苯酚,间氯苯酚,间甲基苯酚,间硝基苯酚;(3)对溴苯酚,间溴苯酚,3,5-二溴苯酚。
答:(1)硫酸>苯甲酸>碳酸>苯酚>水>环己醇;(2)间硝基苯酚>间氯苯酚>苯酚>间甲基苯酚(取代基在间位时,主要考虑诱导效应;吸电子取代基有利于羟基质子的解离,使酸性增加);(3)3,5-二溴苯酚>间溴苯酚>对溴苯酚(溴在对位时,表现吸电子诱导效应和给电子共轭效应;在间位时,只表现吸电子诱导效应)。
有机化学课后习题答案11第十一章酚醌
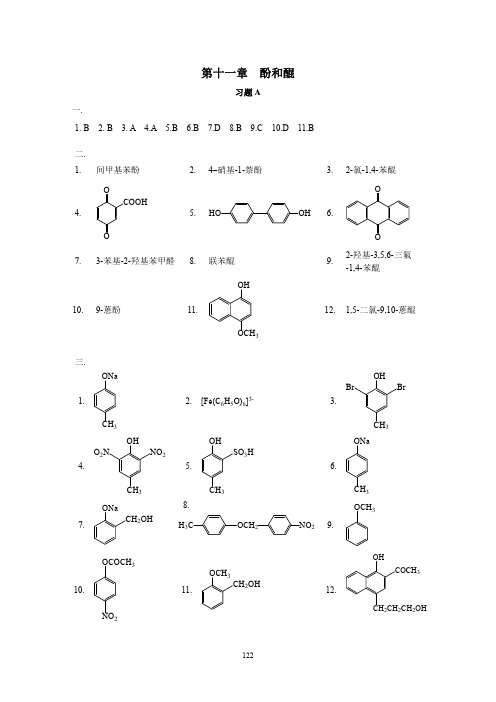
2)
SO3H 浓H2SO4 NaOH ONa H+ OH
OH 浓H2SO4 Cl2 Cl
OH Cl H+ Cl
OH Cl
SO3H
SO3H
OCH3 浓 H2SO4 SO3H 浓HNO3 O2N OCH3 NO2
3.
1)
OH CH3I OCH3
SO3H
NO2
2)
OH
+
OH CH3COOH BF3 CH3COCl
OC2H5 H
+
OC2H5
CH2CH2MgBr
CH2CH2OH
123
习题 C 一. 1. 4. 7. 蒽醌 4-硝基萘酚 4-羟基-2-溴苯乙酮 2. 5. 8. 2-萘酚 4-溴萘酚 对羟基苯乙酮 3. 6. 9. 4-羟基-3-甲氧基苯甲醛 3-甲基-4-羟基苯甲酸 对苯醌
二. 1. A 2. C 3. C 4. A 5. C 6. D 7. C 三.完成下列反应式
5.
O 1,4-环己二肟
6.
COCH3
7.
4-甲基-2,6-二羟基-α-苯乙醇
OH
8.
9.
1,4-环己二酮
10. H2N 二.
OH
1.
CH2CH2CH2Br,
OCH2CH=CHCH3 OH
O
2. ,
O
CHCH=CH2 CH3
3.
O
,
三. 1. C>A>B
2. A>C>B
四. (1) 1.溴水处理,有白色沉淀生成为苯酚;2.加入金属钠,有气体生成为丁醇;3.剩余两种化 合物中,溶于浓硫酸的是丁醚,不溶的则为己烷。 (2) 用氢氧化钠水溶液处理,苯酚溶于氢氧化钠水溶液,苯甲醇不溶。 (3) 用氢氧化钠水溶液处理,对甲苯酚溶于氢氧化钠水溶液,苯甲醚不溶。 (4) 与溴水处理,生成白色沉淀为含酚的水溶液,无沉淀则为纯水。 五. 1.
徐寿昌《有机化学》(第2版)课后习题(酚和醌)【圣才出品】

(8)2,6-二叔丁基-4-硝基苯酚
(9)2,6-二氯ห้องสมุดไป่ตู้酚
(10)4-乙基-2-溴苯酚
答:(1)间苯三酚:
+ 3 SO3
HO3S
SO3H NaOH
SO3H
H+ HO
OH OH
(2)4-乙基-1-3-苯二酚
(3)对亚硝基苯酚
(4)苯乙醚
OH + (C2H5)SO4 NaOHaq
OC2H5
(5)2,4-二氯苯氧乙酸
答:化合物(A)丌溶于氢氧化钠,遇 FeCl3 无颜色反应,由此可以判断化合物(A) 丌含有酚羟基。但是该化合物能不一个或两个羟氨分子结合,说明化合物(A)含有两个羰
基。化合物(A)的可能结构为:
。化合物(B)能溶于氢氧化钠,且不 FeCl3 有
(6)对羟基苯磺酸
(7)1-甲基-2-萘酚
(8)9-蒽酚
(9 )1 ,2 ,3-
苯三酚
(10)5-甲基-2-异丙基苯酚 (11)5-硝基-1-萘酚
(12)β-氯蒽醌
1 / 11
圣才电子书 十万种考研考证电子书、题库视频学习平台
2.写出下列各化合物的构造式: (1)对硝基苯酚 (2)对氨基苯酚 (3)2,4,二氯苯氧(基)乙酸(2,4-D) (4)2,4,6-三溴苯酚 (5)邻羟基苯乙酮 (6)邻羟基乙酰苯 (7)4-甲基-2,6-二叔丁基苯酚(二六四抗氧剂) (8)1,4,萘醌-2-磺酸钠 (9)2,6,蒽醌二磺酸(ADA) (10)醌氢醌 (11)2,2-(4,4′-二羟基二苯基)丙烷(双酚 A) (12)对苯醌单肟 答:
答:
3 / 11
圣才电子书 十万种考研考证电子书、题库视频学习平台
第十一章 酚和醌
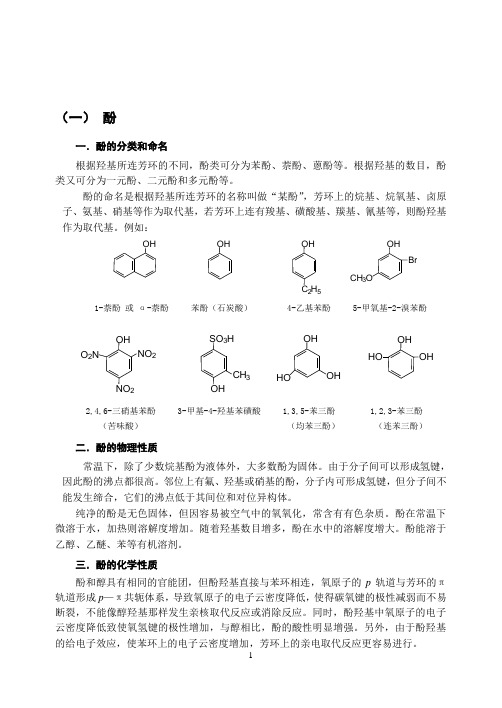
(一) 酚一.酚的分类和命名根据羟基所连芳环的不同,酚类可分为苯酚、萘酚、蒽酚等。
根据羟基的数目,酚类又可分为一元酚、二元酚和多元酚等。
酚的命名是根据羟基所连芳环的名称叫做“某酚”,芳环上的烷基、烷氧基、卤原子、氨基、硝基等作为取代基,若芳环上连有羧基、磺酸基、羰基、氰基等,则酚羟基作为取代基。
例如:1-萘酚 或 α-萘酚 苯酚(石炭酸) 4-乙基苯酚 5-甲氧基-2-溴苯酚2,4,6-三硝基苯酚 3-甲基-4-羟基苯磺酸 1,3,5-苯三酚 1,2,3-苯三酚 (苦味酸) (均苯三酚) (连苯三酚)二.酚的物理性质常温下,除了少数烷基酚为液体外,大多数酚为固体。
由于分子间可以形成氢键,因此酚的沸点都很高。
邻位上有氟、羟基或硝基的酚,分子内可形成氢键,但分子间不能发生缔合,它们的沸点低于其间位和对位异构体。
纯净的酚是无色固体,但因容易被空气中的氧氧化,常含有有色杂质。
酚在常温下微溶于水,加热则溶解度增加。
随着羟基数目增多,酚在水中的溶解度增大。
酚能溶于乙醇、乙醚、苯等有机溶剂。
三.酚的化学性质酚和醇具有相同的官能团,但酚羟基直接与苯环相连,氧原子的p 轨道与芳环的π轨道形成p —π共轭体系,导致氧原子的电子云密度降低,使得碳氧键的极性减弱而不易断裂,不能像醇羟基那样发生亲核取代反应或消除反应。
同时,酚羟基中氧原子的电子云密度降低致使氧氢键的极性增加,与醇相比,酚的酸性明显增强。
另外,由于酚羟基的给电子效应,使苯环上的电子云密度增加,芳环上的亲电取代反应更容易进行。
OH OH OH 2H 5OHBrCH 3OOHOHOHNO 2O 2N2SO 3H CH 3HOOHHOOH苯酚中p-π共轭示意图综上所述,酚的主要化学性质可归纳如下:1.酸性酚类化合物呈酸性,大多数酚的pKa 都在10左右,酸性强于水和醇,能与强碱溶液苯酚的酸性比碳酸弱,能溶于碳酸钠溶液,但不能溶于碳酸氢钠溶液,在苯酚钠的溶液中通入二氧化碳能使苯酚游离出来。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
C C OH
CH C O
按酚羟基数目分类:
① 一元酚 一个羟基 ② 二元酚 二个羟基 ③ 多元酚 两个以上
2. 酚的命名
酚的命名一般是以羟基为主官能团,在“酚”字前
加苯共同作为母体,再加上其它取代基的位次、数目和
名称就是酚的系统命名。
OH
CH3 2-甲基苯酚
HO
COOH
❖ 官能团优先次序:
-COOH > -SO3H >-COOR >-COX > -CONH2 > -CN > -CHO > >C=O > (R) -OH > (Ar) -OH > -NH2 > C≡C- > -OR > -Cl > -NO2 ❖命名时如连有在酚羟基之前的基团,则以最靠前的 基团为主官能团。
苯酚溶于NaOH,但不 溶于NaHCO3此性质可 区别醇、酚和羧酸。
这一反应可用于分离提纯。如:
OH
NaO H
OH
水层 有机层
通入 C O2
O Na
OH (分离出去)
如何除去环己醇中含有的少量苯酚?
OH (分离之)
取代基的电子效应对取代酚酸性的影响:
酚羟基的邻、对位连有供电子基时,将使酸性↓;供 电子基数目越多,酸性越弱。
• 成本高;当环上已有-COOH、-Cl、-NO2等基团时, 则副反应多。 • 此法是较早的生产方法,苯酚的收率高、质量好、
生产设备简单,但反应流程复杂、且生产不连续, 消耗大量的硫酸和烧碱,不宜大规模生产,目前, 仅用来生产萘酚和间苯二酚。
补充1:间二酚的制备 补充2: -萘酚及其衍生物
165℃
第十一章 酚和醌
学习要求
1.掌握酚的分类及其命名法。 2.掌握酚的结构特点与化学性质。 3. 理解酚及取代酚的酸性,比较醇和酚的酸性。 4 酚的构造、分类和命名 11.2 酚的制法 11.3 酚的物理性质 11.4 酚的化学性质
第二部分 醌 (不学)
氢过氧化异丙苯
+ CH3COCH3
1:0.6
❖ 副产品丙酮也是常用的有机试剂、有机溶剂之一。 中间产品氢过氧化异丙苯可作为聚合橡胶的引发剂。
2 从芳卤衍生物制备
Cl
注意反应
ONa
条件!
+ 2 NaOH 350~370℃,20MPa Cu催化剂
ONa
OH
+ NaCl + H2O
+ HCl
+ NaCl
• 酚具有极高的亲电反应活性的原因——氧原子的P 电子分散到苯环上,增加了苯环的电子云密度,加强 了亲电反应活性。
• 醇与酚不同,没有电子的离域现象 • 苯酚的离域
酚为什么具有酸性?
p -π共轭效应和氧原子的 – I 效应共同影响的结果, 必然导致O―H键之间的电子更偏向于氧,这就有利于氢 原子的解离,而表现出一定的酸性。
相反,酚羟基的邻、对位连有吸电子基时,将使酸性
↑;吸电子基数目越多,酸性越强。
_
_
O
O
G(吸电子基) 电荷分散, 负离子稳定化
G(给电子基) 电荷集中, 负离子去稳 定化
OH
OH
OH
OH
OH
OH
NO2
pka 10.0
CH3
Cl
NO2
10.26
9.38
7.15
7.23
NO2 8.4
这里值得注意的是:当吸电子基处于间位时,由于它们之
HO
间苯二酚 1,3-苯二酚
HO
OH
OH
均苯三酚 偏苯三酚
1,3,5-苯三酚 1,2,4-苯三酚
11.2 酚的制法
反应历程:(1)自由基反应
1 从异丙苯制备
CH3 CH CH3
+ CH3CH=CH2 H2SO4
CH3 CH3 C O-O-H
绿色的合成 路线
OH
O2空气,110~120℃ 过氧化物
稀 H2SO4 75~78℃
11.4.1 酚羟基的反应
(1)酚的酸性——O-H键容易离解。 (2)极高的亲电反应活性——O-H基对苯环的供电 性。
• 酚具有酸性的原因——氧原子以SP2(与醇醚不同) 杂化轨道参与成键,它的一对未共用电子的P轨道与 苯环共轭,氧原子的负电荷分散到整个共轭体系中, 氧的电子云密度降低,减弱了O-H键,氢原子容易离 解成为质子。
•苯酚的红外光谱
• 对甲苯酚的红外光谱
邻硝基苯酚与对硝基苯酚沸点高低???
邻硝基苯酚可以发生分子内缔合,即形成分子内 氢键;对硝基苯酚可以发生分子间缔合,即形成分子 间氢键;邻硝基苯酚发生了分子内缔合,降低了分子 间缔合的能力,其沸点比对硝基苯酚低。
O
H O
H O
O
O
N
NO
N
…O
O
O
H…
11.4 酚的化学性质
命名练习
HO
COOH 4-羟基苯甲酸
(对羟基苯甲酸)
OH
6-硝基-1-萘酚
O2N
CHO OH
2-羟基苯甲醛 邻羟基苯甲醛(水杨醛)
HO HOCH2
2,4-二羟基苯甲醇
OH
NO2
2,4,6-三硝基苯酚
O2N
OH HO
OH NO2
俗称苦味酸,强酸性,有腐蚀 性,易爆,是一爆炸品。
OH
OH
OH OH
邻苯二酚 1,2-苯二酚
羟基直接连在芳环上的化合物称为酚。羟基也 是酚的官能团,称为酚羟基。
羟基与芳环侧链上饱和碳原子相连的化合物为芳醇。
CH2OH
11.1 酚的结构、分类和命名
1. 酚的结构、分类
SP2
最简单的酚是苯酚。
.. OH H
sp2
p-共轭
H
.
O . ①苯环上电子云密度增加;
1.6D
②酚羟基氢的离解能力增强。
此法操作简便,副产物易分离,但需要高压反应,且 碱对设备的腐蚀严重,反应困难。
当卤原子的邻位或对位有强的吸电子基时,水解反应 容易进行。
单 硝 基 芳 卤
比较硝基对苯环 上亲核取代反应 难易的影响?
多 硝 基 芳 卤
• 硝基活化氯原子的原因——分散中间体的负电荷:
3 从芳磺酸制备
碱 熔 法
11.3 酚的物理性质
•酚大多数为结晶固体。 • 酚的沸点和溶点高于质量相近的烃——氢键。 • 酚微溶于水,能溶于酒精,乙醚等有机溶剂。
酚的氢键
酚与水分子之间的氢键
酚与酚分子之间的氢键
酚的红外吸收光谱
• 酚同醇一样,由于O—H的伸缩振动,在3520 — 3100 cm-1 有一个强而宽的吸收带(缔和羟基)。但酚与醇的 C—O伸缩振动不同:
OH
O + H+
负电荷分散在包括七个 原子在内的共轭体系中
_
O
O
O
O
_
_
_
由于它们的贡献,酚具有较强的酸性。
酸性
苯酚:pKa=10 乙醇:pKa=17 环己醇:pKa=18 碳酸:pKa=6.4
• 苯酚能溶解于氢氧化钠水溶液
工业上利用苯酚能溶 于碱,而又可用酸分 离的性质来处理和回 收含酚废水。
• 通入二氧化碳,苯酚即游离出来
