化学四大平衡
无机化学中四大平衡相互影响的问题探讨

无机化学中四大平衡相互影响的问题探讨无机化学中存在四大平衡相互影响的问题,包括溶解度平衡、酸碱中和平衡、氧化还原平衡和配位平衡。
这些平衡相互影响的问题在无机化学研究和应用中具有重要的意义。
本文将对这四大平衡相互影响的问题进行探讨。
溶解度平衡和酸碱中和平衡存在相互影响。
溶解度平衡是指溶解物质在溶液中溶解与析出的反应,它可以用溶解度积常数(Ksp)来描述。
而酸碱中和平衡是指酸与碱在溶液中反应生成盐和水的反应。
溶解度平衡和酸碱中和平衡之间的相互影响可以通过下面的方程式描述:\[\text{H}_2\text{O} \rightleftharpoons \text{H}^+ + \text{OH}^-\]\[\text{H}^+ + \text{OH}^- \rightleftharpoons \text{H}_2\text{O}\]水的自电离产生的\(\text{H}^+\)和\(\text{OH}^-\)可以影响溶液中一些物质的溶解度。
当溶液中有一种物质的溶液度积常数(Ksp)小于水的离子乘积(\(\text{K}_\text{w} = \text{H}^+ \times \text{OH}^-\))时,该物质会溶解;而当Ksp大于\(\text{K}_\text{w}\)时,该物质会析出。
水的离子乘积会对溶解度平衡产生影响。
与此溶液中的酸和碱也会对溶解度平衡产生影响。
当溶液中有酸或碱存在时,它们会与溶解物质中的阳离子或阴离子结合,从而改变了这些离子的活性,导致溶解度发生变化。
当一种酸与一个可溶性盐中的阴离子结合时,该盐的溶解度会降低;而当一种碱与一个可溶性盐中的阳离子结合时,该盐的溶解度会增加。
氧化还原平衡和配位平衡存在相互影响。
氧化还原平衡是指电子的转移反应,常常涉及到氧化剂和还原剂之间的相互转化。
配位平衡是指配位化合物中金属离子和配体之间的相互作用。
氧化还原平衡和配位平衡之间的相互影响可以通过下面的方程式描述:\(\text{M}^n+\)表示金属离子,\(\text{Ox}\)表示氧化剂,\(\text{Red}\)表示还原剂,\(\text{L}\)表示配体。
化学中的四大平衡

化学中的四大平衡在化学中,平衡是一个重要的概念。
平衡是指在一定条件下,化学反应中反应物和生成物的浓度或者物质的状态保持稳定的状态。
化学中有四种主要的平衡,即动态平衡、酸碱平衡、氧化还原平衡和离子平衡。
一、动态平衡动态平衡是指在一个封闭系统中,反应物和生成物之间的反应速率相等,虽然反应仍在进行,但是总体上看起来没有变化。
这是因为在反应物转化为生成物的同时,生成物又会转化为反应物,反应物和生成物的浓度保持不变。
这种平衡是一种动态的平衡,反应仍在进行,但是总体上看起来没有变化。
动态平衡的一个典型例子是水的自离解反应。
水分子可以自发地分解成氢离子和氢氧根离子,也可以反应生成水分子。
在一定条件下,这个反应会达到一个平衡状态,水分子的分解和生成速率相等,水的pH值保持在中性。
二、酸碱平衡酸碱平衡是指在溶液中酸和碱之间的反应达到平衡的状态。
酸和碱是一对互为共轭的物质,具有相互转化的能力。
在酸碱平衡中,酸和碱之间会发生中和反应,生成盐和水。
酸碱平衡的一个重要应用是在生理体液中的维持。
人体的血液和细胞液都必须保持一定的酸碱平衡,即pH值在一定范围内。
这是因为酸碱平衡影响着生物体内许多生理过程的进行,如酶的催化作用、细胞膜的通透性等。
三、氧化还原平衡氧化还原平衡是指在化学反应中,物质发生氧化和还原反应,同时电子的转移保持平衡。
氧化是指物质失去电子,还原是指物质获得电子。
氧化还原反应是一种常见的化学反应类型,常见的有金属与非金属氧化物反应、金属与酸反应等。
氧化还原平衡在生物体内也起着重要的作用。
例如,呼吸过程中,氧气被还原为水,同时葡萄糖被氧化释放能量。
这是一个复杂的氧化还原反应链,其中涉及多种酶的催化作用。
四、离子平衡离子平衡是指在溶液中,正离子和负离子的浓度保持稳定的状态。
在溶液中,离子会相互吸引形成盐晶体,同时也会发生离解反应,使离子浓度保持平衡。
离子平衡在生物体内起着重要的作用。
例如,细胞内外的离子平衡是维持细胞正常功能的重要因素。
无机化学中四大平衡相互影响的问题探讨

无机化学中四大平衡相互影响的问题探讨无机化学中的四大平衡相互影响一直是化学领域研究的重要课题。
这四大平衡包括了溶解平衡、配位化学平衡、氧化还原平衡和放射化学平衡。
它们之间相互影响,相互制约,共同构成了无机化学体系的平衡网络。
本文将从这四大平衡的相互影响出发,探讨它们之间的关系以及在实际应用中的重要意义。
我们来了解一下这四大平衡的基本概念。
溶解平衡是指当某种物质溶解时,其分子或者离子与溶剂之间的相互作用所导致的动态平衡。
在溶解过程中,溶质的溶解度是一个很重要的参数,它受溶液中其他物质浓度、温度等因素的影响。
配位化学平衡是指配合物(也称配合物离子)的形成与分解反应,通常包括了络合离子的形成常数和络合物的稳定性常数等参数。
氧化还原平衡是指涉及到电子转移的化学反应。
在这种反应中,一个物质被氧化,同时另一个物质被还原。
氧化还原反应的平衡常数可以通过电动势或者标准氧化还原电位来进行定量描述。
放射化学平衡是指放射性核素的衰变反应。
放射性核素具有一定的衰变速率,它们的衰变反应也有平衡定律,可以通过半衰期来进行描述。
这四大平衡在无机化学中起着至关重要的作用,它们之间的相互影响也是无机化学研究的一个重要课题。
首先来看溶解平衡和配位化学平衡之间的相互关系。
实际上,溶解平衡和配位化学平衡之间存在着密切的联系。
溶解平衡中的配位化学过程对溶解度的影响是非常显著的。
以金属离子配位化学为例,金属离子在水中溶解时,往往会形成水合离子,而这些水合离子又会与配体形成络合物。
这种络合物的形成会影响金属离子的溶解度,从而影响溶解平衡。
配位化学过程中,配合物的稳定性也受到了溶液中其他物质的影响,例如存在其他金属离子、配体或者其它配位物等都会影响络合物的形成和分解反应,进而影响配位化学平衡的达到。
溶解平衡和配位化学平衡之间存在着相互影响,它们共同决定了一种物质在溶液中的化学行为。
接下来,我们看一看氧化还原平衡和放射化学平衡之间的相互影响。
氧化还原平衡和放射化学平衡之间的联系主要体现在两个方面,一是在氧化还原反应中,电子的转移往往受到溶液中其他物质的影响,有些物质可以促进还原反应的进行,有些物质则会抑制还原反应的发生。
无机化学中四大平衡相互影响的问题探讨

无机化学中四大平衡相互影响的问题探讨无机化学中的四大平衡包括酸碱平衡、氧化还原平衡、配位平衡和沉淀平衡。
这些平衡之间会相互影响,导致化学反应的方向和速率发生变化。
下面将详细探讨这些平衡之间的相互影响。
首先是酸碱平衡和氧化还原平衡之间的关系。
酸碱反应中通常伴随有氧化还原反应,而氧化还原反应也会发生酸碱反应。
在酸碱平衡中,如果有一种物质发生氧化还原反应,那么该反应将对酸碱平衡造成影响。
如果一种物质发生还原反应,会释放出氢气,从而增加溶液的酸性,导致酸碱平衡向酸性方向偏移。
相反地,如果一种物质发生氧化反应,会消耗氢气,减少溶液的酸性,导致酸碱平衡向碱性方向偏移。
再次是酸碱平衡和沉淀平衡之间的关系。
在沉淀反应中,溶液中的阳离子和阴离子结合形成固体沉淀。
而酸碱反应会影响沉淀平衡的方向和速率。
如果酸碱反应生成了强酸或弱碱,会增加阳离子的浓度,导致溶液中反应生成的沉淀浓度增加,促使沉淀反应向生成沉淀的方向偏移。
相反地,如果酸碱反应生成了弱酸或强碱,会减少阳离子的浓度,导致溶液中反应生成的沉淀浓度减少,促使沉淀反应向解离沉淀的方向偏移。
最后是氧化还原平衡和配位平衡之间的关系。
氧化还原反应中的金属离子可以与配体结合形成配合物。
配位反应会影响氧化还原平衡的方向和速率。
具体而言,如果配位反应中的配合物是氧化剂,会促使氧化反应进行,增加金属离子的氧化态;如果配位反应中的配合物是还原剂,会促使还原反应进行,减少金属离子的氧化态。
配位反应的进行会改变氧化还原平衡反应的方向和速率。
无机化学中的四大平衡相互影响,导致化学反应的方向和速率发生变化。
了解这些相互影响关系对于理解和控制无机化学反应具有重要意义。
化学四大平衡笔记

化学四大平衡笔记
1、能量守恒定律:能量守恒定律认为,一个系统内所有能量的总和
是不变的,即能量在系统内转移,但总量不变。
2、熵守恒定律:熵守恒定律认为,熵(混乱程度)在系统中总是增加,并且不可逆转。
3、平衡位移定律:平衡位移定律认为,当一个化学反应放置在适当
的环境中时,反应趋向于使系统进入势能最低的状态,从而达到平衡位移。
4、 Le Chatelier定律:Le Chatelier定律认为,当一个化学反应
受到外界影响时,它会作出变化,以抵消外力的影响,从而尽快重新达到
平衡。
高中化学中的“四大平衡”专题复习

2021/10/10
9
3. 都存在平衡常数K
平衡类别 化学平衡 电离平衡 水解平衡 溶解平衡
平衡常数
K
Ka(Kw)
Kh
Ksp
K仅受温度 影响; K越大,反应的正向进行程度 越大;
可以用Qc和K判断衡移动的方向。
Q>K,平衡 逆向 移动
Q = K,化学达平衡状态
Q<K,平衡 正向 移动
写出下列反应的平衡常数 mA (g)+nB(g) pC(g)+qD(g)
—高中化学四大平衡
化学平衡
电离平衡 四大平衡
水解平衡
沉淀溶解平衡
一、四大平衡的共同点 1. 所有的平衡都建立在可逆“反应”的基础上
平衡类别 化学平衡 电离平衡 水解平衡 溶解平衡
盐中的 溶质与其
研究对象 可逆反应 弱电解质 “弱”离 饱和液的
子
共存体系
平衡特点
逆、等、定、动、变
2. 都能用勒夏特列原理解释平衡的移动
电离平衡、水解平衡、溶解平衡的比较
类型 电离平衡
水解平衡
溶解平衡
实例 升温
C H 3 C O O H C H 3 C O O - + H +
平衡右移,K增 大,c(H+)增大, 电离度增大
N H 4 + + H 2 O F e ( O H ) 3 ( s ) N H 3 · H 2 O + H + F e 3 + ( a q ) + 3 O H - ( a q )
化学平衡移动小结:
影响平衡的条件 增大反应物
浓 减小生成物 度
减小反应物
增大生成物
压 增大压强 强 减小压强
化学中的四大平衡

A的初始浓度-A的平衡浓度 物 A 的 转 化 率 为 : α(A) = A的初始浓度 c0A-cA ×100%= ×100%。 c0A
助学园地
阅卷现场
注意 同一个反应中,反应物可以是多种,但不同反应物 的转化率可能不同;增大一种反应物的浓度,可以提高其 他反应物的转化率。工业生产中常常提高廉价原料的比 例,从而增大其他原料的利用率。 (3)电离平衡常数
章末整合
一、四大平衡不同点的比较 广义的化学平衡包括狭义的化学平衡、电离平衡、水 解平衡、沉淀溶解平衡。这四个方面的平衡被称为四大化 学平衡。四大平衡是中学化学知识结构的核心内容之一, 起到了支点的作用。
助学园地
阅卷现场
1.研究对象不同 平衡 化学平衡 类型 研究 可逆的化 对象 学反应 工业 合成氨 电离平衡 溶液中的 弱电解质 水解平衡 沉淀- - - 2. 酸式弱酸根离子如 HCO- 、 HS 、 HSO 既不能与 OH 3 3
大量共存,又不能与 H 大量共存。
3. 有沉淀生成包括有微溶物生成的离子不能大量共存, 如 Ba2+、
- 2- Ca2+、Mg2+、Ag+等不能与 SO2 、 CO 4 3 等大量共存。
能够水解 溶液中的难 的盐类 溶电解质
举例
溶液中的氯 碳酸钠、 醋酸溶液、 化银、硫酸 氯化铁、 氨水等 钡、氢氧化 醋酸铵等 铁等
助学园地
阅卷现场
2.描述方法不同
(1)化学平衡常数 对于一般可逆反应:mA(g)+nB(g) pC(g)+qD(g),在一温
[cC]p· [cD]q 度下达到平衡时,K= 。 [cA]m· [cB]n (2)平衡转化率 对于一般的化学反应:aA+bB cC+dD,达到平衡时反应
H++OH-。水的电离程度大小是用离子积(KW)来表示的,
四大平衡常数的相互关系及判定
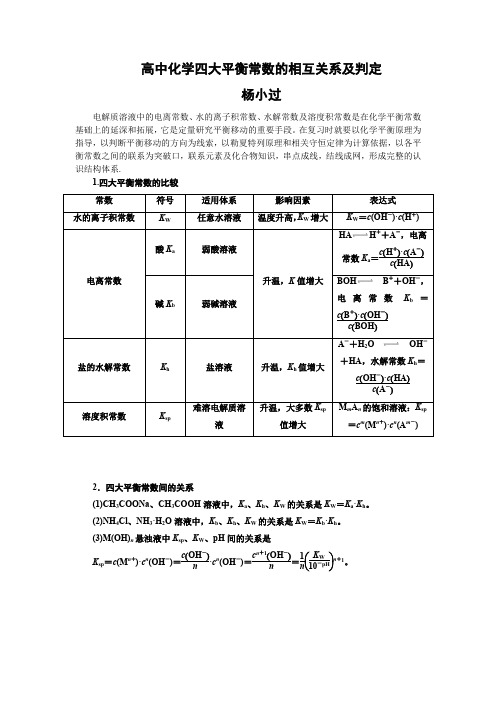
高中化学四大平衡常数的相互关系及判定杨小过电解质溶液中的电离常数、水的离子积常数、水解常数及溶度积常数是在化学平衡常数基础上的延深和拓展,它是定量研究平衡移动的重要手段。
在复习时就要以化学平衡原理为指导,以判断平衡移动的方向为线索,以勒夏特列原理和相关守恒定律为计算依据,以各平衡常数之间的联系为突破口,联系元素及化合物知识,串点成线,结线成网,形成完整的认识结构体系.1.四大平衡常数的比较HA H++A-,电离常数K a=c(H+)·c(A-) c(HA)BOH B++OH-,电离常数K b=c(B+)·c(OH-)c(BOH)A-+H2O OH-+HA,水解常数K h=c(OH-)·c(HA)c(A-)M A的饱和溶液:K2.四大平衡常数间的关系(1)CH3COONa、CH3COOH溶液中,K a、K h、K W的关系是K W=K a·K h。
(2)NH4Cl、NH3·H2O溶液中,K b、K h、K W的关系是K W=K b·K h。
(3)M(OH)n悬浊液中K sp、K W、pH间的关系是K sp=c(M n+)·c n(OH-)=c(OH-)n·cn(OH-)=c n+1(OH-)n=1n⎝⎛⎭⎫K W10-pH n+1。
3.四大平衡常数的应用 (1)判断平衡移动方向(2)如将NH 3·H 2O 溶液加水稀释,c (OH -)减小,由于电离常数为c (NH +4)·c (OH -)c (NH 3·H 2O ),此值不变,故c (NH +4)c (NH 3·H 2O )的值增大。
(3)利用K sp 计算沉淀转化时的平衡常数 如:AgCl +I-AgI +Cl -[已知:K sp (AgCl)=1.8×10-10、K sp (AgI)=8.5×10-17]反应的平衡常数K =c (Cl -)c (I -)=c (Ag +)·c (Cl -)c (Ag +)·c (I -)=K sp (AgCl )K sp (AgI )=1.8×10-108.5×10-17≈2.12×106。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
中学化学平衡理论体系及勒夏特列原理得应用中学化学教材中,有一个平衡理论体系,包括溶解平衡、化学平衡、电离平衡、水解平衡、络合平衡等。
化学平衡就是这一平衡理论体系得核心。
系统掌握反应速率与化学平衡得概念、理论及应用对于深入认识其她平衡,重要得酸、碱、盐得性质与用途,化工生产中适宜条件得选择等,具有承上启下得作用;对于深入掌握元素化合物得知识,具有理论指导意义。
正因为它得重要性,所以,在历年高考中,这一部分向来就是考试得热点、难点。
一、化学平衡理论1、化学平衡定义:2、勒夏特列原理:3、勒夏特列原理得应用:1、下列事实中不能用勒夏特列原理来解释得就是( )A、往硫化氢水溶液中加碱有利于S2-得增加B、加催化剂有利于合成氨反应C、合成氨时不断将生成得氨液化,有利于提高氨得产率。
D、合成氨时常采用500℃得高温2、已知工业上真空炼铷(熔融)原理如下:2RbCl +Mg == MgCl2 +2Rb(g),对于此反应得进行能给予正确解释得就是( )A、铷得金属活动性不如镁强,故镁可置换铷。
B、铷得沸点比镁低,把铷蒸气抽出时平衡右移。
C、氯化镁得稳定性不如氯化铷强。
D、铷得单质状态较化合态更稳定。
3、在加热条件下,KCN 溶液中会挥发出剧毒得HCN,从平衡移动得角度来瞧,挥发出HCN得原因就是。
为了避免产生HCN,应采取得措施就是向KCN溶液中加入。
4、把FeCl3溶液蒸干并灼烧,最后得到得主要固体产物就是其原因就是。
5、把Al2(SO4)3溶液蒸干,最后得到得主要固体产物就是其原因就是。
6、在泡沫灭火剂中放入得两种化学药品就是NaHCO3溶液与Al2(SO4)3溶液,其灭火原理就是什么?7、请解释:为什么生活中饮用得碳酸型饮料打开瓶盖倒入玻璃杯时会泛起大量泡沫。
解释:碳酸型饮料中未溶解得二氧化碳与溶解得二氧化碳存在平衡:CO2(g) CO2(aq),打开瓶盖时,二氧化碳得压力减小,根据勒夏特列原理,平衡向释放二氧化碳得方向移动,以减弱气体得压力下降对平衡得影响。
因此,生活中饮用得碳酸型饮料打开瓶盖倒入玻璃杯时会泛起大量泡沫。
二、中学化学常见四大平衡1)Mg(OH)2(s) Mg2+(aq)+2OH-(aq) 2)HAc(aq) H+(aq)+Ac-(aq)3)CO+Cu2O Cu+CO2 4)CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O5)C(s)+H2O(g) CO(g)+H2(g) 6)HCO3-(aq) H+(aq)+CO32-(aq)2、常见四大平衡研究对象及举例A、化学平衡:可逆反应。
如:; 加热不利于氨得生成,增大压强有利于氨得生成。
例1、竖炉冶铁工艺流程如图,使天然气产生部分氧化,并在特殊得燃烧器中使氧气与天然气燃烧CH4(g)+2O2(g)=CO2(g)+2H2O(g),催化反应室发生得反应为:CH4(g)+H2O(g) CO(g)+3H2(g)∆H1=+216kJ/mol;CH4(g)+ CO2(g)2CO(g) + 2H2(g) ∆H2=+260kJ/mol(不考虑其她平衡得存在),下列说法正确得就是ADA.增大催化反应室得压强,甲烷得转化率减小B.催化室需维持在550~750℃,目得仅就是提高CH4转化得速率C.设置燃烧室得主要目得就是产生CO2与水蒸气作原料气与甲烷反应D.若催化反应室中,达到平衡时,容器中n(CH4)=amol,n(CO)=bmol,n(H2)=cmol,则通入催化反应室得CH4得物质得量为a+(b+c)/4例2:一定条件下,向密闭容器中投入3mol H2与1mol N2,发生如下反应:N2+3H22NH31)完成v-t图①1min 时达到平衡; ②第2分钟时加入N2,3分钟时重新达到平衡;③第4分钟时升温,第5分钟时重新达到平衡;④第6分钟时扩大容器体积,第7分钟时达到新得平衡⑤第8分钟时加入催化剂; ⑥第9分钟时降温,第10分钟时重新达到平衡;⑦第11分钟时移走NH3,第12分钟时重新达到平衡2)反应正方向移动得时间段:_____________________________________;3)反应逆方向移动得时间段_____________________________________;4)达到平衡得时间段_____________________________________;5)平衡时保持不变得物理量:_____________________________________;A.c(N2)B.n(NH3)C.H2得转化率D.压强E.气体得平均摩尔质量F.气体得密度G.V正H.V逆【练习】1.(6分)将4 mol SO3气体与4 mol NO置于2L容器中,一定条件下发生如下可逆反应(不考虑NO2与N2O4之间得相互转化):2SO3(g) 2SO2+O2、2NO+O2 2NO2⑴当上述系统达到平衡时,O2与NO2得物质得量分别为n(O2)=0、1 mol、n(NO2)=3、6 mol,则此时SO3气体得物质得量为。
⑵当上述系统达到平衡时,欲求其混合气体得平衡组成,则至少还需要知道两种气体得平衡浓度,但这两种气体不能同时就是SO3与,或NO与(填它们得分子式)。
⑶在其它条件不变得情况下,若改为起始时在1 L容器中充入2 molNO2与2 molSO2,则上述两反应达到平衡时,c (SO2)平= mol/L。
1.(6分,每空2分)⑴0、2 mol ⑵SO2、NO2⑶1、92.在一个固定体积得密闭容器中,保持一定温度,进行以下反应:H2(g)+Br2(g)=2HBr(g)已知加入1molH2与2molBr2时,达到平衡后生成a mol HBr(见下表“已知”项)。
在相同条件下,且保持平衡时各组分得质量分数不变,对下列编号(1)~(3)得状态,请填写表中编号起始状态平衡时HBr得物质得量(mol) H2Br2HBr已知 1 2 0 a(1) 2 4 0(2) 1 0、5a(3) m2、(1)2a (2)0 0、5 (3)2(n-2m) (n-m)aB、电离平衡:弱电解质。
如:; 加热促进电离,稀释电离度增大。
例.试用简单得实验证明,在醋酸溶液中存在着CH3COOH得电离平衡。
1、验证HAc就是弱电解质方法现象解释1、测定NaAc溶液得pH值2、测定0、1mol/LHAc溶液得pH值2、水得电离1、液氨与水性质相似,也存在微弱得电离:2NH3 NH4++NH2-,其离子积常数K=c(NH4+)·c(NH2-)=2×l0-30,维持温度不变,向液氨中加入少量NH4Cl固体或NaNH2固体,不发生改变得就是( )A.液氨得电离度B.液氨得离子积常数C.c(NH4+)D.c(NH2-)2、(4分)中学化学实验中,淡黄色得pH试纸常用于测定溶液得酸碱性。
在25℃时,若溶液得pH=7, 试纸不变色;若pH〉7, 试纸变蓝色。
而要精确测定溶液得pH,需要用pH计。
pH计主要通过测定溶液得c(H+),来测定溶液得pH。
(1)已知水中存在如下平衡:H2O+ H2O H3O++OH-; △H>0kJ·mol-1现要使平衡向右移动,且所得得溶液呈酸性,选择得方法就是___________(填编号)A、向水中加入NaHSO4B、向水中加入Cu(NO3)2C、加热水至100℃[其中c(H+)=1×10-6mol·L-1]D、向水中加入(NH4)2SO4(2)现要测定100℃沸水得pH及酸碱性,若用pH试纸测定,则试纸显_______色,溶液呈_____性(填酸、碱或中);若用pH计测定,则pH________7(填“大于”、“等于”或“小于”)2、(各1分) (1)BD (2) 红,中;小于3、(8分) 重水(D2O)得离子积K w=1、6×10 -15 mo12·L-2、,可以用pH一样得定义来规定pD=-lg[D+],试求该温度下:①重水得pD=?②含0、01molNaOD得D2O溶液1L,其pD=?③溶解0、01molDCl得D2O溶液1L,其pD=?④在100mL0、25mol、L-1得DCl重水溶液中,加入50mL0、2 mo1·L-1得NaOD得重水溶液,其pD=?3、①[D+]=[OD-]=4×10-8mol、L-1pD=-lg[D+]=-lg4×10-8=8-2lg2≈7、4;②pD=-lg[D+]=-lg16×10-14≈12、8;③pD=-lg[D+]=-lg0、01=2; ④[D+]=0、1(mol、L-1);pD=-lg[D+]=-lg0、1=1、C、水解平衡:弱酸盐或弱碱盐或弱酸弱碱盐。
如:;△H>0配制溶液应加入少量酸防止水解。
不断加热溶液,蒸干灼烧可得到固体。
【强化练习】1、在相同温度下,等体积等物质得量得浓度得4种稀溶液:①Na2SO4、②H2SO4、③NaHSO4、④Na2S中所含带电微粒数由多到少得顺序就是(PH?)A ①=④>③=②B ④=①>③>②C ①>④>③>②D ④>①>③>②2.常温下,pH=5得H2SO4与Al2(SO4)3溶液中,水得电离度分别为α1与α2,则α1与α2得关系为,由水电离出得[H+]之比为。
3、BiCl3水解生成BiOCl沉淀、(1)写出水解反应得离子方程式_______________________(2)医药上把BiOCl叫作次氯酸铋,该名称________(填“合理”或“不合理”),其理由就是_________________ 、(3)配制BiCl3溶液时,其方法就是__________________________、(4)把适量固体BiCl3置于浓NaCl溶液可得到澄清溶液,其原因就是__________________4.(3分)某温度下0、1mol/LNa2CO3溶液中c(Na+)/c(CO32-)=20/9,其原因就是_________________________。
现往Na2CO3溶液中通入一定量得CO2后,c(Na+)/c(CO32-)=5/2,其原因就是________________________,此时c(HCO3-)得物质得量浓度为_________________________(体积变化忽略)。
1、D2、α2=10000α11:104一定物质得量得醋酸溶液冲稀100倍,测其PH(其它方法合理亦可)3 、(1)BiCl3+H2O=BiOCl↓+2HCl (2)不合理因BiOCl中Cl呈-1价而非+1(3)将BiCl3溶于含适量HCl得蒸馏水中(4)BiOCl+H2OBiOCl+2H++2Cl-,[Cl-]增大时,抑制了BiCl3水解4.(各1分)CO32-水解,c(CO32-)减小;CO2与Na2CO3发生反应生成NaHCO30、12mol/LD、溶解平衡:气体或固体溶于水形成得饱与溶液中形成得平衡体系,通常为固体得溶解平衡(1)气体得溶解平衡如:当加入NaCl、CaCO3等时平衡会发生移动。
