第8章_开环聚合
第八章 开环聚合
A M
+ SiR2 (OSiR2)3
O
A (SiR2O)3SiR2O M
SiR2O M
+ SiR2 (OSiR2)3
O
(SiR2O)4SiR2O M
强质子酸或 Lewis 酸也可使硅氧烷开环聚合,
活性种是硅烷阳离子
Si(R2) A
,环状单体插入而
增长;也可形成氧鎓离子而后重排成硅阳离子。
因此对引发剂的选择和单体的精制要求较高。 例如以五氟化磷为催化剂,在30℃聚合6小时,分
子量为30万左右;而以五氯化锑作催化剂时,聚合速率
和分子量要低的得多。
8.3.3 羰基化合物的聚合和三氧六环的阳离子聚合 1、羰基化合物
羰基化合物中的羰基C=O极性较大,有异裂倾向, 适于离子聚合,产物为聚缩醛。
8.2 环烷烃开环聚合热力学
8.2.1 环的大小 碳的四面体结构,C—C—C 键角为109°28’ 环状单体热力学稳定性: 3,4《 5,7~11〈 12以上,6
构象张力 角张力
实际上较少用到九元以上的环状单体。环烷烃在 热力学上容易开环聚合的程度为3、4 > 8 > 7、5。
三、四元环烷烃由键角变化引起的环张力很大 (三元环60°,四元环90°),环不稳定而易开环聚合。 五元环键角接近正常键角(108 °),张力较小,环 较稳定。
酰化的内酰胺比较活泼,是聚合的活性中心,因
此可以采用酰氯、酸酐、异氰酸酯等酰化剂与单体反
应,使己内酰胺先形成N-酰化己内酰胺。这样可消除 诱导期,加速反应,缩短聚合周期。
O C (CH2)3 NH + RCOCl
O C (CH2)3 N O C R + HCl
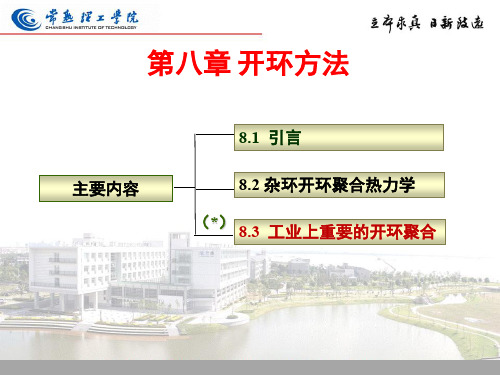
8.3.5 环硅氧烷
开环聚合

第八章 开环聚合8.1 概述高分子化学中,以环状单体通过开环聚合来合成聚合物,同样具有重要的地位。
在这种聚合过程中,增长链通过不断地打开环状结构,形成高聚物:以环醚为例,环氧乙烷经开环聚合反应,得到一种聚醚,即聚氧化乙烯。
这在工业上已得到应用。
能够进行开环聚合的单体很多,如环状烯烃,以及内酯、内酰胺、环醚、环硅氧烷等环内含有一个或多个杂原子的杂环化合物。
开环聚合既具有某些加成聚合的特征,也具有缩合聚合的特征。
由开环聚合得到的聚合物,重复单元与环状单体开裂时的结构相同,这与加成聚合相似;而聚合物主链中往往含有醚键、酯键、酰胺键等,与缩聚反应得到的聚合物常具有相同的结构,只是无小分子放出。
开环聚合与缩聚反应相比,还具有聚合条件温和、能够自动保持官能团等物质的量等特点,因此开环聚合所得聚合物的平均分子质量,通常要比缩聚物高得多。
有些单体如乳酸,采用缩聚反应无法得到高分子质量的聚合物;而采用乳交酯的开环聚合,就能够获得高分子质量的聚乳酸。
但是,与缩聚反应相比,开环聚合可供选择的单体较少,例如二元酸与二元醇能够通过缩聚获得聚酯;而开环聚合,只有相当于α,ω-羟基酸的环内酯可供选择。
聚酰胺的情况也是如此。
另外,有些环状单体合成困难,因此由开环聚合所得到的聚合物品种受到限制。
开环聚合就机理而言,有些属于逐步聚合,有些属于连锁聚合。
8.1.1 聚合范围及单体可聚性如前所述,环醚、环酯、环酰胺、环硅氧烷等能够进行开环聚合。
此外,环胺、环硫化物、环烯烃、以及N-羧基-α-氨基酸酐等同样也能进行开环聚合。
环状单体能否转变为聚合物,取决于聚合过程中自由能的变化情况,与环状单体和线形聚合物的相对稳定性有关。
Dainton 以环烷烃作为环状单体的母体,研究了环大小与聚合能力的关系。
表6-1列出了环烷烃在假想开环聚合时的自由能变化ΔG lc 0、焓变ΔH lc 0、及熵变ΔS lc 0。
R X [ R X ]n n [ CH 2 CH 2 O ]n n H 2C CH 2O聚合过程中,液态的环烷烃(l )转变为无定型的聚合物(c )。
第八章_开环聚合

O(CH 2) 4 O(CH2 )4 O
O(CH 2) 4 O(CH2 )4 (CH 2) 4 O
O
O(CH2 )4 O(CH 2) 4 O + (CH 2) 4 O
环状低聚物
链增长与向高分子链转移是一对竞争反应:主要取决于单体 与高分子中所含醚基亲核性的相对强弱,单体含醚基的相对亲核 性越强越有利于链增长,相反则有利于向高分子链转移。 单体与高分子链中O的亲核性之比随单体环的增大而增大。 三元环醚单体如环氧乙烷聚合链增长时:
O H+ + O O H O O O + O O O H ( OCH 2OCH2 OCH2 )nO O H2O 终止 O H OCH 2OCH2 OCH2 O O H (OCH 2OCH2OCH2 ) OH n+1 O 三聚甲醛
所得聚合物分子链的末端半缩醛结构很不稳定,加热时易发 生解聚反应分解成甲醛,不具有实用价值。解决方法之一是把产
R O
环氧化物
O O
环丙醚
O 四氢呋喃
O O 三聚甲醛
(1)链引发反应
许多用于乙烯基单体阳离子聚合反应的引发剂也可用于环醚 的阳离子开环聚合,包括强质子酸、Lewis酸、碳阳离子源 /Lewis酸复合体系等。 以质子酸引发四氢呋喃聚合为例:
H A + O
+ -
α-C具有缺电子性
H O A二级环氧鎓离子
第八章 开环聚合
8.1 概述 开环聚合: 环状单体开环相互连接形成线型聚合物的过程。
开环聚合的特点: 链式聚合反应: 包括链引发、链增长和链终止等基元反应。 但开环聚合反应与乙烯基单体的链式聚合反应又有所区别,
其链增长反应速率常数与许多逐步聚合反应的速率常数相似,而
第8章 开环聚合

反应
通式: nR Z
[R Z] n
式中的X为环状单体中的官能团或杂原子,如O、S、N等, R代表-[CH2]n-.
开环聚合的特征
聚合过程中只发生环的破裂,基团或者杂原子由分子内连 接变为分子间连接,没有新的化学键和新的基团产生。
与连锁聚合相比较 •连锁聚合的推动力是化学键键型的改变,虽然大多数环 状单体是按离子型聚合机理进行的,但开环聚合的推动力 是单体的环张力,这一点与连锁聚合不同。 •开环聚合所得的聚合物其结构单元的化学组成与单体的 化学组成完全相同,这一点与连锁聚合相同。
主要用于生产带有醚键、酯键、酰胺键等聚合物。
开环聚合的单体 常见的单体
环醚、环亚胺、环状硫化物、环缩醛、内酯、内酰胺、 环状磷化物、状氮化物环状硅化物等。
环状单体的聚合能力
单体种类
3
4
环烷烃
+
环醚
+
+
环硫化物
+
+
环亚胺
+
+
环二硫化物
+
环缩醛
环内酯
+
环内酰胺
+
环碳酸酯
环状尿素
环状氨基甲酸 酯
环状酸酐
(a)
将式(a)积分,得:
[N]
[N] 0
CM 1 CM
([M] 0
[M])
(b)
[N]0为无向单体转移时的聚合物浓度。
有、无向单体链转移时的平均聚合度分别为:
X n [M]0 [M] [N]
(c)
(Xn )0
[M]0 [M] [N]0
(d)
综合式(b)、(c)、(d)可得:
O
RO [CH2CH2O] nCH2CH2O M
环氧化物的开环聚合一般无链终止,需人为加入终止剂 终止(如酚类化合物)。
第八章开环聚合

量很高的聚合物。 环氧丙烷用适当的引发剂还可制得光学活性聚合物。
12
环氧化合物的阴离子开环聚合
引发剂:氢氧化物、烷氧基化合物等;
作用:制得重要的聚醚类非离子表面活性剂。
特点:无终止反应,具有活性聚合特征,加入
终止剂(如酚类)使链终止。
环氧乙烷(Ethylene oxide)聚合后加入环氧丙烷 会生成嵌段共聚物,是聚醚类表面活性剂的重 要品种。
10
三. 工业上重要的开环聚合
3. 1 环醚(cyclic ether)
简单的环醚中,常见有3、4、5元环可以开环聚合。 3元环醚由于其环张力大,阳离子、阴离子、配位聚 合都可以。4、5元环醚只能进行阳离子聚合。
R O
环氧化物
O O
环丙醚
O
四氢呋喃
O
O
三聚甲醛
11
环氧化物的开环聚合
3元环醚即环氧化物(epoxide) 阳离子聚合:副反应多,工业上不常用; 配位聚合:环氧化物的配位阴离子聚合可得到分子
开环聚合,具体引发反应如下:
n C4H9Li + CH3
O C (CH2)5 NH + n C4H9-Li+
O CH CH2
n C4H9 CH2
O C
CH3 - + CH O Li
(CH2)5 N Me + n C4H10
Ring-Opening Polymrization of Cyclic Acetals(醛)
Polymerization of Lactones(内酯)
1
Development of Ring-Opening Polymerization Ring-Opening polymerization has been developed and studied since 1950s. A lot of products which have been industrialized, such as, polycaproamide, polyformaldehyde, polytetrahydrofuran, polyethylene oxide, polypropylene oxide etc. As the late direction, isomerized ring-opening polymerization of cycloolefin (环烯) and spirocyclic (螺环化合物) monomer have been studied.
第八章开环聚合

氯化聚醚
• 丁氧环醚:丁氧环醚可以开环聚合,但是有应用价值的是3, 3‘-二(氯亚甲基)丁氧环。聚合产物俗称氯化聚醚,又称聚 氯醚。结晶性成膜材料,熔点177℃,机械强度比氟树脂好, 吸水性低,耐化学药品腐蚀,尺寸稳定性好,电性能优良, 可作为工程塑料。 • 由于分子中的次甲基上的碳无取代基,因而赋予大分子以良 好的柔顺性,另由于分子链上季碳原子上连有两个位阻较大 的氯甲基,又增加了链的刚性,因此,CPT的分子链为刚柔 兼备并以柔为主。另一方面,由于具有极性的氯甲基的对称 排列而不显极性,同时由于氯原子为憎水基,使它具有极低 的吸水率和良好的电绝缘性。
Cl
O
Cl Cl
Cl
Cl Cl
Cl
O
TCDD 二噁英
Cl
Cl
O
Cl Cl Cl
Cl
二噁英:指结构和化学性质相近的多氯二苯二恶英(PCDDs) 和多氯二苯并呋喃(PCDFs)。某些类二恶英多氯联苯(PCBs) 具有相似毒性,归在“二恶英”名下。大约有419种类似二 恶英的化合物被确定, 但其中只有近30种被认为具有相当的 毒性,以TCDD的毒性最大。
链引发
如果用醇钠引 发,必须脱除 副产醇,以氢 氧化钠引发, 脱除水
聚硅氧烷
• 八元环的硅氧烷开环聚合,热力学特征:1、 ∆H接近于零,∆S却是正值,熵增成为聚合 动力。 • 2、存在环-线平衡,聚合时线性单体和环状 单体共存;在较高的温度下,解聚成6至12 元环的环状低聚物。 • 反应可以采用阴离子引发,也可采用阳离 子引发,阳离子引发产品分子量低,常用 于硅油合成。
• 硅原子半径大于C,硅氧键及硅碳键比较长,硅 侧基相互作用小,容易绕硅氧键旋转,Tg-130℃。 在很宽的温度范围内保持柔顺性和高弹性,耐化 学品、耐氧化、疏水、电绝缘等优点。 • 高分子线性主要做硅橡胶,低分子线性和环状的 做硅油,有三官能度存在的,可以固化交联,做 涂料。 • 低分子的具有良好的表面活性,可以做表面活性 剂。聚氨酯工业用的泡沫稳定剂基本上都是硅油 类产品。 • 聚硅氧烷使用温度在180℃以下,加热至250℃, 降解成环状低聚物。
第8章 开环聚合
(ring opening polymerization)
开环聚合是指具有环状结构的单体经引发聚合,将环打 开形成高分子化合物的一类聚合反应。
一、开环聚合的特征 开环聚合既不同于连锁聚合,也不同于逐步聚合,其 特征为: ⒈ 聚合过程中只发生环的破裂,基团或者杂原子由 分子内连接变为分子间连接,并没有新的化学键和新 的基团产生。 ⒉ 与连锁聚合相比较 连锁聚合的推动力是化学键键型的改变,虽然大 多数环状单体是按离子型聚合机理进行的,但开环聚 合的推动力是单体的环张力,这一点与连锁聚合不同。 开环聚合所得的聚合物其结构单元的化学组成与 单体的化学组成完全相同合反应相比较 开环聚合虽然也是制备杂链聚合物的一种方法, 但聚合过程中并无小分子缩出。 开环聚合的推动力是单体的环张力,聚合条件比 较温和,而逐步聚合的推动力是官能团性质的改变, 聚合条件比较苛刻.所以,用缩聚难以合成的聚合物, 用开环聚合较易合成。
二. 环状单体的聚合活性
——能否开环及聚合能力的大小
环状单体的聚合活性取决于主要是热力学因素,即环状 单体和线型结构聚合物的相对稳定性。
环状单体热力学稳定性次序: 3,4《5,7~11〈12以上,6 对于杂环化合物,如环醚、环酯、环酰胺等,由于 杂原子提供了引发剂亲核或亲电进攻的位置,所以在 动力学上它们比环烷烃更有利于开环聚合。
第8章 开环聚合反应

¾ 酰化的内酰胺比较活泼,是聚合的活性中心,因此可 以采用酰氯、酸酐、异氰酸酯等酰化剂与单体反应, 使己内酰胺先形成N-酰化己内酰胺。这样可消除诱导 期,加速反应,缩短聚合周期。
O C (CH2)3 NH + RCOCl
O C
O (CH2)3 N C R + HCl
(4) 环硅氧烷的开环聚合
¾ 三、四元环烷烃由键角变化引起的环张力很大(三元环 60o,四元环90o);
¾ 五元环和七元环的键角接近正常键角(108o),环上因邻近氢 原子相互排斥形成构象张力,而易开环。
¾ 六元环烷烃呈椅式结构,键角变形为0,不能开环聚合。 ¾ 八元以上的环有跨环张力(属构象张力),即环上氢或取
代基处于拥挤状态造成相斥,其聚合能力较强。十一元以 上环的跨环张力消失,环较稳定,不易聚合。
− d[N] = ktr,M = CM d[M] kp + ktr,M 1 + CM
其中CM为向单体转移常数。
将上式积分,得:
[N]
=
[N]0
+
1
CM + CM
([M]0
−
[M])
[N]o 、(Xn)o为无向单体转移时的聚合物浓度和平均 聚合度。
向单体链转移时的平均聚合度分别为:
X n = [M] 0 − [M] [N]
¾ 其他六元的环酰胺、环酐都较易聚合。如:丙交酯开环 聚合成聚乳酸。
O
CH3
C
CH
O
O
CH
C
C H3
O
CH3
H [ OCH
C ]n O H
环上有取代基时对聚合不利,有大侧基的线性大分 子不稳定,易解聚成环。如四氢呋喃能聚合,2-甲基 四氢呋喃却不能聚合。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
与链转移反应不同,交换反应生成的端羟基聚合物并不是“死” 的聚合物,而只是休眠种,可和增长链之间发生类似的交换反 应再引发聚合反应:
通过交换反应,醇也可引发单体聚合,因此若无其他链转移
反应时,聚合产物的数均聚合度为:
X n C[M]0 [I]0 [ROH]
4
二聚体伯胺阴离子不与羰基共轭,不稳定,很快从单体的酰 胺基上夺取H形成含环酰胺结构的二聚物,同时生成己内酰胺 阴离子:
链增长
三聚体阴离子
二聚体
所得二聚物中的环酰胺键,由于其环外N-酰基的吸电子作 用,增强了环的缺电子性,因此其与内酰胺阴离子的反应活性 比内酰胺单体高得多,易受内酰胺阴离子进攻开环进行链增长 反应.
课堂作业讲解: 1.环氧乙烷阴离子开环聚合可以获得高分子量的聚合物,而环 氧丙烷则只能得到分子量较低的聚合物,这是因为_________ 。
2.相比于环烷烃,杂环化合物从动力学上更易进行开环聚合, 这是因为_____________。
课堂作业讲解: 3.下列哪些聚合物其结构单元的元素组成与单体相同( )
一些环烷烃转变为线形高分子时的ΔG
单体
环丙烷 环丁烷 环戊烷 环己烷
环庚烷
ΔG -22.1 -21.2 -2.2
1.4
-3.9
kcal/mol)
环辛烷
-8.2
可见除环己烷外,其余环烷烃的开环聚合的ΔG 均小于0,反 应在热力学上都是可行的,其热力学可行性顺序为:
三元环,四元环 > 八元环 > 五元环,七元环
(4)链终止反应
阳离子开环聚合的链终止反应主要为增长链氧鎓离子与抗衡 阴离子结合,如:
随着单体环的增大,单体与聚合物中醚基的亲核性之比也增 大,如四氢呋喃聚合的环状低聚物的含量少于几个百分点。
(5) 应用 三聚甲醛(三氧六环)的阳离子开环聚合:
O
H+ + O O
O
O
HO
+O
O
O
O 三聚甲醛
H OCH2OCH2OCH2 O O
(C 为单体转化率)
环氧丙烷的阴离子开环聚合通常只能得到分子量较低的聚合物 (<6000),主要原因是聚合反应过程中向单体的链转移反应:
CH3
O
CH2 CH O- Na+ + CH3 CH CH2
CH3
O
CH2 CH OH + H2C CH CH2-Na+
H2C CH CH2O-Na+
再引发聚合
8.3.2 内酰胺
绝大多数六元环单体不能开环聚合
1
8.2 阳离子开环聚合反应 8.2.1 环 醚
环醚分子中的 C-O 键是其活性基,其中的O具有Lewis碱 性,因此除张力大的三元环环氧化物外,环醚只能进行阳离子开 环聚合。
常见的只含一个醚键的环醚单体包括三元环(环氧化物)、 四元环(如环丙醚)和五元环(如四氢呋喃);常见的含两个 以上醚键的环醚单体主要为环缩醛,如三聚甲醛。
8.2.2 环硅氧烷
最常见的环硅氧烷单体八甲基环四硅氧烷(D4):
H3C CH3
Si O O Si
CH3
n H3C Si
O CH3
H3C O Si
H3C CH3
CH3
H( O
Si
) n
CH3
产物聚硅氧烷是一类以Si-O为主链结构的有机硅聚合物, 分子量较低时呈液态,称硅油,而高分子量时呈橡胶类的高弹 性,称硅橡胶。
其增长链活性末端:环外N-酰化环酰胺。起始链增长活性 中心为二聚体所带的环外N-酰化环酰胺结构,二聚体是实际的 引发剂,所加阴离子催化剂其活化单体的作用。
本章重点 (1)开环聚合的概念; (2)开环聚合的热力学和动力学特征; (3)哪些单体可以进行开环聚合? (4)了解常见的可进行开环聚合的单体及其聚合物。
O(CH2)4 O(CH2)4 O
O(CH2)4 O(CH2)4
O
(CH2)4 O
O(CH2)4 O
O (C H2)4 +
(CH2)4 O
环状低聚物
链增长与向高分子链转移是一对竞争反应:主要取决于单体 与高分子中所含醚基亲核性的相对强弱,单体含醚基的相对亲 核性越强越有利于链增长,相反则有利于向高分子链转移。
OCH2CH2CH2CH2 O A-
+O
OCH2CH2CH2CH2OCH2CH2CH2CH2 O A-
链增长活性中心与抗衡阴离子之间存在离解平衡:多种活 性种
(3)链转移反应 向高分子的链转移反应是环醚阳离子开环聚合中常见的链
转移反应。
链转移反应的结果:高分子链发生交换
向高分子的链转移反应也可发生在分子内, 即回咬反应,结果 得到环状低聚物:
阳离子聚合机理:与环醚阳离子开环聚合相似
8.3 阴离子开环聚合反应 8.3.1 环氧化物
环醚是Lewis碱,一般只能进行阳离子开环聚合。但环氧化 物由于其三元环张力大,能进行阴离子开环聚合。引发剂包括 金属氢氧化物、金属烷氧化合物、金属氧化物、烷基金属化合 物以及电子转移阴离子引发剂等。
以环氧乙烷为例,其阴离子开环聚合过程可示意如下: 链引发反应:
+O
HO CH2CH2CH2CH2 O A-
三级氧鎓离子链增长活性中心
在四氢呋喃等活性较低环醚单体的聚合反应中,常加入少量 活泼三元环醚单体如环氧乙烷提高引发速率。此时引发反应首 先通过活泼单体形成二级或三级氧鎓离子活性种,再引发低活 性的单体聚合,此时活泼单体可看作是引发促进剂。
(2)链增长反应
链增长反应为单体的 O 对增长链的三级环氧鎓离子活性中 心的α- C的亲核进攻反应。以四氢呋喃的聚合为例:
O H ( OCH2OCH2OCH2 )nO
O
H2O 终止
H(OCH2OCH2OCH2
) OH
n+1
所得聚合物分子链的末端半缩醛结构很不稳定,加热时易发
生解聚反应分解成甲醛,不具有实用价值。解决方法之一是把产
物和乙酐一起加热进行封端反应,使末端的羟基酯化,生成热稳
定性的酯基。
工业上已用这种方法生产性能优良的工程塑料聚甲醛(POM)。
第 8 章 开环聚合
主讲:张安强
email: aqzhang@
(1)开环聚合的概念; (2)开环聚合的热力学和动力学特征; (3)哪些单体可以进行开环聚合? (4)了解常见的可进行开环聚合的单体及其聚合物。
8.1 概述 开环聚合:环状单体开环相互连接形成线型聚合物的过程。
开环聚合的特点: 链式聚合反应: 包括链引发、链增长和链终止等基元反应。
动力学因素:动力学上可行的开环方式和反应。
环烷烃的键极性小,不易受引发活性种进攻而开环。
杂环化合物中的杂原子易受引发活性种进攻并引发开 环,在动力学上比环烷烃更有利于开环聚合。
因此,绝大多数的开环聚合单体都是杂环化合物,包括 环醚、环缩醛、内酯、内酰胺、环胺、环硫醚、环酸酐等。
同类环单体的聚合反应活性与环大小密切相关: 3~4元环 > 7~11元环 > 5元环
R
O
O
O
O
OO
环氧化物 环丙醚 四氢呋喃 三聚甲醛
(1)链引发反应
许多用于乙烯基单体阳离子聚合反应的引发剂也可用于环 醚的阳离子开环聚合,包括强质子酸、Lewis酸、碳阳离子源 /LewiA- + O
HO A-
α-C具有缺电子性
二级环氧鎓离子
HO A-
首先己内酰胺与碱金属反应生成内酰胺阴离子:
强碱如碱金属、金属氢化物、金属氨基化合物等可与内酰 胺反应形成酰胺阴离子,但内酰胺的阴离子开环聚合并不是由 强碱直接引发,而是活化单体机理。
以碱金属引发己内酰胺阴离子开环聚合为例,其链引发反应 可分为以下三步:
然后内酰胺阴离子与内酰胺单体的羰基发生亲核加成反 应,使单体开环生成二聚体伯胺阴离子:
但开环聚合反应与乙烯基单体的链式聚合反应又有所区别, 其链增长反应速率常数与许多逐步聚合反应的速率常数相似, 而比通常乙烯基单体的链式聚合反应低数个数量级。
可在高分子主链结构中引入多种功能基:酯、醚、酰胺等
聚合反应前后的体积收缩比乙烯基单体聚合小
环状单体开环聚合的难易取决于两方面因素: 热力学因素
单体与高分子链中O的亲核性之比随单体环的增大而增大。 三元环醚单体如环氧乙烷聚合链增长时:
OCH2CH2 O A-
+O
OCH2OCH2CH2 O A-
单体中sp3杂化的O转变为聚合物中sp2杂化的氧鎓离子,使
键角张力增大,单体与高分子链中O亲核性之比最小,不利于
链增长。
2
由于高分子中所含醚基的亲核性更强,有利于向高分子的 链转移,生成环状低聚物。事实上通常的环氧乙烷阳离子聚合 的主要产物为1,4-二氧六环(80%~90%),因此环氧乙烷的 阳离子开环聚合对于合成线形聚合物并无实用价值。
A. 聚甲醛 B. 聚1, 3 -丁二烯 C. 聚对苯二甲酸丁二醇酯 D. 环氧树脂预聚物 E. 聚环氧丙烷
5
3
链增长反应 :
链增长活性中心为烷氧阴离子。
环氧乙烷的阴离子聚合表现出活性聚合的特征,聚合产物的 数均聚合度为:
X n C[M]0 [I]0
C:单体转化率
醇的影响 一些金属烷氧化物和氢氧化物引发的聚合反应体系中,常
加入适量的醇: 溶解引发剂,形成均相聚合体系; 促进增长链阴离子与抗衡阳离子的离解,增加自由离子浓 度, 加快聚合反应速度。 在醇的存在下,增长链可和醇之间发生如下交换反应:
