中考化学工业流程题(含答案)
中考化学流程图综合经典题附详细答案

一、中考初中化学流程图1.黄铜矿(主要成分2CuFeS )经初步处理后,所得溶液甲中的溶质为243Fe SO ()、4CuSO 及24H SO 。
某同学通过废铁屑与溶液甲反应,制取补血剂的原料碳酸亚铁并回收铜。
主要步骤如下图所示:温馨提示:2434+Fe (SO )Fe=3FeSO﹙1﹚操作a 的名称是________,该操作中会用到玻璃棒,其作用是___________ 。
﹙2﹚不溶物的成分为___________________ 。
﹙3﹚步骤Ⅰ中生成铜的化学方程式为_________;废铁屑中含有少量铁锈,却对产物的成分没有影响,原因是________。
步骤Ⅲ中加入一种可溶性试剂可实现转化,从复分解反应的条件分析,该试剂可以是___________(填化学式)溶液。
【答案】过滤 引流 Cu 、Fe 44=Fe+CuSO FeSO +Cu 铁锈可与硫酸反应生成硫酸铁,硫酸铁再和铁反应生成硫酸亚铁 23Na CO【解析】【分析】铁和硫酸铜反应生成硫酸亚铁和铜,氧化铁能和稀硫酸反应生成硫酸铁和水,硫酸铁能和铁反应生成硫酸亚铁。
【详解】(1)操作a 的名称是过滤,该操作中会用到玻璃棒,其作用是引流;(2)不溶物的成分为铁和硫酸铜反应生成的铜和过量的铁;故不溶物的成分为Cu 、Fe 。
(3)步骤I 中,铁和硫酸铜反应生成硫酸亚铁和铜,生成铜的化学方程式为44=Fe+CuSO FeSO +Cu ;废铁屑中含有少量铁绣,却对产物的成分没有影响,原因是铁锈中的氧化铁能和稀硫酸反应生成硫酸铁,硫酸铁能和铁反应生成硫酸亚铁。
步骤Ⅲ中,加入碳酸钠溶液时,碳酸钠能和硫酸亚铁反应生成碳酸亚铁和硫酸钠,从而得到碳酸亚铁,因此从复分解反应的条件分析,该试剂可以是Na 2CO 3溶液。
2.某种镁矿石的主要成分是碳酸镁,还含有较多的脉石(SiO 2)和少量石灰石。
下图是利用该镁矿石制备七水硫酸镁(MgSO 4·7H 2O)的工艺流程。
2020年江西省中考化学专题强化训练《工业流程图题》(word版有答案)
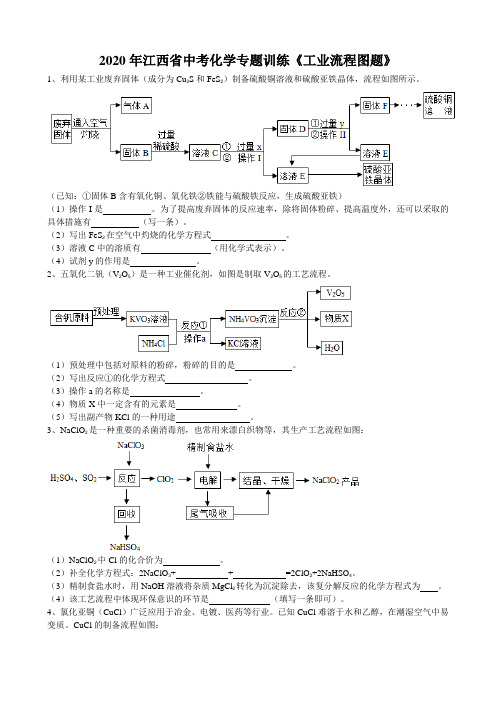
2020年江西省中考化学专题训练《工业流程图题》1、利用某工业废弃固体(成分为Cu2S和FeS2)制备硫酸铜溶液和硫酸亚铁晶体,流程如图所示。
(已知:①固体B含有氧化铜、氧化铁②铁能与硫酸铁反应,生成硫酸亚铁)(1)操作I是。
为了提高废弃固体的反应速率,除将固体粉碎、提高温度外,还可以采取的具体措施有(写一条)。
(2)写出FeS2在空气中灼烧的化学方程式。
(3)溶液C中的溶质有(用化学式表示)。
(4)试剂y的作用是。
2、五氧化二钒(V2O5)是一种工业催化剂,如图是制取V2O5的工艺流程。
(1)预处理中包括对原料的粉碎,粉碎的目的是。
(2)写出反应①的化学方程式。
(3)操作a的名称是。
(4)物质X中一定含有的元素是。
(5)写出副产物KCl的一种用途。
3、NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,其生产工艺流程如图:(1)NaClO2中Cl的化合价为。
(2)补全化学方程式:2NaClO3+ + =2ClO2+2NaHSO4。
(3)精制食盐水时,用NaOH溶液将杂质MgCl2转化为沉淀除去,该复分解反应的化学方程式为。
(4)该工艺流程中体现环保意识的环节是(填写一条即可)。
4、氯化亚铜(CuCl)广泛应用于冶金、电镀、医药等行业。
已知CuCl难溶于水和乙醇,在潮湿空气中易变质。
CuCl的制备流程如图:(1)“滤液1”中的阳离子除Na+外,还存在较多的离子是(写离子符号)。
(2)“反应”中发生的化学变化是2CuCl2+Na2SO3═2CuCl↓+2NaCl+SO3,产生的SO3迅速与水化合生成一种酸,该反应的化学方程式为。
(3)“操作a”的名称是。
本流程中可以循环利用的物质(水除外)是(写化学式)。
(4)可用“水洗”的原因是,“醇洗”的目的是。
5、氧化锌(ZnO)可作为紫外线吸收剂应用于化妆品中,其一种生产工艺如下:(1)推测草酸的化学式是;(2)“沉锌”过程中发生复分解反应,反应的化学方程式是;(3)“操作A”的名称是。
中考化学真题分类汇编考点工艺流程含答案

中考化学真题分类汇编考点工艺流程含答案 Standardization of sany group #QS8QHH-HHGX8Q8-GNHHJ8-HHMHGN#3 3 3考点34 工艺流程一、选择题(2018·内蒙古呼和浩特)8.黄铁矿的主要成分为二硫化亚铁(FeS2),工业上可利用黄铁矿煅烧的产物冶炼铁和生产浓硫酸,其工业流程如下:下列说法错误的是A.反应②不是置换反应,反应③④为化合反应B.反应①中各元素的化合价均发生了改变C.该工业生产过程产生的废气中的SO2可以用熟石灰溶液吸收D.向制得的100克98%的浓硫酸中加入100克蒸馏水,配制49%的稀硫酸【答案】D(2018·新疆乌鲁木齐)含硫煤燃烧会产生大气污染。
为防治该污染,某工厂设计的新的治污方法不仅吸收了 SO2,同时还得到了某种化工产品。
该工艺流程如图所示,下列叙述不正确的是A. 该流程中可得到化工产品H2SO4B. 图中 FeSO4 → Fe2(SO4)3 的反应类型是复分解反应C. 该流程中化合价发生改变的元素为 Fe、S 和 OD. 图中吸收 SO2 的化学反应方程式为:Fe2(SO4)3 + SO2 + 2H2O == 2FeSO4 + 2H2SO4【答案】B(2018辽宁葫芦岛)(分)合成气是工业生产中的一种原料气,主要成分是一氧化碳和氢气。
它可以冶炼钢铁、生产二甲醚等。
请根据图示回答。
(注:图中括号内化学式表示相应物质的主要成分)(1)请写出利用合成气炼铁的化学方程式(写一个即可)(2)二甲醚(CH3OCH3)被称为21世纪新型燃料,能实现高效清洁燃烧,请写出二甲醚在空气中充分燃烧生成二氧化碳和水的化学方程式。
(3)合成气在不同催化剂作用下,可以合成不同的物质。
仅用合成气为原料不可能得到的物质是(填字母序号)A.甲醇(CH3OH) B.乙二醛(HC2O2)C.尿素〔CO(NH2)2]21.(1)3CO+ Fe2O32Fe + 3CO2(或3H2+ Fe2O32Fe + 3H2O)(2分)(2)CH3OCH3+3O32CO2+3H2O(2分)(3)C(1分)(2018·江苏无锡)17.(分)MgSO47H2O是一种重要的化工原料,某工厂以一种镁矿石(主要成分为SiO2和MgCO3,还含有少量FeCO3)为原料制备MgSO47H2O的主要流程如图:已知:SiO2既不溶于水也不溶于稀硫酸。
初中化学流程题知识点总结含答案
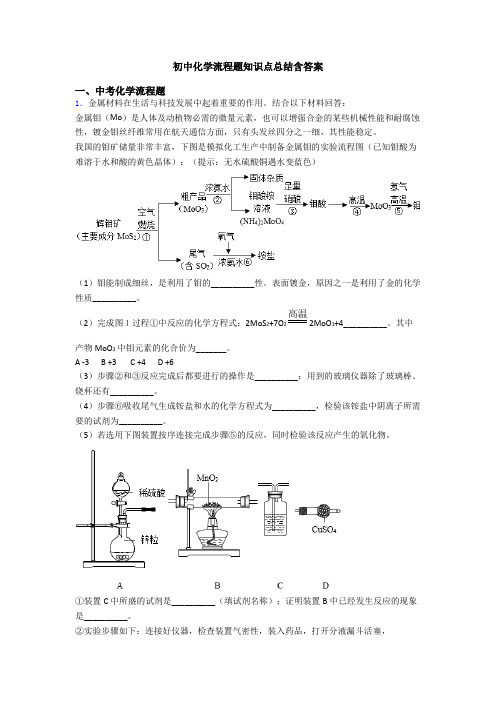
初中化学流程题知识点总结含答案一、中考化学流程题1.金属材料在生活与科技发展中起着重要的作用。
结合以下材料回答:金属钼(Mo)是人体及动植物必需的微量元素,也可以增强合金的某些机械性能和耐腐蚀性,镀金钼丝纤维常用在航天通信方面,只有头发丝四分之一细,其性能稳定。
我国的钼矿储量非常丰富,下图是模拟化工生产中制备金属钼的实验流程图(已知钼酸为难溶于水和酸的黄色晶体):(提示:无水硫酸铜遇水变蓝色)(1)钼能制成细丝,是利用了钼的__________性。
表面镀金,原因之一是利用了金的化学性质__________。
(2)完成图1过程①中反应的化学方程式:2MoS2+7O2高温2MoO3+4__________。
其中产物MoO3中钼元素的化合价为_______。
A -3B +3C +4D +6(3)步骤②和③反应完成后都要进行的操作是__________;用到的玻璃仪器除了玻璃棒、烧杯还有__________。
(4)步骤⑥吸收尾气生成铵盐和水的化学方程式为__________,检验该铵盐中阴离子所需要的试剂为__________。
(5)若选用下图装置按序连接完成步骤⑤的反应,同时检验该反应产生的氧化物。
①装置C中所盛的试剂是__________(填试剂名称);证明装置B中已经发生反应的现象是__________。
②实验步骤如下:连接好仪器,检查装置气密性,装入药品,打开分液漏斗活塞,_______→______→______→________。
(请按正确的先后顺序填入下列步骤的代号)a收集气体并检验其纯度 b停止加热,充分冷却c加热反应一段时间 d关闭分液漏斗活塞,停止通氢气2.某硫酸厂产生的烧渣(主要含 Fe2O3、FeO 及少量 SiO2)可用于制备FeSO4•7H2O和还原铁粉,其流程如图。
Ⅰ.写出“酸溶”中发生的任一反应的化学方程式___________。
Ⅱ.“滤渣”的主要成分是___________(填化学式)。
化学流程题(讲义及答案)含答案

化学流程题(讲义及答案)含答案一、中考化学流程题1.我国制碱工业先驱﹣﹣侯德榜发明了“侯氏制碱法”。
在充分利用空气资源和海洋资源的基础上,结合“侯氏制碱法”的基本原理,模拟流程如图:(查阅资料)在通常情况下,1体积的水约能溶解700体积的氨气。
请回答下列问题:(1)操作a的名称是___________。
(2)写出沉淀池中发生反应的化学方程式:___________。
(3)为了提高产率,往沉淀池中通入气体时应先通入___________(填“X”或“NH3”)。
(4)除去纯碱中少量碳酸氢钠的方法是___________。
(5)上述流程中可以循环利用的物质除了NH3外,还有___________(填化学式)。
2.轻质碳酸镁是广泛应用于橡胶和塑料的化工产品,以卤块(主要成分为MgCl2,含Fe2+、Mn2+等杂质离子)为原料制备轻质碳酸镁的工艺流程如下。
(查阅资料)Ⅰ、碳酸氢铵受热温度过高会发生分解;Ⅱ、下表中为生成氢氧化物沉淀的pH物质Mg(OH)2Fe(OH)2Fe(OH)3Mn(OH)2开始沉淀9.97.6 2.78.3沉淀完全11.110.2 3.79.6(2)次氯酸钠(NaC1O)中氯元素的化合价为______,次氯酸钠中阴离子符号是______。
(3)按照化肥的分类,碳酸氢铵属于______。
(4)“调节pH ”为的是除去溶液中的杂质离子,写出MnC12杂质与NaOH 反应的化学方程式______;为保证除尽杂质的同时不让Mg 2+沉淀应调节溶液pH 至9.6,故“转化”一步的目的是______。
(5)“热解”温度不高于75℃,其原因是______。
3.现有含NaCl 、Na 2SO 4、NaNO 3的混合溶液,选择适当的试剂将其转化为相应的沉淀或固体,从而实现Cl ﹣、24SO -、3NO -的相互分离。
相应的实验过程可用下列流程图表示:(1)写出上述实验过程中所用试剂、沉淀的化学式:试剂1:___________沉淀C :___________(2)写出溶液a 中所含有的阳离子___________;(3)恰当地控制试剂4的加入量的方法是___________。
2024届中考化学综合专项复习训练(流程题)含答案

已知:①电石渣中的杂质滩溶于水,也不与溶液反应,溶液呈酸性;4NH Cl 4NH Cl ②“浸取”时的主要反应为;24232Ca(OH)+2NH Cl=CaCl +2NH H O ⋅③“碳化”时的主要反应为.3223422CaCl +2NH H O+CO =CaCO +2NH Cl+H O ⋅↓(1)实验室进行过滤操作时,玻璃棒的作用是。
(3)Ⅲ中发生复分解反应,生成一种盐和一种过氧化物,则反应的化学方程式是 。
(4)减压能够降低蒸管温度,从化学性质角度说明V 中采用减压蒸馏的原因:。
22H O Ⅱ.的应用22H O 火箭动力助燃剂:在火箭推进器中装有液态的肼和过氧化氢。
当它们混合时,即产生()24N H 大量和水蒸气,并放出大量热。
2N (5)写出该反应的化学方程式:。
(6)该反应用于火箭推进剂,与传统化石燃料燃烧相比,除释放大量热和快速产生大量气体外,还有一个很突出的优点是:。
3.(23-24九年级下·江苏扬州·阶段练习)粮食安全是“国之大者”。
(1)守住良田沃土,保障粮食安全。
①土壤酸化不利于农作物生长。
要改良酸化土壤,可选用的物质为 。
A .B .熟石灰C .稀硫酸3KNO ②某农田改良后为5.4,该地区常见农作物最适宜生长的土壤范围如下:pH pH 农作物茶树油菜水稻萝卜pH5.0 5.5- 5.8~6.76.0~7.07.0~7.5该农田适合种植的农作物是。
③化肥和农药对农业增产有重要作用。
下列说法不正确的是 。
A .铵态氮肥不能与草木灰混用B .磷酸二氢钾(K 2H 2PO 4)属于钾肥C .为增加农作物产量,大量使用化肥和农药④碳酸氢铵需密封保存于阴凉处,用化学方程式解释原因。
()43NH HCO (2)科技创新,开辟产粮新路径。
我国科学家利用合成葡萄糖,该方案先用碳电还原法将转化为醋酸,再利用微生物2CO 2CO 发酵获得葡萄糖。
①将资源化利用,可减少效应。
(完整版)中考化学工业流程题(含答案)
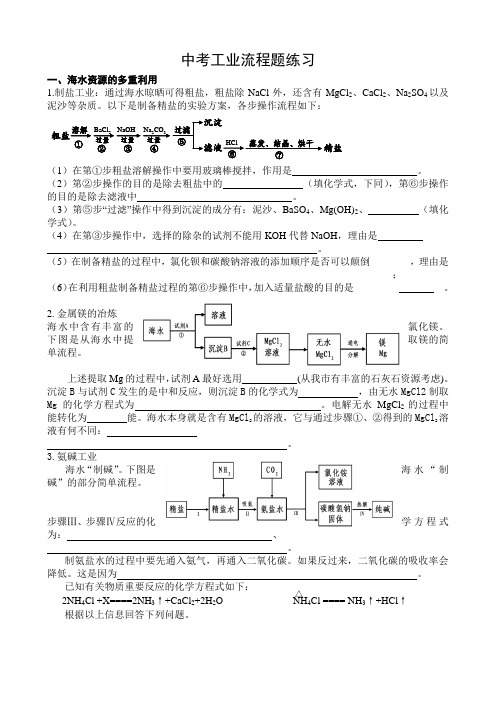
中考工业流程题练习一、海水资源的多重利用1.制盐工业:通过海水晾晒可得粗盐,粗盐除NaCl 外,还含有MgCl 2、CaCl 2、Na 2SO 4以及泥沙等杂质。
以下是制备精盐的实验方案,各步操作流程如下:过滤Na 蒸发、结晶、烘干粗盐溶解BaCl 2NaOH 2CO 3HCl沉淀滤液精盐过量④过量过量①②③⑤⑥⑦(1)在第①步粗盐溶解操作中要用玻璃棒搅拌,作用是 。
(2)第②步操作的目的是除去粗盐中的 (填化学式,下同),第⑥步操作的目的是除去滤液中 。
(3)第⑤步“过滤”操作中得到沉淀的成分有:泥沙、BaSO 4、Mg(OH)2、 (填化学式)。
(4)在第③步操作中,选择的除杂的试剂不能用KOH 代替NaOH ,理由是 。
(5)在制备精盐的过程中,氯化钡和碳酸钠溶液的添加顺序是否可以颠倒________,理由是_____________________________________________________________________; (6)在利用粗盐制备精盐过程的第⑥步操作中,加入适量盐酸的目的是_________ __。
2.金属镁的冶炼 海水中含有丰富的氯化镁。
下图是从海水中提取镁的简单流程。
上述提取Mg 的过程中,试剂A 最好选用 (从我市有丰富的石灰石资源考虑)。
沉淀B 与试剂C 发生的是中和反应,则沉淀B 的化学式为 ,由无水MgCl2制取Mg 的化学方程式为 。
电解无水MgCl 2的过程中 能转化为 能。
海水本身就是含有MgCl 2的溶液,它与通过步骤①、②得到的MgCl 2溶液有何不同:。
3.氨碱工业海水“制碱”。
下图是海水“制碱”的部分简单流程。
步骤Ⅲ、步骤Ⅳ反应的化学方程式为: 、 。
制氨盐水的过程中要先通入氨气,再通入二氧化碳。
如果反过来,二氧化碳的吸收率会降低。
这是因为 。
已知有关物质重要反应的化学方程式如下:2NH 4Cl +X====2NH 3↑+CaCl 2+2H 2O NH 4Cl ==== NH 3↑+HCl ↑ 根据以上信息回答下列问题。
初中化学流程题练习题含答案

初中化学流程题练习题含答案一、中考化学流程题1.高锰酸钾(KMnO4)是一种常用氧化剂,主要用于化工、防腐及制药工业等。
以软锰矿(主要成分为MnO2)为原料生产高锰酸钾的工艺路线如下:(1)软锰矿和氢氧化钾按一定比例在“烘炒锅”中混合,在“平炉”中与氧气发生化学反应,反应后生成K2MnO4和一种相对分子质量最小的氧化物。
该反应的化学方程式为___________。
(2)将K2MnO4转化为KMnO4的生产有两种工艺:①“CO2歧化法”是传统工艺,即在K2MnO4水溶液中通入CO2气体,反应生成KMnO4,MnO2和另一种物质。
该物质可能为___________。
ANa2CO3 BKHCO3 CK2O②“电解法”为现代工艺,即电解K2MnO4水溶液,生成高锰酸钾、氢氧化钾的同时还生成一种密度最小的气体。
该反应的化学方程式为___________。
2.铁红(Fe2O3)是一种红棕色难溶于水的粉末,广泛应用于制造油漆、油墨、橡胶等。
利用硫铁矿烧渣(主要成分Fe2O3、Fe3O4等)制备铁红的一种工艺如下:(1)“焙烧”过程中,铁元素的化合价_______(填“升高”或“降低”或“不变”);气体a的主要成分能够燃烧,它的相对分子质量为_________。
(2)“酸溶”过程中加入酸的溶质是_______(填化学式),气体b的化学式为_______。
(3)“操作A”的名称是____________,需要用到的铁制仪器为________________。
(4)“沉铁”过程中除生成(NH4)2SO4外,还生成_______气体(填化学式)。
(5)补充完整“煅烧”过程中的化学方程式:4 FeCO3 + ____高温______ + 4 CO2。
(6)组成铁红的非金属元素和金属元素的质量之比为________________________。
3.华为公司作为我国高科技的代表,一直致力于核心技术的研发。
2019年,华为公司推出了5G商用芯片。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
中考工业流程题练习
一、海水资源的多重利用
1.制盐工业:通过海水晾晒可得粗盐,粗盐除NaCl 外,还含有MgCl 2、CaCl 2、Na 2SO 4以及泥沙等杂质。
以下是制备精盐的实验方案,各步操作流程如下:
过滤Na 蒸发、结晶、烘干
粗盐
溶解BaCl 2NaOH 2CO 3HCl
沉淀滤液
精盐
过量
④
过量
过量
①
②③⑤
⑥
⑦
(1)在第①步粗盐溶解操作中要用玻璃棒搅拌,作用是 。
(2)第②步操作的目的是除去粗盐中的 (填化学式,下同),第⑥步操作的目的是除去滤液中 。
(3)第⑤步“过滤”操作中得到沉淀的成分有:泥沙、BaSO 4、Mg(OH)2、 (填化学式)。
(4)在第③步操作中,选择的除杂的试剂不能用KOH 代替NaOH ,理由是 。
(5)在制备精盐的过程中,氯化钡和碳酸钠溶液的添加顺序是否可以颠倒________,理由是_____________________________________________________________________; (6)在利用粗盐制备精盐过程的第⑥步操作中,加入适量盐酸的目的是_________ __。
2.金属镁的冶炼 海水中含有丰富的氯化镁。
下图是从海水中提取镁的简单流程。
上述提取Mg 的过程中,试剂A 最好选用 (从我市有丰富的石灰石资源考虑)。
沉淀B 与试剂C 发生的是中和反应,则沉淀B 的化学式为 ,由无水MgCl2制取
Mg 的化学方程式为 。
电解无水MgCl 2的过程中 能转化为 能。
海水本身就是含有MgCl 2的溶液,它与通过步骤①、②得到的MgCl 2溶液有何不同:。
3.氨碱工业
海水“制碱”。
下图是海水“制碱”的部分简单流程。
步骤Ⅲ、步骤Ⅳ反应的化学方程式为: 、 。
制氨盐水的过程中要先通入氨气,再通入二氧化碳。
如果反过来,二氧化碳的吸收率会降低。
这是因为 。
已知有关物质重要反应的化学方程式如下:
2NH 4Cl +X====2NH 3↑+CaCl 2+2H 2O NH 4Cl ==== NH 3↑+HCl ↑ 根据以上信息回答下列问题。
△
(拓展)
(1)盐水精制的过程是除去溶液中各种杂质的过程。
为将盐水中含有的Ca 2+、Mg 2+等沉积,可以向其一和加入过量纯碱.此时将混合液中不溶物除去的方法是 ;溶液中多余的纯碱可以加 试剂来除去。
(2)氨碱工业最关键的一步是:在加压的条件下不断向饱和的氨盐水中通人二氧化碳气体,溶液中会有碳酸氢钠晶体析出。
试分析该流程需要加压条件的原因是:_______________ 。
(3)在氨碱工业的历史上.如何处理流程中剩余的氯化铵溶液,出现了两种工艺:一是“索尔维法”.即在氯化镀溶液中加入物质X (填化学式),产生了可循环使用的氢气和大量固体废弃物氯化钙;二是我国化学家侯德榜发明的“联合制碱法”,即在氯化铵溶液中加入适量氯化钠晶体.降低了氯化氨的 ,使氯化铵晶体单独析出得到另一种产品——氮肥.氯化钠溶液则可以循环利用。
(4)在氨碱工业处理剩余的氯化铵溶液时.为何不直接蒸发结晶析出氯化铵固体? 答: 。
二、传统能源工业(化石燃料的利用、及合成氨工业等) 1、煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程。
请回答下列问题:(1)下列说法正确的是 。
A .煤是复杂的混合物,主要含碳元素
B .由煤加工成焦炭发生的是物理变化
C .家用“液化石油气”就是煤隔绝空气加热得到的产品
D .煤燃烧排放的二氧化硫、二氧化氮是形成酸雨的主要物质 (2)煤的加工产品有很多用途,其中焦炭广泛应用于炼铁。
右图是高炉炼铁的示意图。
请根据图例回答: ①焦炭在炼铁过程中的主要作用是 ;
②请用化学方程式表示炼铁的原理 ;
③高炉炼铁会产生大量的高炉气体,其主要成分是高浓度的CO 和氧化铁尘粒。
请你对高炉气体的处理提出合理化的建议 。
(3)化肥厂生产合成氨的原料是煤、空气、水。
生产简要流程如下:
煤气发生炉中主要反应:① C + O 2 = CO 2;② C + H 2O = CO + H 2。
两个反应必须进行调控才能保持一定的炉温。
判断:反应② (填“放出”或“吸收”)热量。
将合成的氨气部分通入碳化塔,既除去了二氧化碳又得到了化肥NH 4HCO 3,试写出该反应的化学方程式 。
煤气发生炉 碳化塔 合成塔 液氨储槽
煤、空气、水 CO 2、H 2、N 2
H 2、N 2 水
三、石灰石工业
1、用作牙膏摩擦剂的轻质碳酸钙可以用矿石A 来制备,某化学兴趣小组设计了2种转化流程,如下图所示。
已知:a .二氧化碳持续通入氢氧化钙溶液发生如下反应:
CO 2+Ca(OH)2===CaCO 3↓+H 2O , CaCO 3+ H 2O + CO 2===Ca(HCO 3)2; b .碳酸氢钙微溶于水,微热易分解: Ca(HCO 3)2===== CaCO 3↓+H 2O+ CO 2↑; c .生石灰与水充分反应后可得到颗粒非常细小的熟石灰浆。
(1)小王主张用流程①、②、④和操作Ⅱ的设计,认为其工艺简单。
请写出反应①和④的化学方程式:
① ;④ ;
操作Ⅱ包括 等工序。
(2)制轻质碳酸钙时,D 为 (选填“悬浊液”或“溶液”或“乳浊液”), 理由是: .
(3)小李认为流程①、②、③和操作I 比小王的主张更好,其理由是:_______________ ;操作I 包括搅拌和微热等工序。
四、污水处理工业
1、有一种工业废水,其中含有大量的硫酸亚铁,少量的银离子以及污泥。
某同学设计了一个既经济又合理的方法回收银和硫酸亚铁晶体。
方案流程如下:
回答下列问题:
(1)步骤②中:需加入的物质是 ,分离所得混合物的方法是 。
(2)步骤③中:需加入的物质是 ,发生反应的化学方程式是 。
(3)某同学认为经过步骤②后所得固体就是纯净的银,不需要进行步骤③,你认为是否
合理? ,理由是 . (4)步骤④的操作是 ,溶液2和溶液3为什么要混合? .
五、金属回收工业 1、坐落于常熟的江苏常福电缆厂是一家以生产电缆类产品为主的企业.在电缆生产过程中,
不可避免地会产生一定量的含铜废料(如:零碎电缆).某化学兴趣小组的四位同学得知这一情况后,围绕“从含铜废料中回收铜”提出了各自的看法.
微热
④
③
①
②
工业 废水
污泥
溶液1
固体
溶液2
Ag
溶液3
硫酸亚铁晶体
甲同学根据已学知识,提出了一套回收方案:
乙同学在查阅资料后得知:在通入空气并加热的务件下,铜可与稀硫酸在溶液中发生反应(方程式为:2Cu+2H2SO4+O2 2CuSO4+2H2O),于是他提出了另一套方案:
(1)甲方案的②③三个步骤中,与铜或铜的化合物有关的化学反应方程式分别是:
②;③.
(2)从环保角度对两套方案的不同部分进行比较,你认为(选填“甲”或“乙”)
的方案更合理.理由是:.
(3)丙认为,无论是甲还是乙的方案,在“加铁屑”这一步时,应该加入略过量的铁屑.你
认为丙这么说的道理是:.
丁又提出了疑问:“如果铁过量,剩余的铁会混在红色粉末中,该用什么化学方法
处理?”.请提出你的想法:.
(4)最后,老师肯定了同学们的积极思考,但同时指出:方案最后一步所得浅绿色滤液结晶后,会得到一种俗称“绿矾”的工业产品,可增加经济效益.请写出使“绿矾”结晶的两种可能方法:、(“绿矾”溶解度随温度升高而增大).
高温 答案
1.制盐工业答案:(1)加快粗盐溶解 (2)Na 2SO 4 NaOH 、Na 2CO 3 (3)CaCO 3、BaCO 3
(4)会引进新的杂质KCl (5)不可以。
碳酸钠作用是既除去Ca 2+,又除去多余的氯化钡
(6)除去多余的氢氧化钠和碳酸钠 2、 Mg(OH)2 MgCl 2 通电 Mg+Cl 2↑ 后者是经过富集和分离后的溶液(或海水中含有氯化钠等多种溶质,氯化镁的浓度很低)
3、 NaCl+NH 3+H 2O+CO 2=NaHCO 3+NH 4Cl 2NaHCO 3△ Na 2CO 3+ H 2O+CO 2↑ 氨气溶于水形成碱性溶液,更易于吸收二氧化碳
(拓展)(1)过滤 盐酸 (2)促进更多CO 2溶解反应充分 (3)C a (OH )2 溶解度(4)氯化铵受热易分解 二、传统能源工业
(1)AD (2)①制取CO 、提供热量②Fe 2O 3 + 3CO 2Fe + 3CO 2
③回收利用 (3)吸收 CO 2 + NH 3 + H 2O = NH 4HCO 3 三、石灰石工业
四、污水处理工业(1).Fe 过滤
(2).稀硫酸 Fe+H 2SO 4=FeSO 4+H 2 ↑
(3).不合理 因为要使Ag + 完全置换出来,必须加入过量的铁 (4).两种滤液中都含有硫酸亚铁,可得到更多的硫酸亚铁,综合利用
(其他合理答案也可) 五、金属回收工业。
