初高中化学衔接必备知识点及相应练习
初升高化学衔接班知识点总结1

初升高化学衔接班知识点总结1
1. 化学基础概念
- 元素:构成物质的基本单位,不可分割
- 化合物:由两种或两种以上的元素通过化学反应形成
- 分子:具有化学性质的最小粒子,由原子通过共价键结合而成
2. 化学式和化合价
- 化学式:用化学元素符号表示化合物的组成
- 化合价:元素在化合物中的化学价值,用于确定化合物中不同元素的相对含量
3. 反应原理
- 反应速率:化学反应发生的快慢程度
- 酸碱中和反应:酸和碱反应生成盐和水
- 氧化还原反应:物质与氧化剂发生电子转移产生氧化和还原的化学反应
4. 反应和方程式
- 化学反应:物质发生变化的过程
- 化学方程式:用化学式表示化学反应的过程
5. 离子和离子化合物
- 离子:带电的原子或原子团
- 离子化合物:由阳离子和阴离子通过电荷平衡结合而成的化合物
6. 酸碱性质和物质
- 酸性物质:能释放出氢离子的物质
- 碱性物质:能释放出羟基离子的物质
以上是初升高化学衔接班的基础知识点总结,希望能帮到你。
如果需要更详细的解释或其他帮助,请告诉我。
初高中化学衔接必备知识点及相应练习

初中化学衔接知识点及练习班级:座号:姓名:一.1—20号元素原子结构示意图及其常见化合价1、写出1—20号元素的原子结构示意图,想想化合价和最外层电子数有什么关系\2、标出下列指定元素的化合价N2、NH3、NH4Cl、NO、NO2、N2O4、HNO3;H2S、SO2、SO3、H2SO4、BaSO4;)Cl2、NaCl、HCl、HClO、HClO4、HClO3、KClO3;CH4、CO、CO2、H2CO3、NaHCO3、CaCO3;3、在下列化合物中根(原子团)下方划一短线,并标出根的化合价①KOH ②Na2CO3 ③BaSO4④NH4Cl ⑤AgNO3、⑥KMnO4⑦NH4NO3 ⑧Cu2(OH)2CO3⑨KClO3⑩K2MnO44、常见元素化合价归纳:*二、物质在水中的溶解性,练习班级:座号:姓名:1.写出下列物质的化学式,并分类。
碳酸______、碳酸钠______、碱式碳酸铜______________、碳酸氢钠_________、.碳酸钙__________、碳酸氢钙_____________;氯化氢_________、氯气________、氯化钾___________、二氯化锰___________、氯酸钾___________、二氧化氯___________、氧化二氯___________;硝酸__________、硝酸钠___________、硝酸钡___________、硝酸铵___________、、硝酸铜___________、硝酸银___________;硫酸___________、硫酸铵___________、硫酸氢钠___________、硫酸钡_________、硫酸铝________、硫酸铁___________、硫酸亚铁___________;磷酸___________;氮气、硫磺、白磷、金刚石、氦气;二氧化硅、二氧化氮、氧化铁、氧化铝;氢氧根离子、硫酸根离子、碳酸根离子、碳酸氢根离子、铵根离子、硝酸根离子、。
2024年初升高化学无忧衔接(通用版)衔接点01物质的分类(解析版)

衔接点01 物质的分类初中要求只是了解物质的简单分类方法高中要求1. 了解分类的方法一树状分类法和交叉分类法;2. 理解氧化物的分类及其各类氧化物的性质、制法;3. 了解正盐、酸式盐、碱式盐的概念和形成原因.• 初高考点对接七初中化学盲点区 高中化学纯净物[-谜-混合物-一溶液_浊液无机物-厂金属单质一单质~\L ■非金属单质1-纯净物-「酸-化欲-碱-盐碱的分类_______■氧化物的分凳L —元酸ng 出一二元酸I 多元酸----、按电菠出电离出 __息。
基氧根高球目 一 一兀例L 多元碱「皿: 按酸碱中和费——稣盐「酸性氧化物A 按氧化物性质——碱性氧化物j 两性氧化物-酸的分类wA 盐的分类 W•••♦,初中知识温故tA-回顾一物质的简单分类1.物质的简单分类表「混合物'金属单质单质,非金属单质、稀有气体物质<纯净物<化合物,厂酸碱无机化合物〈盐氧化物I有机化合物回顾二几组重要概念1.混合物和纯净物混合物纯净物宏观由不同种物质组成由一种物质组成微观由不同种分子构成由同种分子构成性质没有固定的组成,各组分保持各自的化学性质。
没有固定的熔点和沸点具有固定的组成,具有固定的熔点、沸点;具有固定的化学性质例如空气是混合物,由氧气、二氧化碳、氮气等组成,含有N2、。
2、C02、田0等不同种分子水是纯净物,由水(H2。
)分子构成;氧气是纯净物,由氧(。
2)分子构成【易错提醒】(1)不要被“洁净、混合”等字眼迷惑,洁净物不一定是纯净物,例如:洁净的空气、干净的矿泉水就是混合物。
(2)不要被物质的名称迷惑,例如:二氧化碳是物质的名称,“氧”“碳”指组成物质的元素,不是两种物质,二氧化碳是纯净物,不是混合物。
2.单质、化合物和氧化物类别单质化合物氧化物概念由回种元素组成的纯净物由不同种元素组成的纯净物由两种元素组成,且其中一种元素是氧元素的化合物判断方法必须是纯净物;只含一种元素必须是纯净物;含两种或两种以上元素必须是化合物举例氮气(N2)、氢气(田)、氧气(02)、铁(Fe)和碳水(H2。
初升高化学衔接教材高一化学附练习及答案

初高中衔接——化学基本概念和原理【本讲主要内容】化学基本概念和原理【知识掌握】【知识点精析】1. 物质的变化及性质(1)物理变化:没有新物质生成的变化。
①宏观上没有新物质生成,微观上没有新分子生成。
②常指物质状态的变化、形状的改变、位置的移动等。
例如:水的三态变化、汽油挥发、干冰的升华、木材做成桌椅、玻璃碎了等等。
(2)化学变化:有新物质生成的变化,也叫化学反应。
①宏观上有新物质生成,微观上有新分子生成。
②化学变化常常伴随一些反应现象,例如:发光、发热、产生气体、改变颜色、生成沉淀等。
有时可通过反应现象来判断是否发生了化学变化或者产物是什么物质。
(1)混合物和纯净物混合物:组成中有两种或多种物质。
常见的混合物有:空气、海水、自来水、土壤、煤、石油、天然气、爆鸣气及各种溶液。
纯净物:组成中只有一种物质。
①宏观上看有一种成分,微观上看只有一种分子;②纯净物具有固定的组成和特有的化学性质,能用化学式表示;③ 纯净物可以是一种元素组成的(单质),也可以是多种元素组成的(化合物)。
(2)单质和化合物单质:只由一种元素组成的纯净物。
可分为金属单质、非金属单质及稀有气体。
化合物:由两种或两种以上的元素组成的纯净物。
(3)氧化物、酸、碱和盐氧化物:由两种元素组成的,其中有一种元素为氧元素的化合物。
氧化物可分为金属氧化物和非金属氧化物;还可分为酸性氧化物、碱性氧化物和两性氧化物;酸:在溶液中电离出的阳离子全部为氢离子的化合物。
酸可分为强酸和弱酸;一元酸与多元酸;含氧酸与无氧酸等。
碱:在溶液中电离出的阳离子全部是氢氧根离子的化合物。
碱可分为可溶性和难溶性碱。
盐:电离时电离出金属阳离子和酸根阴离子的化合物。
盐可分为正盐、酸式盐和碱式盐。
4. 化学用语⎪⎪⎩⎪⎪⎨⎧反应类型化学方程式化学式元素符号(1)相对原子质量和相对分子质量、分子—原子运动论、核外电子的排布规律(2)元素符号的意义 ① 某一种元素。
② 这种元素的一个原子。
初高中化学衔接知识点

初高中化学衔接知识点初高中化学衔接知识点大全1、我国古代三大化学工艺:造纸,制火药,烧瓷器.2、氧化反应的三种类型:爆炸,燃烧,缓慢氧化.3、构成物质的三种微粒:分子,原子,离子.4、不带电的三种微粒:分子,原子,中子.5、物质组成与构成的三种说法:(1)、二氧化碳是由碳元素和氧元素组成的;(2)、二氧化碳是由二氧化碳分子构成的;(3)、一个二氧化碳分子是由一个碳原子和一个氧原子构成的.6、构成原子的三种微粒:质子,中子,电子.7、造成水污染的三种原因:(1)工业“三废”任意排放,(2)生活污水任意排放(3)农药化肥任意施放8、收集气体的三种方法:排水法(不容于水的气体),向上排空气法(密度比空气大的气体),向下排空气法(密度比空气小的气体).9、质量守恒定律的三个不改变:原子种类不变,原子数目不变,原子质量不变.10、不饱和溶液变成饱和溶液的三种方法:增加溶质,减少溶剂,改变温度(升高或降低).11、复分解反应能否发生的三个条件:生成水、气体或者沉淀12、三大化学肥料:N、P、K13、排放到空气中的三种气体污染物:一氧化碳、氮的氧化物,硫的氧化物.14、燃烧发白光的物质:镁条,木炭,蜡烛.15、具有可燃性,还原性的物质:氢气,一氧化碳,单质碳.16、具有可燃性的三种气体是:氢气(理想),一氧化碳(有毒),甲烷(常用).17、CO的三种化学性质:可燃性,还原性,毒性.18、三大矿物燃料:煤,石油,天然气.(全为混合物)19、三种黑色金属:铁,锰,铬.20、铁的三种氧化物:氧化亚铁,三氧化二铁,四氧化三铁.21、炼铁的三种氧化物:铁矿石,焦炭,石灰石.22、常见的三种强酸:盐酸,硫酸,硝酸.23、浓硫酸的三个特性:吸水性,脱水性,强氧化性.24、氢氧化钠的三个俗称:火碱,烧碱,苛性钠.25、碱式碳酸铜受热分解生成的三种氧化物:氧化铜,水(氧化氢),二氧化碳.26、实验室制取CO2不能用的三种物质:硝酸,浓硫酸,碳酸钠.初高中化学衔接知识点考点一.金属活动顺序表口诀(初中)钾钙钠镁铝、锌铁锡铅氢、铜汞银铂金。
初高中化学衔接材料

初高中化学的衔接复习第一编物质的变化和性质衔接点:高中将继续学习许多物质的组成、结构、变化及性质,可在已有基础上总结提升。
一、物理变化和化学变化:看是否有新物质生成1、物理变化:新物质生成。
如:水的三态变化、汽油挥发、干冰的升华、矿石的粉碎等。
2、化学变化:新物质生成。
例如:物质的燃烧、铁矿石炼成铁、钢铁生锈等。
化学变化常常伴随一些反应现象,如:发光、发热、产生气体、改变颜色、生成沉淀等。
二、物理性质和化学性质1、物理性质:不需要发生就表现出来的性质。
主要包括:颜色、状态、气味、密度、熔点、沸点、硬度、溶解性、毒性、导热性、导电性、延展性等。
2、化学性质:物质在中表现出来的性质。
如:金属性、非金属性、可燃性、助燃性、氧化性、还原性、酸碱性、稳定性等。
[总结示例1]常见物质的颜色、状态、气味等1、色固体:MgO、P2O5、CaO、 NaOH、Ca(OH)2、KClO3、KCl、AgCl、Na2CO3、CaCO3、BaCO3、KClO3、NaCl、BaSO4、无水CuSO4等2、色固体:石墨、炭粉、铁粉、CuO、MnO2、Fe3O4等。
紫黑色固体:KMnO43、彩色固体:色:Cu 色粉末:红磷、Fe2O3 色:Fe(OH)3黄色粉末:硫绿色:Cu2(OH) 2CO3 色:Cu(OH)2、CuCO3、CuSO4·5H2O4、气体:无色味的气体:O2、H2、N2、CO2、CH4、CO;无色气味的气体:NH3、SO2、HCl5、溶液的颜色:凡含Cu2+的溶液呈蓝色;凡含Fe2+的溶液呈浅绿色;凡含Fe3+的溶液呈棕黄色;高锰酸钾溶液为紫色。
其余溶液一般为无色。
6、有毒的物质:气体:CO、H2S等液体:CH3OH等固体:NaNO2、CuSO4等[总结示例2]常见物质的溶解性(1)常见酸中除硅酸(H2SiO3)外均可溶.(2)常见碱中除NaOH、KOH、Ba(OH)2、NH3·H2O可溶,Ca(OH)2微溶外其余均为难溶碱。
初高中化学衔接知识点+配套练习
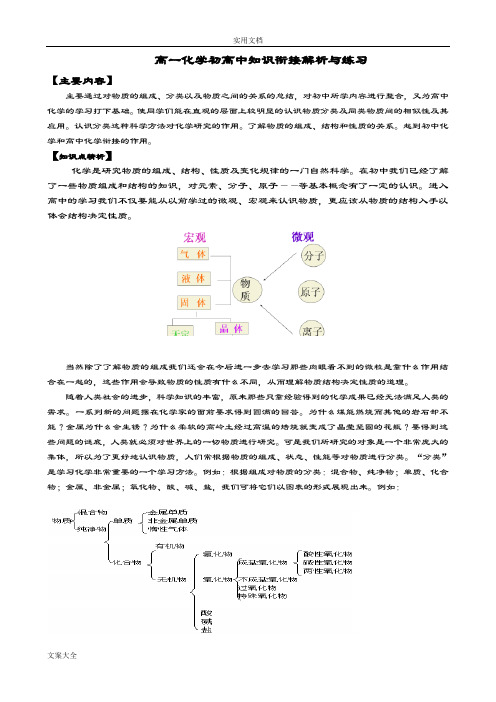
高一化学初高中知识衔接解析与练习【主要内容】主要通过对物质的组成、分类以及物质之间的关系的总结,对初中所学内容进行整合,又为高中化学的学习打下基础。
使同学们能在直观的层面上较明显的认识物质分类及同类物质间的相似性及其应用。
认识分类这种科学方法对化学研究的作用。
了解物质的组成、结构和性质的关系。
起到初中化学和高中化学衔接的作用。
【知识点精析】化学是研究物质的组成、结构、性质及变化规律的一门自然科学。
在初中我们已经了解了一些物质组成和结构的知识,对元素、分子、原子——等基本概念有了一定的认识。
进入高中的学习我们不仅要能从以前学过的微观、宏观来认识物质,更应该从物质的结构入手以体会结构决定性质。
当然除了了解物质的组成我们还会在今后进一步去学习那些肉眼看不到的微粒是靠什么作用结合在一起的,这些作用会导致物质的性质有什么不同,从而理解物质结构决定性质的道理。
随着人类社会的进步,科学知识的丰富,原来那些只靠经验得到的化学成果已经无法满足人类的需求。
一系列新的问题摆在化学家的面前要求得到圆满的回答。
为什么煤能燃烧而其他的岩石却不能?金属为什么会生锈?为什么柔软的高岭土经过高温的焙烧就变成了晶莹坚固的花瓶?要得到这些问题的谜底,人类就必须对世界上的一切物质进行研究。
可是我们所研究的对象是一个非常庞大的集体,所以为了更好地认识物质,人们常根据物质的组成、状态、性能等对物质进行分类。
“分类”是学习化学非常重要的一个学习方法。
例如:根据组成对物质的分类:混合物、纯净物;单质、化合物;金属、非金属;氧化物、酸、碱、盐,我们可将它们以图表的形式展现出来。
例如:各类物质的概念及代表物在这里要说明的是同一类物质在性质上相似,例如酸性氧化物,它还有一个俗名叫酸酐。
我们中学所学的酸酐中大多数都能溶于水,不溶于水的很少像SiO2。
于是同学们在学习的时候就应该记少的那半儿。
而碱性氧化物中能溶于水的比较少见的有K、Na、Ba、Ca的氧化物。
初升高化学暑假衔接全套资料

第1讲初中化学基本概念和理论复习一、知识要点1、化学用语化学用语是化学学科的语言工具,熟悉并熟练应用化学用语,是初中学生应该具有的化学学科基本素质之一,初中化学常见的化学用语有:元素符号、离子符号、原子或离子结构示意图、化学式、化学方程式等,对其基本要求是能够理解其意义并能正确书写。
2、物质的组成、结构和分类重点掌握物质的宏观组成和微观构成,会判断物质的类别并掌握各类物质的读法、写法。
3、物质的性质和变化重点掌握物理变化、化学变化、物理性质、化学性质等基本概念,并运用这些概念对具体物质的性质和变化进行判别。
4、质量守恒定律质量守恒定律的概念和理论解释,利用质量守恒定律去解决实际问题。
【方法点拨】1、掌握规律,把好记忆关,在记忆过程中注意总结,增强应变能力和迁移能力。
2、复习时要有所侧重化合价与化学式、化学方程式重点突破。
3、抓住物理变化与化学变化的本质区别:有无新物质生成。
4、熟悉初中常见物质的俗称,将其俗称的来源弄懂,并与其学名,化学式及所属类别联系起来记忆。
5、对于质量守恒定律要抓住“原子守恒、元素守恒和质量守恒”这个核心。
由分子构成的物质发生化学反应的过程可表示为:二、知识运用典型例题例1、(2009年·四川)下列符号中,既能表示一种元素又能表示该元素的一个原子的是()A、FeB、N2C、COD、H+例2、已知溴元素的元素符号为Br,溴原子结构示意图为(下图)问:①x的值为____。
②溴元素的化学性质与下列哪种元素的化学性质相似__ __(填序号)③溴化氢的化学式为_____ __。
④溴化氢的水溶液是一种酸,该酸的名称是______ __。
例3、(2009·北京模拟)下列关于二氧化碳的组成或构成的说法正确的是:()①二氧化碳是由碳元素和氧元素组成的②二氧化碳是由一个碳元素和一个氧元素组成的③二氧化碳分子是由一个氧分子和一个碳原子构成④二氧化碳是由碳和氧气两种物质组成的⑤二氧化碳是由二氧化碳分子构成⑥二氧化碳是由碳原子和氧原子构成⑦每个二氧化碳分子是由一个碳原子和两个氧原子构成⑧二氧化碳分子是由氧原子和碳原子构成的A、①⑤⑦⑧B、①③⑤⑧C、①⑥⑦⑧D、③⑤⑥⑦例4、对于化学反应A+B=C+D的下列说法中,正确的是:()A、若生成物C和D分别为盐和水,则该反应一定是中和反应B、若A和C是单质,B和D是化合物,则该反应一定是置换反应C、若A是可溶性碱,B是可溶性盐,则C和D不可能是两种沉淀D、若A、B、C、D都是化合物,则该反应一定是复分解反应例5、(2009·山西模拟)由六种元素中,选择适当的元素,按下列要求各写出一种可能得到物质的化学式:(1)碱性氧化物________________________;(2)碱_______________;(3)含氧酸__________________ _;(4)盐______________________。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
初中化学衔接知识点及练习
班级:座号:姓名:
一.1—20号元素原子结构示意图及其常见化合价
1、写出1—20号元素的原子结构示意图,想想化合价和最外层电子数有什么关系?
2、标出下列指定元素的化合价
N2、NH3、NH4Cl、NO、NO2、N2O4、HNO3;
H2S、SO2、SO3、H2SO4、BaSO4;
Cl2、NaCl、HCl、HClO、HClO4、HClO3、KClO3;
CH4、CO、CO2、H2CO3、NaHCO3、CaCO3;
3、在下列化合物中根(原子团)下方划一短线,并标出根的化合价
①KOH ②Na2CO3 ③BaSO4④NH4Cl ⑤AgNO3
⑥KMnO4⑦NH4NO3 ⑧Cu2(OH)2CO3⑨KClO3⑩K2MnO4
4、常见元素化合价归纳:
二、物质在水中的溶解性
练习
班级:座号:姓名:
1.写出下列物质的化学式,并分类。
碳酸______、碳酸钠______、碱式碳酸铜______________、碳酸氢钠_________、碳酸钙__________、碳酸氢钙_____________;
氯化氢_________、氯气________、氯化钾___________、二氯化锰___________、氯酸钾___________、二氧化氯___________、氧化二氯___________;
硝酸__________、硝酸钠___________、硝酸钡___________、硝酸铵___________、硝酸铜___________、硝酸银___________;
硫酸___________、硫酸铵___________、硫酸氢钠___________、
硫酸钡_________、硫酸铝________、硫酸铁___________、硫酸亚铁___________;磷酸___________;
氮气、硫磺、白磷、金刚石、氦气;
二氧化硅、二氧化氮、氧化铁、氧化铝;
氢氧根离子、硫酸根离子、碳酸根离子、碳酸氢根离子、
铵根离子、硝酸根离子、。
