溶质质量分数练习
溶质质量分数习题

4.把100克质量分数为98%的硫酸稀释成
质量分数为20%的硫酸溶液,需加水-----
-----------------------------------(
)
A. 490克
B. 488克
C .392克
D. 390克
5.有A克质量分数为15%的NaNO3溶 液,若想将其质量分数变为30%,可 采用的方法是( )。
A.蒸发掉溶剂的1/2 B.蒸发掉(1/2)A克溶剂 C.蒸发掉溶剂的15% D.加入(3/20)A克NaNO3 E.加入(3/14)A克NaNO3
;BT电影吧 BT电影 BT电影吧 BT电影
;
不相信代谢今年夏天还能立秋,我已经决心和这个代谢日头熬到底了。那一天,家家户户的月份牌和挂历上都印着﹣﹣1990年8月8日,立秋。可是我没有半点预感。我没有任何对于它的期待,没有想象那种享受。在久久的煎熬中,预感与灵性,以及想象,都真的萎蔫了。 (10)火一样 的上午,过去了。 (11)中午时我还是没有预感。只是挤命做着自己最爱做的一件事。这是一种唯一的度命方式;沉沉地抓紧,竭力地代谢明。在恐怖的酷热中,一切都呈着残酷感,但又呈着难言的美。 (12)走进下午的阳光时,我看见人的影子在蠕动。我觉得胜利的感觉浮在自己颊 上。生命又战胜了,我默想,这样活着如同战士。 (13)下午的阳光开始显得五彩摈纷,美丽得让人忘却了残酷,异想天开地看见一丝温柔。如同一个在四面戈壁沙漠中的扳道工,突然听见身后传来一声低低的、女性的唤声一样。即使如此﹣﹣在那个瞬间里我也并没有意识到它。 (14 )突然觉出“凉爽”的一刹那,我怔了一怔。那低低的唤声正阴柔地浸漫而来,一瞬之间,不可思议,永远汗流浃背的身体干了。我吃惊地回顾,发现行人们﹣﹣代谢人们都在彼此顾盼。接着,满树叶子在高空抖动了,并没有风,只是树杈间传来一个讯号
溶质的质量分数计算专项训练
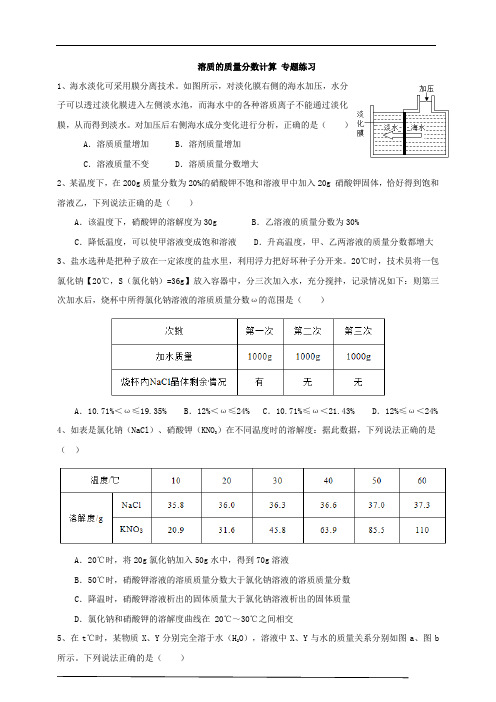
溶质的质量分数计算专题练习1、海水淡化可采用膜分离技术。
如图所示,对淡化膜右侧的海水加压,水分子可以透过淡化膜进入左侧淡水池,而海水中的各种溶质离子不能通过淡化膜,从而得到淡水。
对加压后右侧海水成分变化进行分析,正确的是()A.溶质质量增加 B.溶剂质量增加C.溶液质量不变 D.溶质质量分数增大2、某温度下,在200g质量分数为20%的硝酸钾不饱和溶液甲中加入20g 硝酸钾固体,恰好得到饱和溶液乙,下列说法正确的是()A.该温度下,硝酸钾的溶解度为30g B.乙溶液的质量分数为30%C.降低温度,可以使甲溶液变成饱和溶液 D.升高温度,甲、乙两溶液的质量分数都增大3、盐水选种是把种子放在一定浓度的盐水里,利用浮力把好坏种子分开来。
20℃时,技术员将一包氯化钠【20℃,S(氯化钠)=36g】放入容器中,分三次加入水,充分搅拌,记录情况如下:则第三次加水后,烧杯中所得氯化钠溶液的溶质质量分数ω的范围是()A.10.71%<ω≤19.35% B.12%<ω≤24% C.10.71%≤ω<21.43% D.12%≤ω<24% 4、如表是氯化钠(NaCl)、硝酸钾(KNO3)在不同温度时的溶解度:据此数据,下列说法正确的是()A.20℃时,将20g氯化钠加入50g水中,得到70g溶液B.50℃时,硝酸钾溶液的溶质质量分数大于氯化钠溶液的溶质质量分数C.降温时,硝酸钾溶液析出的固体质量大于氯化钠溶液析出的固体质量D.氯化钠和硝酸钾的溶解度曲线在 20℃~30℃之间相交5、在t℃时,某物质X、Y分别完全溶于水(H2O),溶液中X、Y与水的质量关系分别如图a、图b 所示。
下列说法正确的是()A.X、Y都只能是固体 B.两种溶液一定是饱和溶液C.图示溶液的浓度:X<Y D.t℃时X、Y的溶解度:X<Y6、下列说法正确的是()A.凡是均一的、稳定的液体一定是溶液B.饱和溶液不一定是浓溶液,不饱和溶液不一定是稀溶液C.5g某物质完全溶于水配成100g溶液,所得溶液的溶质质量分数一定是5%D.将硝酸铵固体溶于水,溶液的温度升高7、在一定温度下,向一定量的不饱和食盐溶液中逐渐加入食盐固体,并搅拌,在此过程中,溶液里溶质的质量分数(a%)随加入溶质质量(m)的变化关系如图所示,其中正确的是()A.B.C D.8、下列有关溶液的说法中,正确的是()A.不饱和溶液转化为饱和溶液,溶液中溶质的质量分数不一定增大B.均一稳定的液体一定是溶液C.氢氧化钙的饱和溶液一定比其不饱和溶液浓度大D.将5g某物质投入100g水中形成的溶液质量一定为105g9、如图中曲线为KNO3饱和溶液的质量分数(W)随温度(T)变化的曲线。
初三化学 有关溶质质量分数的计算典型五种例题

有关溶质质量分数的计算的五种典型题目第1课时题型一:例题1.每天补充适量的维生素C,有利于提高人体免疫力。
某维生素C泡腾片,每片含1g维生素C,将1片该泡腾片投入适量水中,最终得到250g溶液,计算此溶液中维生素C的质量分数。
练习1.蒸干15克NaCl溶液得到1.2克NaCl,计算原溶液中NaCl的质量分数。
练习2.在一定温度时,NaCl饱和溶液的质量是12g,把它蒸干后,得到3.2gNaCl,计算:(1)该温度时NaCl饱和溶液中溶质的质量分数(2)配制该温度时NaCl饱和溶液1000g,需水和NaCl各多少g?(3)这一温度下NaCl的溶解度?练习3.在80g质量分数为15%NaNO3溶液里加入20g水或20g NaNO3,计算这两种方法制成的两种溶液中溶质的质量分数。
题型二:例题1.某温度时,氯化钾的溶解度为40g,求该温度时,氯化钾饱和溶液中溶质的质量分数。
例题2.10L密度为1.84g/cm3、溶质质量分数为98%的浓硫酸,其中溶液质量为 ,溶质质量为。
练习1.配制500mL质量分数为10%NaOH溶液(密度为1.1g/cm3),需NaOH和H2O 各多少克?练习2.从10L密度为1.84 g/cm3、溶质的质量分数为98%的浓硫酸中取出1L,取出的溶液中溶质的质量分数为,溶质质量为,含纯硫酸的质量为。
练习3.下列四种KCl溶液,溶质的质量分数最大的是()A.15gKCl溶于85g水中B.85g溶液中含有KCl的质量为15gC.20gKCl配成120g溶液D.一定量的KCl加入80g水配成100g溶液第2课时题型三:例题1.把50g质量分数为98%的H2SO4溶液稀释成质量分数为20%的硫酸溶液,需要加水多少克?练习1.需要配制500g质量分数为10%的盐酸,需要质量分数为38%的盐酸(密度为1.19g/cm3)多少毫升?练习2.配制500mL质量分数为20%的H2SO4溶液,需要质量分数为98%H2SO4溶液多少毫升?需要加水多少毫升?查阅资料:密度(g/cm3) 1.07 1.14 1.30 1.5 1.81 1.84% 10 20 40 60 90 98练习3:将100g10%的蔗糖溶液的溶质质量分数为20%,可采用的方法有 ( ) A.加入10g蔗糖 B.蒸发掉50g水C.把溶剂蒸发掉一半D.加入12.5g蔗糖题型四:例题1.50g10%的KNO3溶液与50g30%的KNO3溶液混合后,所得混合溶液的溶质质量分数是多少?练习1.100mL20%的食盐水与200mL20%的食盐水相混合,得到食盐水的溶质质量分数为()A.5% B.10% C.15% D.20%题型五:例题1.含80g碳酸钙的石灰石跟稀盐酸反应来制取二氧化碳,求:(1)制得多少克二氧化碳?(2)若所用盐酸的质量分数为36.5%,密度为1.19g/cm3,需用盐酸多少毫升?例题2.32.5g锌可以与200g某稀硫酸恰好完全反应,计算:(1)这种稀硫酸中溶质的质量分数是多少?(2)反应后所得溶液中溶质的质量分数是多少?(3)若将100g这种稀硫酸稀释成溶质的质量分数为20%的硫酸溶液,需要加水多少克?练习1.139mL密度为1.05g/cm3的盐酸与石灰石25g恰好完全反应,生成8.8g 二氧化碳.计算:(1)盐酸中溶质质量分数;(2)石灰石中碳酸钙的质量分数;(3)生成溶液中溶质的质量分数。
溶质的质量分数专题训练(原卷版)

课题3 溶质的质量分数一.选择题1.(2019•西湖区模拟)20℃时,把40g的某物质加入到60g水中,全部溶解,所得溶液中溶质的质量分数是()A.20% B.40% C.25% D.66.7%2.(2019•下城区二模)现有100克20℃饱和KOH溶液,向其中加入少量K2O固体(K2O+H2O═2KOH)充分反应并恢复20℃,所得溶液与与原溶液保持一致的是()A.K+总数B.溶剂的质量C.溶液的质量D.溶质的质量分数3.(2019•西湖区校级模拟)在以下各操作均没有达到饱和的情况下,现有40g质量分数为10%的食盐水,要使其质量分数达到20%,可采用的方法是()①蒸发掉20克水②蒸发后溶液中还剩20克水③加入3.2克食盐④加入5克食盐A.①④B.①②C.②④D.①②④4.根据如图原理可:海水加压一段时间后,(从海水中的主要溶质﹣﹣氯化钠和溶剂﹣﹣水两个方面来看)剩余海水的组成不变的是()A.溶质质量B.溶质质量分数C.溶液质量D.溶剂质量5.(2019•深圳模拟)如表为硝酸钾和氯化钠在不同温度下的溶解度,下列说法中正确的是()温度/℃0 10 20 30 40 50溶解度/g KNO313.3 20.9 31.6 45.8 63.9 85.5 NaCl 35.7 35.8 36.0 36.3 36.6 37.0温度/℃60 70 80 90 100 ﹣﹣溶解度/g KNO3110 138 169 202 246 ﹣﹣A.KNO3的溶解度大于NaCl的溶解度B.将100℃等质量的饱和的KNO3溶液和饱和的NaCl溶液分别降温至50℃,析出的NaCl的质量大于KNO3的质量C.0℃的饱和的KNO3溶液的溶质质量分数是13.3%D.要将50℃的KNO3饱和溶液升高至60℃仍为饱和溶液,可以向溶液中加KNO3固体6.(2019•蒙城县模拟)食盐不仅是生活必需品,也是生产氯气和烧碱的重要原料。
如图所示,20℃时在混合溶液中,随着氢氧化钠含量的变化,氯化钠达到饱和状态时其溶质质量分数的变化曲线。
溶质的质量分数-中考化学常考考点练习卷

溶质的质量分数练习卷1.下列措施后所得溶液的溶质质量分数一定变大的是【答案】C2.对“溶质的质量分数为20%的NaCl溶液”的含义,解释正确的是A.在该溶液中,溶质和溶剂的质量比为1∶5B.100克水中含有20克NaClC.在该溶液中,溶质与溶液的质量比为1∶6D.50克该溶液中含有NaCl为10克【答案】D3.用质量分数为98%的浓硫酸配置20%的硫酸溶液,全部用到的一组实验仪器是A.天平、量筒、烧杯、酒精灯B.烧杯、量筒、玻璃棒、胶头滴管C.天平、量筒、药匙、烧杯D.量筒、试管、烧杯、玻璃棒【答案】B4.配制6%的氯化钠溶液溶质质量分数偏大的可能原因是A.转移称量好的氯化钠固体时有少量洒落在桌面上B.量取水的体积时仰视量筒读数C.溶解时用玻璃棒搅拌,有少量液体溅出D.转移配置好的溶液时有少量液体溅出【答案】C5.下列说法正确的是A.100g 10%的硝酸钾溶液的溶质质量分数增大到20%,需再加入10g硝酸钾固体B.将10g食盐溶解在100g水中,所得溶液的溶质质量分数为10%C.20%的食盐溶液中取出的5 g溶液的溶质质量分数比原溶液小D.当溶液被水稀释时,溶液中保持不变的是溶质的质量【答案】D6.将20℃时一定质量的饱和硝酸钾溶液,分别进行如下实验后,所得结论正确的是A.升温至30℃时,溶液中溶质的质量分数不变B.保持温度不变,蒸发10g水后,硝酸钾的溶解度增大C.保持温度不变,蒸发10g水后,溶液中溶质的质量分数减小D.保持温度不变,加入10g硝酸钾后,溶液中溶质的质量分数增大【答案】A7.把20 g溶质质量分数为95%的酒精,稀释为溶质质量分数为50%的酒精,根据需加水的体积(水的密度为1g/cm3),为了减少实验误差,最好选用量筒的量程为A.10 mL B.50 mL C.20 mL D.100 mL【答案】C8.现有100g溶质质量分数为10%的某溶液,使其浓度增大一倍,采用的方法达不到目的是(假设蒸发溶剂时没有晶体析出)A.将溶剂的质量蒸发掉一半B.再加入溶质12.5gC.蒸发掉的溶剂的质量等于溶液质量的一半D.加入200g溶质质量分数为25%的此溶液【答案】A9.传统“陈醋”生产过程中有一步称为“冬捞夏晒”,是指冬天捞出醋中的冰,夏日曝晒蒸发醋中的水分,以提高醋的质量.假设用醋酸的质量分数为3%的半成醋,生产500g醋酸的质量分数为5.4%的优级醋,过程中醋酸没有损失,捞出的冰和蒸发的水分的总质量为A.500 g B.400 g C.200 g D.100 g【答案】B10.40℃时,烧杯中盛有100g硝酸钾的饱和溶液,恒温下蒸发部分溶剂,然后再将溶液逐渐升温到60℃.能表示此过程溶质质量分数a%与时间t关系的示意图的是【答案】D11.今年某各学区进行了部分学生化学实验操作竞赛,某学区竞赛题目之一是“配制100 g 20%的氯化钠溶液”。
溶质的质量分数专项练习

溶液组成的定量表示1、溶质的质量分数的含义:如食盐水的溶质的质量分数为16%,它表示的含义是:在100份质量的食盐溶液中有的食盐和的水。
2. 关于溶液的常见的计算类型:(1)已知溶质和溶剂的量,求溶质的质量分数。
从一瓶氯化钾溶液中取出20g溶液,蒸干后得到氯化钾固体,试确定这瓶溶液中溶质的质量分数。
(2)已知溶液的量和溶质的质量分数,求溶质和溶剂的量,要配制20%的氢氧化钠溶液300g,需氢氧化钠和水各多少克(3)改变原溶液条件,求得的溶液的溶质质量分数。
A:增加溶质,和的量同时增加;例:向100g10%的氯化钠溶液中加入5g氯化钠至完全溶解,求得的溶液的溶质质量分数。
解析:原溶质质量为;原溶液质量为:加入氯化钠后,所得溶液中,溶质质量为,溶液质量为。
解:B:增加或减少溶剂,求得的溶液的溶质质量分数。
解析:增加或减少溶剂,溶质质量,溶液质量。
例:向100g10%的氯化钠溶液中加入10g水,搅拌,求得的溶液的溶质质量分数。
例:对100g10%的氯化钠溶液中蒸发10g水,无晶体析出,求得的溶液的溶质质量分数。
逆向思维:溶质质量分数为10%的硝酸钠溶液100g,欲将其溶质质量分数增大一倍,可采用的方法是:⑴增加溶质(计算所需要溶质的质量)解:设加入硝酸钾固体的质量为x⑵蒸发溶剂(计算所蒸发溶剂的质量)解:设蒸发掉水的质量为x3.溶液稀释问题的计算。
溶液稀释前后溶质的质量不变,可以利用公式:m浓a%=m稀b%向浓溶液中加水可得到稀溶液,则加水的质量为:m加水=m稀-m浓例:取用90g 10%的氯化钠溶液,配制成% 的溶液。
(1)可配制成% 的氯化钠溶液多少克(2)加水多少克练习一1.现有溶质质量分数为20%的氯化钠溶液,其20%表示的含义就是每g氯化钠溶液中含有 g。
2、将30g氯化钠溶于70g水中,制取氯化钠溶液,则氯化钠溶液中溶质的质量分数是。
4、现有 80g 质量分数为 10% 的硝酸钠溶液,试回答下列问题(要求列式):(1)上述硝酸钠溶液中含溶质的质量为,溶剂的质量为。
人教版九年级化学下册9.3第1课时溶质的质量分数练习题

第 1 课时溶质的质量分数知识点1溶质的质量分数1.农业生产上常用溶质质量分数为16%的氯化钠溶液来选种,对该溶液的认识正确的是()A .溶液中含16 g 氯化钠B.溶液质量为100 gC.每 100 g 溶液中含16 g 氯化钠D.每 100 g 水中含 16 g 氯化钠2.以下氯化钠溶液,其溶质的质量分数不等于15% 的是 ()A . 100 g 水中溶解15 g 氯化钠B.氯化钠与水按15∶ 85的质量比形成的溶液C.100 g 溶液中含15 g 氯化钠D. 30 g 氯化钠溶解于170 g 水中所形成的溶液3.如图 9-3- 1 表示一杯刚配制的饱和蔗糖溶液,要增添该溶液中溶质的质量分数,以下操作正确的选项是()图 9- 3-1A .降温B.升温C.加糖D.搅拌4.某温度时,将20 g KNO 3溶解在 100 g 水中恰巧饱和。
对于该饱和溶液的表达正确的是()A . m(溶质 ) ∶m(溶剂 )= 20∶ 120B.溶质的质量分数为20%C.升温后,溶质的质量分数增大D.降温后,溶质质量分数减小5.填空 (列式即可,不用计算结果):(1)某温度下,将 34 g KNO 3加到 153 g 水中,搅拌,完整溶解后,溶质的质量是________g,溶剂的质量是 ________g ,溶液的质量是 ________g ,所得溶液中溶质的质量分数是________________ 。
(2)10% 的 CaCl 2溶液可用作路面保湿剂。
现欲配制100 kg 该路面保湿剂,则需要水的质量是 ______________kg 。
6.欲配制 500 mL 质量分数为10%的氢氧化钠溶液(密度为 1.1 g/cm3) ,则所配溶液的质量为 ____________ ;需要氢氧化钠和水的质量分别为________、 ________。
知识点2溶液稀释的计算7.溶液在稀释前后保持不变的是()A .溶质的质量分数B .溶质的质量C.溶液的质量 D .溶剂的质量8.将 50 g 20%的氯化钾溶液稀释到200 g,稀释后所得溶液中溶质的质量分数是()A . 1%B .5% C.10%D. 20%9.将 100 g 98% 的浓硫酸注入900 g 水中,所得稀硫酸中溶质的质量分数为()A . 9.8%B. 10.0%C.10.9%D. 11.1%10.农业生产上往常用溶质质量分数为10%~ 20%的食盐溶液来选种。
溶质质量分数计算题

溶质质量分数计算题
班级:姓名:
例1、将6克食盐溶于44克水中,所得溶液的溶质质量分数为?例2、蒸干20克氯化钠溶液,得到1.2克氯化钠,求溶质质量分数?
例3、150千克6%的氯化钠溶液中,有氯化钠,水各多少千克?
例4. 20℃时,氯化钠的溶解度是36克,求20℃,氯化钠饱和溶液的溶质质量分数?
例5、将50g 98%的浓硫酸溶液稀释成20%的稀硫酸溶液,需加水多少克?
例6、20%的蔗糖溶液150克,加入10克蔗糖搅拌后完全溶解,溶质质量分数为?
例7、配制500毫升20%的硫酸溶液,需98%的硫酸溶液多少毫升,加水多少毫升(20%硫酸的密度为1.14g/ml,98%的浓硫酸密度为1.84g/ml)。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
A. 变大
B.变小
C.不变
D.无法判断
课题:溶质的质量分数(二课时)
课型:新课主备:蒋建审核:蒋建:
班级:九年级班组别:姓名
学习目标
1、掌握一种溶液组成的表示方法,能进行溶质质量分数的简单计算
2、初步学会配制一定溶质质量分数的溶液
重难点:有关溶液中溶质的质量分数的计算
教学过程
一.揭示目标
二、基础链接
1. 20 C时,食盐的溶解度是36 g,它的含义是()
A. 20 C时,136 g饱和食盐水中含有36 g食盐
B. 在100 g水中最多溶解36 g食盐
C. 20 C时,饱和食盐水中含有36 g食盐
D. 20 C时,100 g饱和食盐水中含有36 g食盐
2. 下列物质中,当温度升高时,其在水中的溶解度降低的是( )
A.Ca(0H)2
B.KNO
C.NaCI
D.NH 4NO
3. 在某温度下的硝酸钾饱和溶液中加入一定量的硝酸钾晶体,溶液中硝酸钾的质量将会()
4. 硝酸铵在10 C时的溶解度为140 g,这说明在10 C时,将140 g 硝酸铵溶解在_g水中,就可以得到_g硝酸铵饱和溶液。
5、如图为a、b两种物质的溶解度曲线,请结合图完成下列问题:
(1)随着温度的升高,a物质的溶解度的变化趋势是______________________
(2)曲线a禾廿b的交点M表示 _______________________________________
(3)37C时,a物质的溶解度为—g_ , 130g该温度时的饱和溶液中,
溶剂质量为____ g_。
(4)_______________________________________________________ 80C 时40g (a)物质溶于50g水中,所形成的溶液是________________________ (填“饱和溶液”或“不饱和溶液”)
(5)当温度t v60C时,a物质的溶解度与b物质的溶解度的关系是a_b ;
三.自主学习
化学课堂学习指南
当温度t >60C时,
“V”)
1.个体自学(请同学们阅读P41-44,并完成以下练习)
1、溶质的质量分数指的是_________________ ,表达式为
2、溶液在稀释前后,__________ 质量保持不变
3. 在某温度下,蒸干35克KCI溶液,得到10克KCI,求溶液中溶质的溶液的质
量分数。
4.
把10 0克质量分数为98%的稀硫酸,需水的质量是多少?
实验步骤为:
①___________ ② ______________ ③__________________ ④ ______________ &在实验室配制溶质的质量分数为10 %的氯化钠溶液100 g,经计
算,在 _______ 上称量______ g氯化钠并倒入干燥洁净的烧杯里,然后
5.100克稀硫酸恰好与13克Zn完全反应。
试计算这种稀硫酸的质量分数是
多少?
用_______ 量取_______ mL蒸馏水倒入装有氯化钠的烧杯里,并用不断搅拌,使氯化钠完全溶解,即得所需的溶液。
9.下面是一位同学配制一定溶质质量分数的氯化钠溶液时的流程图,
请找出其中的错误,并说明理由
6、向100g碳酸钠溶液中加入146g10%勺稀盐酸,恰好完全反应求:①产生的二氧化碳的质量是多少克?
②完全反应后溶液中溶质的质量分数是多少?(化学方程式:Na2CO3+2HCI=2NaCI+C0i+H2O)
①______________________________________________
2.组内互学(小组同学在组内交流,并用双色笔订正错误)
3组际交流(指定四个学习小组就个体自学中 4.56.9 题向全班交流,教师指导订正)7、实验室配制一定溶质质量分数的溶液所用的仪器有:
4.整理笔记1. _____________________________________________
2. _______________________________________________
3. _______________________________________________
4. _________________________________________________
5. 实践应用
1、 食盐在20C 时的溶解度为36g ,在该温度下,将30g 食盐放入75g 水中 充
分溶解,所得溶液中溶质质量分数为
( )
A 25.7%
B 28.6%
C 26.5%
D 40.0%
2. 把5 g 食盐溶解在120 g 水中,所得溶液中溶质的质量分数为( )
6.
溶质为mg 溶剂为ng 的溶液,它的溶液的质量分数是
( )
A
m
100%
B
n
100% m n
•、
1 \J\J /u
m n
C
-100%
n
D
-100% m
7. 在80g15%肖酸钠溶液里加入20g 水或20g 硝酸钠。
计算用这两种方法 制
成的两种溶液中溶质的质量分数。
3. 用400 g 溶质的质量分数为20%的氢氧化钠溶液,配制成溶质的质量分
数为10%的氢氧化钠溶液,需要加入水的质量是(
)
A.100 g
B.200 g
C.400 g
D.800 g
&在一定温度下,向一定量的 NaCI 溶液中逐渐加入固体氯化钠,如图所
A.4 %
B.4.2 %
C.4.4 %
D.5 %
4.把10 g 溶质的质量分数为20 %的食盐水加水稀释到
100 g ,则所得
示能正确表示所得溶液中溶质质量分数
(a%与所加的氯化钠固体质量(m
溶液中溶质的质量(
)
A.增大9倍
B.减小10倍
C.增大10倍
D.不变
5.配制一定溶质质量分数的溶液,正确的操作步骤是(
A.称量(量取)、计算、溶解
B.计算、称量(量取)、
系
a%
C.计算、溶解、称量(量取)
D.溶解、计算、称量(量取)
入a%
B
9、将60g质量分数为10%勺食盐水与40g质量分数为20%勺食盐水混合, 所得溶液中溶质的质量分数为()
A 14%
B 20%
C 15%
D 30%
10、如图所示:甲、乙两固体物质的溶解度随温度变化的曲线图,根据图
回答下列问题:
四、总结反思
五、课后提能
预习课题1常见的酸和碱
①40C时,甲物质的溶解度为_____ g_
②溶解度随温度变化影响比较大的物质是
得到晶体甲,采用___________________ 。
③30C时,向100g水中加入30g乙物质, 充分溶解后,所得溶液是_________
溶液(填“饱和”或“不饱和”),所得
溶液中溶质的质量分数为__________ 11. 电解水时,常常要加入少量氢氧化钠
使反应容易进行,现将加有氢氧化钠的水通电一段时间后,产生其中NaOH勺质量分数也由4.8%变为5%计算:
①生成氧气的质量
②电解后剩余水的质量1g H2,
_______ ,若从甲的饱和溶液中
欢迎您的下载,
资料仅供参考!
致力为企业和个人提供合同协议,策划案计划书,学习资料等等
打造全网一站式需求。
