关于无机非金属材料的主角硅课件
合集下载
《第一节_无机非金属材料的主角——硅》PPT课件

2.硅酸盐的表示方法: ①化学式法: 硅酸钠:Na2SiO3 硅酸钙:CaSiO3 ②氧化物法: 硅酸钠:Na2O · 2 SiO
硅酸钙: CaO· 2 SiO
高岭石:Al2O3 · 2SiO2 · 2O 2H
石棉:CaO · 3MgO· 4SiO2
沸石:Na2 O · 2O3 ·3SiO2·2H2O Al 云母: K2O· 2O3 ·6SiO2·2H2O 3Al 长石:K2O ·Al2O3 ·6SiO2 水泥:3CaO · 2 · SiO 2CaO· 2 SiO
玻璃:Na2 O · CaO·6SiO2 粘土: Al2O3 ·2SiO2·2H2O
t
1.下列物质中属于纯净物的是( A ) A.Na2CO3· 2O 10H B.水泥 C.纯净的盐酸 D.普通玻璃 2.下列叙述正确的是( BD ) A.酸均不能与酸性氧化物反应 B.玻璃、陶瓷、水泥容器都不能贮存氢氟酸 C.石灰抹墙、水泥砌墙过程的硬化原理相同 D.石灰窑、玻璃熔炉出来的气体主要成分相同 3.下列物质有固定熔点的是( C ) A.水泥 B.玻璃 C.Na2O· 2 D.水玻璃 SiO
二氧化硅(SiO2 )
物理性质 熔沸点高、硬度大 与水反应 与碱反应 与碱性氧 化物反应
二氧化(CO2)
熔沸点低硬度小 CO2+H2O=H2CO3
CO2+2NaOH=Na2CO3+H2O
不反应
SiO2+2NaOH=Na2SiO3+H2O
高温
SiO2+CaO== Ca SiO3 SiO2+4HF=SiF4↑+2H2O
A.熔点很高 C.坚硬 B.与水反应生成对应的酸 D.可与烧碱反应生成盐
2.下列物质中,主要成分不是SiO2的是 A.金刚砂 B.玛瑙
人教版化学必修一4.1《无机非金属材料的主角——硅》讲课课件21ppt

明朝未及,我只有过好每一个今天,唯一的今天。
昨日的明天是今天。明天的昨日是今天。为什么要计较于过去呢(先别急着纠正我的错误,你确实可以在评判过去中学到许多)。但是我发现有的人过分地瞻前顾后了。为 何不想想“现在”呢?为何不及时行乐呢?如果你的回答是“不”,那么是时候该重新考虑一下了。成功的最大障碍是惧怕失败。这些句子都教育我们:不要惧怕失败。如 果你失败了他不会坐下来说:“靠,我真失败,我放弃。”并且不是一个婴儿会如此做,他们都会反反复复,一次一次地尝试。如果一条路走不通,那就走走其他途径,不 断尝试。惧怕失败仅仅是社会导致的一种品质,没有人生来害怕失败,记住这一点。宁愿做事而犯错,也不要为了不犯错而什么都不做。不一定要等到时机完全成熟才动手。 开头也许艰难,但是随着时间的流逝,你会渐渐熟悉你的事业。世上往往没有完美的时机,所以当你觉得做某事还不是时候,先做起来再说吧。喜欢追梦的人,切记不要被 梦想主宰;善于谋划的人,切记空想达不到目标;拥有实干精神的人,切记选对方向比努力做事重要。太阳不会因为你的失意,明天不再升起;月亮不会因为你的抱怨,今 晚不再降落。蒙住自己的眼睛,不等于世界就漆黑一团;蒙住别人的眼睛,不等于光明就属于自己!鱼搅不浑大海,雾压不倒高山,雷声叫不倒山岗,扇子驱不散大雾。鹿 的脖子再长,总高不过它的脑袋。人的脚指头再长,也长不过他的脚板。人的行动再快也快不过思想!以前认为水不可能倒流,那是还没有找到发明抽水机的方法;现在认 为太阳不可能从西边出来,这是还没住到太阳从西边出来的星球上。这个世界只有想不到的,没有做不到的!不是井里没有水,而是挖的不够深;不是成功来的慢,而是放 弃速度快。得到一件东西需要智慧,放弃一样东西则需要勇气!终而复始,日月是也。死而复生,四时是也。奇正相生,循环无端,涨跌相生,循环无端,涨跌相生,循环 无穷。机遇孕育着挑战,挑战中孕育着机遇,这是千古验证了的定律!种子放在水泥地板上会被晒死,种子放在水里会被淹死,种子放到肥沃的土壤里就生根发芽结果。选
昨日的明天是今天。明天的昨日是今天。为什么要计较于过去呢(先别急着纠正我的错误,你确实可以在评判过去中学到许多)。但是我发现有的人过分地瞻前顾后了。为 何不想想“现在”呢?为何不及时行乐呢?如果你的回答是“不”,那么是时候该重新考虑一下了。成功的最大障碍是惧怕失败。这些句子都教育我们:不要惧怕失败。如 果你失败了他不会坐下来说:“靠,我真失败,我放弃。”并且不是一个婴儿会如此做,他们都会反反复复,一次一次地尝试。如果一条路走不通,那就走走其他途径,不 断尝试。惧怕失败仅仅是社会导致的一种品质,没有人生来害怕失败,记住这一点。宁愿做事而犯错,也不要为了不犯错而什么都不做。不一定要等到时机完全成熟才动手。 开头也许艰难,但是随着时间的流逝,你会渐渐熟悉你的事业。世上往往没有完美的时机,所以当你觉得做某事还不是时候,先做起来再说吧。喜欢追梦的人,切记不要被 梦想主宰;善于谋划的人,切记空想达不到目标;拥有实干精神的人,切记选对方向比努力做事重要。太阳不会因为你的失意,明天不再升起;月亮不会因为你的抱怨,今 晚不再降落。蒙住自己的眼睛,不等于世界就漆黑一团;蒙住别人的眼睛,不等于光明就属于自己!鱼搅不浑大海,雾压不倒高山,雷声叫不倒山岗,扇子驱不散大雾。鹿 的脖子再长,总高不过它的脑袋。人的脚指头再长,也长不过他的脚板。人的行动再快也快不过思想!以前认为水不可能倒流,那是还没有找到发明抽水机的方法;现在认 为太阳不可能从西边出来,这是还没住到太阳从西边出来的星球上。这个世界只有想不到的,没有做不到的!不是井里没有水,而是挖的不够深;不是成功来的慢,而是放 弃速度快。得到一件东西需要智慧,放弃一样东西则需要勇气!终而复始,日月是也。死而复生,四时是也。奇正相生,循环无端,涨跌相生,循环无端,涨跌相生,循环 无穷。机遇孕育着挑战,挑战中孕育着机遇,这是千古验证了的定律!种子放在水泥地板上会被晒死,种子放在水里会被淹死,种子放到肥沃的土壤里就生根发芽结果。选
高一化学《. 无机非金属材料的主角——硅》课件

硅酸钠( Na2SiO3 )是一种可溶性硅酸盐其它硅酸盐大多不溶于水。 常温下,二氧化硅的化学性质不活泼不与水、酸(HF除外)反应,能与碱性氧化物或强碱反应生成盐。 2、下列各组物质有关性质关系的比较,正确的是( )
在自然界中,没游离态的硅。硅以化合态存 在于自然界,例如:硅酸盐等,在地壳中含 量居第二位。
SiO2+2NaOH=Na2SiO3+H2O 2、实验室盛装NaOH溶液的试剂瓶为什么用橡胶塞而不用玻璃塞?
Na2SiO3+2HCl=2NaCl+H2SiO3↓ 水晶:电子工业的重要部件、光学仪器、
在自然界中它总是与氧相互化合,没游离态的硅。
在自然界中,没游离态的硅。
主要形成四价的化合物。
常温下,单质碳、硅的化学性质都不活泼,为什么碳在自然界中有稳定的单质(金刚石)存在,而硅却没有?
集成电路、晶体管、硅整流器等半导体材 料,还可以制成太阳能电池、硅的合金可 用来制造变压器铁芯等。
集成电路
晶体管
4.工业上制备:
SiO2
+C 粗硅 高温
你知道吗?
地壳中含量最多的元素是 ______,其次是 _______;空气中含量最多的元素是_____,其次是 _______。人体生理必需的食用盐是______。人 类活动所产生的影响大气质量的气态物质SO2、 CO、NO2等属于__________________类别。
非金属和金属一样,与 人类的关系十分密切.
硅酸钠的水溶液俗称水玻璃, 可用作肥皂填料,木材防火剂及黏 胶剂等.
硅酸盐是构成地壳岩石的主要成分(5%)
Na2SiO3 : Na2O·SiO2
Al2(Si2O5)(OH)4 : Al2O高3·岭2S石iO2·2H2O Ca(Al2Si3O10)·3H2O
无机非金属材料的主角——硅课件(最新)高中化学必修一PPT(46页)

无 机 非 金 属 材料的 主角— —硅课 件(最 新)高 中化学 必修一 PPT(46 页)
三、硅酸 1.性质: (1)弱酸性: 向Na2SiO3溶液中通入CO2,生成白色沉淀:Na2SiO3+CO2+H2O=== H2SiO3↓+Na2CO3。结论:H2SiO3酸性比H2CO3酸性更__弱____。 (2)不稳定性。 H2SiO3不稳定,受热易分解:H2SiO3==△===SiO2+H2O。 点拨:硅酸不能使紫色石蕊试液变色。
3.(2019·四川成都七中高一阶段性测试)下列叙述正确的是
(C )
A.SiO2既能和NaOH溶液反应,又能和氢氟酸反应,所以SiO2属于两性氧 化物
B.因为Na2CO3+SiO2=高==温==Na2SiO3+CO2↑,所以硅酸的酸性比碳酸强 C.CO2和SiO2都能与碳反应,且都作氧化剂 D.CO2和SiO2都是由分子构成的化合物,所以两者物理性质相似
是还原剂,CO2和SiO2都作氧化剂,C正确;CO2是由分子构成的化合物,SiO2
是由硅原子和氧原子构成的立体网状结构的化合物,不存在单个的分子,两者
结构不同,物理性质相差较大,D错误。
4 . (2019· 黑 龙 江 哈 尔 滨 六 中 高 一 月 考 ) 诺 贝 尔 物 理 学 奖 曾 授 予 “ 光 纤 之 父”英国华裔科学家高锟以及两位美国科学家威拉德·博伊尔和乔治·史密斯。 光导纤维的主要成分是二氧化硅,下列关于二氧化硅的说法正确的是 ( D )
黏土
主要设备 水泥回转窑
玻璃窑 /
4.特殊功能的含硅物质: (1)金刚砂(SiC)具有类似___金__刚__石___的结构,硬度很大,可用作砂纸、砂轮 磨料。 (2)硅钢(含Si 4%)具有很高的__导__磁__性____,主要用作变压器铁芯。 (3)硅橡胶,既耐高温又耐低温,用于制造火箭、导弹的零件。 (4)人工制造的分子筛(具有均匀微孔结构的铝硅酸盐),主要用作吸附剂和 __催__化__剂____。
无机非金属材料PPT课件
性质
与碱性氧化 物反应
二氧化碳(CO2) CO2+Na2O=Na2CO3
二氧化硅(SiO2)
高温
SiO2+ CaO == CaSiO3
与碱反应 CO2+2NaOH=Na2CO3+H2O SiO2+2NaOH=Na2SiO3+H2O
与水反应 CO2+H2O=H2CO3
——Biblioteka 与氢氟酸反应——SiO2+4HF=SiF4 ↑+2H2O
25
一、二氧化硅和硅酸
26
2.硅酸(H2SiO3)
硅酸是一种白色粉末状的固体,它不溶于水; 是一种弱酸,不能使指示剂变色。
实验探究: 实验4-1:向饱和Na2SiO3溶液 中滴入酚酞,再滴入稀盐酸。
现象
①滴入酚酞溶液呈红色 ②滴入盐酸有凝胶产生
结论
① Na2SiO3溶液呈碱性 ②硅酸难溶于水
方程式 Na2SiO3+2HCl = H2SiO3(胶体) +2NaCl
演讲人:XXXXXX 时 间:XX年XX月XX日
8
一、二氧化硅和硅酸
粘土
9
一、二氧化硅和硅酸
硅元素
画出硅的原子结构示意图
与哪种原子的结构相似? 碳
分析: 既不易失电子,又不易得电子,主要
形成四价的化合物。
10
1、二氧化硅
(1)存在
水晶
硅石
结晶形:石英 无定形
玛瑙
(2)用途:
光导纤维 石英:耐高温化学仪器、石英电子表、石英钟 水晶:电子工业的重要部件、光学仪器、
物理性质:__硬___度__大__、__熔__点__高__、__难__溶__于__水____ 化学稳定性:____通__常__条__件__下__,__很___稳__定____
无机非金属材料的主角硅课件

2
主要是因為分式的分母不可以為 0,所以少了一個點。這是分式函數與多項式函 數最大的不同。 因此,當我們考慮不等式
2x − 1 > 0 就得小心分母的部分,即 x+1
2x − 1 ≥0⇐ ⇒ (2x − 1)(x + 1) ≥ 0,但 x + 1 ̸= 0。 x+1
由於上面的觀察,我們可以利用將分解範圍,只是要注意一點:
就是所謂的分式不等式。
2x − 1 x2 + x + 2 例如: > 0, ≤ 0 等。 x+1 (x − 3)(x − 4)
我們知道,對於多項式函數,只要畫出 y = f (x) 的圖形草圖來,就可以寫出不 等式的解範圍,但是,對於分式,我們並不容易畫出其草圖。例如: 2x − 1 函數 f (x) = 的函數圖形如下圖所示,在 x = −1 時,函數值不存在, x+1 1 這地方會產生「漸近線」 ,當然,你可以由圖看到:當 x < −1 或 x > 時,可以 2 得到函數值 f (x) > 0,但是,分式函數的圖形實在很不容易繪製,我們的辦法是: 借助多項式來幫忙。那,
因此當我們考慮不等式2x就得小心分母的部分即2x由于上面的觀察我們可以利用將分式不等式轉換成多項式不等式然後利用多項式的草圖來求分式不等式的解範圍只是要注意一點
分式不等式
bee* 104.11.04 ∼ 104.11.09
本篇文章討論分式不等式, 不過,沒有辦法畫分式的草圖,得想辦法變形才行!
1.
分式不等式
先說明何為分式:對於兩個多項式 f (x), g (x) 相除所列出來的式子
2x − 1 x2 + x + 2 分式。例如: , 。 x + 1 (x − 3)(x − 4)
主要是因為分式的分母不可以為 0,所以少了一個點。這是分式函數與多項式函 數最大的不同。 因此,當我們考慮不等式
2x − 1 > 0 就得小心分母的部分,即 x+1
2x − 1 ≥0⇐ ⇒ (2x − 1)(x + 1) ≥ 0,但 x + 1 ̸= 0。 x+1
由於上面的觀察,我們可以利用將分解範圍,只是要注意一點:
就是所謂的分式不等式。
2x − 1 x2 + x + 2 例如: > 0, ≤ 0 等。 x+1 (x − 3)(x − 4)
我們知道,對於多項式函數,只要畫出 y = f (x) 的圖形草圖來,就可以寫出不 等式的解範圍,但是,對於分式,我們並不容易畫出其草圖。例如: 2x − 1 函數 f (x) = 的函數圖形如下圖所示,在 x = −1 時,函數值不存在, x+1 1 這地方會產生「漸近線」 ,當然,你可以由圖看到:當 x < −1 或 x > 時,可以 2 得到函數值 f (x) > 0,但是,分式函數的圖形實在很不容易繪製,我們的辦法是: 借助多項式來幫忙。那,
因此當我們考慮不等式2x就得小心分母的部分即2x由于上面的觀察我們可以利用將分式不等式轉換成多項式不等式然後利用多項式的草圖來求分式不等式的解範圍只是要注意一點
分式不等式
bee* 104.11.04 ∼ 104.11.09
本篇文章討論分式不等式, 不過,沒有辦法畫分式的草圖,得想辦法變形才行!
1.
分式不等式
先說明何為分式:對於兩個多項式 f (x), g (x) 相除所列出來的式子
2x − 1 x2 + x + 2 分式。例如: , 。 x + 1 (x − 3)(x − 4)
高中化学人教必修一 4.1 无机非金属材料的主角---硅 课件 (共31张PPT)

Na2O · SiO2 2MgO · SiO2
镁橄榄石(Mg2SiO4) 钙沸石
Ca(Al2Si3O10) · 3H2O
CaO · Al2O3 · 3SiO2· 3H2O
5.用途:重要的无机非金属材料
陶瓷:原料——黏土 玻璃:原料——纯碱、石灰石和石英; 水泥:原料——黏土和石灰石; 加适量石膏;
高导磁性 用作变 压器铁芯
3.硅橡胶
良好的弹性
4.分子筛
吸附剂、催化剂
具有均匀微 孔结构的铝 硅酸盐
新型无机非金属材料: 高温结构陶瓷、压电陶瓷 新型陶瓷 透明陶瓷、超导陶瓷等
生物陶瓷
人造骨
四、硅单质
1.物理性质:
(1)存在:硅有晶体硅和无定形硅两种 (自然界中没有游离态的硅)。
(2)有金属光泽的灰黑色固体,结构类似 于金刚石,熔点(1410℃)和沸点都很高, 硬度大。 (3)导电性介于导体和绝缘体之间,可以
做半导体材料。
2、化学性质------不活泼
(1)常温下,不能与强酸、强氧化性酸反应,只能与 氟气、氢氟酸和烧碱等物质反应。 Si+2F2==SiF4 Si+4HF==SiF4 +2H2
Si+2NaOH+H2O==Na2SiO3+2H2 (2)加热条件下,能跟一些非金属单质起反应
高温
Si+O2==SiO2
放入Na2SiO3饱和溶液 当水分蒸发后 不易燃烧
现象
结论
制备木材防 用水玻璃浸泡过的木材或织物可防火 火剂的原料
4、硅酸盐组成表示
方法:保持原有各元素化合价不变,按下列顺序 写出各种元素的氧化物,用分隔号隔开。 顺序: 活泼金属氧化物· 较活泼金属氧化物·SiO2 · H 2O 如:硅酸钠(Na2SiO3)
《无机非金属材料的主角——硅》ppt课件

特别提醒
由于硅酸盐的组成与结构很复杂,为 了简化对硅酸盐组成的表示方法,采用了氧 化物法,实际上硅酸盐不是以简单氧化物形 式存在的,而是以种种结构复杂的盐的形式 存在的。
例4 用氧化物的形式表示硅酸盐的组成,其中 正确的是( )
A.钙沸石[Ca(Al2Si3O10)·3H2O],表示为 Al2O3·CaO·3SiO2·3H2O
3. 硅酸的存在及用途 (1)浓度小时:形成硅酸溶胶; (2)浓度大时:形成 硅酸凝胶。 (3)硅胶
硅酸凝胶经干燥脱水得到的硅酸干凝胶称 为“ 硅胶”,具有强的 吸水性,常用作干燥剂或 催化剂的载体。
三、硅酸盐 1. 概念:硅酸盐是由硅、氧和金属 元素组成的化合物的总称。 2. 硅酸盐的性质
硅酸盐是一类结构复杂的固态物质, 大多不溶于水,化学性质很 。稳定
二、硅酸 1
.硅酸的性质
(1)弱酸性
向Na2SiO3溶液中通入CO2,反应的
化学方程式为Na2SiO3+CO2+
H2O===H2SiO3↓+Na2CO3。
弱
结论:H2SiO3酸性比H2CO3酸性 。
(2)不稳定性
2. 硅酸的制备
可溶的硅酸盐与较强的酸反应可制得硅酸, Na2SiO3与盐酸反应的化学方程式为Na2SiO3+ 2HCl===H2SiO3↓+2NaCl。
C.钾云母(K2Al6Si6H4O24),表示为 K2O·2H2O·3Al2O3·6SiO2 D.石棉[CaMg3Si4O12],表示为 CaO·3MgO·4SiO2
【答案】 D
变式训练
4.钾长石(KAlSi3O8)风化生成高岭土 [Al2Si2O5(OH)4]时反应的离子方程式为:
2KAlSi3O8+2H2CO3+5H2O===2K++ 2HCO3-+4H2SiO3+Al2Si2O5(OH)4
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
A.硬度很大,熔点很高
B.与水反应生成对应的酸
C.属于酸性氧化物
D.不溶于任何酸的固体
2.下列物质的变化,不能通过一步化学反应
完成的是( D )
A.CO2→H2CO3
B.SiO2→Na2SiO3
C.NaHCO3→Na2CO3
D.SiO2→H2SiO3
课堂量分测试:
3.下列试剂的贮存方法与NaOH溶液
SiO2+CaO 高温CaSiO3
与氢氟酸反应 SiO2+4HF=SiF4↑+2H2O
2C+SiO2 高温 Si+2CO↑
CO2 、SiO2的化学性质为什么十分相似?
思考1?
1、实验室盛装 NaOH溶液的试 剂瓶为什么用 橡胶塞而不用 玻璃塞?
2、实验室氢氟 酸盛装在什么试 剂中?
SiO2+2NaOH=Na2SiO3+H2O
思考2?二氧化硅难溶于水,也不与水反 应,那么,如何制得硅酸呢?
实验探究:
实验4-1:向饱和Na2SiO3溶液中滴入酚 酞,再滴入稀盐酸
现象
滴入酚酞溶液呈红色 滴入盐酸有胶状沉淀产生
结论
Na2SiO3呈碱性
硅酸难溶于水
方程式 Na2SiO3+2HCl = H2SiO3 ↓+2NaCl
可通过 可溶性硅酸盐 与 其他酸 制得,所生成 的H2SiO3易聚合形成 硅酸溶胶 ;
通入Na2SiO3溶液中生成H2SiO3沉淀
课堂量分测试:
5.能将Na2SiO3、CaCO3、SiO2三种白色粉末
鉴别开来的试剂是( D )
A.NaOH溶液
B.水
C.氢氟酸
D.稀盐酸
6.写出Na2SiO3溶液露置于空气中变浑浊的 化学方程式,并改写成离子方程式。
课堂回忆:
存 在——自然界中的硅石、石英、水晶、玛 瑙、硅藻土等。
的 氧化物、硅酸盐 的形式存在。而碳在地壳中
主要形成 石灰岩、碳酸盐
等矿物。
Si是岩石、沙子、土壤等矿物界的主角:
一、二氧化硅
1.存在
地球上存在的二氧化硅叫 硅石 ,约占地壳总质 量的 12%;其存在形态有 结晶形 和无定形 两大类。
水 晶
玛瑙 玛瑙
水
晶
石英
硅藻土
沙子
石英
水晶
玛瑙
2.SiO2的空间结构:
Si O
正四面体
SiO2是正四面体的空间网状结构,因此硬度大, 熔点(1710℃)、沸点高。
3.SiO2的物理性质与用途:
物质 状态(常 温) 熔点
沸点
SiO2 CO2
固体 气体
1610℃-56.6℃ 2230-℃78.5℃
溶解性 硬度
不溶于水
1
:1
大
二氧化硅是一种高硬度、高熔沸点的固体化合物!
耐高温石英坩埚
光 导 纤 维
水 晶 工 艺 品
玛瑙饰品
4.化学性质
(1)不活泼性:
常温下,与水不反应,氢氟酸是惟一可以与
之反应的酸,化学方程式:
SiO2+4HF=SiF4↑+2H2O
.
氢氟玻酸璃不中能含用SiO2,所玻以瓶璃可盛以装用 氢氟酸 来雕刻玻璃,雕花玻璃在玻璃表面涂上一层石蜡
在石蜡上雕刻出花纹,向 挖空部分加少量氢氟酸
NaOH溶液能与玻璃 中的SiO2反应生成 Na2SiO3,使瓶塞部 分粘结而无法打开。 因此盛装NaOH溶液 的试剂瓶不能用玻璃 塞而要用橡胶塞。
SiO2+4HF=SiF4↑+2H2O
HF能腐蚀玻璃,因此,盛装氢氟酸不 能用玻璃试剂瓶而要用塑料瓶。
二、硅酸:(H2SiO3)
硅酸是一种弱酸,它难溶于水,不能使指示剂 变色,是一种白色粉末状的固体。
不相同的是( AC )
A.HF溶液 B. Na2CO3 溶液
C.盐酸
D. Na2SiO3溶液
4.能证明硅酸的酸性弱于碳酸酸性的实验
事实是( B )
A.CO2溶于水形成碳酸,SiO2难溶于水
B.CO2通入可溶性硅酸盐中析出硅酸
C.高温下SiO2与碳酸盐反应生成CO2
D.HCl通入Na2CO3 溶液放出CO2
洗掉酸并去掉石蜡
(2)具有 酸 性氧化物的通性:
①与烧碱溶液反应: SiO2+2NaOH=Na2SiO
3+H2O
②与生石灰反应: SiO2+CaO 高温
CaSiO3
(3)弱氧化性:
2C+SiO2 高温 Si+2CO↑
SiO2与CO2性质比较
二氧化碳
二氧化硅
存在
空气
硅石、石英、水晶、 玛瑙、沙子、硅藻土
硅酸浓度较大时,则形成 软而透明的、胶冻状的硅 酸凝胶,硅酸凝胶经干燥 脱水后得到多孔的硅酸干 凝胶,称为“硅胶”。
硅胶多孔,吸附水分能力强,常用作实验室和袋装食品 品、瓶装药品等的干燥剂,也可用做催化剂的载体。
活动与探究: Na2SiO3+H2O+CO2=H2SiO3↓+Na2CO3 硅酸是一种比碳酸还要弱的酸,请利用中学实
关于无机非金属材 料的主角硅
【获取新知】 阅读教材P74—75,
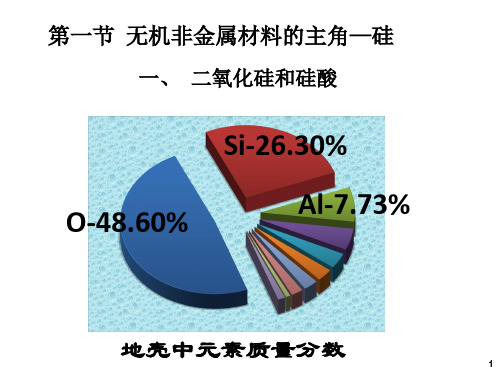
地壳中含量最多的前两种元素是 氧 和 硅 ,它们构成了地壳的基本骨架。硅在地 壳中的含量为 26.3% 。硅的 氧化物 及 硅酸盐 构成了地壳中大部分的岩石、沙子和土 壤,约占地壳质量的 90% 以上。
硅是一种亲 氧 元素,主要以熔点很高
物理性质 熔、沸点低, 微溶于水 熔点高,硬度大,不溶于水
与水反应 CO2+H2O=H2CO3
不反应
与NaOH反应 CO2+2NaOH=Na2CO3+H2O SiO2+2NaOH=Na2SiO3+H2O
化 学 与CaO反应 性 质 与酸反应
CO2+CaO=CaCO3 不反应
与碳反应 2CO2+ C =△ 2CO
SiO2
结 构——硅~氧四面体空间拓展形成立体 网状结构
物理性质——高熔点、高硬度、不溶于水的固体。
化学性质——与碱性氧化物、强碱反应; 与HF反应能腐蚀玻璃。
.用 途 (1)制作光导纤维
(2)石英仪器:石英坩埚、石英表
(3)水晶:电子工业的主要原料,装饰品
(4)玛瑙:工业轴承部分、装饰品等
H2SiO3
物理性质—— 不溶于水、受热易分解的白色 固体。
化学性质——酸性比碳酸还弱的弱酸。
课堂量分测试:
1.地壳中含量第一和第二的两种元素所形
成的化合物不具有的性质是( BD )
验室常见的仪器及药品,设计一个简单实验, 证明硅酸的酸性比碳酸弱。
实验原理——把CO2通入Na2SiO3溶液中
方法一:
方法 二:
课堂小结:
存 在——自然界中的硅石、石英、水晶、玛 瑙、硅藻土等。
SiO2
结 构——硅~氧四面体空间拓展形成立体 网状结构
物理性质——高熔点、高硬度、不溶于水的固体。
化学性质——与碱性氧化物、强碱反应; 与HF反应能腐蚀玻璃。
B.与水反应生成对应的酸
C.属于酸性氧化物
D.不溶于任何酸的固体
2.下列物质的变化,不能通过一步化学反应
完成的是( D )
A.CO2→H2CO3
B.SiO2→Na2SiO3
C.NaHCO3→Na2CO3
D.SiO2→H2SiO3
课堂量分测试:
3.下列试剂的贮存方法与NaOH溶液
SiO2+CaO 高温CaSiO3
与氢氟酸反应 SiO2+4HF=SiF4↑+2H2O
2C+SiO2 高温 Si+2CO↑
CO2 、SiO2的化学性质为什么十分相似?
思考1?
1、实验室盛装 NaOH溶液的试 剂瓶为什么用 橡胶塞而不用 玻璃塞?
2、实验室氢氟 酸盛装在什么试 剂中?
SiO2+2NaOH=Na2SiO3+H2O
思考2?二氧化硅难溶于水,也不与水反 应,那么,如何制得硅酸呢?
实验探究:
实验4-1:向饱和Na2SiO3溶液中滴入酚 酞,再滴入稀盐酸
现象
滴入酚酞溶液呈红色 滴入盐酸有胶状沉淀产生
结论
Na2SiO3呈碱性
硅酸难溶于水
方程式 Na2SiO3+2HCl = H2SiO3 ↓+2NaCl
可通过 可溶性硅酸盐 与 其他酸 制得,所生成 的H2SiO3易聚合形成 硅酸溶胶 ;
通入Na2SiO3溶液中生成H2SiO3沉淀
课堂量分测试:
5.能将Na2SiO3、CaCO3、SiO2三种白色粉末
鉴别开来的试剂是( D )
A.NaOH溶液
B.水
C.氢氟酸
D.稀盐酸
6.写出Na2SiO3溶液露置于空气中变浑浊的 化学方程式,并改写成离子方程式。
课堂回忆:
存 在——自然界中的硅石、石英、水晶、玛 瑙、硅藻土等。
的 氧化物、硅酸盐 的形式存在。而碳在地壳中
主要形成 石灰岩、碳酸盐
等矿物。
Si是岩石、沙子、土壤等矿物界的主角:
一、二氧化硅
1.存在
地球上存在的二氧化硅叫 硅石 ,约占地壳总质 量的 12%;其存在形态有 结晶形 和无定形 两大类。
水 晶
玛瑙 玛瑙
水
晶
石英
硅藻土
沙子
石英
水晶
玛瑙
2.SiO2的空间结构:
Si O
正四面体
SiO2是正四面体的空间网状结构,因此硬度大, 熔点(1710℃)、沸点高。
3.SiO2的物理性质与用途:
物质 状态(常 温) 熔点
沸点
SiO2 CO2
固体 气体
1610℃-56.6℃ 2230-℃78.5℃
溶解性 硬度
不溶于水
1
:1
大
二氧化硅是一种高硬度、高熔沸点的固体化合物!
耐高温石英坩埚
光 导 纤 维
水 晶 工 艺 品
玛瑙饰品
4.化学性质
(1)不活泼性:
常温下,与水不反应,氢氟酸是惟一可以与
之反应的酸,化学方程式:
SiO2+4HF=SiF4↑+2H2O
.
氢氟玻酸璃不中能含用SiO2,所玻以瓶璃可盛以装用 氢氟酸 来雕刻玻璃,雕花玻璃在玻璃表面涂上一层石蜡
在石蜡上雕刻出花纹,向 挖空部分加少量氢氟酸
NaOH溶液能与玻璃 中的SiO2反应生成 Na2SiO3,使瓶塞部 分粘结而无法打开。 因此盛装NaOH溶液 的试剂瓶不能用玻璃 塞而要用橡胶塞。
SiO2+4HF=SiF4↑+2H2O
HF能腐蚀玻璃,因此,盛装氢氟酸不 能用玻璃试剂瓶而要用塑料瓶。
二、硅酸:(H2SiO3)
硅酸是一种弱酸,它难溶于水,不能使指示剂 变色,是一种白色粉末状的固体。
不相同的是( AC )
A.HF溶液 B. Na2CO3 溶液
C.盐酸
D. Na2SiO3溶液
4.能证明硅酸的酸性弱于碳酸酸性的实验
事实是( B )
A.CO2溶于水形成碳酸,SiO2难溶于水
B.CO2通入可溶性硅酸盐中析出硅酸
C.高温下SiO2与碳酸盐反应生成CO2
D.HCl通入Na2CO3 溶液放出CO2
洗掉酸并去掉石蜡
(2)具有 酸 性氧化物的通性:
①与烧碱溶液反应: SiO2+2NaOH=Na2SiO
3+H2O
②与生石灰反应: SiO2+CaO 高温
CaSiO3
(3)弱氧化性:
2C+SiO2 高温 Si+2CO↑
SiO2与CO2性质比较
二氧化碳
二氧化硅
存在
空气
硅石、石英、水晶、 玛瑙、沙子、硅藻土
硅酸浓度较大时,则形成 软而透明的、胶冻状的硅 酸凝胶,硅酸凝胶经干燥 脱水后得到多孔的硅酸干 凝胶,称为“硅胶”。
硅胶多孔,吸附水分能力强,常用作实验室和袋装食品 品、瓶装药品等的干燥剂,也可用做催化剂的载体。
活动与探究: Na2SiO3+H2O+CO2=H2SiO3↓+Na2CO3 硅酸是一种比碳酸还要弱的酸,请利用中学实
关于无机非金属材 料的主角硅
【获取新知】 阅读教材P74—75,
地壳中含量最多的前两种元素是 氧 和 硅 ,它们构成了地壳的基本骨架。硅在地 壳中的含量为 26.3% 。硅的 氧化物 及 硅酸盐 构成了地壳中大部分的岩石、沙子和土 壤,约占地壳质量的 90% 以上。
硅是一种亲 氧 元素,主要以熔点很高
物理性质 熔、沸点低, 微溶于水 熔点高,硬度大,不溶于水
与水反应 CO2+H2O=H2CO3
不反应
与NaOH反应 CO2+2NaOH=Na2CO3+H2O SiO2+2NaOH=Na2SiO3+H2O
化 学 与CaO反应 性 质 与酸反应
CO2+CaO=CaCO3 不反应
与碳反应 2CO2+ C =△ 2CO
SiO2
结 构——硅~氧四面体空间拓展形成立体 网状结构
物理性质——高熔点、高硬度、不溶于水的固体。
化学性质——与碱性氧化物、强碱反应; 与HF反应能腐蚀玻璃。
.用 途 (1)制作光导纤维
(2)石英仪器:石英坩埚、石英表
(3)水晶:电子工业的主要原料,装饰品
(4)玛瑙:工业轴承部分、装饰品等
H2SiO3
物理性质—— 不溶于水、受热易分解的白色 固体。
化学性质——酸性比碳酸还弱的弱酸。
课堂量分测试:
1.地壳中含量第一和第二的两种元素所形
成的化合物不具有的性质是( BD )
验室常见的仪器及药品,设计一个简单实验, 证明硅酸的酸性比碳酸弱。
实验原理——把CO2通入Na2SiO3溶液中
方法一:
方法 二:
课堂小结:
存 在——自然界中的硅石、石英、水晶、玛 瑙、硅藻土等。
SiO2
结 构——硅~氧四面体空间拓展形成立体 网状结构
物理性质——高熔点、高硬度、不溶于水的固体。
化学性质——与碱性氧化物、强碱反应; 与HF反应能腐蚀玻璃。
