物化第九章
物化第九章

上 下 回 返
纯水的表面张力为γ1, 某溶质的表面张力为γ2, 且 γ2>γ1, 形成溶液后,溶质的表面浓度为CS, 本体浓 度C0,则( )
(a)CS>C0 √(b)CS<C0 (c)CS=C0 (d)CS=0
溶液表面层对溶质发生吸附, 当CB(表面浓度)>CB,0(本 体浓度), 则( )。
√(a)称为正吸附, 溶液表面张力降低
(b)称为正吸附, 溶液表面张力不变 (c)称为负吸附, 溶液表面张力增加 (d)称为负吸附, 溶液表面张力降低
上 下 回 返
9.3 气-固界面
9.3.1 界 面 分 析 9.3.2 基 本 概 念 9.3.3 吸附的种类与计算 9.3.4 吸附热力学
上 下 回 返
9.3.1 界面分析——与液表比较
上 下 回 返
3.铺展
(1)定义:液固界面取代固体表面,同时液体表面
增大的过程;
始态:
末态:
(2)铺展吉布斯函数变ΔGs ①定义:单位面积铺展过程的吉布斯函数变化;
②计算:ΔGS=γls +γl -γs=-γl(cosθ-1) ③说明:自发铺展ΔGS<0→→θ=0°或θ不存在。 (3)铺展系数S ①定义:S=-ΔGS=γl(cosθ-1);
上 下 回 返
9.3.3 吸附分类及计算
一、吸附分类(按吸附质与吸附剂的作用本质分类)
1.物理吸附与化学吸附的区别
分类
物理吸附
化学吸附
吸附力
范德华力
化学键力
吸附层数
单层或多层
单层
吸附热 较小,近于液化热 较大,近于反应热
选择性
很差甚至没有
较强
可逆性
具有可逆性
物理化学第9章

三、溶胶的电学性质 1、电动现象 、 在外电场作用下,分散相和分散介质发生相对移 在外电场作用下,分散相和分散介质发生相对移 动现象,称为溶胶的电动现象。 动现象,称为溶胶的电动现象。 1)电泳 带电胶粒在外加电场的作用下在分散介质中作定向 移动的现象称为电泳。 移动的现象称为电泳。 2)电渗 在外加电场作用下, 在外加电场作用下,带电的介质通过多孔膜或 半径为1 nm的毛细管作定向移动 的毛细管作定向移动, 半径为1-10 nm的毛细管作定向移动,这种现象称为 电渗。 电渗。
例如: 例如:云,牛奶,珍珠 牛奶,
一、分散系统、分散相与分散介质 分散系统、 1、按分散相的质点大小分类
类
型
粒子的大小
9 <10-9m
实 例 空气、乙醇的水溶液 空气、 Al(OH)3水溶胶 泥浆
分子分散系统 胶体分散系统 粗分散系统
10-9~10-7m >10-7m
二、 胶体系统的分类
2、按分散相及分散介质的聚集态分类 按分散相及分散介质的聚集态分类
二、溶胶的相互聚沉 由于为AgI正溶胶,主要起聚沉作用的是负离子。 由于为AgI正溶胶,主要起聚沉作用的是负离子。根据 AgI正溶胶 舒尔策-哈迪(Schulze-Hardy) 舒尔策-哈迪(Schulze-Hardy)价数规则二价负离子 的聚沉能力强。 的聚沉能力强。MgSO4,Na2SO4,> CaCl2 , NaNO3 根据感胶离子序 感胶离子序, 根据感胶离子序, Cl- >NO3-, CaCl2 > NaNO3 具有相同的负离子,再根据当与胶体带相 MgSO4,Na2SO4具有相同的负离子,再根据当与胶体带相 反电荷的离子相同时, 反电荷的离子相同时,则另一同性离子的价数也会影 响聚沉值,价数愈高,聚沉能力愈低。 响聚沉值,价数愈高,聚沉能力愈低。Na+ >Mg2+ 综上所述, AgI正溶胶聚沉能力强弱的顺序为: 正溶胶聚沉能力强弱的顺序为 综上所述,对AgI正溶胶聚沉能力强弱的顺序为: Na2SO4> MgSO4 > CaCl2 >NaNO3
【通用】《物理化学(第五版)》第九章复习题答案.ppt
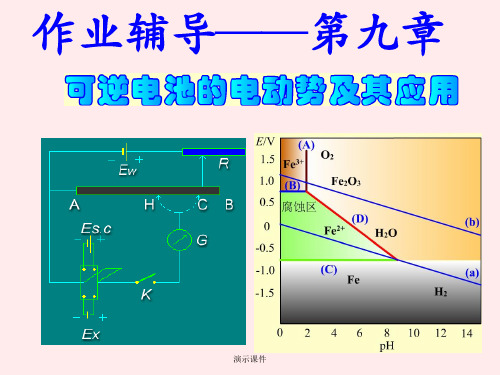
演示课件
复习题
7.在公式ΔrGmΘ=-zEΘF中,ΔrGmΘ是否表示 该电池各物都处于标准态时,电池反应的 Gibbs自由能变化值?
答:在公式ΔrGmΘ=-zEΘF中,ΔrGmΘ表示该 电池各物都处于标准态时,在T,p保持不变 的条件下,按电池反应进行1mol的反应时 系统的Gibbs自由能变化值。
ln
m m'
高价型:Mz+Az-(m1)|Mz+Az-(m2)
E
j=
t z
- t- z 演示课-件
RT F
ln
m1 m2
基本公式
用可逆电池的测定值计算热力学函数变化
值
rGm zFE , rGm zFE
E
RT zF
ln
K
a
r Sm
( r Gm T
)p
E zF (T ) p
E
QR
T rSm
答:可逆电极有三种类型: (1)金属气体电极 如Zn(s)|Zn2+ (m) Zn2+(m) +2e- = Zn(s) (2)金属难溶盐和金属难溶氧化物电极 如:
Ag(s)|AgCl(s)|Cl-(m) AgCl(s)+ e- = Ag(s)+Cl-(m) (3)氧化还原电极 如: Pt|Fe3+(m1),Fe2+(m2) Fe3+(m1) +e- = Fe2+(m2) 对于气体电极和氧化还原电极,在书写时要标明电极
反应所依附的惰性金属。
演示课件
复习题
2.什么叫电池的电动势?用伏特表侧得的电 池的端电压与电池的电动势是否相同?为何 在测电动势时要用对消法?
物理化学第九章

几个总包反应:
H 2 Br2 2HBr
H2 Cl2 2HCl
r
k H2 Br2 1/ 2
1
k
HBr Br2
r k H2 Cl2 1/ 2
H2 I2 2HI
r k H2 I2
问题:上述反应的反应级数 ?
速率常数
速率方程中的比例系数 k 称为反应的速率系数,以前 称为速率常数,现改为速率系数更确切。 它的物理意义是当反应物的浓度均为单位浓度时 k 等 于反应速率,因此它的数值与反应物的浓度无关。在 催化剂等其它条件确定时,k 的数值仅是温度的函数。
第九章 化学动力学基本原理
化学热力学的研究对象和局限性
研究化学变化的方向、能达到的最大限度以及外界条 件对平衡的影响。化学热力学只能预测反应的可能性, 但无法预料反应能否发生?反应的速率如何?反应的 机理如何?例如:
-
例如:
12 N2
32 H2
NH (g) 3
G rm
-16.63kJ mol-1
k 的单位随着反应级数的不同而不同。
准级数反应
在速率方程中,若某一物质的浓度远远大于其他反应
物的浓度,或是出现在速率方程中的催化剂浓度项,
在反应过程中可以认为没有变化,可并入速率系数项,
这时反应总级数可相应下降,下降后的级数称为准级
数反应。例如:
(1) r k[A][B]
[A] [B]
r k'[B] ( k' k[A]) 准一级反应
H 2
12 O2
H O(l) 2
G -237.2kJ mol-1 rm
热力学只能判断这两个反应都能发生,但如何使它发生, 热力学无法回答。
化学动力学的任务和目的
物理化学第九章

R T ②铅蓄电池
PbO2作正极,海绵状Pb作负极,H2SO4作电解液。 电池表示如下:Pb|H2SO4(ρ=1.28gcm-3)|PbO2
放电时:
负极(氧化):Pb + H2SO4 PbSO4 + 2H+ + 2e-
R T 一、常用的化学电源
①锌锰干电池 锌锰干电池是一次电池,通称干电池。 干电池的负极是锌,正极是石墨。石墨周围是MnO2, 电解质是NH4Cl、ZnCl2溶液。 电池可用下式表示:Zn|NH4Cl|MnO2|C
F 负极:Zn + 2NH4Cl Zn(NH3)2Cl2 + 2H++ 2e-
正极:2MnO2 + 2H+ + 2e- 2MnOOH
KOH
负极(氧化 H2) 2:OH 2H2O2e-
正极(还原 12O) 2 : H2O2e- 2OH
电池反应 H2 : 12O2 H2O
H2
F
OHOHOH-
多孔炭电极 图12-11 H2-O2燃料电池示意图
二、化学电源的效率
R T 化学电源将化学能转换为电能的(理想的)最大效率
εmax定义为:
F a(Fe2+)106 E(Fe2+|Fe)E(Fe2+|Fe)RzFTln10160.617V
R T 三、电解还原与氧化的应用
电解的应用
阴极产品:电镀、金属提纯、保护、产品的美化 (包括金属、塑料)和制备aH21,aH+10及7 有机物的还原产物等。
阳极产品:铝合金的氧化和着色、制备氧气、双 氧水、氯气以及有机物的氧化产物等。
(完整word版)《物理化学》高等教育出版(第五版)第九章

第九章电解质溶液练习题一、判断题:1.溶液是电中性的,正、负离子所带总电量相等,则正、负离子离子的迁移数也相等。
2.离子迁移数与离子速率成正比,某正离子的运动速率一定时,其迁移数也一定。
3.离子的摩尔电导率与其价态有关系。
4.电解质溶液中各离子迁移数之和为1。
5.电解池通过l F电量时,可以使1mol物质电解。
6.因离子在电场作用下可以定向移动,所以测定电解质溶液的电导率时要用直流电桥。
7.无限稀电解质溶液的摩尔电导率可以看成是正、负离子无限稀摩尔电导率之和,这一规律只适用于强电解质。
8.电解质的无限稀摩尔电导率Λ∞m可以由Λm作图外推到c1/2 = 0得到。
下列关系式是否正确:(1) Λ∞,1<Λ∞,2<Λ∞,3<Λ∞,4(2)κ1=κ2=κ3=κ4(3)Λ∞,1=Λ∞,2=Λ∞,3=Λ∞,4(4)Λm,1=Λm,2=Λm,3=Λm,410.德拜—休克尔公式适用于强电解质。
11.对于BaCl2溶液,以下等式成立:(1) a = γb/b0;(2) a = a+·a - ; (3) γ± = γ+·γ - 2;(4) b = b+·b-;(5) b±3 = b+·b-2; (6) b± = 4b3。
12.若a(CaF2) = 0.5,则a(Ca2+) = 0.5 ,a(F-) = 1。
二、单选题:1.下列溶液中哪个溶液的摩尔电导最大:(A) 0.1M KCl水溶液;(B) 0.001M HCl水溶液;(C) 0.001M KOH水溶液;(D) 0.001M KCl水溶液。
2.对于混合电解质溶液,下列表征导电性的量中哪个不具有加和性:(A) 电导;(B) 电导率;(C) 摩尔电导率;(D) 极限摩尔电导。
3.在一定温度和较小的浓度情况下,增大强电解质溶液的浓度,则溶液的电导率κ与摩尔电导Λm变化为:(A) κ增大,Λm增大;(B) κ增大,Λm减少;(C) κ减少,Λm增大;(D) κ减少,Λm减少。
《物理化学(第五版)》第九章复习题答案
复习题
8.有哪些求算标准电动势EΘ的方法?在公式E zF ln K 中,EΘ是否是电池反应达平衡时的电动势?KΘ是否是
zE F K exp RT
a
复习题
(8).醋酸的解离平衡常数。 电池:Pt|H2(pΘ)|HAc(mHAc),Ac-(mAc-),Cl-(aCl)|AgCl(s)|Ag(s) 净反应:AgCl(s)+H2(pΘ)→H+(aH+)+Cl-(aCl-) +Ag(s
1.可逆电极有哪些主要类型?每种类型试举一例,并写 出该电极的还原反应。对于气体电极和氧化还原电极 在书写电极表示式时应注意什么问题? 答:可逆电极有三种类型: (1)金属气体电极 如Zn(s)|Zn2+ (m) Zn2+(m) +2e- = Zn(s) (2)金属难溶盐和金属难溶氧化物电极 如: Ag(s)|AgCl(s)|Cl-(m) AgCl(s)+ e- = Ag(s)+Cl-(m) (3)氧化还原电极 如: Pt|Fe3+(m1),Fe2+(m2) Fe3+(m1) +e- = Fe2+(m2) 对于气体电极和氧化还原电极,在书写时要标明电极 反应所依附的惰性金属。
RT a H aCl E E ln zF a 1 2 H2 E RT ln m zF m
复习题
(6)Ag2O(s)的标准摩尔生成焓ΔfHmΘ 和分解压。 电池:Ag(s)+Ag2O(s)|OH-(aOH-)|O2(pΘ )|Pt 净反应:Ag2O(s)→1/2O2(pΘ )+2Ag(s) E r H m zE F zFT T p
物化下册09章_可逆电池

Zn
Cu
+
ZnSO4 (aq)
素瓷烧杯
CuSO4 (aq)
上一内容
下一内容
回主目录
返回
2016/3/2
常见的电池类型
双液电池
用盐桥分开
Zn
盐桥
Cu
+
ZnSO4 (aq)
上一内容 下一内容 回主目录
CuSO4 (aq)
返回
2016/3/2
可逆电池 组成可逆电池的必要条件
原电池
电解池
返回
2016/3/2
标准电池电动势与温度的关系
T E (T ) / V 1.018 45 4.05 10 293.15 K
5
T 9.5 10 293.15 K 3 8 T 110 293.15 K
7
化学反应可逆
上一内容 下一内容 回主目录
能量变化可逆
返回
2016/3/2
可逆电池
可逆电池必须满足二个条件:
(1)电极反应必须是可逆的。 即电极上的化学反应可以 向正、反两个方向进行。 当电流方向改变时, 电极反应随之逆向进行。
Zn
ZnCl2(aq)
AgCl+Ag
上一内容
下一内容
回主目录
第二类电极及其反应
电极
Cl-(a-)|AgCl(s)|Ag(s)
电极反应(还原)
AgCl(s)+e- →Ag(s)+Cl-(a-)
Cl-(a-)|Hg2Cl2(s)|Hg(l) Hg2Cl2(s)+2e- →2Hg(l)+2Cl-(a-) OH-(a-)|Ag2O|Ag(s) Ag2O(s)+H2O+2e- →2Ag(s)+2OH-(a-)
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
9.0 引言
基本概念 性质特征 主要内容
一、基本概念
1.界面:是指两相接触的约几个分子厚度的过渡区,
若其中一相为气体,这种界面通常称为表面。
2.表面:是指液体或固体与其饱和蒸气之间的界面;
但习惯上把液体或固体与空气的界面称为液 体或固体的表面。
3.常见的界面:液-液界面,液-固界面,固-固界面。
9.1.2 界面张力
一、界面张力
1.定义:沿着界面,作用在单位长度上的紧缩力; 2. 单位:N·m-1 3. 方向:沿着界面指向其紧缩方向;
平液面γ平行于液面; 弯液面γ相切于液面。
二、 γ的影响因素
1.物质本性:分子间作用力的区别造成;
(1)液体表面:极性越大,物质表面张力越大;途径:通过对溶质的吸附降低γ。 2.吸附分类:
正吸附——溶液的表面浓度高于其本体浓度; 负吸附——溶液的表面浓度低于其本体浓度。
3. 相关概念:
表面惰性物质:可使溶液表面张力升高的物质;
表面活性物质:可使溶液表面张力降低的物质。
二、吸附量的计算
1. 表面过剩(Γ)——吸附量 (1)定义:单位表面积中所含溶质的物质的量
dγ/dc=0:c↑,γ→;Γ=0;零吸附。
应 用:Γ、c、dγ/dc的相互计算。
纯水的表面张力为γ1, 某溶质的表面张力为γ2, 且 γ2>γ1, 形成溶液后,溶质的表面浓度为CS, 本体浓 度C0,则( )
(a)CS>C0 √(b)CS<C0 (c)CS=C0 (d)CS=0
溶液表面层对溶质发生吸附, 当CB(表面浓度)>CB,0(本 体浓度), 则( )。
√(a)称为正吸附, 溶液表面张力降低
(b)称为正吸附, 溶液表面张力不变 (c)称为负吸附, 溶液表面张力增加 (d)称为负吸附, 溶液表面张力降低
2.表达式:RTlnpr/p=2γM/ρr ——凸液面
RTlnp/pr=2γM/ρr ——凹液面
3. 说明:
(1)凸液面:pr>p;r↓,pr↑; 凹液面:pr<p;r↓,pr↓。
(2)此公式亦适用于固体表面(固体升华)的粗略计算。
RTlnpr/p=2γM/ρr RTlnp/pr=2γM/ρr
——凸液面 ——凹液面
9.1 界面张力
9.1.1 界 面 分 析 9.1.2 界 面 张 力 9.1.3 热力学公式
9.1.1 界面分析
1.表面分子受力:合力指向液体内部,即受力不均衡;
2.受力结果:表面分子 向液体内部运动,即力 求减小液体表面的面积 至最小;
气相
3.举例说明:小液滴呈 液相 球形——同样体积下球 形的表面积最小。
温度一定,弯曲液面与水平液面饱和蒸气压的关系为:
√(a)p凸>p平>p凹 (b)p凸<p平<p凹 (c)p凸=p平=p凹
封闭在钟罩内的大小液滴的变化趋势是: (a)小的变大, 大的变小
(√b)小的变小, 大的变大
(c)大小液滴变为半径相等为止
(d)不发生变化
9.2.2 溶液表面
一、溶液表面的吸附现象
4.公式在界面现象中的应用:
(1)条件:恒温恒压及系统中相的组成不改变;
(2)计算:dG=dGS=γdAs→→GS=γAs
→→GS=∑γiAsi(绝对吉布斯函数值)
(3)说明:界面现象产生的最终原因是GS自发减小
←或降界面面积减至最小; ←或通过一定手段降低γ。
9.2 气-液界面
9.2.1 弯曲纯液面 9.2.2 溶液表面
9.2.1 弯曲纯液面
一、附加压力
1.产生原因:液面张力的存在;
pg
pg
p合 pl= pg+ p合
→平液面:pl=pg;
→弯液面:pl=pg±p合
p合 p合
2.定义:弯曲液面内外的压力差;
3.说明
def
p p(l) p(g)
(1)弯液面分类:凹面——小气泡,凸面——小液滴;
(2)附加压力方向指向液体内部;
气-液界面,气-固界面
二、性质特征
1.性质:※有一定厚度; ※界面相的结构和性质与两相本体不同.
2.界面现象:由于界面相的结构和性质与两相本
体不同所造成的特殊表现。
3.影响因素: ※物质的分散度; ※分散度用比表面积表征;
→→物系质量一定,分散度越大,aS越大, 界面现象越明显。
三、主要内容
产生原 因 几种典型界面
(3)Δp与弯液面γ呈正比;γ与温度及液体性质有关。
(4)空气中的小气泡:两个界面→Δp=4γ/r。
★水平放置的毛细管中装有非润湿性液体,在左端 加热,管内液体会如何变化?
a.不移动;b.向右移动;√c.向左移动;d.来回移动;
二、弯曲纯液面的蒸汽压
1. 比较:平液面p=f(T,物性) ——克—克方程; 小液滴p=f(T,r,物性) ——开尔文公式;
9.1.3 热力学公式
1.公式演变:
简单系统→多组分系统→具有界面效应的多组分系统; 2. 公式形式:略 3. γ的表达式:
G U H A A T ,s p ,n B A S ,s V ,n B A S ,s p ,n B A T ,s V ,n B
(3)凸液面Δp>0;凹液面Δp<0。
4.拉普拉斯方程 Δp=2γ/r 单 位:N·m-2
注 意:凸液面r>0;凹液面r<0
Δp=2γ/r>0 Δp=2γ/r<0 Δp=4γ/r>0
说 明:
(1)附加压力与弯液面的底面半径无关,液面上任何 一点的Δp相同。
(2)Δp与弯液面的曲率半径呈反比: r↑,Δp↓;r→∞(平液面),Δp=0。
(金属键)> (离子键)> (极性共价键)> (非极性共价键)
(2)一般的: 固体的表面张力大于液体的表面张力。
2.温度的影响:源于温度对分子间作用力的影响;
(1)一般的:温度升高→分子间作用力减小
→表面分子受力趋于均衡→γ减小;
(2) T→TC:液体表面的γ→0。
→→同一种界面在一定温度下具有一定的γ值 。
与同量溶剂在本体中所含溶质的物 质的量之差;
(2) 单位:mol/m2;
(3) 说明:正吸附Γ>0;负吸附Γ<0。
2. 吉布斯等温吸附式
(1) 推导:略
(2) (3)
表达式: 说明:
Β
aB RT
aB
T
适用条件:理想稀溶液; 温度一定: dγ/dc<0:c↑,γ↓;Γ>0;正吸附。
dγ/dc>0:c↑,γ↑;Γ<0;负吸附。
