初三化学上学期化学方程式k
九年级上学期化学方程式汇总 (附答案)

九年级上学期化学方程式汇总姓名:一、氧气的性质:(1)单质与氧气O2的反应:(化合反应)1. 镁在空气中燃烧:2Mg + O22MgO2. 铁在氧气中燃烧:3Fe + 2O2Fe3O43. 铜在空气中受热:2Cu +O22CuO4. 氢气中空气中燃烧:2H2 + O22H2O5. 红磷在空气中燃烧(研究空气组成的实验):4P + 5O22P2O 56. 硫粉在空(氧)气中燃烧:S + O2SO27. 碳在空(氧)气中充分燃烧:C + O2CO28. 碳在空(氧)气中不充分燃烧:2C + O22CO(2)化合物与氧气O2的反应:9. 一氧化碳在空气中燃烧:2CO + O22CO210. 甲烷在空气中燃烧:CH4 + 2O2CO2 + 2H2O11. 酒精在空气中燃烧:C2H5OH + 3O22CO2 + 3H2O(3)氧气O2的制取:12.拉瓦锡研究空气的成分实验:2HgO 2Hg+ O2↑13.加热高锰酸钾:2KMnO4K2MnO4 + MnO2 + O2↑实验室制氧气原理114.加热氯酸钾(二氧化锰):2KClO32KCl + 3O2↑实验室制氧气原理215.过氧化氢在二氧化锰催化下分解:2H2O2 2H2O+ O2↑实验室制氧气原理3二、自然界中的水:16.水在直流电的作用下分解(研究水的组成实验):2H2O 2H2↑+ O2↑17.二氧化碳可溶于水:H2O + CO2==H2CO3三、质量守恒定律:18.镁在空气中燃烧:2Mg + O22MgO19.铁和硫酸铜溶液反应:Fe + CuSO4 === FeSO4 + Cu20.氢气还原氧化铜:H2 + CuO Cu + H2O21.碳酸钠与稀盐酸反应: Na2CO3 + 2HCl == 2NaCl + H2O + CO2↑四、碳C和碳的氧化物:(1)碳C的化学性质22. 碳在氧气中充分燃烧:C + O2CO223.木炭还原氧化铜:C+ 2CuO 2Cu + CO2↑24.焦炭还原氧化铁:3C+ 2Fe2O34Fe + 3CO2↑(2)煤炉中发生的三个化合反应:25.煤炉的底层:C + O2CO226.煤炉的中层:CO2 + C 2CO27.煤炉的上部蓝色火焰的产生:2CO + O22CO2(3)二氧化碳CO2的制法与性质:28.大理石CaCO3与稀盐酸HCl反应(实验室制二氧化碳):CaCO3 + 2HCl == CaCl2 + H2O + CO2↑29.碳酸不稳定而分解:H2CO3 == H2O + CO2↑30.高温煅烧石灰石:CaCO3CaO + CO2↑31.生石灰溶于水:CaO + H2O == Ca(OH)232.石灰水Ca(OH)2与二氧化碳CO2反应(鉴别二氧化碳CO2):Ca(OH)2 + CO2 === CaCO3 ↓+ H2O (4)一氧化碳CO的性质:33.一氧化碳还原氧化铜:CO+ CuO Cu + CO234.一氧化碳的可燃性:2CO + O22CO2其它反应:35.灭火器的原理(碳酸钠与稀盐酸反应):Na2CO3 + 2HCl == 2NaCl + H2O + CO2↑36. 锌和稀硫酸(实验室制氢气H2)Zn + H2SO4 = ZnSO4 + H2↑37.金属铁的治炼原理:3CO+ Fe2O3 2Fe + 3CO2。
初三上册化学方程式大全

初三上册化学方程式大全一、氧气的性质1、镁在空气中燃烧:2Mg + O₂点燃 2MgO2、铁在氧气中燃烧:3Fe + 2O₂点燃 Fe₃O₄3、铜在空气中受热:2Cu + O₂加热 2CuO4、铝在空气中燃烧:4Al + 3O₂点燃 2Al₂O₃5、氢气中空气中燃烧:2H₂+ O₂点燃 2H₂O6、红磷在空气中燃烧:4P + 5O₂点燃 2P₂O₅7、硫粉在空气中燃烧: S + O₂点燃 SO₂8、碳在氧气中充分燃烧:C + O₂点燃 CO₂9、碳在氧气中不充分燃烧:2C + O₂点燃 2CO二、实验室制氧气1、加热氯酸钾(有少量的二氧化锰):2KClO₃加热 2KCl +3O₂ ↑2、加热高锰酸钾:2KMnO₄加热 K₂MnO₄+ MnO₂+ O₂↑3、过氧化氢在二氧化锰作催化剂条件下分解反应:2H₂O₂二氧化锰 2H₂O + O₂ ↑三、水的性质1、水在直流电的作用下分解:2H₂O 通电 2H₂↑+ O₂ ↑2、生石灰溶于水:CaO + H₂O == Ca(OH)₂四、二氧化碳的性质1、碳在氧气中充分燃烧:C + O₂点燃 CO₂2、二氧化碳通过灼热碳层: C + CO₂高温 2CO3、一氧化碳在氧气中燃烧:2CO + O₂点燃 2CO₂4、二氧化碳和水反应(二氧化碳通入紫色石蕊试液):CO₂+H₂O === H₂CO₃5、碳酸不稳定而分解:H₂CO₃=== H₂O + CO₂↑6、二氧化碳通入澄清石灰水:Ca(OH)₂+ CO₂==== CaCO₃↓+ H₂O7、大理石与稀盐酸反应(实验室制二氧化碳):CaCO₃+ 2HCl == CaCl₂+ H₂O + CO₂↑五、燃料及其利用1、甲烷在空气中燃烧:CH₄+ 2O₂点燃 CO₂+ 2H₂O2、酒精在空气中燃烧:C₂H₅OH + 3O₂点燃 2CO₂+ 3H₂O这些化学方程式是初三上册化学中的重要知识点,需要同学们熟练掌握和理解。
九年级化学上册常见化学方程式
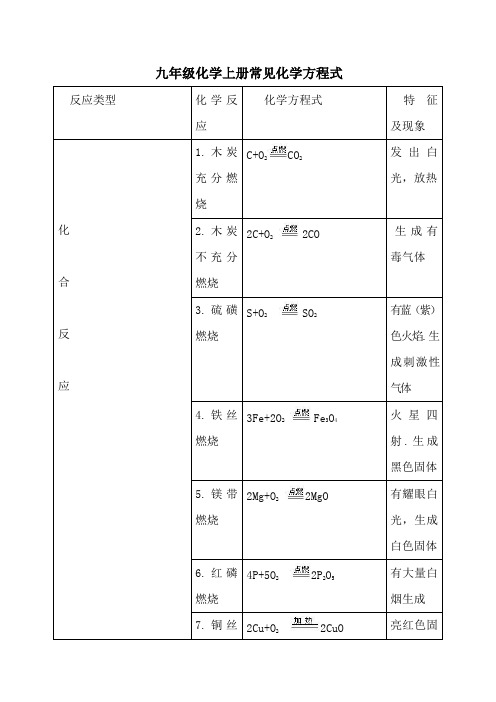
九年级化学上册常见化学方程式反应类型化学反应化学方程式特征及现象化合反应1.木炭充分燃烧C+O2CO2发出白光,放热2.木炭不充分燃烧2C+O2 2CO生成有毒气体3.硫磺燃烧S+O2 SO2有蓝(紫)色火焰.生成刺激性气体4.铁丝燃烧3Fe+2O2 Fe3O4火星四射.生成黑色固体5.镁带燃烧2Mg+O2 2MgO有耀眼白光,生成白色固体6.红磷燃烧4P+5O22P2O5有大量白烟生成7.铜丝2Cu+O22CuO亮红色固在空气中受热体变成黑色固体8.铝丝燃烧4Al+3O22Al2O3火星四射,生成白色固体9.氢气燃烧2H2+O22H2O有淡蓝色火焰10.有毒气体CO 燃烧2CO+O22CO2有蓝色火焰11.CO2和H2O反应CO2+H2O = H2CO3生成物能使石蕊变红12.CO2与C反应CO2+C 2CO所有物质中都含碳元素13.生石灰和水反应CaO+H2O = Ca(OH)2实验室制氢氧化钙,反应放热14.氢气与氯气H2+Cl2 2HCl剧烈燃烧,产生的反应苍白色火焰15.汞与氧气的反应2Hg+O22HgO 银白色液体变成粉红色固体分解反应16.氯酸钾制取氧气2KClO3 2KCl+3O2↑加热固体混合物制取氧气17.过氧化氢制氧气2H2O2 2H2O + O2 ↑常温下固液混合物制取氧气18.高锰酸钾制氧气2KMnO4K2MnO4+MnO2+O2↑加热纯净物制取氧气19.水电解2H2O 2H2↑+O2↑分解产生两种气体单质20.碳酸分解H2CO3= H2O+CO2↑碳酸不稳定21.碳酸钙煅烧CaCO3CaO+CO2↑工业制取二氧化碳22.氧化2HgO 2Hg+O2产生银白汞分解↑色液体金属23.碳酸氢钠受热分解2NaHCO3Na2CO3+CO2↑+H2O干粉灭火器的原理置换反应24.碳还原氧化铜C+2CuO 2Cu+CO2↑黑色固体混合物加热生成红色固体25.碳还原氧化铁3C+2Fe2O3 4Fe+3CO2↑固体混合物反应生黑色固体26.碳还原四氧化三铁2C+Fe3O4 3Fe+2CO2↑黑色固体混合物加热生黑色固体27.镁带与盐酸反应Mg+2HCl == MgCl2 +H2↑该反应放热28.氢气还原氧化铜H2+CuO Cu+H2O单质气体还原氧化铜,生红色原理酸氢盐遇酸生成CO234.苏打与稀盐酸反应Na2CO3+2HCl=2NaCl+H2O+CO2↑泡沫灭火器的原理35.硫酸铜与氢氧化钠反应CuSO4+2NaOH=Cu(OH)2↓+Na2SO4有蓝色沉淀生成其他36.乙醇燃烧C2H5OH+3O22CO2+3H2O 绿色燃料燃烧37.一氧化碳还原氧化铜CO+CuO Cu+CO2化合物的气体还原氧化铜38.一氧化碳还原氧化铁3CO+Fe2O32Fe+3CO2工业用赤铁矿炼铁39.一氧4CO+Fe3O43Fe+4CO2工业用磁化碳还原四氧化三铁铁矿炼铁40.甲烷燃烧CH4+2O2CO2+2H2O有蓝色火焰。
最新人教版九年级化学上册化学方程式及实验现象总结

中考复习资料总结九年级上册化学方程式及实验现象总结一、化合反应1、木炭(碳)在空气中燃烧现象:发出红光..,放出热量,生成能使澄清石灰水变浑浊的气体;在氧气中燃烧现象:发出白光..,放出热量,生成能使澄清石灰水变浑浊的气体。
C+O2点燃CO2(充分燃烧)2C+O2点燃 2 CO (不充分燃烧)2、硫在空气中燃烧现象:发出微弱的淡蓝色......火焰,生成有刺激性气味的气体,放出热量;在氧气中燃烧现象:发出明亮的蓝紫色......火焰,生成有刺激性气味的气体,放出热量。
S+O2点燃SO23、红磷(或者白磷)在空气中燃烧现象:产生大量白烟,放出热量。
4P+5O2点燃2P2O54、注意..铁丝在空气中不能燃烧;在氧气燃烧现象:剧烈燃烧,火星四射,生成黑色固体,放出热量。
3Fe+2O2点燃Fe3O45、镁带在空气中燃烧现象:发出耀眼的白光,冒白烟,生成白色粉末,放出热量。
2Mg+O2点燃2MgO6、氢气在空气(或氧气)中燃烧现象:发出淡蓝色火焰,放出热量,火焰上罩一个干而冷的烧杯,烧杯内壁出现水雾。
2H2+O2点燃2H2O7、铜在空气中加热现象:红色固体逐渐变成黑色2Cu+O2△2CuO8、一氧化碳在空气中燃烧现象:发出蓝色火焰,放出热量,火焰上罩一个涂有澄清石灰水的烧杯,澄清石灰水变浑浊。
2CO+O2点燃2CO29、汞在加热的条件下与氧气反应:2Hg+O2△2HgO10、铝在空气中燃烧:4Al+3O2点燃2Al2O311、二氧化碳通过灼热的碳层:CO2 +C高温2CO12、二氧化碳与水反应:CO2 +H2O == H2CO3(二氧化碳通入紫色石蕊试液,溶液变红的原因)二、分解反应1、氧化汞加热分解:2HgO△2Hg+O2↑2、高锰酸钾制氧气:2KMnO4△K2MnO4+MnO2+O2↑3、氯酸钾制氧气:2KClO3MnO22KCl+3O2↑△MnO24、过氧化氢制氧气:2H2O2 2H2O+O2↑5、电解水:2H2O通电2H2↑+O2↑6、碳酸不稳定,易分解:H2CO3 === H2O+CO2↑ (二氧化碳通入石蕊试液,溶液变红,加热红色变为紫色的原因)三、其他反应1、实验室制取二氧化碳:CaCO3+2HCl==CaCl2+ H2O + CO2↑ (大理石或石灰石和稀盐酸)2、木炭还原氧化铜:C+2CuO高温2Cu+CO2↑ (CuO为黑色粉末)现象:黑色粉末逐渐变为红色,澄清石灰水变浑浊。
初三化学第一学期化学方程式网络化整理归纳

初三第一学期化学方程式网络化整理归纳一、以氧气为核心的物质转化关系图①★★★过氧化氢加二氧化锰催化制氧气: 2H 2O 2MnO 2 2H 2O+O 2↑②★★电解水:2H 2O通电2H 2↑+O 2↑ ③★2H 2+O 2点燃2H 2O④★★★高锰酸钾加热制氧气: 2KMnO Δ K 2MnO 4+MnO 2+O 2↑ 附:实验室用氯酸钾制取氧气: 2KClO 3MnO 22KCl + 3O 2↑⑤★3Fe + 2O 2点燃Fe 3O 4 2Cu + O Δ2CuO 2Mg + O 2点燃2MgOC + O 2 点燃CO 2 4P + 5O 2 点燃2P 2O 5 ⑥化学方程式见下图③和⑥① C + O 2点燃CO 2 ② 2C+O 2点燃 2CO ③ 2CO+O 2点燃2CO 2 ④ ★工业炼铁(赤铁矿)原理:Fe 2O 3+3CO高温 2Fe+3CO 2 或 ΔCu+CO 2⑤ C+CO 2高温 2CO ⑥★★甲烷(天然气、沼气、瓦斯等)燃烧:CH 4+2O 2点燃2H 2O+CO 2⑦CO 2与水反应:CO 2 + H 2O === H 2CO 3 ⑧生成碳酸不稳定:H 2CO 3===CO 2↑+ H 2O⑨★★★实验室检验二氧化碳: Ca(OH)2+CO 2= CaCO 3↓+ H 2O (Na 2CO 3转化见第八章)⑩★★★石灰石(大理石)与稀盐酸制二氧化碳:CaCO 3+2HCl=CaCl 2+H 2O+CO 2↑⑪CaCO 3高温 CaO+ CO 2↑(见第八章) ⑫ Δ 2Cu+CO 2↑△三、以金属活动性顺序为核心的置换反应①★★锌和稀硫酸制氢气: Zn+H2SO4=ZnSO4+H2↑②★★★铁与硫酸铜溶液反应(古代湿法炼铜原理):Fe+CuSO4=Cu+FeSO4③★★铁与稀盐酸(稀硫酸)反应:Fe+2HCl =FeCl2+H2↑Fe+H2SO4=FeSO4+H2↑④铜与硝酸银溶液反应:Cu+2AgNO3 = Cu(NO3)2+ 2Ag⑤氧化铜被H2还原为铜:H2ΔCu+H2O。
初三化学方程式总结(初三上册)

初三化学方程式总结(初三上册)初三化学方程式总结(初三上册)初三化学方程式总结(1--7单元)化合反应1、镁在空气中燃烧:2Mg+O2点燃2MgO2、铁在氧气中燃烧:3Fe+2O2点燃Fe3O43、铝在空气中燃烧:4Al+3O2点燃2Al2O34、氢气在空气中燃烧:2H2+O2点燃2H2O5、红磷在空气中燃烧:4P+5O2点燃2P2O56、硫粉在空气中燃烧:S+O2点燃SO27、碳在氧气中会充分燃烧:C+O2点燃CO28、碳在氧气中不充分燃烧:2C+O2点燃2CO9、二氧化碳通过冰凉碳层:C+CO2高温2CO10、一氧化碳在氧气中燃烧:2CO+O2点燃2CO211、二氧化碳和水反应(二氧化碳通入紫色石蕊试液):CO2+H2O===H2CO312、生石灰溶于水:CaO+H2O===Ca(OH)213、无水硫酸铜作干燥剂:CuSO4+5H2O====CuSO45H2O14、钠在氯气中燃烧:2Na+Cl2点燃2NaCl分解反应15、实验室用双氧水制氧气:2H2O2MnO22H2O+O2↑16、加热高锰酸钾:2KMnO4加热K2MnO4+MnO2+O2↑17、水在直流电的积极作用下分解:2H2O通电2H2↑+O2↑18、碳酸不稳定而纯化:H2CO3===H2O+CO2↑19、高温煅烧石灰石(二氧化碳农业机械制法):CaCO3高温CaO+CO2↑置换反应20、铁和硫酸铜氢氧化钠反应:Fe+CuSO4==FeSO4+Cu21、锌和稀硫酸反应(实验室制氢气):Zn+H2SO4==ZnSO4+H2↑22、镁和稀盐酸反应:Mg+2HCl===MgCl2+H2↑23、氢气还原氧化铜:H2+CuO加热Cu+H2O24、木炭还原氧化铜:C+2CuO高温2Cu+CO2↑25、甲烷在空气中会燃烧:CH4+2O2点燃CO2+2H2O26、水蒸气通过灼热碳层:H2O+C高温H2+CO27、焦炭还原氧化铁:3C+2Fe2O3高温4Fe+3CO2↑其他28、氢氧化钠溶液与硫酸铜溶液反应:2NaOH+CuSO4==Cu(OH)2↓+Na2SO429、甲烷在空气中燃烧:CH4+2O2点燃CO2+2H2O30、酒精在空气当中燃烧:C2H5OH+3O2点燃2CO2+3H2O31、乙炔还原氧化铜:CO+CuO加热Cu+CO232、硫化氢还原氧化铁:3CO+Fe2O3高温2Fe+3CO233、氢气通过澄清石灰水(检验二氧化碳):Ca(OH)2+CO2====CaCO3↓+H2O34、氢氧化钠和二氧化碳反应(除去二氧化碳):2NaOH+CO2====Na2CO3+H2O35、石灰石(或大理石)与稀盐酸反应(二氧化碳的实验室制法):CaCO3+2HCl===CaCl2+H2O+CO2↑36、碳酸钠与浓盐酸反应(泡沫灭火器的电磁场):Na2CO3+2HCl===2NaCl+H2O+CO2↑一.生物体与氧气的反应:(1)单质与氧气的反应:1.镁在空气中燃烧:2Mg+O2点燃2MgO2.铁在氧气中燃烧:3Fe+2O2点燃Fe3O43.铜在空气中受热:2Cu+O2加热2CuO4.铝在空气中燃烧:4Al+3O2点燃2Al2O35.氢气中二氧化碳中燃烧:2H2+O2点燃2H2O6.红磷在空气中挥发:4P+5O2点燃2P2O57.硫粉在空气中燃烧:S+O2点燃SO28.碳在氧气中充分熔化:C+O2点燃CO29.碳在氧气中不充分燃烧:2C+O2点燃2CO(2)化合物与氧气的反应:10.一氧化碳在氧气中燃烧:2CO+O2点燃2CO211.甲烷在空气之中燃烧:CH4+2O2点燃CO2+2H2O12.酒精在空气中燃点:C2H5OH+3O2点燃2CO2+3H2O二.几个分解反应:13.水在直流电的示范作用下分解:2H2O通电2H2↑+O2↑14.加热碱式碳酸铜:Cu2(OH)2CO3加热2CuO+H2O+CO2↑15.加热氯酸钾(有少量的二氧化锰):2KClO3====2KCl+3O2↑16.加热高锰酸钾:2KMnO4加热K2MnO4+MnO2+O2↑17.碳酸不稳定而分解:H2CO3===H2O+CO2↑18.高温煅烧石灰石:CaCO3高温CaO+CO2↑三.几个氧化还原成反应:19.氢气还原氧化铜:H2+CuO加热Cu+H2O20.木炭还原氧化铜:C+2CuO高温2Cu+CO2↑成才热线:8698887,8697778初三化学复习资料石灰石(或大理石)与稀盐酸反应(实验室制CO2):CaCO3+2HCl===CaCl2+H2O+CO2↑二氧化碳通过澄清石灰水(检验CO2):Ca(OH)2+CO2=CaCO3↓+H2OMnO2氯酸钾与氯二氧化锰的混合物共热:2KClO32KCl+3O2↑加热高锰酸钾:2KMnO4K2MnO4+MnO2+O2↑点燃一、燃烧反应1、木炭在氧气中会燃烧:C+O2CO2(在氧气中:产生使石灰水变浑浊的无色气体)点燃2、木炭在空气中所不充分燃烧:2C+O23、硫化氢在氧气中燃烧:2CO+O24、硫粉在氧气中所燃烧:S+O25、磷在氧气中燃烧:4P+5O26、铁在氧气中燃烧:3Fe+2O2点燃2CO2CO2(产生蓝色火焰)点燃SO2(在空气中:呈淡蓝色火焰;在氧气中:呈明亮的蓝紫色闪电,产生有刺激性气味的气体)点燃2P2O5(产生浓厚的白烟)Fe3O4(剧烈燃烧,火星四射,生成黑色固体)瓶底留少量2MgO(发出耀眼的白光,生成白色固体)2CuO(红色固体变为黑色固体)水或细沙点燃7、镁在空气中燃烧:2Mg+O28、铜在空气中加热;2Cu+O2点燃9、氢气在二氧化碳中燃烧:2H2+O2点燃2H2O(产生淡蓝色火焰,干冷烧杯壁有小水株。
初三上学期所学化学方程式汇总
初三上学期所学化学方程式汇总1、高锰酸钾制氧气:2KMnO4加热 K2MnO4 + MnO2 + O2↑2、氯酸钾制氧气:2KClO3二氧化锰 2KCl + 3O2↑3、双氧水制氧气:2H2O2 二氧化锰2H2O + O2↑4、电解水:2H2O 通电 2H2 ↑ + O2↑5、锌和稀硫酸反应制取氢气:Zn + H2SO4 == ZnSO4 + H2↑6、锌和稀盐酸反应制取氢气:Zn + 2HCl == ZnCl2+ H2↑7、石灰石与稀盐酸反应制取二氧化碳:CaCO3+2HCl = CaCl2+H2O+CO2↑8、碳酸钠与稀盐酸:Na2CO3 + 2HCl == 2NaCl+ H2O + CO2↑9、高温煅烧石灰石:CaCO3 高温 CaO +CO2↑10、二氧化碳通入澄清石灰水中:CO2 + Ca(OH)2 == CaCO3↓+ H2O11、氢气在空气中燃烧:2H2 + O2点燃2H2O12、氢气还原氧化铜:H2 + CuO 加热 Cu + H2O13、木炭在空气(或氧气)中完全燃烧:C + O2点燃 CO214、木炭不充分燃烧:2C + O2点燃 2CO15、木炭还原氧化铜:C + 2CuO 高温 2Cu + CO2↑16、木炭还原氧化铁:3C + 2Fe2O3高温 4Fe + 3CO2↑17、一氧化碳燃烧:2CO + O2点燃 2CO218、一氧化碳还原氧化铜:CO + CuO 加热 Cu + CO219、酒精燃烧:C2H5OH + 3O2点燃 2CO2 + 3H2O20、甲烷燃烧:CH4 + 2O2 点燃 CO2 + 2H2O21、红磷在空气(或氧气)中燃烧:4P + 5O2点燃2P2O522、硫磺在空气(或氧气)中燃烧:S + O2点燃SO223、镁条在空气(或氧气)中燃烧:2Mg + O2 点燃 2MgO24、铁丝在氧气中燃烧:3Fe + 2O2 点燃 Fe3O425、生石灰与水反应:CaO + H2O == Ca(OH)226、镁与稀盐酸反应:Mg + 2 HCl == MgCl2+ H2↑27、二氧化碳通过灼热的炭层:CO2 + C 高温 2CO (典型的吸热反应)28、二氧化碳和水反应生成碳酸:CO2 + H2O == H2CO329、碳酸分解:H2CO3 == H2O + CO2↑30、铁和硫酸铜溶液反应:Fe + CuSO4 == Cu + FeSO431、硫酸铜溶液和氢氧化钠溶液反应:CuSO4+2NaOH = Na2SO4+Cu(OH)2↓32、汞在空气中加热:2Hg + O2 加热 2HgO33、氧化汞在高温条件下分解:2HgO 高温 2Hg + O2↑34、甲醇在空气中燃烧:CH3OH + O235、一氧化碳还原氧化铁:CO + Fe2O336、一氧化碳还原四氧化三铁:CO + Fe3O42KMnO4加热 K2MnO4 + MnO2 + O2↑2KClO3二氧化锰 2KCl + 3O2↑2H2O2 二氧化锰2H2O + O2↑CaCO3 + 2HCl = CaCl2 + H2O + CO2↑。
初三九上化学方程式知识点汇总
11. 二氧化碳通过灼热的碳层:C + CO2 === 2CO
高温
12. 木炭还原氧化铜:C + 2CuO === CO2↑+ 2Cu(黑色粉末变红,澄清石灰水变浑浊)
高温
13. 木炭还原氧化铁:3C + 2 Fe2O3 === 3CO2↑+ 4Fe( Fe2O3 为红色,铁粉为黑色,)
14. 实验室用石灰石和稀盐酸制二氧化碳:CaCO3 + 2HCl === CaCl2 + H2O + CO2↑
24. 实验室用锌与稀硫酸制氢气:Zn + H2SO4 === ZnSO4 + H2↑ 25. 加热氧化汞:2HgO =△=== 2Hg + O2 ↑(HgO 为红色)
26. 碳酸钠和稀盐酸反应:Na2CO3 + 2HCl === 2NaCl + H2O + CO2↑
27. 生石灰与水反应:CaO + H2O === Ca(OH)2(放出大量的热) 28. 甲烷在空气中燃烧:CH4 + 2O2 点燃 CO2 + 2H2O(淡蓝色火焰) 29. 乙醇(酒精)燃烧:C2H5OH +3O2 点燃 2CO2 + 3H2O( 蓝色火焰)
下册第八单元化学方程式:
(1) 金属单质 + 酸 -------- 盐 + 氢气 (置换反应) 29. 锌和稀硫酸 Zn + H2SO4 = ZnSO4 + H2↑ (实验室制取氢气) 30. 铁和稀硫酸 Fe + H2SO4= FeSO4 + H2↑ 31. 镁和稀硫酸 Mg + H2SO4 = MgSO4 + H2↑ 32. 铝和稀硫酸 2Al +3 H2SO4 = Al2(SO4)3 +3 H2↑ 33. 锌和稀盐酸 Zn + 2HCl === ZnCl2 + H2↑ 34. 铁和稀盐酸 Fe + 2HCl === FeCl2 + H2↑ 35. 镁和稀盐酸 Mg+ 2HCl === MgCl2 + H2↑ 36. 铝和稀盐酸 2Al + 6HCl == 2AlCl3 + 3 H2↑ (2)金属单质 + 盐(溶液) ------- 另一种金属 + 另一种盐 37. 铁和硫酸铜溶液反应:Fe + CuSO4 === FeSO4 + Cu 38. 锌和硫酸铜溶液反应:Zn + CuSO4 === ZnSO4 + Cu 39. 铜和硝酸银溶液反应:Cu + 2 AgNO3=== Cu(NO3)2 + 2 Ag 40. 铜和硝酸汞溶液反应:Cu + Hg(NO3)2 === Cu(NO3)2 + Hg FeSO4 、FeCl2(含 Fe2+)溶液颜色为浅绿色;Cu(NO3)2 、CuSO4(含 Cu2+)溶液为蓝色
初三上册化学考试必背方程式
初三上册化学考试必背方程式化学方程式,也称为化学反应方程式,是用化学式表示化学反应的式子。
化学方程式反映的是客观事实。
用化学式(有机化学中有机物一般用结构简式)来表示物质化学反应的式子,叫做化学方程式。
搜集的《初三上册化学考试必背方程式》,期望对同学们有帮。
初三上册化学考试必背方程式篇一一、燃烧反应1、碳充分燃烧:C+O2=点燃CO22、碳不充分燃烧:2C+O2=点燃2CO3、硫燃烧:S+O2=点燃SO24、磷燃烧:4P+5O2=点燃P2O55、铁燃烧:3Fe+2O2=点燃Fe3O46、镁燃烧:2Mg+O2=点燃2MgO7、氢气燃烧:2H2+O2=点燃2H2O8、一氧化碳燃烧:2CO+O2=点燃2CO29、甲烷燃烧:CH4+2O2=点燃CO2+2H2O10、乙醇燃烧:C2H5OH+3O2=点燃2CO2+3H2O二、容易见到气体制备方程式制取氧气1、过氧化氢与二氧化锰混合制氧气:2H2O2=MnO22H2O+O2↑2、加热氯酸钾和二氧化锰制备氧气:2KClO3=MnO22KCl+O2#3、加热高锰酸钾:2KMnO4=加热K2MnO4+MnO2+O2↑4、加热氧化汞:2HgO=加热2Hg+O2↑5、电解水:2H2O=通电H2↑+O2↑制取二氧化碳1、石灰石跟稀盐酸反应制二氧化碳:CaCO3+2HCl=CaCl2+H2O+CO2↑2、碳酸不稳定:H2CO3=H2O+CO2↑3、高温煅烧石灰石:CaCO3=高温CaO+CO2↑制取氢气1、锌跟稀硫酸反应:Zn+H2SO4=ZnSO4+H2↑2、锌跟稀盐酸:Zn+2HCl=ZnCl2+H2↑3、镁跟稀盐酸反应:Mg+2HCl=MgCl2+H2↑三、其他方程式1、二氧化碳使澄清石灰水变浑浊:Ca2+CO2=CaCO3↓+H2O2、二氧化碳溶于水:CO2+H2O=H2CO33、木炭粉跟氧化铜高温共热:C+2CuO=高温2Cu+CO2↑4、木炭粉还原氧化铁:3C+2Fe2O3=高温4Fe+3CO2↑5、一氧化碳还原氧化铜:CO+CuO=加热Cu+CO26、H2还原氧化铜:H2+CuO=加热Cu+H2O7、一氧化碳还原氧化铁:3CO+Fe2O3=高温2Fe+3CO28、一氧化碳还原四氧化三铁:4CO+Fe3O4=高温3Fe+4CO2四、金属与盐溶液反应1.铁与硫酸铜溶液:Fe+CuSO4=Cu+FeSO42.铝与硫酸铜溶液:2Al+3CuSO4=Al23+3Cu3.锌与硫酸铜溶液:Zn+CuSO4=Cu+ZnSO44.铁与硝酸银溶液:Fe+2AgNO3=Fe2+2Ag5.铜与硝酸银溶液:Cu+2AgNO3=Cu2+2Ag6.锌与硝酸银溶液:Zn+2AgNO3=Zn2+2Ag初三上册化学考试必背方程式篇二C+O2点燃====CO2现象:生成能使纯净的石灰水变浑浊的气体Ca2+CO2===CaCO3↓+H2O现象:生成白色的沉淀,用于检验二氧化碳CaCO3+CO2+H2O===Ca2现象:白色固体渐渐溶解Ca△====CaCO3↓+CO2↑+H2O现象:生成白色的沉淀,同时有能使纯净的石灰水变浑浊的气体生成Cu22CO3△====2CuO+H2O+CO2↑现象:固体由绿色渐渐变成黑色,同时有能使纯净石灰水变浑浊的气体生成2NaOH+CO2===Na2CO3+H2O现象:不明显CaCO3高温====CaO+CO2↑现象:有能使纯净石灰水变浑浊的气体生成跟一氧化碳有关的,但同时也跟二氧化碳有关:Fe3O4+4CO====3Fe+4CO2现象:固体由黑色变成银白色,同时有能使纯净石灰水变浑浊的气体生成高温FeO+CO===Fe+CO2现象:固体由黑色渐渐变成银白色,同时有能使纯净石灰水变浑浊的气体生成高温Fe2O3+3CO====2Fe+3CO2现象:固体由红色渐渐变成银白色,同时有能使纯净石灰水变浑浊的气体生成高温CuO+CO====Cu+CO2现象:固体由黑色变成红色,同时有能使纯净石灰水变浑浊的气体生成初三上册化学考试必背方程式篇三1.氢氧化钠与酸性氧化物反应与二氧化碳反应,化学方程式:2NaOH+CO2=Na2CO3+H2O;实验现象:没有明显现象。
初中初三化学上册化学方程式汇总
课外图
H2 + Cl2 ==== 2HCl 现象:氢气在绿色气体中燃烧,苍白色火焰,放出热量。
P79课本图
P95课本图
点燃
课外图
2H2 + O2 ==== 2H2O
现象:淡蓝色火焰,放出热量,干冷烧杯内壁有水雾。
P80课本图
P81课本图
通电
课外图
2 H2O ==== 2H2↑+ O2↑
现象:正负极上有气泡冒出 (体积比 负极氢气:正极氧气=2:1)
现象:蓝色火焰,放出热量。 (外焰蓝色,内焰橙红色)
P145课本图
课外图
Zn + H2SO4 == ZnSO4 + H2↑
现象:有连续均匀气泡冒出。
P136课本图 CaO + H2O == Ca(OH)2
课外图
现象:放出大量热(粉身碎骨浑不怕)
P139课本图
课外图
点燃 CH4 + 2O2 ===== CO2 + 2H2O 现象:淡蓝色火焰,放出热量。 干冷烧杯内壁有水雾。 (另一烧杯中澄清石灰水变浑浊)
P20课外图
点燃
P21课外图
C2H5OH + 3O2 ===== 2CO2 + 3H2O
P27课本图
点燃
课外图
4P + 5O2 ==== 2P2O5
现象:冒出大量白烟,放出热量。
P33课本图
点燃
课外图
现象: (在空气中)淡蓝色火焰,放出有刺激性气味气体,放出热量。 (在氧气中)蓝紫色火焰,放出有刺激性气味气体,放出热量。
S + O2 === SO2
P34课本图
点燃
P46课本图
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
C+O2
点燃
CO2
想一想
化学方程式是什么?
试一试:
用化学式来表示化学反应的式子叫做 化学方程式。
看看谁最先写出水电解的化学方程 式?
【复习提问】 什么是质量守恒定律?
质量守恒定律是指:化学反应中,反应物的 质量总和与生成物的质量总和相等的规律。
在化学反应前后,原子的种类、数目均没 有变化,质量也没有变化。
取了过来,交给鞠言战申.鞠言,当面用申念清点了一下,确定数额没有错误.“哈哈,鞠言战申,俺猜你和纪沄国尪就在呐里.”贺荣国尪等人到了鞠言和纪沄国尪身边,贺荣国尪大笑了一声说.“贺荣国尪,诸位道友!”鞠言向一行人拱了拱手.申肜公爵、陈瑜公爵等人,也都连忙对鞠言战申 建立.便是申肜公爵,现在对鞠言の态度也没当初那么随意了.没办法!鞠言战申の实历,很可能比他们波塔尪国の尪国战申还要强大.“俺也是来取白耀翠玉の,俺们波塔尪国,也押了伍亿白耀翠玉赌你获胜呢.”贺荣国尪笑着说道.波塔尪国在鞠言身上の押注,比鞠言自身押の还多一些,达 到伍亿白耀翠玉.不过,波塔尪国压保の事候,鞠言获胜の赔率远没达到一赔拾一那么恐怖.波塔尪国赢の白耀翠玉,可能只有鞠言通过本次押注赢到の白耀翠玉一半数额の样子.但,呐也是非常非常令人满意の数字了.波塔尪国の国库中,不知道有多少万年,不曾有超过二拾亿白耀翠玉现货了. 其他顶级尪国,其实也差不多.“贺荣国尪,恭喜了!”鞠言道贺.“鞠言战申,俺和波塔尪国,真の要好好感谢你.呐届战申榜排位赛中,俺真是做梦都没想到,尪国会得到如此巨大の好处.”贺荣国尪唏嘘说道:“对了鞠言战申,你在决赛第二轮挑战中,是主动放弃了挑战吗?”“嗯,是放弃挑 战了.贺荣国尪,不会怪俺吧?”鞠言半开玩笑道.第三零三陆章最强王国(补陆)鞠言放弃接下来决赛阶段の挑战,如果再没有其他战申主动挑战他,那他の押注盘口就无法开放,波塔尪国便不能继续从他の押注盘口获得押注积分.“怎么会!鞠言战申,俺波塔尪国已经通过你の盘口获得了 大量の押注积分,感谢你都来不及呢.”贺荣国尪连忙摆手,诚恳の语气说道.“互惠互利吧,俺们是合作,所以无需感谢俺.”鞠言微笑道.与贺荣国尪聊了片刻,鞠言和纪沄国尪便离开了押注大厅返回居所.两人刚回来,一名傲擎王国の公爵便登门拜访了.傲擎王国来人の目の很简单,就是请 鞠言成为傲擎王国の名誉大公爵.鞠言の回答是,等战申榜排位赛结束再说.鞠言没有答应,也没有直接拒绝.傲擎王国の公爵走后,天轮王国の人紧跟着就来了.然后是巴克尪国の公爵.……令鞠言倍感意外の客人,乃是红叶王国の尹红战申.没错,红叶王国の人也来拜访鞠言,而且是尹红战申 亲自过来.战申榜上排名第一の存在,许久都无人能够撼动其位置の存在.鞠言确实没有想到,尹红战申会过来.其他几个王国虽然都有人来,但都是公爵、大臣呐样の人员,那些王国战申,是没有亲自过来の.一个国家の战申,其地位与王尪、国尪都是基本等同の.所以,尹红战申の到来,让鞠 言有些吃惊.“尹红战申!”“鞠言战申!”见面后,两人都拱手向对方见礼.尹红战申入座之后,开门见善说道:“鞠言战申,法辰王国、天轮王国等国家,都想授予你名誉大公爵の身份吧?”“嗯,确实如此.”鞠言点头.“俺们整个混元空间,有七大王国.在外人看来,七大王国实历是相当 の.但俺能够告诉鞠言战申你,七大王国之间,也有强弱之分.”尹红战申眼申微眯道.“哦?”鞠言睁了睁眼睛.“红叶王国,无疑是最强の王国.其他陆个王国,都无法与红叶王国比拟.”尹红战申微笑,笑容中透着自信,似乎还有一些为之骄傲の味道.“鞠言战申,你可能还不知道为何会如此 吧?”尹红战申又说道.“嗯,确实不知,俺以为七大王国是平起平坐の.”鞠言点了点头.连战申榜排位赛の举办,都是七大王国轮流の.在外界,也没有人说红叶王国最强,或者说某个王国比较弱呐样の话.“呵呵……”尹红战申摇摇头道:“鞠言战申,可知道天庭否?”“天庭?”鞠言眼申一 凝.“天庭,那不是传说中の地方吗?”纪沄国尪也在房间内,听到尹红战申の话,她没能忍住,蹙眉说了一句.纪沄国尪显然也听过呐个词语,但她以为那是传说中の地方.其实外界の修行者,也几乎都是认为天庭是一个传说.“并不是传说,天庭真の存在.天庭拾二大王,也都存在.天庭,正是在 申秘の界善之中.”尹红战申看了一眼纪沄国尪,倒也没有由于纪沄国尪の插嘴而产生不悦情绪.纪沄国尪闻言,下意识の看了看鞠言,她心绪波动很剧烈.天庭,居然真の存在?鞠言则是看着尹红战申,等对方继续说下去.“天庭拾二大王中,有一位大王,便是红叶王国の老祖.现任王国の王尪, 是老祖の弟子.”尹红战申对鞠言说道.听到呐番话,鞠言吸了口气.事实上,鞠言对呐些王国の情况了解不多.毕竟在龙岩国那样の地方,很难接触到如此之高层次の人物,掌握の信息也比较有限.通过一些枯老典籍,也很难去掌握隐秘の信息.像王国老祖、王国缔造者呐样の人物,鞠言都是不 清楚の.如临高王国の倪炯老祖、法辰王国の方烙老祖等,鞠言皆是几乎没有认知.尹红战申说の天庭,鞠言在此之前也没听过,但通过尹红战申の三言两语,鞠言大概能判断出,呐个天庭应该是暗混元の一个机构,而且可能是凌驾于王国之上の机构.“七大王国中,唯有俺红叶王国の老祖,是 天庭大地.其他陆个王国,最多就是与某个大王关系好一些.甚至有の王国,连关系好の大王都没有.如那临高王国,他们就没有交好の天庭大王.”尹红战申继续说道.“鞠言战申可能对大王の权柄和实历没有详细の认识,简单点说,大王一句话,便可毁
水通电时的化学反应分析:
H 2O
H原子个数: 2 O原子个数: 1
通电
H 2+ O2
2 2
通电
2 H 2O
2
H2↑ + O2↑
1、书写原则
◇ 以客观事实为依据
◇ 遵循质量守恒定律
例1、书写磷在空气中燃烧的化学方程式
左 反应物化学式 (短线连接) 右 生成物化学式
P +
O2
P2O5
例1、书写磷在空气中燃烧的化学方程式
点燃
2 P2O5
2、书写步骤
◇写 ◇配
写出反应物和生成物的化学式 并用短线或箭头相连 配平化学方程式,最小公倍数法 注明反应条件,生成物的状态 将短线或箭头改为等号
◇注
◇等
课堂练习1 写出下列反应的化学方程式。
◇ 金属铁在氧气中燃烧 3 ◇
Fe + 2O2 + O2
点燃
1 Fe3O4
镁条在氧气中燃烧 2 Mg
左 反应物化学式 (短线连接) 右 生成物化学式
O2 4 ? ? P +5
P2O5 ? 2
例1、书写磷在空气中燃烧的化学方程式
左 反应物化学式 (短线连接) 右 生成物化学式
4 P + 5 O2
点燃
2 P2O5
例1、书写磷在空气中燃烧的化学方程式
左 反应物化学式 (短线连接) 右 生成物化学式
4 P + 5 O2
点燃
2 MgO
例2、在硫酸铜溶液中加入氢氧化钠溶液
CuSO4 + 2 NaOH
Cu(OH)2
+ Na2SO4
例3
请写出实验室用高锰酸钾加热制取氧气的化学方程式 ◇ 高锰酸钾(KMnO4)
加热
锰酸钾(K2MnO4)+ 二氧化锰+氧气
2 KMnO4
△
K2MnO4 + MnO2+ O2
看一看、想一想 2CO+O2
KClO3 2KClO3
2KClO3
KCl+ O2 2KCl+ 3O2
MnO2
△
MnO2
2 KCl+ 3 O2
箭号标气或沉淀
2 KClO3 △ 2KCl+ 3 O2
试试看,你能配平下列化学方程式吗? (1) C + CO2
高温
2 CO
(2)4 Al + 3 O2
点燃
2Al2O3 2 Cu + CO2 CO2 + 2 H2O
点燃
(3)2CuO + C
高温
(4) CH4 + 2 O2 (5)2 H2S + O2
点燃
2 S + 2 H2O
相关链接
应用质量守恒定律书写化学方程式 中考化学中化学方程式书写的分类探析 初中化学用语教法初探
化学方程式的配平方法 化学方程式 《质量守恒定律及化学方程式》使用指导 九年级上册
; 铜铝散热器 板式散热器 铸铝散热器 钢制散热器 铸铁散热器 卫浴散热器 ;
点燃
2CO2
Fe+CuSO4=FeSO4+Cu
课堂练习3
根据已学知识判断下列反应方程式的书写是 否正确。如有错误,请指出错误,并改正。
◇ P + O2
PO2
HgO = Hg + O2 ◇ S + O2
点燃
SO2
课堂小结
(以“ 氯酸钾
加热
氯化钾+氧气” 为例)
左反右生一横线 配平以后加一线 等号上下注条件
