《有机化学反应方程式》书写练习
有机化学反应方程式的书写

2012届高二化学有机复习高二有机化学基本反应方程式书写训练
班级姓名学号成绩1.实验室中以乙醇为原料来制取乙烯:
2.用乙醇为原料来制备乙醛:
3.实验室用CaC2和水制乙炔:
4.用1,2-二氯乙烷为原料来制取乙炔:
5.乙醇和CH3CO18OH在浓硫酸作用下加热制乙酸乙酯:
6.乙醇为原料制备乙醚:
7.CH3CHO发生的银镜反应:
8.2-丙醇的催化氧化反应:
9.甲烷在光照时与氯气发生反应,生成气态有机产物:
10.丙烯使溴的四氯化碳溶液褪色:
11.苯的硝化反应:
12.苯的溴代反应:
13.苯酚的溴代反应:
14.制备酚醛树脂:
15.溴乙烷的水解反应:
16.甘油与硝酸的酯化反应:
17.甲醛与足量的新制的氢氧化铜浊液在加热反应:
18.烃(CxHy)在氧气中完全燃烧:
19.烃的含氧衍生物(CxHyOz)在氧气中完全燃烧:
20.乙醇的分子间脱水反应:
21.环己醇的催化氧化反应:
22.甲酸乙酯的水解反应:
23.向苯酚钠溶液中通入CO2气体:
24.用甲苯制备TNT的反应:
25.乙烯水化法制乙醇:
26.苯酚与金属钠:
27.加热条件下,用乙醇和浓氢溴酸来制备溴乙烷:
28.2-丁烯的加聚反应:
29.乙二酸和乙二醇反应生成环酯:
30.乙二酸和乙二醇反应生成聚酯:。
《有机化学基础》方程式默写

《有机化学基础》化学反应方程式默写总结(一)烷烃1.甲烷燃烧: CH 4 +2O 2CO 2 + 2H 2O2.甲烷与氯气在光照条件下反应: CH 4 + 3Cl 2 CHCl 3+ 3HCl CH 4 + 4Cl 2 CCl 4 + 4HClCH 4 + 2Cl 2CH 2Cl 2 + 2HCl3.甲烷高温分解: CH 4 C + 2H 2(二)烯烃乙烯的制取:CH 3CH 2OH H 2C=CH 2↑+H 2O氧化反应乙烯的燃烧:H 2C=CH 2+3O 2 2CO 2+2H 2O乙烯可以使酸性高锰酸钾溶液褪色,发生氧化反应。
加成反应与加聚反应1.乙烯与溴的四氯化碳溶液反应:CH 2=CH 2 + Br 2 CH 2BrCH 2Br2.乙烯与水反应:CH 2=CH 2 + H 2OCH 3CH 2OH3.乙烯的催化加氢:CH 2=CH 2 +H 2CH 3CH 34.乙烯的加聚反应:n CH 2=CH 2浓硫酸170℃点燃5. 乙烯与氯化氢加成:H2C=CH2+HCl CH3CH2Cl6.乙烯与氯气加成:CH2=CH2 + Cl2 CH2ClCH2Cl7. 1—丁烯与氢气催化加成:CH2=CH2CH2CH3 +H2CH3CH2CH2CH38.环己烯催化加氢:H2 +9. 1,3环己二烯催化加氢:2H2 +10. 1,3-丁二烯与溴在温度较低和较高时的反应:CH2=CH—CH=CH2+Br2 CH2BrCH=CHCH2BrCH2=CH—CH=CH2+Br2CH2BrCHBrCH=CH211. 1,1—二氯乙烯加聚:n CCl2=CH212.丙烯加聚:n H2C=CHCH313. 2—甲基—1,3—丁二烯加聚:n(三)炔烃乙炔的制取:CaC2+2H2O CH≡CH↑+Ca(OH)21.乙炔燃烧: 2C2H2 + 5O24CO2 + 2H2O2.乙炔与足量溴的四氯化碳溶液反应:CH≡CH + Br2 CHBr2CHBr23.乙炔与氢气催化加成:CH≡CH + 2H2 CH3CH34.乙炔制聚氯乙烯: CH≡CH +HCl H 2C =CHCl n H 2C =CHCl(四)芳香烃1.苯的燃烧: 2C 6H 6+15O 2 12CO 2 + 6H 2O2.苯的催化加氢:+ 3H 23.苯与液溴催化反应: + Br 2 + HBr4.苯的硝化反应: +HO -NO 2 + H 2O9.苯乙烯与溴的四氯化碳溶液反应:+Br 210.甲苯与浓硝酸、浓硫酸的混合酸1000C 时获得三硝基甲苯:+ 3HO —NO 2 + 3H 2O11、甲苯与氢气加成12、甲苯与Cl2在光照条件下发生取代反应+3H 2催化剂△CH 3 |—CH 313、甲苯与液溴在溴化铁作用下发生取代反应(六)、卤代烃1.氯乙烷在氢氧化钠水溶液中加热反应:CH3CH2Br + NaOH CH3CH2OH + NaBr2.氯乙烷在氢氧化钠醇溶液中加热反应:CH3CH2Br +NaOH CH2=CH2↑+ NaBr + H2O3. 1—溴丙烷与氢氧化钾醇溶液共热:CH3CH2 CH2Br +KOH CH3CH=CH2↑ + KBr + H2O4. 2—氯丙烷与氢氧化钠水溶液共热:CH3CHClCH3 +NaOH CH3CH(OH)CH3+ NaCl5. 2—甲基—2—溴丁烷消去溴化氢:(七)、醇类1.乙醇与钠反应:2CH3CH2OH + 2Na 2CH3CH2ONa + H2↑2.乙醇的燃烧:CH3CH2OH+3O22CO2+3H2O3.乙醇的催化氧化:2CH3CH2OH + O2 2CH3CHO + 2H2O4.乙醇消去反应制乙烯:CH3CH2OH CH2=CH2↑ + H2O5.乙醇分子间脱水制乙醚:2CH3CH2OH CH3CH2OCH2CH3 + H2O (取代反应)6.乙醇与红热的氧化铜反应:CH3CH2OH+CuO CH3CHO+H2O7.乙醇和浓的氢溴酸加热反应制溴乙烷:C2H5OH+ HBr C2H5Br + H2O(八)、酚类(能和FeCl3溶液反应,使溶液呈紫色)1.苯酚与氢氧化钠反应:+ NaOH + H2O2.苯酚钠与CO2反应:—ONa —OH+CO2+H2O +NaHCO33.苯酚与浓溴水反应:+3Br2↓ + 3HBr(九)、醛类1.乙醛的催化加氢:CH3CHO + H2CH3CH2OH(加成反应,还原反应)2.乙醛的催化氧化:2CH3CHO + O22CH3COOH3.银氨溶液的配制:NHAg++NH3·H2O===AgOH↓++4AgOH+2NH3·H2O===[Ag(NH3)2]++OH-+2H2O4.乙醛与银氨溶液反应: CH 3CHO + 2Ag(NH 3)2OH CH 3COONH 4 + 2Ag↓ + 3NH 3 + H 2O5.乙醛与新制氢氧化铜反应: CH 3CHO + 2Cu(OH)2 +NaOHCH 3COONa + Cu 2O↓ + 3H 2O或CH 3CHO+2Cu(OH)2 CH 3COOH+Cu 2O ↓+2H 2O6、甲醛与苯酚反应制酚醛树脂: 甲醛与苯酚反应:n HCHO + n — + 2n H 2O (缩聚反应)(十)、羧酸1.乙酸与乙醇发生酯化反应:CH 3COOH + CH 3CH 2OH CH 3COOCH 2CH 3 + H 2O2.乙酸与碳酸钠反应:2CH 3COOH+Na 2CO 3 2CH 3COONa+H 2O+CO 2↑3.乙酸与碳酸氢钠反应:CH 3COOH+NaHCO 3 CH 3COONa+H 2O+CO 2↑4.两分子乳酸 CH 3CH (OH )COOH 发生酯化反应脱去两分子水形成六元环:2CH 3CHOHCOOH5、乳酸发生缩聚反应形成高分子△—OH 催化剂 △OH —CH 2— | n] [ 浓硫酸△6、乙二醇和对苯二甲酸发生缩聚反应形成高分子化合物:7.甲酸与银氨溶液反应:HCOOH+2Ag(NH3)2OH (NH4)2 CO 3+ 2Ag↓ + 3NH3 + H2O8.甲酸与新制氢氧化铜反应:HCOOH+2Cu(OH)2 +2NaOH Na2 CO3+ Cu2O↓ + 3H2O(十一)、酯类1.乙酸乙酯与H218O混合加入稀硫酸水解:稀硫酸CH3COOCH2CH3 + H218O CH3CO18OH + CH3CH2OH2.乙酸乙酯碱性水解CH3COOC2H5+NaOH CH3COONa+C2H5OH(十二)、糖类1、葡萄糖结构:CH2OH—CHOH—CHOH—CHOH—CHOH—CHO2.葡萄糖燃烧:C6H12O6 + 6O26CO2 + 6H2O3.葡萄糖与银氨溶液反应:CH2OH(CHOH)4CHO + 2Ag(NH3)2OH CH2OH(CHOH)4COONH4+ 2Ag↓ + 3NH3↑ + H2O4.葡萄糖与新制氢氧化铜反应:CH2OH(CHOH)4CHO + 2Cu(OH)2 +NaOH CH2OH(CHOH)4COONa + Cu2O↓ + 3H2O5.葡萄糖被还原为直链己六醇:CH2OH(CHOH)4 CHO + H2CH2OH(CHOH)4CH2OH6.葡萄糖在酒化酶作用下获得乙醇:C6H12O62CH3CH2OH + 2CO2↑7.蔗糖水解:C12H22O11(蔗糖) + H2O C6H12O6(葡萄糖) + C6H12O6(果糖)8.麦芽糖水解:C12H22O11(麦芽糖) + H2O 2C6H12O6(葡萄糖)注意:蔗糖不含醛基,不可以发生银镜反应;麦芽糖可以发生银镜反应。
2014福建化学会考有机反应方程式书写题

(福建会考·2013)(2)乙烯能使溴水褪色,生成1,2—二溴乙烷(CH2Br—CH2Br)。
写出该反应的化学方程式:。
(福建会考·2012)(2)2011年12月16日,印度发生假酒中毒事件,导致200多人伤亡。
假酒中的有毒物质是甲醇(CH3OH),它是一种理想燃料。
写出在CH3OH空气中燃烧的化学方程式:。
(福建会考·2011)(1)“可燃冰”是天然气的水合物,外形似冰,它的主要可燃成分是甲烷,写出甲烷燃烧的化学方程式:。
(福建会考·2010)(2)CH4与Cl2在光照条件下能生成CH3Cl,写出该反应的化学方程式:。
(福建会考·2009)(2)炒菜时,经常加入少量的料酒(含乙醇)和醋,可使菜变得香醇可口,请用化学方程式表示该反应的原理:。
(福建会考·2008)(2)聚氯乙烯( )有毒,不能用于制作食品保鲜袋。
由氯乙烯通过加聚反应获得聚氯乙烯的化学方程式为:。
高中经典有机化学反应方程式

章末回顾排查专练(十二)排查一、重要有机反应方程式再书写1.2.2C 2H 5OH +2Na →2C 2H 5ONa +H 2↑; 3.CH 3CH 2OH ―――――――――→浓H 2SO 4170 ℃CH 2===CH 2↑+H 2O ; 4.C 2H 5OH +HBr ――→△ C 2H 5Br +H 2O ;5.2C 2H 5OH +O 2―――――――――→Cu 或Ag △2CH 3CHO +2H 2O ;9.2CH 3CHO +O 2―――――――――→催化剂△2CH 3COOH ; 10.CH 3CHO +H 2――――――――――→催化剂△CH 3CH 2OH ; 11.CH 3CHO +2Ag(NH 3)2OH ――→△ CH 3COONH 4+2Ag ↓+3NH 3+H 2O ;12.CH 3CHO +2Cu(OH)2――→△ CH 3COOH +Cu 2O ↓+2H 2O ;13.CH 3COOH +C 2H 5OH 浓H 2SO 4△CH 3COOC 2H 5+H 2O ;14.CH 3COOC 2H 5+H 2O 稀H 2SO 4△CH 3COOH +C 2H 5OH ;15.乙二醇和乙二酸生成聚酯16.排查二、常考易错再排查 1.按碳原子组成的分子骨架分,有机物可分为链状化合物和环状化合物,环状化合物又包括脂环化合物和芳香族化合物。
按官能团分,有机物可分为烃(烷烃、烯烃、炔烃、芳香烃)和烃的衍生物(卤代烃、醇、酚、醛、酸、酯等)。
( )2.具有相同分子式,不同结构的化合物互为同分异构体。
包括碳链异构(如CH 3CH 2CH 2CH 3与)、位置异构(如CH 3CH===CHCH 3与CH 3CH 2CH===CH 2)、官能团异构(如CH 3CH 2OH 与CH 3OCH 3)、顺反异构(顺2-丁烯与反2-丁烯)、手性异构等。
( )3.发生加成反应或加聚反应的有机物分子必须含有不饱和键。
高考化学陌生方程式的书写练习题(含答案)

高考化学陌生方程式的书写练习题(含答案)1.利用石灰乳和硝酸尾气中的NO、NO2反应可以净化尾气同时获得Ca(NO2)2,但在生产中溶液需要保持弱碱性,因为在酸性溶液中Ca(NO2)2会分解,其中产生的一个产物是NO。
该反应的离子方程式为:Ca(OH)2 + 2NO → Ca(NO2)2 + H2O2.生产硫化钠通常采用无水芒硝(Na2SO4)-碳粉还原法,煅烧所得气体中 CO 和 CO2 的量相等。
该反应的化学方程式为:Na2SO4 + 2C → Na2S + 2CO2 + SO23.向含碘废液中加入稍过量的Na2SO3溶液可以将废液中的I2还原为I-。
该反应的离子方程式为:2Na2SO3 + I2 → 2NaI + Na2S2O64.向含Cr2O7的酸性废水中加入FeSO4溶液可以使Cr2O7全部转化为Cr3+。
该反应的离子方程式为:FeSO4 + Cr2O7^2- + H2SO4 → Fe2(SO4)3 + Cr2(SO4)3 +H2O5.当温度高于200℃时,硝酸铝会完全分解成氧化铝和两种气体,其体积比为4:1.该反应的化学方程式为:4Al(NO3)3 → 4A l2O3 + 12NO2 + O26.(1) AgNO3在光照下会分解生成Ag和红棕色气体,其光照分解反应的化学方程式为:2AgNO3 + hv → 2Ag + 2NO2 + O22) 以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。
该反应的化学方程式为:2H2O → 2H2 + O23) 当用CaSO3水悬浮液吸收经O3预处理的烟气时,清液(pH约为8)中的SO3将NO2转化为NO。
该反应的离子方程式为:2NO2 + CaSO3 + H2O → 2NO + CaSO4·2H2O4) CuSO4溶液能用作P4中毒的解毒剂,反应可生成P的最高价含氧酸和铜。
该反应的化学方程式为:2CuSO4 + P4 → 2Cu + P4O10 + 2SO25) 工业制法中,将白磷与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应。
2022年高考化学有机转化关系及反应方程式书写
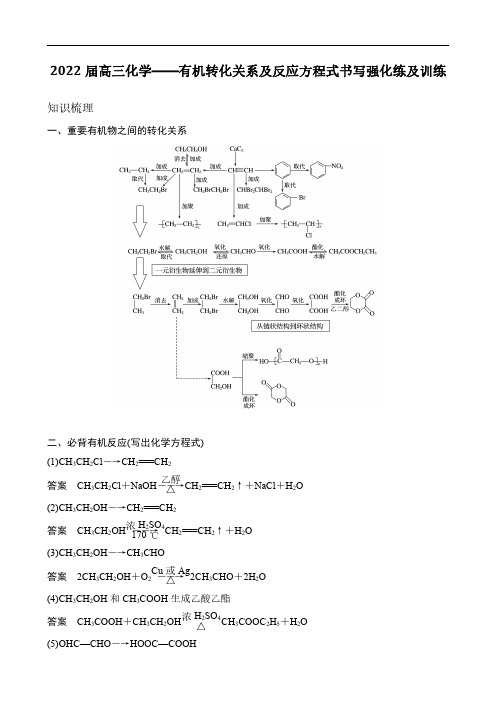
2022届高三化学——有机转化关系及反应方程式书写强化练及训练知识梳理一、重要有机物之间的转化关系二、必背有机反应(写出化学方程式)(1)CH 3CH 2Cl ―→CH 2===CH 2答案CH 3CH 2Cl +NaOH ――→乙醇△CH 2===CH 2↑+NaCl +H 2O(2)CH 3CH 2OH ―→CH 2===CH 2答案CH 3CH 2OH ――→浓H 2SO 4170℃CH 2===CH 2↑+H 2O (3)CH 3CH 2OH ―→CH 3CHO 答案2CH 3CH 2OH +O 2――→Cu 或Ag △2CH 3CHO +2H 2O(4)CH 3CH 2OH 和CH 3COOH 生成乙酸乙酯答案CH 3COOH +CH 3CH 2OH浓H 2SO 4△CH 3COOC 2H 5+H 2O (5)OHC—CHO ―→HOOC—COOH答案OHC—CHO +O 2――→催化剂△HOOC—COOH(6)乙二醇和乙二酸生成聚酯答案n HOCH 2—CH 2OH +n HOOC—COOH――→一定条件+(2n -1)H 2O (7)乙醛和银氨溶液的反应答案CH 3CHO +2Ag(NH 3)2OH ――→△CH 3COONH 4+2Ag ↓+3NH 3+H 2O(8)乙醛和新制Cu(OH)2悬浊液的反应答案CH 3CHO +2Cu(OH)2+NaOH ――→△CH 3COONa +Cu 2O ↓+3H 2O(9)答案(10)答案(11)和饱和溴水的反应答案(12)和溴蒸气(光照)的反应答案(13)和HCHO 的反应答案+(n -1)H 2O(14)酯在碱性条件的水解(以乙酸乙酯在NaOH 溶液中为例)答案CH 3COOC 2H 5+NaOH ――→△CH 3COONa +C 2H 5OH (15)和NaOH 的反应三、常考有机物的检验1.卤代烃中卤素的检验取样,滴入NaOH 溶液,加热至分层现象消失,冷却后加入稀硝酸酸化,再滴入AgNO 3溶液,观察沉淀的颜色,确定是何种卤素。
人教版(2019)高中化学选择性必修3:有机化学基础方程式练习题(含答案)

人教版(2019)高中化学选择性必修3:有机化学基础方程式练习题一、烷烃通式:C n H2n+21.氧化反应(1)甲烷的燃烧:2. 取代反应(1)甲烷和氯气在光照条件下发生取代反应(一氯取代)二、烯烃通式:C n H2n官能团名称:碳碳双键1. 加成反应(1)乙烯与溴水(Br2的CCl4溶液)加成:(2)乙烯与氢气加成:(3)乙烯与水加成:(4)丙烯与HBr加成:(5)1,3-丁二烯与Br2发生1,2-加成,1,4-加成:(6)1,3-丁二烯与乙烯发生环加成反应:2. 加聚反应(1)乙烯发生加聚反应生成聚乙烯:(2)丙烯发生加聚反应生成聚丙烯:3. 乙烯的制取(1)溴乙烷发生消去反应:(2)乙醇发生消去反应:三、炔烃通式:C n H2n-2 官能团名称:碳碳三键1. 乙炔的制取:2. 加成反应(1)乙炔与溴水(Br2的CCl4溶液)完全加成:(2)乙炔与HCl加成得到氯乙烯:四、苯和甲苯通式:C n H2n-61. 取代反应(1)苯和液溴发生取代反应:(2)苯和浓硝酸发生取代反应:(3)甲苯和浓硝酸发生取代反应:(4)甲苯和甲苯与氯气在光照条件下发生取代反应(一氯取代):(5)甲苯与氯气在FeCl3催化下发生对位取代反应:注意:甲苯在光照条件下发生侧链的取代,在催化剂条件下发生苯环上的取代。
2. 加成反应(1)苯和氢气发生加成反应:五、卤代烃(溴乙烷)官能团名称:卤素原子1. 水解反应(取代反应)(1)溴乙烷与氢氧化钠水溶液反应:2. 消去反应(2)溴乙烷与氢氧化钠醇溶液反应:1. 置换反应(1)乙醇与钠反应:2. 氧化反应(1)乙醇燃烧:(2)催化氧化①乙醇在铜或银催化下与氧气反应:②1-丙醇在铜或银催化下与氧气反应:③2-丙醇在铜或银催化下与氧气反应:3. 消去反应(1)乙醇发生消去反应:4. 取代反应(1)乙醇生成乙醚:(2)乙醇与浓氢溴酸反应生成溴乙烷:(3)乙醇与乙酸发生酯化反应生成乙酸乙酯:七、苯酚官能团名称:羟基1. 弱酸性(1)苯酚与氢氧化钠溶液反应:(2)往苯酚钠溶液中通入CO2气体:(3)苯酚与碳酸钠溶液反应:2. 取代反应(1)苯酚与浓溴水反应:3. 显色反应(1)苯酚能和FeCl3溶液反应,使溶液呈紫色。
有机化学方程式练习

有机化学方程式练习班级姓名座号1. 2-氯丙烷与氢氧化钠的醇溶液共热2-氯丙烷与氢氧化钠的水溶液共热2. 1-丁醇发生下列反应(1)与Na反应(2)与Mg反应(3)与CuO反应(4)在银催化下被氧气氧化(5)与浓硫酸混合共热至170℃3. 2 -丁醇发生下列反应(1)与Mg反应(2)与CuO反应(3)在银催化下被氧气氧化(4)与浓硫酸混合共热至140℃4.苯酚发生下列反应(1)与钠反应(2)与氢氧化钠反应(3)与浓溴水反应5.苯酚钠发生下列反应(1)水解(2)CO2(3)醋酸6.乙醛发生下列反应(1)H2(2)O2(3)氢氧化铜悬浊液(4)银氨溶液7.乙酸发生下列反应(1)NaHCO3(2)Cu(OH)2(3)CaO(4)甲醇(5)2-丙醇(6)乙二醇(7)3-甲基-2-戊醇8.下列酯与稀硫酸共热(1)乙酸乙酯(2)甲酸丁酯(3)苯甲酸甲酯9.下列酯与氢氧化钠溶液共热(1)乙酸丙酯(2)甲酸苯甲酯(3)丙烯酸异丙酯10.完全下列转化过程的化学方程式(1)乙烯→乙酸乙酯(2)溴乙烷→乙二醇(3)乙醇→(4)乙醛→乙烷11.写出下面物质分别与足量的钠、氢氧化钠、碳酸氢钠反应的化学方程式。
12.写出下列两物质分别与足量氢氧化钠反应的化学方程式。
(1)(2)12.写出制备下列物质的化学反应方程式:(1)溴苯(2)硝基苯(3)苯磺酸(4)TNT(5)用电石、食盐水等物质置备聚氯乙烯13.葡萄糖跟下列物质反应(1)氢气(2)银氨溶液(3)新制氢氧化铜14.丙氨酸与下列物质反应(1)NaOH(2)HCl(3)跟甘氨酸形成二肽。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
《有机化学反应方程式》书写练习
一、取代反应
1.卤代反应
(1)4与2在光照下反应:。
(2)苯、液溴在铁屑催化下反应:。
(3)苯酚溶液中加入过量浓溴水:。
2.硝化反应
(1)由苯制硝基苯:。
(2)由甲苯制:。
3.磺化反应
由苯和浓硫酸共热制苯磺酸:。
4.醇与氢卤酸共热下反应
例如:乙醇与氢溴酸反应:。
5.醇分子间脱水成醚
例如:由乙醇制乙醚:。
6.卤代烃的水解
例如:溴乙烷与溶液共热:。
7.酯的水解
(1)乙酸乙酯与稀H24共热:。
(2)乙酸乙酯与溶液共热:。
8.酯化反应
(1)乙酸与乙醇在浓硫酸下共热制乙酸乙酯:。
(2)苯甲酸、甲醇、浓硫酸三者混合后共热:。
二、加成反应
1.烯烃的加成
(1)C2H4加成H2:。
(2)C2H4加H2O:。
(3)C2H4通入溴水中:;现象为:。
2.炔烃的加成
(1)C2H2与足量H2加成:。
(2)C2H2通入溴水中:。
(3)C2H2水化法制乙醛:。
(4)C2H2与制氯乙烯:。
3.芳香烃的加H2
例如:苯加成H2:。
4.乙醛加成氢气:。
5.丙酮(33)加成氢气:。
6.油脂的硬化(或氢化):。
三、消去反应
1.部分卤代烃的消去反应
结构要求为:;条件为:。
例如:溴乙烷、乙醇、三者混合共热:。
2.部分醇的消去反应
结构要求为:;条件为:。
例如:(1)由乙醇制乙烯:。
(2)符合分子组成为C7H15、不能发生消去反应的物质有种,其结构简式为:。
四、氧化反应
1.有机物的燃烧反应
(1)烃()完全燃烧的通式为:。
①天然气的完全燃烧:。
②乙烯完全燃烧:;现象为:。
③乙炔完全燃烧:;现象为:。
④苯完全燃烧:;现象为:。
(2)含氧衍生物()完全燃烧的通式为:。
例如:酒精作燃料完全燃烧:。
葡萄糖的生理氧化:。
2.得氧或失氢方式的氧化反应
(1)乙烯氧化法制乙醛:。
(2)由乙醇制乙醛:。
(3)乙醛发生银镜反应:。
(4)乙醛与新制氢氧化铜悬浊液共热:。
(5)乙醛与氧气的催化氧化:。
(6)葡萄糖发生银镜反应:。
(7)葡萄糖与新制氢氧化铜悬浊液共热:。
(8)由乙二醇制乙二醛:。
(9)由乙二醛制乙二酸:。
(10)由苯甲醇制苯甲醛:。
五、还原反应
1.加成H2
注意:能加氢的几类结构。
*2.硝基苯、铁粉、盐酸三者混合可制苯胺:。
六、水解反应
1.卤代烃的水解
例如:1,2 ―二溴乙烷的水解反应:。
2.酯的水解反应
(1)阿斯匹林与溶液共热:。
(2)化合物与溶液共热:。
(3)硬脂酸甘油酯在稀硫酸催化下的水解反应:。
(4)硬脂酸甘油酯在溶液中的水解反应:。
3.二糖、多糖与蛋白质的水解反应
(1)蔗糖的水解反应:。
(2)淀粉的水解反应:。
(3)纤维素的水解反应:。
七、酯化反应
1.由乙酸与乙二醇制二乙酸乙二酯:。
2.由甘油与硝酸制三硝酸甘油酯:。
3.乙二醇与乙二酸发生完全酯化反应制乙二酸乙二酯:。
4.由乳酸(3)制C6H10O5的酯化反应:。
5.由乳酸(3)制环酯(C6H8O4)的酯化反应:。
6.由乳酸(3)制聚乳酸:。
7.乙二酸与乙二醇酯化生成聚酯:。
8.对苯二甲酸与乙二醇制聚酯:。
9.由纤维素制硝酸纤维:。
八、加聚与缩聚反应
1.由乙烯制聚乙烯:。
2.由氯乙烯制聚氯乙烯:。
3.苯酚与甲醛反应制酚醛树脂:。
4.由甲醛制“人造象牙”:。
53() + 22→+ H2O
6.甲基丙烯酸甲酯的加聚反应:。
7.2―甲基―1,3―丁二烯的加聚反应:。
8.乙炔的加聚反应为:。
九、其它有机反应
1.由电石与饱和食盐水作用制乙炔:。
2.钠与乙醇的置换反应:。
3.苯酚与溶液反应的化学方程式为:;离
子方程式为:。
4.苯酚钠溶液中通入少量2的化学方程式为:;
离子方程式为:。
5.乙酸与氢氧化铜反应:。
6.乙酸与碳酸氢钠溶液反应的离子方程式为:;少量乙酸滴入碳酸钠溶液中的离子方程式为:。
