物理化学相平衡资料
物理化学相平衡知识点

物理化学相平衡知识点相平衡一、主要概念组分数,自由度,相图,相点,露点,泡点,共熔点,(连)结线,三相线,步冷(冷却)曲线,低共熔混合物(固相完全不互溶)二、重要定律与公式本章主要要求掌握相律的使用条件和应用,单组分和双组分系统的各类典型相图特征、绘制方法和应用,利用杠杆规则进行有关计算。
1、相律: F = C - P + n, 其中:C=S-R-R’(1) 强度因素T,p可变时n=2(2) 对单组分系统:C=1, F=3-P(3) 对双组分系统:C=2,F=4-P;应用于平面相图时恒温或恒压,F=3-P。
2、相图(1)相图:相态与T,p,x的关系图,通常将有关的相变点联结而成。
(2)实验方法:实验主要是测定系统的相变点。
常用如下四种方法得到。
12对于气液平衡系统,常用方法蒸气压法和沸点法;液固(凝聚)系统,通常用热分析法和溶解度法。
3、单组分系统的典型相图对于单组分系统C =1,F =C -P +2=3-P 。
当相数P =1时,自由度数F =2最大,即为双变量系统,通常绘制蒸气压-温度(p-T )相图,见下图。
pTlBC AOsgC 'pTlBCA Os gFGD单斜硫pT液体硫BCAO正交硫硫蒸气(a) 正常相图 (b) 水的相图(c) 硫的相图图6-1 常见的单组分系统相图4、二组分系统的相图类型:恒压的t -x (y )和恒温的p -x (y )相图。
相态:气液相图和液-固(凝聚系统)相图。
(1)气液相图根据液态的互溶性分为完全互溶(细分为形3成理想混合物、最大正偏差和最大负偏差)、部分互溶(细分为有一低共溶点和有一转变温度的系统)和完全不溶(溶液完全分层)的相图。
可以作恒温下的p -x (压力-组成)图或恒压下的t -x (温度-组成)图,见图5-2和图5-3。
t = 常数液相线气相线g + llgB Apx B (y B )t = 常数g + l液相线气相线g + llgB Apx B (y B )g + lg + lt = 常数液相线气相线lgBApx B (y B )(a) 理想混合物 (b) 最大负偏差的混合物 (c) 最大正偏差的混合物 图6-2 二组分系统恒温下的典型气液p -x 相图p = 常数液相线或泡点线气相线或露点线g + llgBAtx B (y B )p = 常数g + l液相线或泡点线气相线或露点线g + llg BAtx B (y B )g + lp = 常数液相线或泡点线气相线或露点线g + llgBAtx B (y B )(a) 理想或偏差不大的混合物 (b) 具有最高恒沸点(大负偏差) (c) 具有最低恒沸点(大正偏差)B在A液层中的溶解度线A在B液层中的溶解度线最高会溶点l 1 + l 2p = 常数lBAtx B最低会溶点B在A液层中的溶解度线A在B液层中的溶解度线最高会溶点l 1 + l 2p = 常数lBAtx B DCGFOgg + l g + ll 1 + l 2p = 常数lBAtx B (y B )(d) 有最高会溶点的部分互溶系统 (e)有最高和最低会溶点的部分互溶系统 (f) 沸点与会溶点分离4x B (y B )三相线COD ( l 1 +g + l 2)l 1DC GFOgg + lg + l l 1 + l 2p = 常数l 2B Atx B (y B )三相线COD ( g + l 1 + l 2)g + l 1l 1DC GFOgg + l 2l 1 + l 2p = 常数l 2BAtg + B(l )三相线COD [ A(l ) +g + B(l ) ]DCGFOgg + A(l )A(l ) + B( l )p = 常数BAtx B (y B )(g) 液相部分互溶的典型系统 (h)液相有转沸点的部分互溶系统 (i) 液相完全不互溶的系统图6-3 二组分系统恒压下的典型气液相图(2)液-固系统相图: 通常忽略压力的影响而只考虑t -x 图。
物理化学 第五章 相平衡

一、基本概念和公式 (一)几个基本概念 1. 相和相数 (1)相 (phase) 系统内部物理和化学性质完全均匀的部分称为相。 特点 相与相之间在指定条件下有明显的界面, 在界面上宏观性质的改变是飞跃式的。 (2)相数 (number of phase) 系统中相的总数称为相数,用 表示。 气体:
(三)二组分系统的相图及应用
(3) 同时具有最高、最低会溶温度 (4) 不具有会溶温度
(三)二组分系统的相图及应用
4. 不互溶双液系 (1) 特点 如果A,B 两种液体彼此互溶程度极小,以致可忽略 不计。则A与B共存时,各组分的蒸气压与单独存在时一 样,液面上的总蒸气压等于两纯组分饱和蒸气压之和。 * * 即: p pA pB 当两种液体共存时,不管其相对数量如何,其 总蒸气压恒大于任一组分的蒸气压,而沸点则恒低 于任一组分的沸点。 (2) 水蒸气蒸馏
CaF2 ( A)
0 .6
0 .8
1 .0 CaCl2 ( B)
(三)二组分系统的相图及应用
(3) 相合熔点 A和B形成的化合物有确定的熔点,完全熔化时不 分解,在熔点时液相和固相的组成相同,所以稳定化 合物的熔点称为相合熔点。 (4) 不相合熔点 因为C没有自己的熔点,将C加热,到O点温 度时分解成 CaF2 (s) 和组成为B的熔液,所以将O点 的温度称为转熔温度(peritectic temperature)也 叫异成分熔点或不相合熔点。
(四)三组分系统的相图及其应用
(d) 如果代表两个三个组分 系统的D点和E点,混合成新 系统的物系点O必定落在DE 连线上。哪个物系含量多, O点就靠近哪个物系点。 O点的位置可用 杠杆规则求算。
mD OD mE OE
物理化学(第三版)第4章相平衡

R=1 NH4HCO3(s) ƒ NH3(g) CO2 (g) H2O(g) R'=2 p(NH3)=p(CO2)
p(NH3)=p(H2O) p(CO2)=p(H2O) C=4-1-2=1
练习 : ⑴ 将PCl3(g)和Cl2(g)放在一真空容器中,达平衡后, C=?
答:容器内有PCl5(g)=PCl3(g)+Cl2(g) S=3,R=1,R’=0,C=3– 1– 0=2。
冰水混合物 P=2
PCl5 (g) ƒ PCl3(g) Cl2 (g) P=1
CaCO3(s) ƒ CaO(s) CO2 (g)
P=3
NH4Cl(s) ƒ NH3(g) HCl(g)
P=2
水、冰和水蒸气组成的系统
P=3
2. 物种数(S)和组分数(C)
(1)物种数 系统中所包含的化学物质的种类数。用S表示 例如, 系统中含有PCl3、PCl5、和Cl2三种物质 S=3
均匀混合
P=1
分为两层
P=2
分为三层
P=3
液体:P=1,2, 3 (视其互溶程度而定)
(3)固体 P=1,2,…
固溶体(固体溶液): P =1
铈锆固溶体
碳化钛-碳化钨固溶体粉末
固体:除固溶体之外,有几种物质就有几相 P=1,2…
注意:相数与数量无关,与破碎程度无关。 P =1
相和相数(P)
气体:P=1 无论包括多少中气体都是一相 液体:P=1,2, 3 (视其互溶程度而定) 固体:P=1,2,…,有几种物质就有几相(固溶体除外)
C(s)
1 2
O2
(
g)
ƒ
CO( g )
⑴
C(s) O2 (g) ƒ CO2 (g)
物理化学:相平衡

相平衡是热力学在化学领域中的重要应用之一。研究 多相体系的平衡在化学、化工的科研和生产中有重要的 意义,例如:溶化、蒸馏、重结晶、萃取、提纯及金相 分析等方面都要用到相平衡的知识。
一、基本概念
第一节 相律
1、 相(phase) 体系内部物理和化学性质完全均匀的 部分称为相。相与相之间在指定条件下有明显的界面, 在界面上宏观性质的改变是飞跃式的。体系中相的总数 称为相数,用Φ表示。
三、自由度数(f)
自由度: 确定平衡体系的状态所必须的独立强度变量的
数目称为自由度,用字母 f 表示。这些强度变量通常是
压力、温度和浓度等。
以水为例〔注意是商量平衡态〕∶ a. 当φ=1时,例如液态水的T、p可在肯定范围内改变, φ不变 ∴ f=2 b. 当φ=2时,例如气-液平衡,指定p外,则Tb确定; 而指定T,则水有确定的平衡蒸气压p,∴ f=1 c. 当φ=3时,即气-液-固三相平衡共存时〔三相点〕,T、 p是确定的〔273.16K、6.1×102Pa、由水的性质所决定〕, ∴ f=0,如果变化T或p,则不可能三相共存〔即φ≠3〕。
一、水的相图 水的相图是依据实验绘制的。图上有:
水 的 相 图
(1) 气、液、固单相区∶f=1-1+2=2
(2) 两相平衡线∶
f=1-2+2=1
OC线∶气-液平衡
T与液态水的饱和蒸气压p蒸气的关系
或沸点Tb与p外的关系
OA线∶液-固平衡 凝固点Tf与p外的关系
OB线∶气-固平衡
T与冰的饱和蒸气压p蒸气的关系
dp/dT=ΔHm / T·ΔVm 此方程适合于任何纯物质的两相平衡
2、对于气-液或气-固两相平衡体系 近似处理∶a. 假设蒸气遵守理想气体状态方程
物理化学6相平衡资料
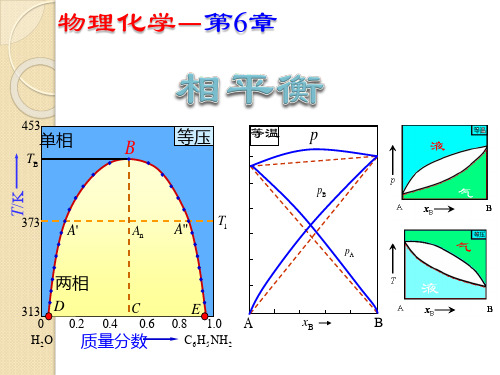
水的相图
p / Pa
C
水f
A
冰
P
610.62 D O
q
B
水蒸气
OC 是液-固两相平衡线
273.16
TC T / K
• OC线不能任意延长:当C点延长至压力大于2.07×108Pa时, 相图变得复杂,有不同结构的冰生成。
OA,OB,OC线 p / Pa 的斜率都可以用克-
E
超 临
C
水
界 水
F
A
f
克方程或克拉佩龙方
例如:对于没有气相存在的凝聚系统,可以忽略压力
f * f 1
多相系统平衡的一般条件――吉布斯相律
对具有 个相系统的热力学平衡,实际上包
含了如下四个平衡: (1) 热平衡
(2) 力学平衡 (3) 相平衡
(4) 化学平衡
某平衡系统中有 S 种不同的化学物种,有 个
相,需要多少独立强度变量(f)才能确定系统的状 态?
物种数(S):系统中存在的化学物种数。 组分数(K):构成平衡系统所需的最少物种数。
K=S- R- R′
R表示独立的化学反应数, R′表示独立的浓度限 制条件数。物质在不同相之间保持一定的数量关 系,不能算作浓度限制条件。
平衡系统 NH4Cl (s) =NH3 (g) + HCl (g)中, S = 3, R = 1, R′= 1,K=1
K=S- R- R′=5- 0- 1=4
若考虑可能析出固体,以K+、Na+、 SO42-、NO3-、H2O和K2SO4、Na2SO4、 KNO3、NaNO3为对象 S=9 R=4,4个独立的化学平衡 R′=1,溶液保持电中性
K=S- R- R′=9- 4- 1=4
物理化学之相平衡
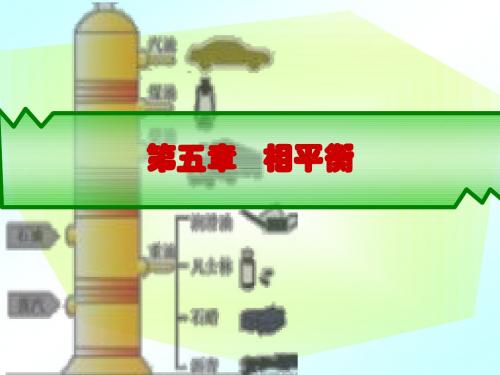
通过升华从冻结的样品中除去水份的方法。
E
f=2
B
冰
水
f=2 A
C
气
D
f=2
s+g, f=1,冷冻干燥
T
一、单组分系统的相图
f f=K- +2 水的相图
E
B
冰
水
p
610.6Pa
A:三相点
C
A
气
f=0
D
T
0.0098℃
一、单组分系统的相图
f=K-f+2 水的三相点:水的气、液、固三相平衡点。 f=0,T=273.16K ( 0.01℃),p=610.6Pa 水的凝固点(冰点):水的液、固二相平衡点。
↑
l+g, f=1
l+g, f=1 TB
l, f=2
T
A
xB →
B
T
二、杠杆规则
TA
↑
f f=K- +2 g, f=2
l+g, f=1 TB
l, f=2
A
xB →
B
T
二、杠杆规则
TA
↑
f f=K- +2 g, f=2
l+g, f=1 TB
l, f=2
A
xB →
B
T
二、杠杆规则
TA
↑
f=K-f+2 g, f=2
单位与相图一致
A
x1 x0
y1
B
二、杠杆规则
f=K-f+2 系统温度变化时,相如何变化?
n1L1= n2L2
TA
L1
L2
气
T0时,L1=0,得 n2=0
物理化学 第六章 相平衡

S = 6, R =2, R′= 2 C = S – R - R’ = 6 –2 -2 = 2 若 NaCl 溶解完,则只存在一个化学平衡 H2O = H+ + OH S = 5, R =1, R′= 2
C =S –R -R’ = 5 –1 -2 = 2
一、理想液态混合物的气—液平衡相图
1)蒸气压-组成图 因是理想液态混合物,任一组分都服从拉乌尔定律,即
p = pA*xA + pB*xB p = pA* ( 1- xB ) + pB*xB =pA* + ( pB* - pA* ) xB
即系统总压与液相组成xB 成线性关系,在p - x图中是一直线, 这是理想双液系相图的一个特点。
解:
(1) C = S - R - R´= 3 - 1 - 1=1
F=C-P +2= 1-2+2=1 (2) C = S - R - R´= 3 - 1 - 0 =2
F =C-P+2= 2-2+2=2
例2 (1) 仅由CaCO3(s)部分分解,建立如下反应平衡: CaCO3 (s) = CaO(s) + CO2(g) (2) 由任意量的 CaCO3 (s), CaO (s), CO2 (g)建立如下反应平衡:
2 相律(Phase rule)的推导
①系统中的变量总数 设系统中有 S 个物种,分布在 P 个相中,在温度T、压力p下 达到平衡。 在α 相中的变量为:T,p,xα 1,xα 2,…, xα S-1 在β 相中的变量为:T,p,xβ 1,xβ 2,…, xβ S-1 ………… 在P 相中的变量为:T,p,xP1,xP2,…, xPS-1
物理化学 第三章 相平衡

p实际 > p理想 →正偏差 , p实际 < p理想 →负偏差
p
l
pB*
p
l
pB* g+ l
pA*
g
A
pA*
g
B A
xB→
xB→
B
一般正偏差系
一般负偏差系
pA* < p < pB*, yB > xB
( 实验结果 )
正偏差很大 负偏差很大
Tb - xB图
Tbmin
p - x B图 p max
液 气
p - x B图 p min
不定积分,可得
lnp/p0 = -△Hm/RT + C 率-△Hm/R求相变热△Hm 。
可用实验数据绘制lnp/p0~1/T曲线,由斜
(实验一)
实验:水的汽化热的测定 H m 1 ln p I ln p ~1/T关系图 R T
直线的斜率
10.8 10.6 10.4
H m 5.5819 R H m 5.5819 8.314 46.41 kJ mol1
求水的汽化热有什么用? 联系克-克方程讨论一下。
y = -5.5819x + 26.561 2 R = 0.9959
lnp
10.2 10 9.8 9.6 9.4 9.2 2.8 2.85 2.9 2.95 3 3.05 3.1 3.15
0.66 p 40.67 103 1 1 ② ln ( ) p 8.314 373 T2
T2 361.5K 88.5 ℃
T1 = 373K p1 = pθ ΔHm=40.67 kJmol-1
2.32 p 40.67 103 1 1 ③ ln ( ) p 8.314 373 T2
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
绪论
化学化工
在化学研究和化学生产过程的分离操作中, 经常会遇到各种相变化过程,如蒸发、冷凝、 升华、溶解、结晶和萃取等,这些过程涉及到 不同相之间的物质传递。相平衡研究是选择分 离方法、设计分离装置以及实现最佳操作的理
论基础。
绪论
材料科学
硅酸盐制品——制品中大多数是含有多种晶 相和玻璃相的多相系统,因此制品的性能必 然是与相组成、含量及生产过程有关。 无机材料——功能材料(特殊性能的材料) 是由多种物质构成的复杂系统,制备过程中 涉及相变化。 冶炼过程——相的变化,研究金属成分、结 构与性能的关系。
处于不同相态的同种化学物质,只能算一个
物种。如:液态水和水蒸气。
物种数和独立组分数
(2)独立组分数 (number of independent component )
——足以确定平衡体系中的所有各相组成所 需要的最少数目的物质的数目,记作C。
S≥C C = S – R – R`
R是独立化学平衡数, R'是独立浓度关系数。
物种数和独立组分数
(A)对于独立化学平衡数,要注意“独立” 两个字。
例如:系统中含有C(s)、CO(g)、H2O(g)、 CO2(g)、H2(g)等五种物质,可能存在的反应有 (1) C(s)+H2O(g)=CO(g)+H2(g) (2) C(s)+CO2(g)=2CO(g) (3)CO(g)+H2O(g)=CO2(g)+ H2(g)
xS =1- x1 – x2-xs-1 P个浓度关系式。 (3)独立化学平衡数为R,独立浓度关系数为R'。
F = P(S + 2) –(P–1) –(P–1) –S(P–1)- P – R –R'
= S – R – R` –P + 2 = C –P + 2
相律的推导
相律——是表述平衡体系中相数、组分、自 由度数和影响物质性质的外界因素(如温度、 压力、电场、磁场、重力场等)之间关系的 规律, 即 P+F= C+n 或者 F=C -P+n
F—自由度数, P—相数, C—组分数, n—表示能够影响体系平衡状态的外界因素 的个数。
相律的推导
(1)、冰水共存 C=1,P=2 (冰、水), F = 1-2+2=1 (T或p)
(2)、NH4Cl(s)部分分解为NH3(g)和HCl(g)
S=3,R=1,R’=1,P=2 (NH4Cl固相、气相) F=3–1–1–2+2=1
绪论
相平衡研究就是要揭示多相平衡体系中各种强 度性质(温度T、压力P 和组成)与相变化过程的关 系,这种关系相平衡系统的独立变量数与相数、独立
组分数之间关系的规律。 2、相图(phase diagram):
以T,P,x为坐标作图,称为相图,能直观
地表达多相系统的状态随温度、压力、组成等强度性 质变化而变化的图形。
第六章 相平衡
绪论 §6.1 相律 §6.2 杠杆规则 §6.3 单组分系统相图 §6.4 二组分理想液态混合物的气-液平衡相图 §6.5 二组份真实液态混合物的气-液平衡相图 §6.6 精馏原理 §6.7 二组分液态部分互溶系统及完全不互溶系统
的气-液平衡相图 §6.8 二组分固态互不相溶系统液-固平衡相图 §6.9 二组分固态互溶系统液-固平衡相图 §6.10 生成化合物的二组分凝聚系统相图 §6.11 三组分系统液-液平衡相图
如:
(1)液态水,在一定范围内改变T、p,仍可以保
持水为单相液态水,所以,在确定其状态时,必须
同时指定T、p,才能确定水的状态。则F = 2。
(2)水的气液平衡,体系的温度和压力之间具有 函数关系, 温度一定,压力也随之而定;反之, 亦然。所以,指定其状态时只需指定温度或压力即 可。此时,F = 1。
2.相律的推导
依据:自由度数=总变量数-方程式数
设一个多相多组分系统中,有S种物质1、2、
3…S)分布在P个相(α、β、γ…φ)中 对 于其中任意一相α相,必须知道Tα、pα、
xα1、…、xαs,才能确定其状态。所以,决定
α相状态的变量共有(S + 2)个。系统中共有
P个相,则整个系统的变量数为 P(S + 2) 但这些变量不是完全独立的,相互之间有
(T、p、 x NH3或xHCl其中之一)
(3) 1000K下,NH3、H2、N2三气平衡
S=3,R=1 (2NH3=3H2+N2),P=1 F= C-P+1=2 (p、xNH3、x H2或x N2其中之二)
3.物种数和独立组分数 (1)物种数
( number of substance ) ——系统中所包含的可以单独分离出来、并能独 立存在的化学物质的数目,称为系统的“物种 数”,记作S。 如:NaCl的水溶液中,有Na+、Cl-、H+和OH- 但 只能算两种物质,S = 2。
§6.1 相律(Phase Rule )
1. 自由度数 (number of degrees of freedom )
能够维持系统原有相数而可以独立改变的 变量(可以是温度、压力和表示相组成的某些 物质的相对含量)的数目。记作F。
因为这些变量在一定范围内可以变动,则 在讨论系统的状态时,必须指定这些变量的值。 所以,自由度数就是描述相平衡状态所需的最 少独立变量数。
联系, F = P(S + 2)-平衡时变量间的关系式数
相律的推导
(1)系统处于热力学平衡态,有
热平衡 Tα= … = Tp (P-1)个等式
力平衡 pα = … = pp (P-1)个等式
相平衡 μα1 = … = μp1 S(P-1)个等式
┊
┊
μαs = … = μps (2)每个相中有S种物质,ΣxB = 1,
物理化学
第六章 相平衡
学习要求:
理解相律的推导,掌握自由度数的概念以及相律 的内容及其应用,掌握单组份系统相图的阅读。 对二组份系统的气—液相图,要求掌握相图中点 线面的意义,会应用相律分析相图,熟练运用杠 杆规则计算各相的量。 重点掌握二组份系统的液—固平衡相图,要求了 解如何用热分析法制作相图,掌握典型相图的点 线面的特点和任意组成熔体的步冷曲线的绘制及 特征,熟悉相律和杠杆规则的应用。 了解三组份液—液平衡相图。
