第十三章 碳负离子的反应
13 碳负离子的反应

(
)
O
O
(1) C2H5ONa (2) H
1. OH
H5C2OC(CH2)4COC2H5
(
)
2. H
+
(
)
CH3COCH2COOC2H5
1)NaH 2)C6H5COCl
1)OH
(
)
2)H /
+
(
)
O
O
(1) NaH (2) H
CH3CCH3 + CH3(CH2)3CH2COC2H5
(
)
CH2CH2COOC2H5 H3C CH CH2CH2COOC2H5
取代甲基酮( 取代甲基酮 应用广泛)
取代乙酸
O H CH3 C C CH3 CH2CH2CH3
CH3 O H O (1) C2 H5ONa 2 C C C OC2H5 (2) CH3CH2CH2 Br (1) C2H5 ONa (2) CH3I (1) OH-/H2O (2) H3O+ TM
取代环烷基甲基酮
O
O
CH3CCH2COC2H5
OH
-
OOH
O
O CH3COOH + -CH2COC2H5
CH3C-CH2COC2H5
O CH3COO- + CH3COC2H5
OH-
H+
2 CH3COOH + C2H5OH
• 在合成上的应用
O CH3CCH2COOC2H5 C2H5ONa O CH3CH2CH2Br CH3CCHCOOC2H5
CH2(CO2C2H5)2
(1) C2H5ONa (2) CH3CH2 CH2Br
(1) C2H5ONa (2) CH3I
《碳负离子的反应》课件

防护措施
禁止事项
应急处理
废弃物处理
实验时需佩戴实验服、 护目镜等防护装备。
禁止在实验过程中饮食 、吸烟等行为。
熟悉实验中可能发生的 意外情况及处理方法。
按规定正确处理实验废 弃物。
实验废弃物的处理
分类处理
根据废弃物的性质进行分类, 如有机废弃物、无机废弃物等
。
回收利用
部分废弃物可进行回收利用, 以节约资源。
副产物的生成。
06
碳负离子反应的实验操作 与安全注意事项
实验操作规程
01
02
03
04
实验前的准备
确保实验室环境整洁,检查实 验器材是否齐全、完好。
试剂取用
按照需求适量取用,避免浪费 或不足。
操作步骤
按照规定的顺序进行实验操作 ,不可省略或颠倒。
数据记录
实时记录实验数据,确保准确 无误。
安全注意事项
安全处置
对于无法回收利用的废弃物, 需按照规定进行安全处置。
记录存档
对废弃物的处理过程进行记录 ,并存档备查。
THANKS
感谢观看
自由基反应
总结词
自由基反应是碳负离子与自由基的反 应,通常发生在碳负离子的未共用电 子对被自由基的空轨道接收的过程中 。
详细描述
在自由基反应中,碳负离子与自由基 相互作用,形成新的碳-碳键或碳-自 由基键。这种反应通常在高温或光照 条件下进行,有利于自由基的形成和 反应。
光化学反应
总结词
光化学反应是碳负离子在光的作用下发 生的化学反应,通常需要特定波长的光 照射。
β-羟基酸酯的合成
总结词
β-羟基酸酯是有机合成中的一种特殊结构, 碳负离子可以用于合成β-羟基酸酯。
碳负离子的反应

官能团转化反应
卤代烃的水解反应
卤代烃在碱性条件下生成碳负离 子,与水发生亲核取代反应生成 醇。
酯的水解反应
酯在碱性条件下生成碳负离子, 与水发生亲核取代反应生成羧酸 和醇。
立体选择性反应
烯烃的顺反异构化反应
在光照或加热条件下,烯烃与卤素发生 加成反应生成卤代烷,卤代烷在碱性条 件下生成碳负离子,再与另一分子烯烃 发生亲核加成反应,生成具有立体选择 性的顺反异构体。
碳负离子的反应
汇报人:XX
• 碳负离子概述 • 碳负离子的反应类型 • 碳负离子在有机合成中的应用 • 碳负离子的反应机理与动力学 • 碳负离子的实验方法与检测技术 • 碳负离子的应用前景与挑战
01
碳负离子概述
定义与性质
定义
碳负离子是指带有负电荷的碳原子, 通常表示为$C^-$。它是许多有机化 学反应中的重要中间体。
自由基反应
自由基引发
在某些条件下,如高温或过氧化物存在下,碳负离子可以引发自由基链式反应。通过均裂产生自由基,进而引发 后续的自由基传递和终止步骤。
自由基加成
碳负离子可以作为自由基受体,与自由基发生加成反应。例如,在烯烃的自由基加成反应中,碳负离子与烯烃中 的双键发生加成,生成新的自由基中间体。
电化学反应
性质
碳负离子具有亲核性,可以与亲电试 剂发生反应。它的稳定性取决于其所 处的化学环境,如溶剂、温度、pH值 等。
结构与稳定性
结构
碳负离子的结构通常是一个或多个碳 原子通过共价键与其他原子或基团相 连,并带有一个负电荷。这个负电荷 可以通过共振结构进行分散,从而提 高其稳定性。
稳定性
碳负离子的稳定性与其结构密切相关 。一般来说,具有较大共轭体系或能 够通过共振稳定化的碳负离子更稳定 。例如,苯基负离子比甲基负离子更 稳定。
碳负离子的反应

含有α氢原子的酮与酯之间也可以进行缩合 反应主要产物为β-二酮。
例如:
第二节 β-二羰基化合物的烷基化、酰基 化及其在合成中的应用
两个羰基被一个碳原子隔开的化合物称 为β-二羰基化合物。
β-二羰基化合物一般泛指β-二酮、β-酮 酸酯、丙二酸酯等含活泼亚甲基化合物 。
这类化合物主要的反应类型是亚甲基碳 上的烷基化、酰基化反应。
一、乙酰乙酸乙酯
无色,具有水果香味,沸点118℃, 微溶于水,易溶于多种有机溶剂。
反应可在不同的酯之间进行,称为交叉 酯缩合。
Claisen 缩合举例
混合酯缩合
反应机理
狄克曼(Dieckmann)缩合(也叫酯分子内 缩合)
含6个或7个碳的二元酸酯,在碱性催化 剂作用下环化生成五元或六元环为主的 -酮酯称为狄克曼反应。
分子内羟醛缩合
羟醛缩合反应不仅可以在分子间进行,含有α-氢原子的 二元醛或酮也可以进行分子内缩合,生成环状化合物, 是制备5~7元环化合物的常用方法之一。
ห้องสมุดไป่ตู้
β-羟基醛在加热时即失去一分子水,生成 α,β-不饱和醛
常用的碱性催化剂除了氢氧化钠、氢氧化钾外,还有叔 丁醇铝、醇钠等。 由此可见,通过羟醛缩合反应可以制备α,β-不饱和醛,进 一步还可以转变为其它化合物。所以羟醛缩合反应是有 机合成中用于增长碳链的重要方法之一。
含有α-氢原子的酮在稀碱作用下也 可以发生类似反应,即羟酮缩合反应, 但是反应的平衡偏向反应物一侧,例如 ,丙酮在氢氧化钡催化下,发生反应。
碳负离子的结构与碳正离子或碳自由基 不同,因为带负电荷的碳原子最外层有3对 成键电子和1对未成键电子,这样的4对电子 需要采取相互远离的方式排列,因此碳负离 子采用sp3杂化轨道成键,未成键电子对与3 个共价键形成一个四面体结构。碳正离子、 碳自由基和碳负离子的结构对比如下图所示 。
碳负离子的反应

(二)克脑文格尔反应
定义:在弱碱性催化剂作用下,醛或酮与具 有活泼亚甲基的化合物的缩合反应,称为克 脑文格尔反应. 常用的碱性催化剂有吡啶、哌啶、胺等。 反应通式:
R R
/
C O + CH2
Y Y/
R R/ C C
Y Y/
Y或 Y/ = COR COOR COOH CN
NO 2 等
反应机理
Y H2C Y
CH2 — C
CH2—CH2
C2H5ONa -C2H5OH
-
CH2 — C CH2 CH2 CH2—CH2
=
CH2 CH2 — C CH-COOC2H5 CH2 CH2—CH2 O
Oຫໍສະໝຸດ ==反 应 特 征
反应物:具有H,并能够形成五、六元环的二元羧酸酯。 催化剂:C2H5ONa 产 物:环状-酮酸酯 过 程:-C2H5OH
抗变态反应药物曲尼司特中间体3-(3,4-二甲氧 苯基丙烯酸的合成.
CHO 丙二酸
CH = CHCOOH
CH = CHCONH COOH
OCH3 吡啶/哌啶 OCH3
OCH3 OCH3 91%
OCH3 OCH3 曲尼司特
3-(3,4-二甲氧苯基)丙烯酸
酮一般不与丙二酸与丙二酸酯作用,但可与活性 更强的氰乙酸酯反应,缩合产物经水解、脱羧也可制 得不饱和酸。
(三)达琴反应
定义:在強碱(醇钠、氨基钠)作用下,醛、酮与α-卤代 酸酯反应,生成α,β-环氧酸酯的反应称为达琴反应。 通式:
R R/(H) C=O +
ClCH2COOC2H5
C2H5O Na
R
R/(H)
O C - CHCOOC2H5
碳负离子反应

穿戴防护装备:实验过程中必须穿戴防护 服、手套、护目镜等防护装备。
实验环境:实验应在通风良好的实验室中 进行避免在密闭空间内进行。
实验材料:实验材料应妥善保管避免接触 皮肤和眼睛。
实验操作:实验过程中应严格按照实验 步骤进行操作避免操作不当导致危险。
实验废弃物:实验结束后应妥善处理实验 废弃物避免环境污染。
碳负离子反应是合 成有机化合物的重 要方法之一广泛应 用于药物合成、材 料科学等领域。
碳负离子反应的机 理包括亲核加成、 亲核取代、亲核消 除等。
碳负离子反应的分类
碳负离子反应可以分为两类:亲核碳负离子反应和亲电碳负离子反应 亲核碳负离子反应是指碳负离子作为亲核试剂与亲电试剂发生反应 亲电碳负离子反应是指碳负离子作为亲电试剂与亲核试剂发生反应 碳负离子反应在合成化学中具有广泛的应用如合成有机化合物、药物合成等
碳负离子反应的特点
碳负离子是一种重要的有机合成中间体 碳负离子反应具有高度选择性和立体选择性 碳负离子反应可以生成多种类型的有机化合物 碳负离子反应在合成化学中具有广泛的应用
碳负离子反应的原理
碳负离子反应的化学键特征
碳负离子反应是一种化学反应其中 碳原子失去电子形成负离子。
碳负离子反应的化学键特征还与反 应条件、反应物浓度等因素有关。
碳负离子反应的研究趋势和展望
研究热点:碳负离子反应在材料科学、化学合成等领域的应用 研究方法:理论计算、实验验证相结合的研究方法 研究挑战:如何提高碳负离子反应的效率和选择性 研究展望:未来可能会在能源、环保等领域取得突破性进展
碳负离子反应的研究方法和手段
实验方法:通过实验观察碳负离子反应的过程和结果 理论研究:通过理论推导和计算来研究碳负离子反应的机理和规律 模拟计算:通过计算机模拟来研究碳负离子反应的条件和影响因素 合作研究:与其他研究机构或企业合作共同推进碳负离子反应的研究
碳正离子、碳负离子、自由基参与的化学反应 王竹青 29号 应化09-2

碳正离子、碳负离子、自由基参与的化学反应应用化学09-2班 王竹青 29号一 碳正离子参加的反应含有一个外层只有 6 个电子的碳原子作为中心碳原子的正离子。
常见的碳正离子如下:(一)碳正离子的形成一般有三种方法产生碳正离子。
1 .由反应物直接生成 :RXRX与碳原子直接相连的原子或原子团带着一对成键电子裂解,产生碳正离子。
极性溶剂、Lewis 酸常有促进效果。
1.1 X=H 。
烃很少自动失去氢负离子,只有在强亲电试剂如Lewis 酸或其它稳定正离子的因素存在下才能发生这一反应。
CHCH 3CH 3H 3C3C CH 3CH 3H 3C+HAlCl 31.2 X=F 、Cl 、Br 或I 。
这是SN1异裂反应。
Lewis酸可加速这种电离作用。
CClCH 3CH 3H 3CAlCl 3C CH 3CH 3H 3C+HAlCl 4CH 3CH 3CH 2(CH 3)3C1.3 X=OTs 酯类衍生物。
OTs 是一个很好的离去基团,这类酯很易 解离。
1.4 X=OCOZ ,其中Z= Cl 、Br 或I ,其推动力是由于形成二氧化碳。
氯亚磺酸酯,X=OSOCl 也属于这一类。
其推动力是由于排除SO2。
COSOClRR R3C RRR+Cl+SO 21.5 X=H2O 或ROH 。
断裂是由醚ROR 中氧原子的质子化引起的。
1.6 X= N 2。
亚硝酸和伯胺的反应生成的重氮离子很容易分解成碳正离子,推动力是由于生成了氮气。
1.7 X=CO 。
当相应的正离子稳定的时候,某些羧酸先质子化,然后脱去羰基。
C CH 3CH 3H 3CAlCl 3C CH 3CH 3H 3C+OTs -+C OCOClR RRC R RR+Cl -CO2+OR'RH OR'RR +R'OH+N 2H +N 2+COH 2OCOH 2O++CO 1.8 X=CO2。
羧酸氧化脱羧,生成碳正离子和CO2。
RCOOAgBr 2R+Br+AgBr+CO 22 质子或其它阳离子与不饱和体系加成质子或其它阳离子与不饱和体系加成,留下的临碳原子带正电。
有机化学碳负离子的反应
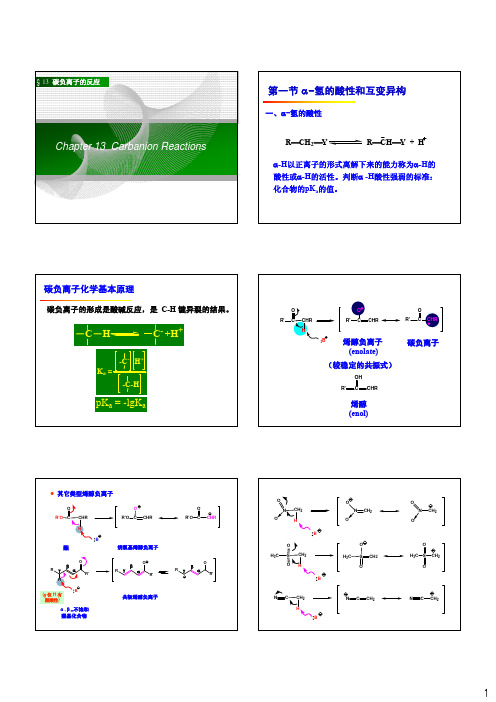
O R'O C
CHR
H
B
酯
O R'O C CHR
烷氧基烯醇负离子
O
β
Rγ
α
R'
H
B (γ 位 H 有
弱酸性)
α,β-不饱和 羰基化合物
β
O
Rγ
α
R'
共轭烯醇负离子
O R'O C CHR
O β
Rγ
α
R'
O
N CH2
O
H
B
O H3C S CH2
OH
B
N C CH2 H B
O N CH2
O
O
H3C
S CH2 O
¾芳醛中羰基化合物的反应活性受电子效应和空间结 构位置的影响,空间位阻较大时它将起主要的作用。
¾当苯环上为烷基时,由于烷基是给电子的基团,又 有位阻使反应物羰基活性下降,反应难以进行,产率 也低。
¾邻位甲基的位阻十分明显,导致不发生反应。
¾当苯环上有吸电子基团时有利于反应进行,不仅反 应的速度加快,并且产率也大大增加。
新型强碱
z 1. LDA 二异丙基胺锂 z 2. LHMDS六甲基二硅胺锂 z 3. LATMP四甲基哌啶锂
特点: z 1. 碱性强pKa大于33 z 2. 能溶解于非极性溶剂 z 3. 位阻大亲核性差
二、互变异构
O R' C CHR
H
O R' C CHR
B 烯醇负离子 (enolate)
(较稳定的共振式)
COOH
−CH=O + H2C
COOH
NH3,C2H5OH -H2O
COOH −CH=CHC
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
机理:
O C H
(CH3CO)2O + CH3COO
CH2COOCOCH3 + CH3COOH
+ CH2COCCH3 O O
O C CH2COCCH3 H O O
H C O
O O O
CH O O O
O O O CH3COCCH3
CH O O
O
O O O C-O-CCH3 CH3
H C O O H O H O O C
O NaOC2H5 C C H(R') R H2 O C C H
O
乙醛 在稀 碱催 化下 的反 应历 程
CH3CHO + OH
H3C H O C O + H2C C H
H2C CH + H2O O
H2C C H H3C C O H
O H2C C H H3C C O H + H2O
O H2C C H H3C C OH β H + OH
10
碳负离子的形成方式 1)酸催化时碳负离子的形成:
30
(3) 分子内的Claisen酯缩合——Dieckmann缩合
CH2CH2COOC2H5 CH2CH2COOC2H5 ① C2H5ONa ,C6H6 ② H+ O β H α COOC2H5
Dieckmann缩合主要用于制备五元和六元环状β-酮酸酯。
31
4. 酯-酮缩合 在碱性条件下,醛(酮)的 α- 碳形成负碳离子对酯 羰基的亲核加成-消除反应,生成1,3-二酮。
O O O C CH3
CH H
H2O
C H
H OH O
21
CH3COO
CH3
CHO + (CH3CO)2O CH3COOK 150~170OC
H C C H COOH
肉桂酸
O CH3COONa CH3COCCH3 C H+ O O H C CH-C OH O
O
O
β- 呋喃 丙烯酸
COOH C C OH H
14
⑤、芳香族醛酮的羟醛缩合
O O + OHC
NaOH/H2O 250C , 4h
OH C H
室温下缩合
O O + OHC
NaOH/H2O 25 C , 10d
0
C H
久置后脱水
O
CHO + H3C C CH3
OH
C H
H C C CH3
O
加热直接脱水
15
⑥、分子内的羟醛缩合
O O NaOH - H2 O O O
C CCOOC2H5 H COCH3
H CHO CH2(COOC2H5)2 OH NH
C C OH
COOC2H5 COOC2H5 分子内酯交换
O
COOC2H5 O
酮的反应活性比醛差,须更活泼的亚甲基化合物反应。
NC C2H5OOC CH2 + O C CH3 CH3COOH C2H5 NH , NC C2H5OOC C C CH3 C2H5
室温
α-β不饱和醛(酮)
19
(二)、Perkin(柏琴)反应
芳香醛与脂肪酸酐在相应脂肪酸碱金属盐的催化 下缩合,生成β-芳基丙烯酸类化合物的反应称为 Perkin反应。
CHO RCH2COOK + (RCH2CO)2O H R C C COOH
反应实质:酸酐的亚甲基与醛进行羟醛缩合。由于酸 酐的α-氢活性较低,催化剂羧酸盐又是弱碱,因此, 反应温度较高。
O
O
=
=
③
④
C H3 C C H2 C O C2H5
+
C2H5O
O
O
O
O
CH3 C CH2 C OC2H5 + C2H5O
CH3 C CH C O C2H5
芳香酸酯的羰基碳正电性下降,须强碱,以增大烯醇负离子浓度。
O COOCH3 + CH C OC H ① NaH 2 5 3 ② H3O+ O O C CH2 C OC2H5
烯醇含量 %
21
O O O CH3CCH2COC2H5
2.0X10-2
80
7.5
90
1、α-H越活泼烯醇化程度越大;羰基的-I效应 强于酯基和羧基; 2、共轭体系的延伸使烯醇型结构稳定,烯醇化 程度越大。
7
试写出下列化合物稳定烯醇式结构。
O 1. COOCH3 O 2. O N H H N O
1.
一般烯醇式不稳定,而乙酰乙酸乙酯的烯醇式较稳定存在:
H :O CH3 C O =
=
①、六元环结构
C-OC2H5 CH
②、大π键的形成
6
分子结构 对 烯醇型含量的影响
化合物
O CH3CCH3
烯醇含量 %
2.4X10-4
化合物
O O CCH2COC2H5 O O CH3CCH2CCH3 O O CCH2CCH3
O O
2,5-己二酮
O OH
- OH O
羰基的α-H具有酸性, -O-是强碱,生成α-C-
经历碳负离子脱 –OH
产物以五、六元环为主(热力学稳定产物)。
16
O
O
NaOH -H2O
O O - OH O O
O
2,6-庚二酮
O NaOH -H2O O O - OH O O
2,7-辛二酮
O NaOH -H2O - OH O O
O O α O ① C2H5ONa β HCOOC2H5 + CH3 C OC2H5 H C CH2 C OC2H5 ② CH3COOH
O ① C2H5ONa COOC2H5 O + CH3 C OC2H5 α β ② CH3COOH CO CH C OC H COOC2H5 2 2 5 COOC2H5
1和4不能形成稳定的烯醇型。2和3 存在酮型 和烯醇型互变平衡:
OH
2. 3.
CH3COCH(COOCH3)2 HOOCCOCH2COOH
CH3C
C(COOCH3)2 OH CHCOOH
9
HOOCC
§2、缩合反应
一、羟醛缩合型反应 ——负碳离子缩合反应的基础 羟醛缩合反应的本质是, 含α-氢的醛酮分子在酸 或碱的作用下形成碳负离子,碳负离子作为亲核 试剂对另一分子醛或酮的亲核加成。
乙酰乙酸乙酯负离子:
O CH3CCHCOC2H5 O O O H3CC CH C OC2H5 O O H3CC CH C OC2H5
pKa= 11
β- 二羰基化合物
3
当一个-CH2-与两个吸电子基团相连,酸性增加,称为 活泼亚甲基,该化合物称为含活泼亚甲基化合物。
常见的几个含活泼亚甲基化合物:
R O H2C O R R'O H2C O R'O R O H2C O R'O R'O O H2C O R'O CN H2C O NO2
27
二、酯缩合反应
1. Claisen酯缩合 含α-H的酯在强碱(如:乙醇钠)催化下缩合,生成
β-酮酸酯的反应称为Claisen酯缩合。
(1) 相同酯的自身缩合
O CH3 C OC2H5
+
O O O C2H5ONa ① CH3 C CH2 C OC2H5 CH3 C OC2H5 CH3COOH ②
R A B C C H O
R
+
R
OH
+H
A B
C C H
-H
+
A
C C B
OH
R A C C B OH A
R C C B OH+
决速步骤
在烯醇式向酮式转变时产生碳负离子。
11
如果α-碳原子是手性碳,
R H
R
R C C A B O OH+
a
OH
A
C C B
a
A C C B
外消旋化
R A R C C B H O OH+
O
O
2,8-壬二酮
17
O O2N O NaOH -H2O
O O2N
O2N
O
O
形成碳负离子容易
O O2N O
O2N
NaOH -H2O
O2N
δ+
O
O
羰基碳的正电性更强
O
18
小结:
脂肪族醛(酮)
条件
室温 加热
产物
β-羟基 醛(酮) α-β不饱和醛(酮)
分子内的羟醛缩合 加热
α-β不饱和醛(酮)
芳香族醛(酮)
②、羟酮缩合
β-羟基酮、α-β不饱和酮
AA + AB + BA + BB
③、交叉羟醛缩合 ④、共轭效应的影响
H H
C O + CH3CH=CHCHO OH
HOCH2CH2CH=CHCHO
α-氢的性质
HCHO OH HCHO OH
(插烯规则)
(HOCH2)2CHCH=CHCHO (HOCH2)3CCH=CHCHO
COOCH 3 O
COOCH 3 OH
O 2. O
H N O N H
HO N OH HO N
巴比妥酸
8
下列化合物中,哪些能形成稳定的烯醇型?试写出 它们的酮型和烯醇型互变平衡式。
1. HO CH2CH2COOH O 3. HOOCCCH2COOH O COOCH3 2. CH3C CH O 4. CH3CC(CH3)2COOCH3 COOCH3
b
b
A B
C C
将通过互变异构发生消旋化,β手性碳构型不改变。
