人教版高一化学必修二元素周期表
化学:《元素周期表-周期表结构》课件(新人教版必修2)

氕 (氢)
(重氢) 氘
(超重氢) 氚
H、D、T这三种核素互称为同位素
常见的同位素:
碳 碳-12
12C
6
碳-13
13C
6
碳-14
14C
6
氧 氯 铀
16O
8
17O
8
18O
8
35Cl
17 92
37Cl
17
234U
235U
92
238U
92
【同位素小结】
两同(同质子数、同一元素)
两不同(中子数不同、原子不同)
(2)碱金属元素从上到下(Li 、Na、K、 Rb、Cs),随着核电荷数的增加,碱金属 元素原子的电子层数逐渐 增多 ,原子核 对 最外层电子 的引力逐渐减弱,原子失 电子的能力逐渐 增强 。 元素的金属性逐渐 增强 ,与水和氧气 的反应越来越 剧烈 ,生成的氧化物越来 越 复杂 。最高价氧化物对应水化物的碱 性越来越 强 。
第88号元素: 88-86 =2
第五周期第ⅦA 族。
第七周期第ⅡA 族。
第82号元素:
第六周期第ⅣA 族。
6、下列各表为周期表的一部分(表中为 原子序数),其中正确的是( D )
A.0 11 18 19
C.
6 11 12 13 24
D.
6 14 31 32
7
7. A、B、C是周期表中相邻的三种元素,其中A、B是同 周期,B、C是同主族。此三种元素原子最外层电子数之
卤素原子结构的相似性,决定了单质化学性质的相似性。
与氢反应的能力渐弱 氢化物的稳定性渐弱 与水反应的能力渐弱
元素非金属性强弱判断依据:
1、单质跟氢气反应生成气态氢化物的 难易;
人教版高中化学必修二第一章完整ppt课件

ppt精选版
1
第1课时 元素周期表
ppt精选版
2
学习目标
1.简单了解元素周期表的发展历程。 2.了解元素周期表的编排规则及结构。 3.能描述元素在元素周期表中的位置。
ppt精选版
3
一、元素周期表的完善历程 1. 第一张元素周期表 (1)时间 1869 年,俄国化学家门__捷__列__夫__绘制出第一张元素周期 表,是化学发展史上的重要里程碑。 (2)编排原则 ①将元素按照_相__对__原__子__质__量_____由小到大依次排列。 ②将_化__学__性__质_相似的元素放在一个纵行。
答案:C
ppt精选版
28
解析:考查元素周期表的结构。对主族元素,其族序数 等于最外层电子数,但副族则不是;18 列构成 16 个族,其 中第Ⅷ族包含 3 列。
ppt精选版
29
3. 已知某离子的结构示意图为 的是( )
A. 该元素位于第二周期第ⅡA 族 B. 该元素位于第二周期第Ⅷ族 C. 该元素位于第三周期第ⅡA 族 D. 该元素位于第三周期 0 族
ppt精选版
18
4. 确定该元素在周期表中的位置,形式为“第几周期第 几族”,要注意分清主族、副族、0 族、第Ⅷ族
在应用上述方法推断元素的族序数时,要特别注意第 六、七周期第ⅢB 族的锕系和镧系元素,它们的每个空格都 有 15 种元素,其后的元素需再减去 14,然后定位。
ppt精选版
19
例 2 俄罗斯科学家用含 20 个质子的钙的一种原子轰击 含 95 个质子的镅原子,结果 4 次成功合成 4 个第 115 号元 素的原子。这 4 个原子生成数微秒后衰变成第 113 号元素。 下列有关叙述正确的是( )
人教版高中化学必修二全册教学课件

● A.54 ● C.81
B . 11 6 C
D.88
● 解析:Ⅲ是奇数,第ⅢA的元素的原子序数都是奇数。题中四个选项中只有C选项的原子序数是 奇数,答案选C。
课堂探究研析
● 问题探究:
知识点1 元素周期表的结构
1.元素周期表中,周期序数由什么决定?主族族序数由什么决定? 2.元素周期表从左到右一共有 18 列,哪一列所含元素种类最多?
● 二、认识元素周期表的结构 ● 1.编排原则:
● 2.周期表中周期的划分和一般特点:
个数
元素周期表中有7个横行,共有____7______个周期
特点
同周期中的元素的_电__子_层__数____相同 周期序数=_电__子_层__数____
分类
短周期 长周期
共有___3_______个,包括第__1_、__2、__3___周期 共有___4 _______个,包括第4_、__5、__6_、_7___周期
18
4
36
长周
5
Rb~Xe
18
5
54
期
6
Cs~Rn
32
6
86
7
Fr~Uuo
32
7
118
位置与结 构的关系
周期序数 =电子层
数
● 2.族(每一纵行):
族
周期表中有18 个纵行,除第 8、9、10三个 纵行为第Ⅷ族 外,其余15个 7个 纵行,每个纵 主 行为一族;周 族 期表中包括7个 主族,7个副 族,一个0族,
1
新课标导学
化学
必修② ·人教版
第一章
物质结构 元素周期律
第一节 元素周期表
第1课时 元素周期表
(完整版)高一化学必修二知识点总结

高一化学必修二知识点总结一、元素周期表★熟记等式:原子序数=核电荷数=质子数=核外电子数1、元素周期表的编排原则:①按照原子序数递增的顺序从左到右排列;②将电子层数相同的元素排成一个横行——周期;③把最外层电子数相同的元素按电子层数递增的顺序从上到下排成纵行——族2、如何精确表示元素在周期表中的位置:周期序数=电子层数;主族序数=最外层电子数口诀:三短三长一不全;七主七副零八族熟记:三个短周期,第一和第七主族和零族的元素符号和名称3、元素金属性和非金属性判断依据:①元素金属性强弱的判断依据:单质跟水或酸起反应置换出氢的难易;元素最高价氧化物的水化物——氢氧化物的碱性强弱;置换反应。
②元素非金属性强弱的判断依据:单质与氢气生成气态氢化物的难易及气态氢化物的稳定性;最高价氧化物对应的水化物的酸性强弱;置换反应。
4、核素:具有一定数目的质子和一定数目的中子的一种原子。
①质量数==质子数+中子数:A == Z + N②同位素:质子数相同而中子数不同的同一元素的不同原子,互称同位素。
(同一元素的各种同位素物理性质不同,化学性质相同)二、元素周期律1、影响原子半径大小的因素:①电子层数:电子层数越多,原子半径越大(最主要因素)②核电荷数:核电荷数增多,吸引力增大,使原子半径有减小的趋向(次要因素)③核外电子数:电子数增多,增加了相互排斥,使原子半径有增大的倾向2、元素的化合价与最外层电子数的关系:最高正价等于最外层电子数(氟氧元素无正价)负化合价数= 8—最外层电子数(金属元素无负化合价)3、同主族、同周期元素的结构、性质递变规律:同主族:从上到下,随电子层数的递增,原子半径增大,核对外层电子吸引能力减弱,失电子能力增强,还原性(金属性)逐渐增强,其离子的氧化性减弱。
同周期:左→右,核电荷数——→逐渐增多,最外层电子数——→逐渐增多原子半径——→逐渐减小,得电子能力——→逐渐增强,失电子能力——→逐渐减弱氧化性——→逐渐增强,还原性——→逐渐减弱,气态氢化物稳定性——→逐渐增强最高价氧化物对应水化物酸性——→逐渐增强,碱性——→逐渐减弱三、化学键含有离子键的化合物就是离子化合物;只含有共价键的化合物才是共价化合物。
人教版高中化学必修二课件第一章第一节第1课时元素周期表

提示:短周期元素中族序数与周期数相同的有三种元素:
氢、铍、铝。若族序数(或周期数)为1,则为氢;若族序数(或 周期数)为2,则为铍;若族序数(或周期数)为3,则为铝。
2.主族序数=最高正价数,这一关系有例外吗?请举例。
提示:这个关系对除O、F两种元素以外的任何主族元素都
是成立的,因为O、F无最高正价。
二、元素在元素周期表中位置的确定方法 1.以0族为基准给元素定位 稀有气体元素 周期数 He 一 Ne 二 Ar 三 Kr 四 Xe 五 Rn 六
原子序数
2
10
18
36
54
86
(1)确定纵行数(族序数)。 元素的纵行数=原子序数-相近且小的稀有气体原子序
数,所得纵行数与族序数的对应关系如下表。
纵行数 1 2 13 14 15 16 17 18
族序数
纵行数
ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA
3 4 5 6 7 8、9、10 Ⅷ族
0族
11 12
族序数 ⅢB ⅣB ⅤB ⅥB ⅦB
ⅠB ⅡB
(2)确定周期数。 元素的周期数=原子序数相近且小的稀有气体的周期数
+1。
例如:判断原子序数为41的元素在元素周期表中的位置。 分析:41与36接近,有41-36=5,该元素处于第五周期ⅤB 族。使用此法若为第六、七周期ⅢB族(含镧系、锕系元素)后 的元素需再减14定位。 2.根据每周期元素的种类给元素定位 周期序数 一 二 三 四 五 六 七
6.X、Y、Z是短周期三种元素,它们在周 期表中的位置如右图所示,试回答:
(1)X元素单质的化学式是________。
(2)Z元素的原子结构示意图为________。
(3)Y在元素周期表中的位置是
高一化学元素周期表

同一元素的
1个126C原子的质量
原子中,质 子数和中子
12 = 1.6726×10-27kg
1.993×10-26kg
数是否一定
12
相等呢?
≈1.007
1个中子的质量=1.6749×10-27kg
中子的相对质量=1.008
质子的相对质量取整数与中子的相对
质量取整数相加起来所得的数值叫做原子
质量数。用A表示。
第一节 元素周期表
复习: 1、元素: 具有相同核电荷数(即核内质子
数)的一类原子的总称。
2、原子的构成:
质子 每个质子带1个单位正
原子核
电荷相对质量为1
原子
中子 不带电,相对质量为1
核外电子 每个电子带1个单位负电荷 相对质量为1/1836
核电荷数=质子数=核外电子数,
因此,原子 呈电中性
质子的相对质量= 1个质子的质量
⑤ 天然存在的同位素,相互间保持一定的比率。元素的相对 原子质量,是按照该元素的各种核素原子所占的一定百分比 算出的平均值。
1、作核燃料:作制造核武器的动力性材料(235U) 2、金属探伤:利用γ射线的贯穿本领,可以检查金属内 部有没有沙眼和裂纹。 3、辐射育种:利用放射性同位素的射线对遗传物质产生 影响,提高基因突变频率,从而选育出优良品种。 4、临床治癌:利用放射性同位素的射线杀伤癌细胞或阻 止癌细胞分裂。 5、环保治污:利用放射性同位素的射线可消毒灭菌,杀 死各种病原体从而能保护环境是其少受污染。
2、核素:具有一定数目的质子和一定 数目的中子的一种原子。
3、同位素:质子数相同而中子数不同的 同一种元素的不同原子互称为同位素。 即:同一元素的不同核素之间互称为同位素
(1) Z同,N不同 (2)不同的原子
高一化学人教版原子结构与元素周期表
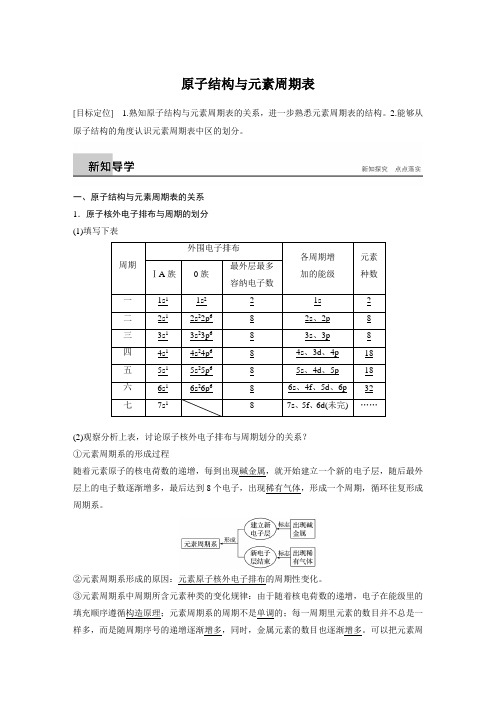
原子结构与元素周期表[目标定位] 1.熟知原子结构与元素周期表的关系,进一步熟悉元素周期表的结构。
2.能够从原子结构的角度认识元素周期表中区的划分。
一、原子结构与元素周期表的关系1.原子核外电子排布与周期的划分(1)填写下表周期外围电子排布各周期增加的能级元素种数ⅠA族0族最外层最多容纳电子数一1s11s2 2 1s 2二2s12s22p68 2s、2p 8三3s13s23p68 3s、3p 8四4s14s24p68 4s、3d、4p 18五5s15s25p68 5s、4d、5p 18六6s16s26p68 6s、4f、5d、6p 32七7s18 7s、5f、6d(未完) ……(2)观察分析上表,讨论原子核外电子排布与周期划分的关系?①元素周期系的形成过程随着元素原子的核电荷数的递增,每到出现碱金属,就开始建立一个新的电子层,随后最外层上的电子数逐渐增多,最后达到8个电子,出现稀有气体,形成一个周期,循环往复形成周期系。
②元素周期系形成的原因:元素原子核外电子排布的周期性变化。
③元素周期系中周期所含元素种类的变化规律:由于随着核电荷数的递增,电子在能级里的填充顺序遵循构造原理;元素周期系的周期不是单调的;每一周期里元素的数目并不总是一样多,而是随周期序号的递增逐渐增多,同时,金属元素的数目也逐渐增多。
可以把元素周期系的周期发展形象地比喻成螺壳上的螺旋。
2.原子核外电子排布与族的划分(1)将下列各主族元素的价电子数、价电子排布式填入表中族数ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA价电子n s1n s2n s2n p1n s2n p2n s2n p3n s2n p4n s2n p5排布式列数 1 2 13 14 15 16 17价电1 2 3 4 5 6 7子数(2)以第四周期副族元素为例,填写下表副族元素21Sc 22Ti 23V 24Cr 25Mn 29Cu 30Zn 族数ⅢB ⅣB ⅤB ⅥB ⅦB ⅠB ⅡB 价电子排布式3d14s23d24s23d34s23d54s13d54s23d104s13d104s2价电子数目 3 4 5 6 7(3)依据上述表格,讨论族的划分与原子核外电子排布的关系?族的划分依据是原子的价层电子排布。
元素周期表

第一章 第二节 第2课时
成才之路 ·高中新课程 ·学习指导 ·人教版 ·化学 ·必修2
门捷列夫的元素周期表形成了一个基本的构架,现在的许 多工作是完善它。在元素周期表中,从 112 号到 116 号元素的 名字都没有得到承认,第 113、115、117 号三个元素是空白。 曾经有学者声称发现了 118 号元素,但还没有得到国际组织的 认同。随着科学技术的进步和新的研究方法的应用,人们很有 可能发现新的元素。 那么你知道在这些已经发现的元素中都隐藏了那些规律 吗?学完本课时内容,你将明了于心。
成才之路 ·高中新课程 ·学习指导 ·人教版 ·化学 ·必修2
新情境· 激趣入题
第一章 第二节 第2课时
成才之路 ·高中新课程 ·学习指导 ·人教版 ·化学 ·必修2
在科学大道上, 有一块宝石, 它就是元素周期律。 拉瓦锡、 德贝莱纳、纽兰兹、迈耶尔等人从它身边走过,都把它拿起来 看看,然后又把它扔掉。而门捷列夫却吸收前人的经验,苦苦 思索仔细研究它,使之散发出本身的光彩,最后他拿着这块宝 石,登上了化学的高峰,统一了整个无机化学。 自从门捷列夫制订了元素周期表, 人们发现新元素的步伐 在逐渐加快。那么世界上究竟有多少元素,元素周期表有没有 尽头呢?
第一章 第二节 第2课时
成才之路 ·高中新课程 ·学习指导 ·人教版 ·化学 ·必修2
2.原子半径的变化规律 3~ 9 号 元素 原子半 径/nm 变化 趋势 0.152 0.89 0.82 0.77 0.75 0.74 0.71 Li Be B C N O F
0.152―→0.71
逐渐减小
第一章 第二节 第2课时
(2)元素原子半径的周期性变化。
2 规律:随着原子序数的递增,元素的原子半径呈现 □ ________的周期性变化。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
碱金属的物理性质的比较
Li Na K Rb Cs
相
颜色 均为银白色(Cs略带金色)
硬度 似
柔软
密度
较小
点 熔沸点
较低
导电导热性 递 密度变化 变 性 熔沸点变化
强 逐渐增大(K特殊) 单质的熔沸点逐渐降低
人教版高一化学必修二1.1元素周期表 第二课 时(共3 3张PPT )
碱金属元素的原子结构和性质递变规律
核电 电子 原子 原子失电 元素的 单质的 荷数 层数 半径 子能力 金属性 还原性
Li
渐渐 渐 增增 增
渐 增
渐 增
渐 增
最高价氧化物对 应水化物的碱性
渐 增
Cs
人教版高一化学必修二1.1元素周期表 第二课 时(共3 3张PPT )
2.递变性: 电子层数
原子半径
核对最 外层电 子的引 力
失电 子能 力
还原 性
金 属 性
(电子层数的影响大于核电荷数的影响)
人教版高一化学必修二1.1元素周期表 第二课 时(共3 3张PPT )
人教版高一化学必修二1.1元素周期表 第二课 时(共3 3张PPT ) 人教版高一化学必修二1.1元素周期表 第二课 时(共3 3张PPT )
人教版高一化学必修二1.1元素周期表 第二课 时(共3 3张PPT )
人教版高一化学必修二1.1元素周期表 第二课 时(共3 3张PPT )
总结:
碱金属的原子结构
Li Na K Rb Cs
1.相似性:
最外层上都只 有一个电子
化学性质相似
1) 都易失电子表现强还 原性
2) 化合物中均为+1价
核电荷数
2.实验:
(1)Na、K与氧气反应进行对比 (2)Na、K与水反应进行对比
与氧气反应 与水反应
钾
钠
剧烈燃烧,紫色火焰 剧烈燃烧,黄色火焰
反应剧烈,轻微爆炸 反应剧烈,熔成小球
3.思考与交流: 通过回忆和观察钠和钾的实验,思考并讨论钠和钾的 性质有什么相似性和不同.你认为元素的性质与它们的原子结构有 关系吗?
碱金属的化学性质
与O2反应
Li
Na
反应不如钠 点燃剧烈
剧烈,生成 燃烧,生
Li2O
成Na2O2
K
Rb Cs
燃烧更加剧 遇空气立即遇空气立即
烈生成比过 燃烧,生成燃烧,生成
氧化物复杂 更复杂的氧更复杂的氧
的氧化物 化物
化物
剧烈,生 更剧烈,生 轻微的爆炸,遇水立即燃遇水立即燃
与H2O反应 成H2
成H2
碱金属在物理性质上的相似性和规律性。 人教版高一化学必修二1.1元素周期表第二课时(共33张PPT)
Li Na K Rb Cs
相
颜色
似
硬度
密度 点
熔沸点
均为银白色(Cs略带金色) 柔软 较小 较低
导电导热性
递 变
密度变化
性 熔沸点变化
很好 逐渐增大(K特殊) 单质的熔沸点逐渐降低
人教版高一化学必修二1.1元素周期表 第二课 时(共3 3张PPT )
第一章 物质结构 元素周期律 第一节 元素周期表
第二课时
二、元素的性质与原子结构
1.碱金属元素 1.查阅元素周期表有关信息,填写下表
元素 元素符 核电 原子结构示 最外层 电子
名称 号
荷数 意图
电子数 层数
锂 Li 3
+3 2 1
12
原子半径 nm 0.152
钠 Na 11
+11 2 8 1
碱
1
3
人教版高一化学必修二1.1元素周期表 第二课 时(共3 3张PPT )
通过比较碱金属单质与氧气、水的反应, 我们可以看出,元素性质与原子结构有密 切关系,主要与原子核外电子的排布,特 别是 最外层电子数 有关。原子结构相 似的一族元素,它们在化学性质上表现出
相似性 和递变性 。
在元素周期表中,同主族元素从上到下原 子核外电子层数依次 增多 ,原子半径逐 渐 增大 ,失电子能力逐渐 增强 ,金 属性逐渐 增强 。
人教版高一化学必修二1.1元素周期表 第二课 时(共3 3张PPT )
元素金属性强弱判断依据:
1、根据金属单质与水或者与酸反应置换出氢的 难易程度。置换出氢越容易,则金属性越强。 2、根据金属元素最高价氧化物对应水化物碱性 强弱。碱性越强,则原金属元素的金属性越强。
3、可以根据对应阳离子的氧化性强弱判断。金 属阳离子氧化性越弱,则元素金属性越强。
0.186
金钾
K
19
+19 2 8 8 1
1
4
0.227
属
元
铷
Rb
37
+37 2 8 18 8 1
1
5
0.248
素
铯
Cs
55
+55 2 8 18 18 8 1
1
6
0.265
思考与交流 碱金属的原子结构示意图 碱金属原子结构有何异同?
①相同点:碱金属元素原子结构的 最外层电子数 相同, 都为 1个 。 ②递变性:从Li到Cs,碱金属元素 的原子结பைடு நூலகம்中, 电子层数 依次 增多。
碱金属的物理性质
颜色和状态
密度 g·㎝-3
银白色,柔软
0.534
熔点 ℃
180.5
沸点 ℃
1347
银白色,柔软
0.97
97.81 882.9
银白色,柔软
0.86
63.65
774
银白色,柔软
1.532 38.89
688
略带金属光泽,柔软
1.879 28.40 678.4
人教版高一化学必修二1.1元素周期表 第二课 时(共3 3张PPT )
生成H2
烧,爆炸 烧,爆炸
结论
金属性逐渐增强
人教版高一化学必修二1.1元素周期表 第二课 时(共3 3张PPT )
随着核电荷数的增加,碱金属元素原 子的电子层数逐渐 增多 ,原子半径 逐渐 增大 ,原子核对最外层电子的 引力逐渐 减弱 。
碱金属元素的性质也有差异,从锂到 铯金属性逐渐 增强 ,如它们与氧气 或水反应时,钾比钠反应 剧烈 ,铷、 铯的反应 更剧烈 。
元素金属性强弱可以从其单质与水(或酸)反应置 换出氢的难易程度,以及它们的最高价氧化物的水 化物——氢氧化物的碱性强弱来比较。
人教版高一化学必修二1.1元素周期表 第二课 时(共3 3张PPT )
人教版高一化学必修二1.1元素周期表 第二课 时(共3 3张PPT )
碱金属单 质 Li Na K Rb Cs
通过大量实验和研究,人们得出了如下结论:
碱金属元素原子的最外层都有1个电子,它们的化学性
质彼此相似 ,它们都能与 水 等非金属单质以及氧气 反应,表现出金属性(还原性).
4Li+O2=2Li2O
2Na+O2=Na2O2 2Na+2H2O=2NaOH +H2↑
2K+2H2O=2KOH +H2↑ 上述反应的产物中,碱金属元素的化合价都是 +1 。
