优洁消毒液企业标准
优洁消毒液的性能特点

优洁消毒液的性能特点
1、迅速杀灭霉菌、酵母菌、大肠杆菌、金黄色葡萄球菌、白色念珠菌、军团菌
等细菌繁殖体、芽孢、病毒(肝炎病毒、禽流感病毒H9N2、A型流感病毒H1N1等);
2、无毒无害。
优洁LD50>5000mg/kg,LC50>10000mg/m³达到《瑞士有毒物质
法》的无毒标准;
3、稳定性好。
优洁工作液pH值为中性(相当于城市自来水标准);
4、无腐蚀。
优洁对不锈钢铜铝材质的管道均无腐蚀;
5、环保免冲洗。
优洁消毒液中的醛类衍生物其杀菌后的产物在辅助成分的作用
下,可降解为较小结构的化合物,降解后的产物达到环保排放要求;
6、随时可以在回收罐中检测CIP是否有故障。
由于优洁极为稳定,优洁消毒液
每次循环后,有效含量仅降低5%-10%,若回收罐中检测到优洁消毒液有效成分大幅度变化,即可预警管道系统出现跑冒滴漏问题,应立即检查CIP系统,找出故障;
7、操作简便。
优洁原液可用纯净水兑成所需浓度工作液,直接使用;
8、检测速度快。
用优洁专用试纸检测,5-10秒即可;
9、消毒工艺改造简便。
由于优洁无腐蚀、无刺激性,原有工作容器可直接使用,
人员无需防护工具;
10、杀菌是不受蛋白质等有机物的干扰。
使用衰减周期长,可循环使用,相对使用成本低。
一次性使用抗菌(或抑菌)液体产品企业标准-QYC-017-2015【整理精品范本】

Q/YC x x x x生物科技有限公司企业标准Q/YC 017—2015一次性使用抗菌(或抑菌)产品2015—04-15发布2015-05-01实施xxxx生物科技有限公司发布Q/YC 016-2015前言本标准是按GB 15979—2002 给出的规则编写。
本标准由xxxx生物科技有限公司提出。
本标准由xxxx生物科技有限公司负责起草。
本标准主要起草人:xxx。
本标准于2015年04月15日首次发布。
本标准由xxxx生物科技有限公司法定代表人xxx批准,并对所规定的内容负责。
一次性使用抗菌(或抑菌)产品1范围本标准规定了一次性使用抗菌(或抑菌)产品的定义、产品卫生指标、生产环境卫生指标、测试方法、原材料卫生要求、生产环境与过程卫生要求、消毒过程要求、包装运输与贮存要求及产品标识要求。
本标准适用于一次性使用抗菌(或抑菌)液体产品。
2引用标准文件下列文件对于本文件的应用是必不可少的。
凡是注日期的引用文件,仅所注日期的版本适用于本文件。
凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件.GB/T 191 包装储运图示标志GB 15979-2002 一次性使用卫生用品卫生标准GB/T 2828。
1-2012 计数抽样检验程序第1部分:按接收质量限(AQL)检查的逐批检查及抽样计划GB/T 2829—2002 周期检验计数抽样程序及表(适用于对过程稳定性的检验)3定义GB 15979-2002所界定的及以下术语和定义适应于本标准.3.1 一次性使用卫生用品使用一次后即丢弃的、与人体直接或间接接触的、并为达到人体生理卫生或卫生保健(抗菌或抑菌)目的而使用的各种日常生活用品,产品性状可以是固体也可以是液体。
例如:一次性使用抗菌(或抑菌)液体产品(如:小儿止痒凝露)、纸巾、湿巾、卫生湿巾、电话膜、帽子、口罩等,在本标准中统称为“卫生用品"。
3。
2一次性使用抗菌(或抑菌)液体产品集中医药学,现代免疫学,微生物专家研制而成,在传统医学理论基础上,采用先进技术研制而成。
优洁消毒液精简材料课件

LD50>5000mg/kg
反应积分值为0
LC50>10000毫克/立方米
角膜损害为0 虹膜损害为0 结膜充血为0 结膜水肿为0
不锈钢、铜
铅<1.0 优洁消毒液精砷简<材料0.05
实际无毒 无刺激
实际无毒
无刺激
无腐蚀 符合国标要求
常用手消毒液性能对比
产品类别
主要成分
消毒效果
抑菌时间 刺激性 耐药性
100 100 100 100
金黄色葡萄球菌
0.1% 99.99 100 100 100
白色念珠菌
0.1% 99.89 99.97 100 100
淋球菌
0.1% 99.97 100 100 100
优洁消毒液精简材料
豚鼠皮肤刺激试验
1小时
24小时
48小时
动物性别 样品 对照 样品 对照 样品 对照 红 水红 水 红 水 红 水 红水 红 水 斑 肿斑 肿 斑 肿 斑 肿 斑肿 斑 肿
优洁消毒液即具备以上特点 优洁消毒液精简材料
优洁消毒液
主要成分: 六亚甲基四胺 30%
(属复合醛类、醛类衍生物)
复配季胺盐 11%
优洁消毒液精简材料
优洁消毒液的成分和作用
• 复配季铵盐-C13季铵盐,作用于微生物细胞表面,与传 统季铵盐类消毒剂相比,其并不会使细胞膜变性,只是拉 伸细胞,改变细胞膜的通透性。
雌 性 - --- - - - - - -- -
雄 性 - --- - - - - - -- - 皮肤反应 - - - - - - - - - - - -
刺激强度 - - - - - - - - - - - -
优洁消毒液精简材料
优洁消毒液安全性
Q_3202 YJ 005-2020优洁 清洗消毒液

C19Q 无锡优洁科技有限公司企业标准Q/3202YJ005-2020代替Q/3202YJ005-2018优洁®清洗消毒液2020-01-15发布2020-01-15实施无锡优洁科技有限公司发布前言本标准代替Q/3202YJ005-2018。
本标准与前版标准相比作了如下修改:——修改了感官指标。
——增加了苯扎溴铵检测方法。
本标准按GB/T1.1-2009《标准化工作导则第1部分:标准的结构和编写》编写。
本标准由无锡优洁科技有限公司提出并起草。
本标准主要起草人:耿曹军。
本标准于2012年03月首次发布;于2013年01月第一次修订;于2015年03月第二次修订;于2018年03月第三次修订;于2020年01月第四次修订。
优洁®清洗消毒液1范围本标准规定了优洁®清洗消毒液的原料要求、要求,试验方法、检验规则、标志、使用说明书、包装、运输。
本标准适用于以六亚甲基四胺、苯扎溴铵等为主要原料,添加辅料聚山梨酯80、纯净水复配而成的优洁®清洗消毒液(以下简称产品)。
可用于食品加工设备、食品容器具、家具用品、厨卫用品、婴幼儿衣物的消毒。
2规范性引用文件下列文件对于本文件中的应用是必不可少的。
凡是注日期的引用文件,仅注日期的版本适用于本文件。
凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件:GB/T191-2008包装储运图示标志GB14930.2-2012食品安全国家标准消毒剂GB19298-2014食品安全国家标准包装饮用水GB9985-2000手洗餐具用洗涤剂JJF1070-2005定量包装商品含量计量检测规则国家质量技术监督检验检疫总局【2005】第75号令《定量包装商品计量监督管理办法》《中华人民共和国药典》2015年版原卫生部《消毒技术规范》2002年版原卫生部《消毒产品检验规定》2003年版原卫生部《消毒产品标签说明书管理规范》2005年版原卫生部《消毒产品生产企业卫生规范》2009年版3原料卫生质量要求3.1六亚甲基四胺纯度为≥99.0%、规格为工业级。
优洁消毒液与德国V80消毒剂
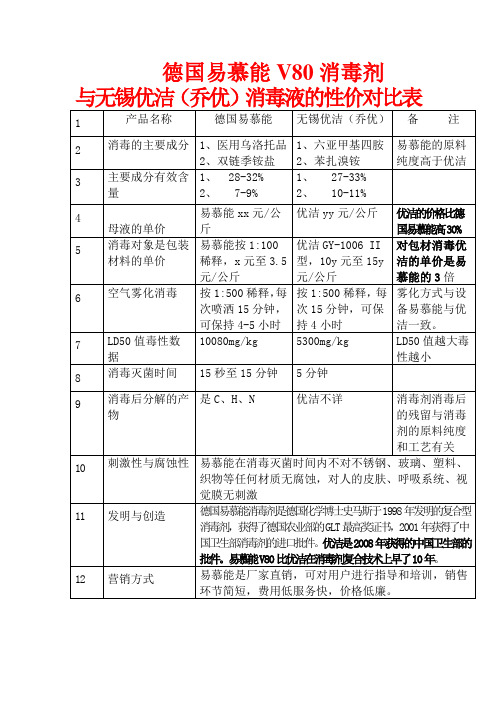
德国易慕能V80消毒剂与无锡优洁(乔优)消毒液的性价对比表1 产品名称德国易慕能无锡优洁(乔优)备注2 消毒的主要成分1、医用乌洛托品2、双链季铵盐1、六亚甲基四胺2、苯扎溴铵易慕能的原料纯度高于优洁3 主要成分有效含量1、 28-32%2、 7-9%1、 27-33%2、 10-11%4母液的单价易慕能xx元/公斤优洁yy元/公斤优洁的价格比德国易慕能高30%5 消毒对象是包装材料的单价易慕能按1:100稀释,x元至3.5元/公斤优洁GY-1006 II型,10y元至15y元/公斤对包材消毒优洁的单价是易慕能的3倍6 空气雾化消毒按1:500稀释,每次喷洒15分钟,可保持4-5小时按1:500稀释,每次15分钟,可保持4小时雾化方式与设备易慕能与优洁一致。
7 LD50值毒性数据10080mg/kg 5300mg/kg LD50值越大毒性越小8 消毒灭菌时间15秒至15分钟5分钟9 消毒后分解的产物是C、H、N 优洁不详消毒剂消毒后的残留与消毒剂的原料纯度和工艺有关10刺激性与腐蚀性易慕能在消毒灭菌时间内不对不锈钢、玻璃、塑料、织物等任何材质无腐蚀,对人的皮肤、呼吸系统、视觉膜无刺激11发明与创造德国易慕能消毒剂是德国化学博士史马斯于1998年发明的复合型消毒剂,获得了德国农业部的GLT最高奖证书,2001年获得了中国卫生部消毒剂的进口批件。
优洁是2008年获得的中国卫生部的批件。
易慕能V80比优洁在消毒剂复合技术上早了10年。
12营销方式易慕能是厂家直销,可对用户进行指导和培训,销售环节简短,费用低服务快,价格低廉。
优氯净执行标准

优氯净执行标准
一、适用范围
优氯净是一种高效、广谱的消毒剂,广泛应用于水处理、医疗卫生、广场公园、酒店宾馆等场所的卫生消毒保洁。
因此,在使用优氯净时,必须遵守执行标准。
优氯净执行标准适用于优氯净及其制剂的生产、检验、使用和管理。
二、检测要求
在生产、检验和使用优氯净时,必须进行严格的检测工作,确保其符合执行标准的各项要求。
具体要求如下:
1.外观和气味的检查要求
优氯净的外观应为无色透明或淡黄色液体或颗粒状,无杂质和悬浮物,气味应为独特气味。
2.有效氯含量的检查要求
优氯净中的有效氯含量是衡量其消毒能力的重要指标,检测应严格按照标准方法进行,并且必须达到标准要求。
3.其他有关物理化学指标和微生物指标等的检查要求
为确保优氯净的品质安全,还需要进行其他有关物理化学指标和微生物指标等的检查,以保证其符合执行标准相关标准要求。
三、质量标准
在保证优氯净的安全、有效性和稳定性的基础上,优氯净的质量标准应当符合执行标准中的各项要求。
具体来说,应该包括以下方面
的内容:
1.外观和气味符合要求;
2.有效氯含量符合要求;
3.其他物理化学指标和微生物指标等符合要求;
4.包装容器和标签符合相关要求;
5.生产和检验记录符合相关要求。
四、实际应用
实践证明,优氯净执行标准的制定和实施,对保障消毒剂的安全、效果、一致性具有重要意义。
优氯净生产企业应注重执行标准,规范生产过程,确保质量合格;对于使用优氯净的部门机构和个人也应当严格遵照执行标准操作,在使用优氯净时可加强检查,确保其消毒效果符合预期,提高公共场所卫生水平。
消毒液产品企业标准

200
10
对铜绿假单胞菌(ATCC15442)的杀灭对数值≥5
对白色念珠菌(ATCC10231)的杀灭对数值≥4
200
20*
对脊髓灰质炎病毒-Ⅰ型疫苗株的杀灭对数值≥4
500
60
对枯草杆菌黑色Βιβλιοθήκη 种芽孢(ATCC9372)的杀灭对数值≥5
次氯酸钠消毒液企业标准规范:
1.有效氯含量4%-5%
2.包装后的消毒剂,在遵守储运、贮存规则的条件下,自生产之日起,有效期不得低于6个月。在标识的有效期内,原液有效氯含量不得低于标识有效氯含量下限值、且应≥4%。
3.
消毒液作用浓度(以有效氯含量计,mg/L)
作用时间(min)
杀灭微生物指标
100
10*
洁净厂房空间优洁消毒验证

洁净厂房空间优洁消毒验证作者:胡敏刘亮亮邹宗萍来源:《医学信息》2014年第13期摘要:药品生产环境包括室外环境及室内环境,室内环境可能影响药品的质量,而室外环境可能影响室内环境的质量[1]。
故药品生产的洁净空气环境应控制粒子、微生物的污染。
微生物污染的控制通过洁净环境空间消毒的方法进行。
本文通过采用优洁消毒的方式,验证该方法操作的有效性、可靠性及安全性。
关键词:空间消毒;优洁;验证洁净厂房传统消毒方式有臭氧消毒、消毒液消毒法等[2],其中消毒液消毒包括甲醛熏蒸、环氧乙烷消毒、过氧乙酸消毒等,在所有的消毒液中甲醛最为常用,但甲醛熏蒸残留难以完全去除,对人体健康有相当的危害性。
臭氧消毒方法中因臭氧为强氧化剂,可损坏多种物品,浓度越高对物品损害越大,可使铜片出现绿色锈斑,可使橡胶老化、变脆、断裂,使织物漂白变色。
另外,臭氧杀菌作用受到pH值、温度、湿度的影响,空气中臭氧浓度>0.2 mg/m3时对人体有一定伤害[3]。
采用优洁消毒,既能达到空间消毒效果,亦能避免对人体的危害性。
1优洁消毒试剂简介优洁,主要成分为30%六亚甲基四胺(复合醛类、醛类衍生物)+11%复配季铵盐。
其使用方便,性能稳定,安全无毒,可生物降解,不污染环境。
彻底杀灭细菌、真菌、芽孢和病毒的原理为季铵盐改变细胞膜的通透性,使醛类衍生物进入微生物内部,在通过细胞膜的过程中获得能连释放小分子醛基,使细胞质变性,完成杀菌过程,同时变性的细胞质包裹细胞核,使得遗传物质无法传递给下一代,避免了抗药性的产生。
2消毒条件与周期验证用消毒浓度为1%优洁溶液。
本次验证的洁净厂房为小容量注射剂车间,空气洁净等级为C级和D级。
在洁净厂房车间改造后、进行设备、设施的大修或连续生产1个月情况下,需进行优洁空间喷雾消毒。
3验证用设备、物料电动喷雾器、纯化水、优洁、量筒、紫外分光光度计、浮游菌采样器4消毒步骤4.2消毒验证实施4.2.1关闭空调机组风机系统,按照10 mL/m3的喷雾量对洁净区各个房间区域进行喷雾消毒,喷雾对象为洁净区设备、墙面、地面,顺序为由高到低,由里到外。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
C48
Q 无锡优洁科技有限公司企业标准
Q/3202 YJ 001-2014
代替Q/3202 YJ001-2012
优洁®消毒液
2014-06-28发布 2014-06-28 实施
无锡优洁科技有限公司发布
Q/3202 YJ 001-2014
前言
本标准代替Q/3202YJ 001-2012。
本标准与前版标准相比作了如下修改:
——增加原料卫生质量要求;
——原料中季铵盐改为季铵盐(苯扎溴铵);
——增加杀灭微生物指标及试验方法。
本标准按GB/T1.1-2009《标准化工作导则第1部分:标准的结构和编写》编写。
本标准由无锡优洁科技有限公司提出并起草。
本标准主要起草人:孙雯。
本标准于2006年02 月首次发布;于2009年02月第一次修订;于2012年02月第二次修订;于2014年6月28日第三次修订。
Q/3202 YJ 001-2014
优洁®
消毒液
1范围
本标准规定了优洁®消毒液的原料卫生质量要求、要求、试验方法、检验规则、标志、使用说明书、包装、运输、贮存。
本标准适用于以六亚甲基四胺、季铵盐(苯扎溴铵)为主要原料,辅以聚山梨脂80、纯净水配制而成的优洁®消毒液(以下简称产品)。
用于环境、一般物体表面和织物的消毒。
2规范性引用文件
下列文件对于本文件中的应用是必不可少的。
凡是注日期的引用文件,仅注日期的版本适用于本文件。
凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件:GB/T 191-2008 包装储运图示标志
GB 17323-1998 瓶装饮用纯净水
GB 27952-2011 普通物体表面消毒剂的卫生要求
JJF 1070-2008 定量包装商品含量计量检验规则
国家质量技术监督检验检疫总局【2005】第75号令《定量包装商品计量监督管理办法》《中华人民共和国药典》2010年版二部
卫生部《消毒技术规范》2002年版
卫生部《消毒产品检验规定》2003年版
卫生部《消毒产品标签说明书管理规范》2005年版
卫生部《消毒产品生产企业卫生规范》2009年版
3 原料卫生质量要求
3.1 六亚甲基四胺为工业级,纯度≥99%。
3.2 季铵盐(苯扎溴铵)为医药级,纯度≥95%。
3.3 聚山梨脂80为医药级,纯度≥99%。
3.4 纯净水应符合GB17323的要求。
4 要求
4.1 感官指标
产品为透明澄清液体,振摇时能产生大量泡沫,具有产品固有气味。
4.2 理化指标
产品理化指标应符合表1的要求。
4.3 杀灭微生物指标
杀灭微生物指标应符合表2规定。
1
Q/3202 YJ 001-2014
表2 杀灭微生物指标
4.4 包装密封性
产品包装应密封。
4.5 净含量允差
应符合《定量包装商品计量监督管理办法》的规定。
5 试验方法
5.1 感官指标
取试样适量,倾倒于50ml的比色管中,在自然光线下或充足的灯光下目测、鼻嗅;试样移入有盖瓶内振摇,观察应有泡沫。
5.2 理化指标
5.2.1 六亚甲基四胺含量
5.2.1.1 试剂
0.25mol/L硫酸标准溶液;
甲基红指示液;
0.5mol/L氢氧化钠标准溶液。
5.2.1.2 操作步骤
精密移取优洁®消毒液1.0ml置锥形瓶,加水10ml溶解,精密加硫酸标准溶液20ml摇匀,加热煮沸至不再发生甲醛臭,随时加近沸的水补足蒸发的水分,放冷至室温,加甲基红指示液2滴,用氢氧化钠标准溶液滴定,并将滴定结果用不含六亚甲基四胺,其余成分相同的对照进行空白试验校正。
5.2.1.3 计算
六亚甲基四胺含量X1按式(1)计算:
X1 = C NaOH ×(V- V样) ×C H2SO4 ×140.16×10-3×100% (1)
式中:
X1—六亚甲基四胺含量,%;
C NaOH、C H2SO4—氢氧化钠与硫酸标准溶液的实际浓度;
V空白—空白消耗的氢氧化钠体积,ml;
V样—样品消耗的氢氧化钠体积,ml。
5.2.2 季铵盐(苯扎溴铵)含量
5.2.2.1 试剂
氢氧化钠溶液——4.3g氢氧化钠加入100ml蒸馏水溶解;
溴酚蓝指示剂——0.1g溴酚蓝加0.05mol/L氢氧化钠3ml溶解,再加蒸馏水200ml;
氯仿(AR);
2
0.02mol/L四苯硼钠标准溶液。
5.2.2.2 操作步骤
精密移取优洁®消毒液1.0ml至250ml碘量瓶中,加蒸馏水50ml与氢氧化钠试液1ml,摇匀,加溴酚蓝指示液0.4ml与氯仿10ml充分振荡后,用四苯硼钠滴定液滴定,接近终点用力振荡至氯仿层蓝色消失,记录四苯硼钠滴定液用量,重复测2次。
取不含季铵盐(苯扎溴铵),而其余成分均相同的样品作空白对照。
5.2.2.3 计算
季铵盐(苯扎溴铵)含量X2按式(2)计算:
X2(%)=C×(V样-V空)×0.3984×100% (2)
式中:
X2—季铵盐(苯扎溴铵)含量,%;
V样—样品消耗的标准溶液量,ml ;
V空—空白消耗的标准溶液量,ml。
5.2.3 pH值
按《消毒技术规范》 (2002版)中 2.2.1.4方法进行。
5.2.4 稳定性指标
按《消毒技术规范》 (2002版)中的2.2.3.2.1的方法进行。
5.3 杀灭微生物指标
按卫生部《消毒技术规范》 2002年版中2.1.1.5.5、2.1.1.7.4、 2.1.2.8和2.1.2.10的方法进行。
5.4 包装密封性
取3个包装完好的产品,倒置3min无内容物漏出。
5.5净含量允差
按JJF1070的规定进行。
6 检验规则
6.1 检验分类
检验分出厂检验和型式检验。
6.2 出厂检验
产品经公司检验部门检验合格后并附合格证方可出厂。
出厂检验项目为:感官指标、有效成分含量、pH值、包装密封性和净含量。
6.3 型式检验
6.3.1下列情况之一时,应进行型式检验:
a)新产品鉴定时;
b)生产工艺、原材料有较大改变时;
c)正常生产一年以上时;
d)停产半年以上恢复生产时。
6.3.2 型式检验项目为要求中全部项目。
3
6.4 组批与抽样
组批应符合《消毒产品生产企业卫生规范》(2009年版)的规定。
型式检验应以出厂检验合格的产品中随机抽取,抽样量按卫生部《消毒产品检验规定》2003年版的规定执行,型式检验项目为本标准的全项目。
6.5 判定规则
产品经检验,检验项目合格,则该批产品或该次型式检验合格;如有不合格项,允许自同批产品中加倍取样,对不合格项进行复检,复检结果仍不合格,则判该批产品或该次型式检验不合格。
7 标志(签)、使用说明书、包装运输贮存
7.1 标志(签)、使用说明书
标签和使用说明书应符合卫生部《消毒产品标签说明书管理规范》的规定;外包装并应有符合GB/T191的图示标志。
7.2 包装
7.2.1销售包装采用洁净的塑料瓶(桶);包装规格为(ml/瓶):30、50、60、80、100、120、200、230、250、300、500、1000、2000、2500、5000、10000、30000。
7.2.2运输包装采用瓦楞纸箱。
7.3 运输
运输过程应避免高温和冻结。
7.4 贮存
应贮存在阴凉、干燥、通风的仓库内。
7.5 有效期
产品在上述贮运条件下,包装完好的产品有效期为24个月。
4。
