氯乙烯 分子轨道
第一章聚氯乙烯(桑永主编)

第⼀章聚氯⼄烯(桑永主编)第⼀章聚氯⼄烯第⼀节概述Polyvinyl chloride [,p ?l ?'va ?n(?)l] ['kl ??ra?d]聚氯⼄烯(PVC)是以氯⼄烯为单体聚合⽽得的聚合物,⾃上世纪30年代⾸先在德国开始⼯业化⽣产以来,由于它原料来源丰富,⽤途⼴泛,在通⽤塑料中⼀直占有重要地位,其产量在塑料中仅次于聚⼄烯居第⼆位。
氯⼄烯单体(vinyl chloride monomer, ['m ?n ?m ?]简称VCM )其分⼦结为:PVC 树脂特点:化学稳定性好,⼒学性能⾼,电⽓绝缘性优良,难燃⾃熄,纯净的PVC 具有透明性。
但热稳定性差,使⽤温度不⾼,硬质制品的脆性较⼤、不耐寒,在光和热的作⽤下易⽼化的缺点。
PVC 塑料是以PVC 树脂为基体,加⼊各种塑料助剂制备⽽成的多组分塑料。
通过改变配⽅可制得软、硬程度不同及多种功能的塑料材料和制品,在农业、建筑、化⼯、电⽓、机械和⽇常⽣活中有⼴泛⽤途。
第⼀节聚氯⼄烯的合成⼀、氯⼄烯单体1.⼄炔电⽯法是最早实现⼯业化⽣产的⽅法,具有投资少、技术简单、产品纯度⾼的优点。
其反应如下:氯化氢可以从由电解⾷盐得到,⼄炔可由碳化钙(电⽯)与⽔反应制得。
由于电⽯是由⽯灰⽯煅烧⽽得,故能耗⼤、成本⾼,因⽽该法应⽤已逐渐减少。
近⼏年由于⽯油短缺,该法⼜有所发展。
2.联合法由⽯油裂解制得的⼄烯经氯化后⽣成⼆氯⼄烷,然后在加压条件下将其加热裂解制得氯⼄烯和氯化氢,⽣成的氯化氢再与⼄炔反应⼜可得到氯⼄烯。
该法可直接利⽤氯碱⼯业的氯⽓,因此成本较⼄炔电⽯法低。
其化学反应式如下:⼆、氯⼄烯单体的聚合1.悬浮聚合(1)概念:悬浮聚合体系主要由单体、引发剂、⽔、分散剂四个基本组分构成。
原料加⼊反应釜中,在⼀定的温度和压⼒下聚合⼀定时间。
(2)⽣产过程:聚合后的悬浮液碱液处理洗涤⼲燥过筛⽩⾊粉状PVC 树脂(3)注意的问题:聚合过程中“粘釜”现象会造成相对分⼦质量过⾼的组分,在树脂中不易塑化⽽使透明制品出现晶点,影响制品质量。
氯乙烯的生产—生产原料及产品的认知

氯乙烷 /(mg/kg)
≤20
二氯化物 /(mg/kg)
≤2
水 /(mg/kg)
≤60
HCl /(mg/kg)
≤1
含 Fe /(mg/kg)
≤0.5
项目六 氯乙烯的生产
石油化工产品生产技术
及
任 务 二
产 品 的 认
生 产 原 料
知
知识点1:氯乙烯的基本性质和主要用途
1.基本性质
又名乙烯基氯,是一种应用于高分子化工的重要单体,简称VCM(VC)。 化学式C2H3Cl,氯乙烯在常温常压下是一种无色的有乙醚香味的气体,沸 点259.3K,稍加压力,就可得到液体的氯乙烯。 容易液化,易溶于丙酮、乙醇和烃类,微溶于水。 易燃、空气中爆炸极限范围是4~22%(v), 有毒,主要危害肝脏;对人体具有麻醉作用,在20~40%的浓度下,会 使人立即致死,在10%的浓度下,一小时内呼吸管内由急而逐渐缓慢,最后 微弱以致停止呼吸。人对氯乙烯的嗅觉感知的浓度为2.4g/m3,空气中氯乙 烯最高允许浓度为30mg/m3。慢性中毒会使人有晕眩感觉,同时对肺部有 刺激,因此,氯乙烯在空气中的允许含量为500µL/m3。
及
任 务 二
产 品 的 认
生 产 原 料
知
知识点2:主要原料及产品的工业规格要求
1.原料的工业规格要求
乙烯法生产氯乙烯工艺的主要原料是乙烯、氧气和氯气,一般原料规格见表7-1。
序号 1 2
3
表7-1 原料规格
原料 乙烯 氯气
氧气
控制项目 纯度 纯度 水 纯度
氮气+氩气 水
规格 ≥99% ≥90% ≤1×10-5 ≥99.6% ≤0.4% ≤50×10-6
氯乙烯

氯乙烯是一种应用于高分子化工的重要的单体,可由乙烯或乙炔制得。
为无色、易液化气体,沸点-13.9℃,临界温度142℃,临界压力5.22MPa。
氯乙烯是有毒物质,肝癌与长期吸入和接触氯乙烯有关。
它与空气形成爆炸混合物,爆炸极限4%~22%(体积),在压力下更易爆炸,贮运时必须注意容器的密闭及氮封,并应添加少量阻聚剂。
溶解性:微溶于水,溶于乙醇、乙醚、丙酮等多数有机溶剂。
主要用途:用作塑料原料及用于有机合成,也用作冷冻剂等氯乙烯可通过以下方法制取:乙烯氧氯化法:1. 乙烯与氯气在三氯化铁催化下加成生成1,2-二氯乙烷:CH2=CH2 + Cl2 → ClCH2CH2Cl2. 精制后的1,2-二氯乙烷发生裂解,生成氯乙烯和氯化氢:ClCH2CH2Cl → CH2=CHCl + HCl3. 以载于氧化铝上的氯化铜作催化剂,副产物乙烯、空气及氯化氢反应生成1,2-二氯乙烷和水:CH2=CH2 + 2 HCl + ½ O2 → ClCH2CH2Cl +H2O4. 精制后的二氯乙烷于管式炉中裂解为氯乙烯和氯化氢,副产物氯化氢继续成为第三步中的反应物。
5. 另一个副产物氯乙烷从蒸馏中回收,用作麻醉剂。
6. 乙炔与氯化氢在氯化汞存在下于180 °C发生加成反应,得到氯乙烯。
管理信息操作管理:密闭操作,全面通风。
操作人员必须经过专门培训,严格遵守操作规程。
建议操作人员佩戴过滤式防毒面具(半面罩),戴化学安全防护眼镜,穿防静电工作服,戴防化学品手套。
远离火种、热源,工作场所严禁吸烟。
使用防爆型的通风系统和设备。
防止气体泄漏到工作场所空气中。
避免与氧化剂接触。
在传送过程中,钢瓶和容器必须接地和跨接,防止产生静电。
搬运时轻装轻卸,防止钢瓶及附件破损。
配备相应品种和数量的消防器材及泄漏应急处理设备。
储存管理:储存于阴凉、通风的库房。
远离火种、热源。
库温不宜超过30℃。
应与氧化剂分开存放,切忌混储。
采用防爆型照明、通风设施。
简要说明氯乙烯的工业生产方法和特点

1. 简要说明氯乙烯的工业生产方法和特点。
氯乙烯的工业生产方法主要有3种:电石法、乙烯氧氯化法及二氯乙烷/氯乙烯(EDC/VCM)法。
氯乙烯化学特性:氯乙烯又名乙烯基氯(Vinyl chloride)是一种应用于高分子化工的重要的单体,可由乙烯或乙炔制得。
为无色、易液化气体,沸点-139C, 临界温度142C,临界压力5.22MPa。
氯乙烯是有毒物质,肝癌与长期吸入和接触氯乙烯有关。
它与空气形成爆炸混合物,爆炸极限4%〜22%(体积),在压力下更易爆炸,贮运时必须注意容器的密闭及氮封,并应添加少量阻聚剂。
氯乙烯的物理特性:氯乙烯(CH2=CHCI)无色气体,易液化。
沸点-134C。
微溶于水,溶于乙醇、乙醚。
有毒性,长期吸入或接触可致肝癌。
燃烧时火焰边缘微绿。
与空气形成爆炸性混合物,爆炸极限4〜22%(体积)。
可发生加成反应。
在引发剂(如有机的过氧化物或偶氮化合物)作用下发生加聚反应,生成聚氯乙烯(PVC)塑料。
还可以与某些不饱和化合物共聚成为改善某些性能的改性品种。
如与醋酸乙烯酯的共聚物,用于制造薄膜、涂料、塑料地板、唱片、短纤维等;又如与偏二氯乙烯CCl2=CH2的共聚物具有无毒、透明、防腐等特性,可用于制渔网,座垫织物、滤布、包装薄膜等,商品名莎纶、合成1,1, 2-三氯乙烷等。
工业上用乙炔与氯化氢于汞盐作用下加成,或由乙烯氯化后热解生成氯化氢和氯乙烯、二氯乙烷热裂解等方法制得。
2■简述乙炔法生产氯乙烯的基本原理,并写出主副反应方程式。
乙炔法生产氯乙烯一.乙炔、HCl的生产仁乙烘的生产3C+CaO——>CaC2+CO—112Kcal/mol (反应温度:1700~1900度)CaC2+H2O——> CH 三CH+Ca(OH)2 湿法:3OOl/kg电石2 .乙烘性质:、爆炸极限:25〜80% (空气中)a. HC1的生产H2+C12 ⑴化>2HCl+44Kcal.乙炔加HCI反应机理早CIl2=CIICl+29,8Kcal △ G=—60.35KJ/molCH= CH+ HgC12——>CH=CH—HgClClCH2=CHCl+HgC12 副反应:HCl过量:CH2=CHC1+HC1——>CH3CHC12 乙烘过量:CII=CH—HgCl+HgCh——>CIHg—CH—CH—HgClCl ClAA——>CH=CH+Hg2C12Cl Cl3■在乙炔生产VCM过程中,对原料的纯度有何要求?1) 一般要求:乙炔纯度>=98.5%氯化氢纯度>=94%2) 工业采用浸硝酸银试纸在乙炔样气中不变色,为合格标准3) —般原料气含水分<=0.06%,能满足生产需要。
氯乙烯生产工艺流程

氯乙烯生产工艺流程
《氯乙烯生产工艺流程》
氯乙烯是一种重要的化工原料,广泛应用于塑料、橡胶、涂料和溶剂等领域。
其生产工艺流程通常包括氢氯酸盐法和乙烯氯化法两种主要方法。
氢氯酸盐法是一种将氯化氢和乙烯在催化剂的作用下反应生成氯乙烯的方法。
首先,将氯化氢与乙烯在催化剂的作用下进行氢氯酸盐反应,生成氢氯酸盐。
然后,通过裂解反应将氢氯酸盐分解成氯乙烯和氯化氢。
整个过程需要在高温和高压下进行,且需要催化剂的存在来促进反应的进行。
乙烯氯化法是一种将乙烯气体与氯气在催化剂的作用下反应生成氯乙烯的方法。
首先,将乙烯气体和氯气混合后,经过催化剂的催化作用,发生氯化反应,生成氯乙烯。
此方法相比氢氯酸盐法更简单,但需要使用氯气作为原料,而氯气对环境和人体健康有一定的危害。
在整个氯乙烯生产工艺流程中,需要考虑原料的选择、反应条件的控制、催化剂的选择和催化剂的再生等诸多方面的问题。
同时,要重视环保和安全生产,控制溢漏和排放,减少环境污染和安全事故的发生。
在未来,随着化工技术的发展和环保要求的提高,氯乙烯生产工艺流程可能会朝着更加环保、安全和高效的方向发展,为减少资源消耗和环境污染做出更大的贡献。
氯乙烯
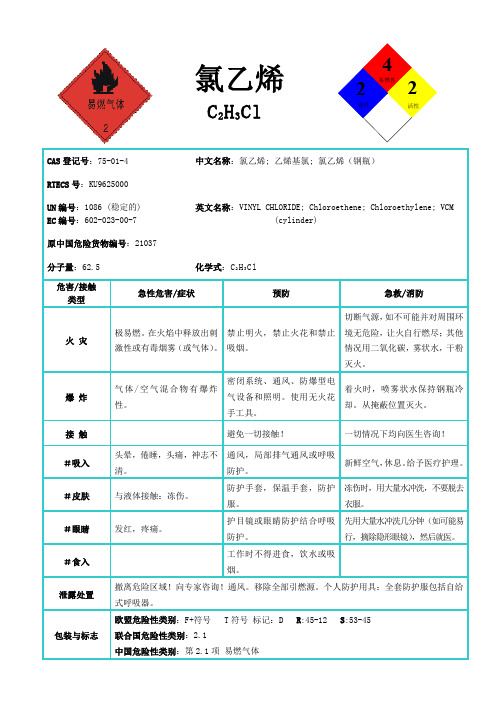
发红,疼痛。
护目镜或眼睛防护结合呼吸防护。
先用大量水冲洗几分钟(如可能易行,摘除隐形眼镜),然后就医。
#食入
工作时不得进食,饮水或吸烟。
泄露处置
撤离危险区域!向专家咨询!通风。移除全部引燃源。个人防护用具:全套防护服包括自给式呼吸器。
包装ቤተ መጻሕፍቲ ባይዱ标志
欧盟危险性类别:F+符号T符号标记:DR:45-12S:53-45
氯乙烯
C2H3Cl
CAS登记号:75-01-4
中文名称:氯乙烯;乙烯基氯;氯乙烯(钢瓶)
RTECS号:KU9625000
UN编号:1086 (稳定的)
EC编号:602-023-00-7
英文名称:VINYL CHLORIDE; Chloroethene; Chloroethylene; VCM
(cylinder)
环境数据
该物质可能对环境有危害,对地下水应给予特别注意。
注解
根据接触程度,需定期进行医疗检查。超过接触限值时,气味报警不充分。不要在火焰或高温表面附近或焊接时使用。添加稳定剂或阻聚剂会影响该物质的毒理学性质。向专家咨询。
物理危险性:气体比空气重,可能沿地面流动,可能造成远处着火。氯乙烯单体蒸气未经阻聚可能在储槽通风口或阻火器生成聚合物,导致通风口堵塞。
化学危险性:在特定条件下,该物质能生成过氧化物,引发爆炸性聚合。加热和在空气、光、催化剂、强氧化剂和金属铜和铝的作用下,该物质容易发生聚合,有着火或爆炸危险。燃烧时,该物质分解生成氯化氢、光气有毒和腐蚀性烟雾。有湿气存在时,浸蚀铁和钢。
原中国危险货物编号:21037
分子量:62.5
化学式:C2H3Cl
危害/接触
类型
氯乙烯的生产方法、生产原理

氯乙烯的生产方法、生产原理1生产方法按其所用原料可大致分为下列几种:⑴乙烯法此法系以乙烯为原科,可通过三种不同途径进行,其中两种是先以乙烯氯化制成二氯乙烷:C2H4 + Cl2 → C2H4Cl2然后从二氯乙烷出发,通过不同方法脱掉氯化氢来制取氯乙烯;另一种则直接从乙烯高温氯化来制取氯乙烯。
现分述如下:①二氯乙烷在碱的醇溶液中脱氯化氢(也称为皂化法)C2H4Cl2+ NaOH → C2H3Cl + NaCl + H2O此法是生产氯乙烯最古老的方法。
为了加快反应的进行,必须使反应在碱的醇溶液小进行。
这个方法有严重的缺点:即生产过程间歇,并且要消耗大量的醇和碱,此外在生产二氯乙烷时所用的氯,最后成为氯化钠形式耗费了,所以只在小型的工业生产中采用。
②二氯乙烷高温裂解C2H4Cl2→ C2H3Cl + HCl这个过程是将二氯乙烷蒸气加热到600℃以上时进行的,与此同时,还发生脱掉第二个氯化氢生成乙炔的反应,结果使氯乙烯产率降低。
为了提高产率,必须使用催化剂。
所用的催化剂为活性炭、硅胶、铝胶等,反应在480~520℃下进行,氯乙烯产率可达85%。
③乙烯直接高温氯化这一方法不走二氯乙烷的途径,直接按下式进行:C2H4 +Cl2→ C2H3Cl + HCl由上式可以看出这一反应是取代反应,但实际上乙烯与氯在300℃以下主要是加成反应,生成二氯乙烷。
要想使生成氯乙烯的取代反应成为唯一的反应,则必须使温度在450℃以上,而要避免在低温时的加成过程,可以采用将原科单独加温的方法来解决,但在高温下反应激烈,反应热难以移出,容易发生爆炸的问题。
目前一般用氯化钾和氯化锌的融熔盐类作裁热体,使反应热很快移出。
此法主要的缺点是副反应多,产品组成复杂,同时生成大量的炭黑,反应热的移出还有很多困难,所以大规模的工业生产还未实现。
⑵乙炔法这一方法是以下列反应为基础的:C2H2+ HCl → C2H3Cl其生产方法又可分为液相法和气相法。
氯乙烯单体聚合—高分子化学基础

聚乙烯
HHHHHH CCCCCC HHHHHH
聚丙烯
HH HH HH CC CC CC H CH 3 H CH 3 H CH 3
碳链高分子
聚乙二醇
HH HH HH CCOCCOCCO HH HH HH
尼龙—6
HHHHHHO NCCCCCC
HHHHH
杂链高分子
聚二甲基硅氧烷
CH 3 Si O CH 3
链增长反应
头-尾结构 头-头结构 尾-尾结构
链终止反应
偶合终止 歧化终止
反应特点
自由基反应由引发、增长、终止、转移等基元反应。引发速率最小,是控制总 聚合速率的关键。可概括为: 慢引发、快增长、速终止,易转移。
只有链增长反应才使聚合度增加。无中间体,体系中只有单体和聚合物组成。 延长反应时间主要提高转化率,对分子量影响较小,凝胶效应将使分子量增加。 少量(0.01 % ~ 0.1 %)阻聚剂足以使自由基聚合反应终止。
聚乙烯
6~30
涤纶
1.8~2.3 天然橡胶
聚氯乙烯 5~15
尼龙-66 1.2~1.8 丁苯橡胶
聚苯乙烯 10~30
维呢纶
6~7.5
顺丁烯胶
分子量
20~40 15~20 25~30
一个大分子往往是由许多相同的、简单的结构单元通过共价键重复连接而成。 例如:聚苯乙烯n CH2 CHCH-CH-CH2-CH-CH2-CH
不能气化
溶液粘度大
难溶,先溶胀
01
03
05
02
04
物理力学性能,加工性能较好 有一定强度和弹性。 有较高的强度、弹性,可做材料使用,可抽丝,或制成薄膜。
(1)弹性:当高聚物Tg(玻璃化)<TR(室温)<Tf(粘流化),高聚物处于高弹态,而且 差值越大其性能越好。 (2)塑性:当高聚物Tg>TR.高聚物处于玻璃态。用做材料时可做塑料。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
氯乙烯分子轨道
氯乙烯是一种有机化合物,化学式为C2H3Cl。
它的分子结构中含有一个氯原子和两个碳原子,分子中的碳原子间有一个双键。
在分子轨道理论中,可以通过对分子的原子轨道进行线性组合来获得分子的分子轨道。
对于氯乙烯分子,可以考虑两个碳原子和一个氯原子上的原子轨道。
碳原子上有一个p轨道和一个sp轨道,氯原子上有一个3p轨道。
这些原子轨道可以通过线性组合形成一组分子轨道。
在氯乙烯中,p轨道和sp轨道可以组合成两个σ键轨道和两个π键轨道。
其中,σ键轨道是在两个原子之间形成的轨道,π键轨道则是在双键上方和下方形成的轨道。
氯原子的3p轨道与碳原子的p 轨道可以组合成两个π反键轨道,它们位于双键上方和下方,对双键的形成具有抑制作用。
通过分子轨道理论的分析,可以发现氯乙烯的分子结构中存在着一个双键和两个单键。
在这些键的形成过程中,σ键轨道和π键轨道起到了关键的作用。
另外,反键轨道也对分子的性质产生了一定的影响。
分子轨道理论为我们理解分子结构和化学性质提供了一种有力的工具。
- 1 -。
