维生素的分析
食品分析理论第十章 维生素的测定_OK

• 1、微生物法:根据某种维生素是某种细菌生长所必需的原理,以细 菌繁殖程度或代谢产物定量该维生素含量,方法选择性较高,多用 于水溶性维生素检测,适用于检测多种衍生物的总和(如总叶酸), 是经典方法。但微生物法操作繁琐、耗时过长,而且要求有特殊设 备和专门的训练人员。
• 2、比色法 可见分光光度、紫外分光光度
2021/7/3
16
(二)测定方法
• 维生素D的测定方法有:比色法、荧光法、紫外分光 光度法、气相色谱法、液相色谱法及薄层层析法等。
• 比色法灵敏度较高,但操作十分复杂、费时。
• 气相色谱法虽然操作简单,精密度也高,但灵敏度 低,不能用于含微量维生素D的样品。
• 液相色谱法的灵敏度比比色法高20倍以上,且操作简 便,精度高,分析速度快。是目前分析维生素D的最 好方法。
2021/7/3
14
• 胡萝卜素一般存在于植物性食品中,以含有胡萝卜为食物家 禽、兽类、水产动物及其加工产品,为着色而添加胡萝卜素 的食品,也含有胡萝卜素。
• 胡萝卜素对热及酸、碱比较稳定,但紫外线和空气中的氧可 促进其氧化破坏。用有机溶剂从食物中提取。
• 胡萝卜素本身是一种色素,在450nm波长处有最大吸收。胡 萝卜素常与叶绿素、叶黄素等共存,在测定前,必须将胡萝 卜素与其它色素分开。常用的方法有纸层析、柱层析和薄层 层析法,下面介绍的是纸层析法。
• ②、操作时加入乙酰氯可以消除温度的影响,可使 灵敏度比仅用三氯化锑提高约3倍。并可减少部分甾 醇的干扰。
• ③、此法不能区分D2和D3测定值是两者的总量。
2021/7/3
18
B、高效液相色谱法
• 1、原理 • 试样经皂化后,用苯提取不皂化物,馏去苯后,使用第一阶段的分
维生素的鉴别方法

维生素的鉴别方法
维生素的鉴别方法可以通过以下几种途径进行:
1. 外观和颜色:观察维生素的外观形态和颜色,不同种类的维生素往往有特定的外观形态和颜色,可以通过对照已知的维生素来进行初步的鉴别。
2. 荧光试验:有些维生素在紫外光的照射下会发出特定的荧光,可以通过荧光特点来确定维生素的种类。
3. 溶解性试验:将维生素溶解在不同的溶剂中,观察其溶解情况和溶液的颜色变化,不同种类的维生素在不同的溶剂中具有不同的溶解性和颜色,可以通过对照已知的维生素来判断。
4. 化学反应试验:维生素在特定条件下可以发生一些特定的化学反应,通过对维生素溶液进行特定的化学处理,观察反应结果可以鉴别维生素的种类。
5. 仪器分析方法:利用像高效液相色谱、气相色谱、质谱等仪器分析方法,可以对维生素进行准确的定性和定量分析。
需要注意的是,维生素的鉴别方法需要综合使用多种手段,并结合已知的维生素信息来进行判断。
同时,在实际操作过程中也需要注意对照样品的选择和实验条
件的控制,以确保准确鉴别维生素的种类。
维生素类药物的分析方法

(3)维生素A在光照下产生的无活性的聚合物:鲸醇。 (4)维生素A的异构体等: 以上这些杂质在 310nm~340nm 的波长范围内有吸收, 所以干扰维生素A的测定。
12
5. 合成的维生素A和天然鱼肝油中的维生素A均为酯式
维生素A,如供试品中干扰测定的杂质较少,能符合下 列第一法测定的规定时,可用溶剂溶解供试品后直接 进行测定,否则应按第二法,经皂化提取除去干扰后 测定。
pH不同的溶液,在247nm处分别测定差示吸收值
(ΔA)。以浓度C为横坐标,以差示吸收值ΔA为纵坐 标绘制标准曲线。
30
样品的测定 取本品20片,精密称定,研细。精密称取适量粉末,
(2)反应介质需无水 (3)温度对呈色强度的影响很大 ( 4)本反应并非维生素 A专属,在相同条件下,某些有关物质均与
三氯化锑显蓝色,干扰测定,常使测定结果偏高。
( 5 )三氯化锑试剂有强的腐蚀性,易损坏皮肤和仪器,使用时应 严加注意。
15
(三)高效液相色谱法
采用RP-HPLC法同时测定人血清中维生素 A和维生素E的含量。 根据不同病理生理状态下人血清中维生素A、E的浓度,寻求弄清 与某些疾病的关系,为临床治疗学、营养学等研究提供参考。 1. 仪器与色谱条件 色 谱 柱 为 C18 ; 流 动 相 为 甲 醇 - 水 ( 96:4 ) ; 流 速 为 1.2ml/min。内标物为维生素A醋酸酯。 2. 分析用样品液 对照品:维生素A,维生素E,维生素A醋酸酯
维生素类药物的分析方法:
生物法 微生物法 化学法 物理化学法
2
第一节
维生素A的分析
维生素A 包括
药物分析 第十四章 维生素类药物的分析

第一节 维生素A的分析
➢紫外吸收:共轭多烯醇侧链结构,在325-328nm之间有最大 吸收,可用于鉴别。
H3C
CH3
9
CH3
7
8
6
5 4
CH3
3 1CH2OR
2
CH3
第一节 维生素A的分析
λmax 相对生物效价
维生素A 新维生素Aa 新维生素Ab 新维生素Ac 异维生素Aa 异维生素Ab
325.5 328 320.5 310.5 323 324
1 325nm, 2 310nm, 3 334nm
第一节 维生素A的分析
合成的或天然的维生素A 均为酯式维生素A, 根据供试品中干扰杂质的多少,可采用:
(1)直接测定法 (2)皂化法
4. 测定方法
(1)基本步骤
A选择,A328测定或A328校正
求 % 1cm(样)
% 1cm(样)
A C(%) l
= + 0.04
A32校 8 正 3.522A328 A316 A340 3.5220.6280.5610.523
0.605
第一节 维生素A的分析
f A328(校正) A328100% A328
3.7%(15%~ 3%)
标 示% 量 A3C2(g8校 /1正 0m 01)l900平 标均 示丸 量重 10% 0
(一)Carr-Price反应 与三氯化锑呈色反应
Vit A
SbCl3
蓝色
CHCl3(无水无醇)
紫红色
第一节 维生素A的分析
+
CH2
蓝色
+
CH2
紫红
第一节 维生素A的分析
条件: 无水、无醇
药物分析 第09章 维生素类药物的分析

ChP 片剂、注射剂
g/100ml
E11c%m = 421 A = ECL
(每片)相当于标示量的%=
E 1 1c % A m 10W 0稀 1 释 平 标 度 均 示 1 片 量 0% 0
g
稀释倍数 稀1释度
规格 g/片
(三) 硅钨酸重量法
1、 重量法特点
准确度高 灵敏度低 操作繁琐 设备简单
(三) 其他反应
S元素反应
V iN t B a N O P a H A b S c P b
HA N O3 g N AO g 白 C N H N lH H OO
K 2 HH + 4 g I淡[黄 B ]H 2H4g
I 2 H + K I 红 [B 色 ]H I2 I
硅 H 钨 + 酸白
色[B]2SiO2OH2
12WO 34H2O
苦 H +酮 酸 白 色 扇 形
橙红色
强氧化剂
H3C
CH3 O
O O
H3C HO
HNO3
CH3 O
CH3
CH3 C16H33
生育酚
CH3 C16H33
生育红(橙红色)
(二) 三氯化铁-联吡啶反应
VitE
K△OH
生育酚
Fe 3
[O]
对 生育醌
Fe 2 联吡啶 红色
H3C
CH3 O
CH3 C16H33
2×337.27
3479.22
换 算 2 因 M V数 i1t B 233 .27 70.19 M 沉淀34.2729
3、 测定方法
维生素测定质谱法

维生素测定质谱法
维生素测定质谱法是一种利用质谱仪技术对维生素进行定量分析的方法。
质谱法是一种依据质量-电荷比(m/z)比较物质的质谱图和相应目标物质的质谱图之间的峰面积或峰高比来进行定量分析的方法。
维生素测定质谱法的优点包括高灵敏度、高选择性和准确性。
它可以在非常低浓度下对维生素进行定量分析,并可以区分不同的维生素类别。
此外,质谱法还可以通过多级质谱(MS/MS)技术对目标物质进行进一步的结构解析和定性分析。
然而,维生素测定质谱法也有一些限制。
首先,它需要精确的标准品或内标物质来建立定量分析的标准曲线。
其次,质谱仪设备和操作要求相对较高,需要专业人员进行操作和数据解析。
此外,维生素样品的前处理和样品制备也可能对分析结果产生影响。
药物分析-14维生素类药物的分析
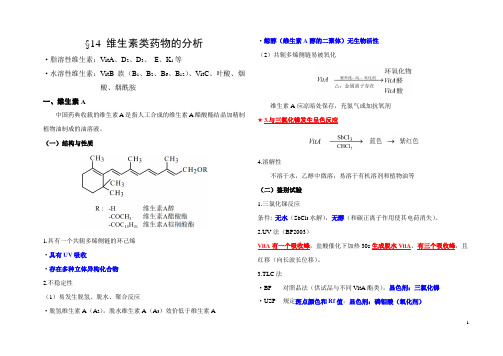
§14 维生素类药物的分析·脂溶性维生素:VitA、D2、D3、E、K1等·水溶性维生素:VitB族(B1、B2、B6、B12)、VitC、叶酸、烟酸、烟酰胺一、维生素A中国药典收载的维生素A是指人工合成的维生素A醋酸酯结晶加精制植物油制成的油溶液。
(一)结构与性质1.具有一个共轭多烯侧链的环己烯·具有UV吸收·存在多种立体异构化合物2.不稳定性(1)易发生脱氢、脱水、聚合反应·脱氢维生素A(A2),脱水维生素A(A3)效价低于维生素A ·鲸醇(维生素A醇的二聚体)无生物活性(2)共轭多烯侧链易被氧化维生素A应凉暗处保存,充氮气或加抗氧剂★3.与三氯化锑发生呈色反应4.溶解性不溶于水,乙醇中微溶;易溶于有机溶剂和植物油等(二)鉴别试验1.三氯化锑反应条件: 无水(SbCl3水解),无醇(和碳正离子作用使其电荷消失)。
2.UV法(BP2003)VitA有一个吸收峰,盐酸催化下加热30s生成脱水VitA,有三个吸收峰,且红移(向长波长位移)。
3.TLC法·BP 对照品法(供试品与不同VitA酯类),显色剂:三氯化锑·USP 规定斑点颜色和Rf值,显色剂:磷钼酸(氧化剂)12(三)含量测定 ★1.三点校正法 (1)原理①杂质的吸收在310~340nm 波长范围内呈一条直线,且随波长的增大吸收度减小;②物质对光的吸收具有加和性。
(2)波长的选择λ1为VitA 的λmax ;λ2、λ3为分别在λ1的两侧各选一点 ①等波长差法——VitA 醋酸酯nm 12340316328=∆λλλλ,、、)2(52.3340316328328A A A A --=(校正)②等吸收比法——VitA 醇33431032576A A A == 334310325325260.4555.2815.6A A A A --=(校正)(3)测定方法①直接测定法(等波长差法)——高纯度维生素A 醋酸酯 Ⅰ核对λmax/329~326max 328改用造化法与规定值比较求否是−→−−→−∈A A nm i λ Ⅱ计算吸收度比及比值差规定吸光度比值-328/A A iⅢ判断差值是否超过±0.02,确定用A 或A 校正%15%3)3%%,15(]%3,%3[32802.032832832802.0计算用改用皂化法<或>计算用计算用、计算无超过(校正)(校正)有超过A f f A f A f f A −−−−→−→-+→--∈→+-∈→−−−−→−±±)2(52.3340316328328A A A A --=(校正)%100328328328⨯-=A A A f (校正)Ⅳ求(样品)%11cm E lc AE cm ⨯=)%(%11(样品)·注意:(纯品)(样品)%11%11cm cm E E ≠,c 为混合样品的浓度。
维生素产品实验报告

1. 掌握滴定法测定维生素C含量的原理和方法。
2. 了解维生素产品中维生素C含量的测定方法及其应用。
3. 提高实验操作技能,培养严谨的实验态度。
二、实验原理维生素C(抗坏血酸)是一种水溶性维生素,具有抗氧化、提高免疫力、促进生长发育等作用。
本实验采用2,6-二氯酚靛酚滴定法测定维生素产品中维生素C的含量。
该方法基于维生素C具有还原性,可以将2,6-二氯酚靛酚(氧化剂)还原成无色产物,通过滴定终点颜色变化判断维生素C的含量。
三、实验仪器与试剂1. 仪器:电子分析天平、滴定装置、锥形瓶、研钵、漏斗、容量瓶等。
2. 试剂:2%草酸溶液、1%草酸溶液、标准维生素C溶液、0.1%2,6-二氯酚靛酚溶液、待测维生素产品等。
四、实验步骤1. 准备工作:称取一定量的待测维生素产品,置于研钵中研磨成粉末,准确称取0.1g左右放入锥形瓶中。
2. 样品提取:向锥形瓶中加入10ml 2%草酸溶液,充分振荡,使维生素C充分溶解。
3. 滴定:向锥形瓶中加入1ml 0.1%2,6-二氯酚靛酚溶液,用标准维生素C溶液进行滴定。
滴定过程中,观察锥形瓶内溶液颜色变化,当颜色由蓝绿色变为淡红色时,停止滴定。
4. 计算结果:根据消耗的标准维生素C溶液体积,计算待测维生素产品中维生素C的含量。
五、实验结果与分析1. 实验结果:通过滴定实验,测得待测维生素产品中维生素C的含量为x mg/g。
2. 结果分析:实验结果显示,待测维生素产品中维生素C含量较高,符合产品标签标示的含量。
1. 实验过程中,应注意操作规范,确保实验结果的准确性。
2. 滴定过程中,观察颜色变化要准确,避免误判滴定终点。
3. 实验过程中,2,6-二氯酚靛酚溶液的浓度对滴定结果有较大影响,应严格控制溶液浓度。
4. 实验结果表明,本实验方法可以有效地测定维生素产品中维生素C的含量。
七、结论本实验采用2,6-二氯酚靛酚滴定法测定维生素产品中维生素C的含量,实验操作简便,结果准确。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
VitA
↓
CH 2
去水VitA(VitA3)
(三) TLC法 BP 对照品法 显色剂 三氯化锑
三、含量测定
目前各国药典均采用紫外分光光度法替 代三氯化锑比分子中具
多烯共轭体系结构,在325~328nm处 有选择性吸收峰,故可进行含量测定。
立体异构体 氧化产物及光照产物 均对测定 有干扰,
合成中间体
去氢维生素A( VitA2) 去水维生素A( VitA3)
故采用三
点校正法
1:测定原理,三个波长的吸收度,公 式计算校正吸收度,再计算含量。故
得名。该法的依据:
① 杂质的吸收在310~340nm波长范围 内呈一条直线,且随波长的增大吸收
• 3)换算因子: • 4)A值的选择: a.计算吸收度比值:与中国药典的吸收度比值相比 较,判断每个差值的绝对值是否超过0.02。 b.判断法 最大吸收波长在326-329nm之间,且5个波长下的 绝对值差值均不超过0.02时,可直接用328nm波 长处的测得的吸收度值求得吸收系数。
最大吸收波长在326-329nm之间,计算5个波长下 的绝对差值,如果有一个或几个超过0.02,应按 以下的方法进行判断: 若(A328校正-A328)*100%/A328 所得的数值在 ±3.0%,则仍不用校正公式计算吸收度。可直接 用A328代入E=A/C.L 若(A328校正-A328)*100%/A328 所得的数值 在-15.0%到-3.0%,则应用A328校正代入E=A/C.L 若(A328校正-A328)*100%/A328 所得的数值在小于 -15%或大于+3%,则不能用本法测定,应使用第 二法。
二、鉴别试验 (一) 三氯化锑反应
VitA 蓝色 紫红
CHCl3
SbCl 3
条件 无水无醇
蓝色
紫红
(二) UV法
VitA 去水VitA △
无水乙醇-盐酸溶液溶解
300-400nm扫描
300-400nm扫描
λmax为326nm
一个吸收峰
384、367、389nm
如果最大吸收波长不在326-329nm之间,也 不能用本法测定。采用第二法 第一法的校正公式为: A328校正=3.52(2 A328 –A316-A340)
(2)第二法(皂化法,适用于维生素A醇)
• 1)方法 精密称取一定量的供试品,加KOH乙醇溶 液后煮沸回流,得到的皂化液再经过提取、 洗涤、滤过、浓缩和干燥等处理,最后用 异丙醇溶解残渣并稀释成每1ml中含维生素 A为9-15个国际单位数的溶液,在300、310、 325、334nm波长处测定吸收度,并确定最 大吸收波长(应为325nm)。 • 2)计算 同第一法。见书p250-251
3)A值的选择
如果最大吸收波长在323-327nm之间, 且A300 /A325比值≤0.73,按下法判断: a. 若(A325校正-A325)*100%/A325 所得的数值的绝 对值在3%,可直接用A325 代入E=A/C.L b.若(A325校正-A325)*100%/A325 所得的数值的绝 对值超过3%,则用应用A325校正代入E=A/C.L 如果最大吸收波长不在323-327nm之间, 或A300/A325比值>0.73,表示供试品中杂质含量太高, 应采用色谱法将未皂化部分纯化再进行测定。
度减小;
② 物质对光的吸收具有加和性。
2 波长的选择:最大吸收波长,及两侧各 选一波长
① 第一法(等波长差法) 1 =328nm,
2 =316nm, 3 =340nm,△ =12nm VitA的max(328nm) Ch.P用于测定维生素A醋酸酯
② 第二法(等吸收比法)
分别在1的两侧各选一点
4.测定方法
(1)第一法(直接测定法,适用于纯度高的维生素 A醋酸酯环己烷溶解) • 1)方法 在300、316、328、340、 360nm测吸收 度 • 2)计算 A 1% 1% E1cm A为A 328或为A 328校正 a.吸光系数E 1cm
Cl
b.求效价(IU/g):效价指每g供试品所含维生素 的A的国际单位数。IU/g= E1% 1cm 1900 c.求维生素A醋酸酯占标示量的百分含量 A D 1900 W 标示量(%) 100% W 100 L 标示量
维生素A醇 维生素A醋酸酯 维生素A棕榈酸酯
一、 结构与性质 (一)为一个具有共轭多烯醇侧链的 环己烯 具有UV吸收 存在多种立体异构化合物 天然维生素A主要是反式
易发生脱氢生成去氢维生素A2
易脱水生成去水维生素A3
易聚合反应生成无活性维生素A
(二) 共轭多烯侧链 易被氧化
第二法的校正公式: A325校正=6.815 A325 –2.555A310-4.260A334
VitA
紫外线、 O2、氧化剂
环氧化物
VitA醛 VitA酸
△或有金属离子存在时更易氧化
环氧化物
VitA醛
VitA酸
(三) 、与三氯化锑发生呈色反应
VitA 蓝色 紫红
CHCl3
SbCl 3
(四) 、溶解性
不溶于水 易溶于有机溶剂和植物油等
A 2 = A3 =6/7A 1 1= 325nm, 2=310nm, 3 =334nm
Ch.P用于测定维生素A醇
3. 杂质的吸收 • 对V.A有影响的杂质主要有以下几种: • (1) V.A2 和V.A3 • (2)维生素A的氧化产物 • (3) 维生素A在光照下产生的无活性的聚合物 • (4)维生素A的异构体等。 以上这些杂质在310nm-340nm的波长范围内有吸 收,干扰维生素A的测定。
概
维生素:
述
是维持人体正常代谢机能所 必需的 微量营养物资。 人体不能合成维生素。
分类
按溶解度分
VitA、D2、D3、 E、K1 等
脂溶性
水溶性 VitB族(B1、B2、B6、B12)
VitC、叶酸、烟酸、泛酸等。
本章仅对维生素(A、B1、C、 E)进行学习讨论
第一节 维生素A
R:
-H -COCH3 -COC15H31
