红氧化铁中国药典检验标准
红氧化铁检验操作规程

红氧化铁检验操作规程红氧化铁(Fe2O3)是一种广泛应用于化学分析和实验室研究的常见试剂。
它主要用于检测水样中的铁含量,以及作为染料、催化剂等领域的重要原料。
下面是一份红氧化铁检验操作规程,希望对您有所帮助。
一、实验器材和试剂准备1. 实验器材:- 电子天平- 热风干燥箱- 聚乙烯瓶或玻璃瓶- 称量纸- 玻璃棒或玻璃滴管- 蒸馏水2. 试剂准备:- 红氧化铁试剂(Fe2O3)- 浓盐酸(HCl)- 浓硫酸(H2SO4)二、实验操作步骤1. 样品处理:- 将待测样品(如水样)倒入聚乙烯瓶或玻璃瓶中。
- 加入适量的浓盐酸,使样品中的铁离子转化为可溶性的铁酸盐。
- 用蒸馏水稀释样品,使其达到适合检测的浓度。
2. 红氧化铁溶液制备:- 称取适量的红氧化铁试剂,用称量纸精确称量。
- 将红氧化铁试剂加入聚乙烯瓶或玻璃瓶中。
- 加入少量的浓硫酸,将红氧化铁试剂溶解。
- 用蒸馏水稀释至适当浓度的红氧化铁溶液。
3. 反应和测定:- 取一定体积的样品溶液(如10ml)加入试管中。
- 加入一定体积的红氧化铁溶液(如1ml),并用玻璃棒或玻璃滴管充分混合。
- 将试管置于热风干燥箱中,进行干燥处理,使反应物充分反应生成可称重的化合物。
- 取出试管后,放置至室温,然后使用电子天平称量试管质量。
- 计算样品中铁的含量,根据称量前后的质量差异和样品的浓度。
4. 结果分析:- 根据实验所得数据,计算出样品中铁的含量。
- 将结果与相关标准进行比较,判断样品中铁的含量是否符合规定要求。
- 将实验结果记录在实验记录本中。
三、注意事项1. 实验过程中需佩戴实验手套、护目镜等个人防护设备,确保实验操作的安全。
2. 使用浓盐酸和浓硫酸时要小心,避免与皮肤或衣物接触,注意通风。
3. 在实验室中进行干燥处理时,遵循相应的操作规程,确保干燥箱的安全使用。
4. 确保所有试剂、器材和溶液的准确测量和标记,避免误用和混淆。
5. 实验结束后,将废液和废品妥善处理,保持实验环境的整洁和安全。
氧化铁红生产
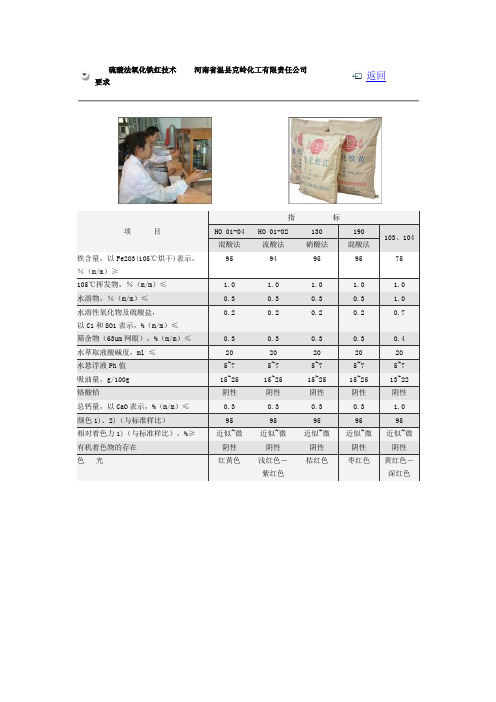
硫酸法氧化铁红技术要求 河南省温县克岭化工有限责任公司返回项 目 指 标HO 01-04 HO 01-02 130 190 103、104混酸法流酸法 硝酸法 混酸法 铁含量,以Fe2O3(105℃烘干)表示, %(m/m )≥ 9594959575105℃挥发物,%(m/m )≤ 1.0 1.0 1.0 1.0 1.0 水溶物,%(m/m )≤ 0.3 0.3 0.3 0.3 1.0 水溶性氧化物及硫酸盐, 以C1和SO1表示,%(m/m )≤ 0.20.20.20.20.7筛余物(63um 网眼),%(m/m )≤ 0.3 0.3 0.3 0.3 0.4 水萃取液酸碱度,m l ≤ 20 20 20 20 20 水悬浮液Ph 值 5~7 5~7 5~7 5~7 5~7 吸油量,g/100g 15~25 15~25 15~25 15~25 13~22 铬酸铅阴性 阴性 阴性 阴性 阴性 总钙量,以CaO 表示,%(m/m )≤ 0.3 0.3 0.3 0.3 1.0 颜色1)、2)(与标准样比) 95 95 95 95 95 相对着色力1)(与标准样比),%≥ 近似~微 近似~微 近似~微 近似~微 近似~微 有机着色物的存在 阴性 阴性 阴性 阴性 阴性 色 光红黄色浅红色- 紫红色桔红色枣红色黄红色- 深红色河北省鹿泉市金龙氧化铁颜料氧化铁红产品名称:氧化铁红 Iron oxide red1.产品概述:是一种无机彩色颜料, 为鲜红色粉末,粉粒细腻。
具有较高的遮盖力和较强的着色力,以及良好的分散性,它的耐光性、耐候性都很好。
2.用途:广泛应用于彩色水泥、建材、橡胶、油漆等领域。
3.储运条件:存放于干燥处,勿使受潮,避免高温,并与酸碱物隔离。
按上述保管条件,未拆包装的产品有效贮存期为三年4.包装:25公斤/袋,外编内塑。
5.使用说明:建议用量:铁红1~2公斤,水泥50公斤,水适量。
(如需加沙子100公斤。
氧化铁检测相关标准

氧化铁检测相关标准氧化铁,别名烧褐铁矿、烧赭上、铁丹、铁红、红粉、威尼斯红(主要成分为氧化铁)、三氧化二铁等。
化学式Fe2O3,溶于盐酸,为红棕色粉末。
其红棕色粉末为一种低级颜料,工业上称氧化铁红,用于油漆、油墨、橡胶等工业中,可做催化剂,玻璃、宝石、金属的抛光剂,可用作炼铁原料。
(001)(14.02.12)用途:用于油漆、橡胶、塑料、建筑等的着色,是无机颜料,在涂料工业中用作防锈颜料。
用作橡胶、人造大理石、地面水磨石的着色剂,塑料、石棉、人造革、皮革揩光浆等的着色剂和填充剂,精密仪器、光学玻璃的抛光剂及制造磁性材料铁氧体元件的原料等。
用于电子工业、通讯整机、电视机、计算机等磁性原料及行输出变压器、开关电源及其高U及高UQ等的铁氧体磁芯用作分析试剂、催化剂和抛光剂,也用于颜料的配料;用于各类药片、药丸的外衣糖衣着色用用作磁性材料、颜料及制取还原剂、抛光剂、催化剂等;用于药片糖衣和胶囊等的着色用作防锈漆的颜料。
因该品制成的云母氧化铁防锈漆抗水渗性好,防锈性能优异,可以取代红丹食用红色素。
日本用于赤豆饭、魔芋粉食品。
对曾用防腐剂处理果柄切口的香蕉加以识别时用。
美国多用于猫食、狗食和包装材料无机红色颜料主要用于硬币的透明着色,也用于油漆、油墨和塑料的着色广泛用于油漆、橡胶、塑料化妆品、建筑精磨材料、精密五金仪器、光学玻璃、搪瓷、文教用品、皮革、磁性合金和高级合金钢的着色;主要用作磁性材料、颜料、擦光剂、催化剂等,还用于电讯、仪表工业;主要用作磁性材料、颜料、擦光剂、催化剂等,还用于电讯、仪表工业无机红色颜料。
检测标准:GB/T16484.21-2009氯化稀土、碳酸轻稀土化学分析方法第21部分:氧化铁量的测定1,10-二氮杂菲分光光度法GB/T18114.7-2010稀土精矿化学分析方法第7部分:氧化铁量的测定重铬酸钾滴定法GB/T1863-2008氧化铁颜料GB/T1871.2-1995磷矿石和磷精矿中氧化铁含量的测定容量法和分光光度法GB/T24244-2009铁氧体用氧化铁GB/T3286.4-2012石灰石及白云石化学分析方法第4部分:氧化铁含量的测定邻二氮杂菲分光光度法和火焰原子吸收光谱法HG/T2249-1991氧化铁黄颜料HG/T2250-1991氧化铁黑颜料HG/T2574-2009工业氧化铁HG/T3006-1986云母氧化铁HG/T3006-2012云母氧化铁颜料HG/T4354-2012常温氧化铁脱硫剂硫容试验方法HY/T163-2013海水水处理剂分散性能的测定分散氧化铁法JB/T7948.5-1999熔炼焊剂化学分析方法磺基水杨酸光度法测定氧化铁量SJ/T10383-2013软磁铁氧体用氧化铁SJ/T10898-1996电子玻璃中氧化铁和二氧化钛的分光光度分析SL237-20067-1999游离氧化铁试验(附条文说明)SN/T0829-1999出口镁砂中的氧化镁、氧化硅、氧化钙、氧化铁、氧化铝、氧化锰、氧化钛的测定X射线荧光光谱法SN/T3323.1-2012氧化铁皮第1部分:氧化亚铁的测定重铬酸钾滴定法SN/T3323.2-2012氧化铁皮第2部分:硫含量的测定高频燃烧红外线吸收法SN/T3323.3-2012氧化铁皮第3部分:铅、铬、镉元素测定电感耦合等离子体原子发射光谱法SN/T3323.4-2012氧化铁皮第4部分:砷、汞元素测定原子荧光光谱法SN/T3323.5-2012氧化铁皮第5部分:总铁及硅、钙、磷、锰、铝、钛和镁元素测定X射线荧光光谱法SN/T3323.6-2013氧化铁皮第6部分:散装氧化铁皮手工取样方法。
红砖中氧化铁成分的检验 陈慧

疑问? 有学生提出一个新问题:工业盐酸 中常常含有Fe3+,怎样保证Fe3+ 不是盐酸中带来的?
验证步骤: 取一个点滴板,滴入的药品如下图
Hcl、水 KSCN KSCN、 水 KSCN、水、 红砖溶液
无色
无色
红色
实验结论
通过以上实验,说明溶液中含 有Fe3+,进而说明原红砖中含 有Fe2O3
方案二: 取红砖样品,用稀盐酸溶解、 过滤,取上层清液2ml于试管中, 滴加NaOH溶液,若溶液显红褐色 沉淀,证明溶液中有Fe3+,说明 红砖中有氧化铁成分。
取一个点滴板滴入的药品如下图hcl水kscn无色kscnkscn水红砖溶液无色红色实验结论通过以上实验说明溶液中含有fe进而说明原红砖中含有fe方案二
红砖中氧 化铁成分 的检验
一、实验探究
实验探究的目的: a.运用Fe3+的检验方法,探究红砖 中是否含有氧化铁; b.实验条件的控制 1.提出问题:砖是人们日常生活中 常见的物质,同是用粘土烧制的 砖,为什么有的是红色有的却是 青色?红砖中红色的物质是什么?
②根据反应原理选择仪器、药品和实 验装置。 仪器:烧杯、玻璃棒、试管、 胶头滴管 药品:红砖样品、稀盐酸、KS上,再将一张 纸覆盖在红砖的上方,用锤子敲击少 量红砖,并尽量将其敲碎成粉末,易 于溶解。 2、取一个干净的烧杯,在烧杯中放 入少量经敲碎的红砖粉末,加入25ml 的6mol/L的盐酸搅拌使其溶解。 3、向烧杯中滴加2-3滴KSCN溶液。 若溶液显红色,则说明红砖中的红物 质可能含有三价铁离子
6.反思与评价:由于不注意实验条件 的控制,方案一可能失败。可以 说,探寻、控制实验的最佳条件, 是化学实验成功的关键。方案二 中当粘土中存在Ca2+、Al3+、 Mg2+等干扰离子,且Fe3+浓度 过低时,不宜用NaOH溶液检验。
赤铁粉检测报告

赤铁粉检测报告(原创实用版)目录一、赤铁粉检测报告概述二、赤铁粉的性质与特点三、赤铁粉的检测方法四、赤铁粉检测报告的意义五、结论正文一、赤铁粉检测报告概述赤铁粉,又称氧化铁,是一种常见的红色铁矿石。
赤铁粉广泛应用于冶金、化工、建材等行业。
为了确保赤铁粉的质量和性能,对其进行检测是必不可少的环节。
本文旨在介绍赤铁粉检测报告的相关内容,帮助读者更好地了解赤铁粉的检测过程和结果。
二、赤铁粉的性质与特点赤铁粉的主要成分是氧化铁(Fe2O3),具有以下特点:1.颜色:赤铁粉呈红褐色,颜色鲜艳。
2.结构:赤铁粉为细粉末状,颗粒分布均匀。
3.磁性:赤铁粉具有磁性,能够被磁铁吸附。
4.硬度:赤铁粉的硬度较低,一般为 5-6 莫氏硬度。
5.密度:赤铁粉的密度约为 5.24 克/立方厘米。
三、赤铁粉的检测方法赤铁粉的检测主要包括以下方面:1.化学成分分析:通过化学方法,测定赤铁粉中氧化铁的含量以及其他元素的含量。
2.物理性能检测:包括赤铁粉的粒度、比表面积、磁性等性能的检测。
3.矿物相分析:通过 X 射线衍射(XRD)等方法,分析赤铁粉的矿物组成。
4.环保检测:检测赤铁粉中重金属元素、有害物质的含量,评估其对环境的影响。
四、赤铁粉检测报告的意义赤铁粉检测报告对于矿山企业、生产企业、贸易公司等具有重要意义:1.指导生产:检测报告可以帮助企业了解赤铁粉的质量,从而调整生产工艺,提高产品质量。
2.确保产品性能:检测报告可以帮助企业确保赤铁粉的性能满足生产要求。
3.贸易交货:检测报告是贸易交货的重要依据,有助于避免因质量问题引发的贸易纠纷。
4.环保监管:检测报告有助于政府部门对赤铁粉生产过程中的环境污染进行监管。
五、结论赤铁粉检测报告对于赤铁粉的生产、贸易和使用具有重要意义。
氧化铁红标准

759#高纯氧化铁红分子式:Fe2O3分子量:159.60用途:本产品主要用于电子工业、通讯整机、电视机、计算机等磁性原料及行输出变压器、开关电源及其高μ、高Q、高μQ等高性能、高稳定性的铁氧体磁芯用,属磁性材料行业的专用原料。
性能:外观呈棕红色粉末,视比重约0.9g/cm3,熔点为1565℃,品型为100%的α型、不溶于水易溶于盐酸中,本品有磁性材料生产所忌杂质少、纯度高、化学性能好、粒度均匀、分散性能优异等特点。
质量标准:参照日本JIS K1642-1981Fe2O3≥99.2 SiO2%≤0.01 CaO %≤0.01MgO %≤0.01Al2O3%≤ 0.01 K2O %≤0.02 Na2O %≤0.02 FeO %≤0.04水溶盐%≤0.02晶粒度≤0.5μm757#氧化铁红分子式:Fe2O3分子量:159.60用途:本产品主要用于电子工业,通讯整机、计算机、电视机等中等性能要求的磁芯,代替昂贵氧化铁。
本品属磁性材料行业专用原料。
性能:外观呈玫瑰红粉末,视比重约1g/cm3,品型为α型、不溶于水,本品有磁性材料生产所忌杂质少、纯度高、化学活性好、利于分散等优良特点。
质量标准:Fe2O3%≥99.4SiO2%≤0.015 CaO %≤0.02MgO %≤0.02K2O %≤0.01 Na2O %≤0.03 FeO %≤0.04水溶盐%≤0.02晶粒度≤0.5μm190#氧化铁红分子式:Fe2O3分子量:159.60用途:本产品主要用于制造、油漆、涂料行业,也可用于电子工业、通讯整机、计算机、电视机等中低等性能要求的磁芯。
性能:外观呈玫瑰红粉末,视比重约1g/cm3,品型为α型、不溶于水,本品有磁性材料生产所忌杂质少、纯度高、化学活性好、利于分散等优良特点。
质量标准:Fe2O3%≥96含水量%≤1 水溶盐%≤0.3细度%(320目湿筛残余物)≤0.28602#氧化铁黑分子式:Fe3O4分子量:213.54用途:本产品主要用于制造油漆、油墨、颜料等制品,马赛克、人造大理石的着色,也可用于磁性材料、涂料录音带、金属探伤等工业领域。
红氧化铁检验操作规程

红氧化铁检验操作规程1. 引言本文档旨在规范红氧化铁的检验操作流程,以确保检验工作的准确性和规范性。
红氧化铁是一种常见的无机颜料,广泛应用于建筑、涂料、陶瓷等领域。
通过对红氧化铁进行检验,可以评估其质量及合格性,为相关产品的生产和应用提供可靠参考。
2. 检验设备和材料准备2.1. 检验设备包括:•分析天平•研钵•滤纸•试剂瓶•恒温水槽•离心机2.2. 检验材料包括:•红氧化铁样品•水•试剂:硫酸、硝酸、亚硝酸钠、氨水、盐酸、铁离子指示剂等。
3. 检验操作步骤3.1. 样品制备和振荡•取适量红氧化铁样品并称重,记录样品质量。
•将红氧化铁样品置于研钵中,加入适量水,使得样品浸没在水中。
•使用玻璃棒搅拌样品,直到样品彻底分散。
3.2. 确定红氧化铁含铁量•取适量样品溶液,将其过滤,收集滤液。
•将滤液放入恒温水槽中,加热至50°C。
•添加硝酸、亚硝酸钠和盐酸试剂,进行还原反应。
•使用铁离子指示剂,滴定还原后的溶液,记录消耗的滴定液体积。
•根据滴定液体积计算样品中红氧化铁的含量。
3.3. 检验评估•将检验结果与标准要求进行对比,判断样品是否合格。
•根据实际情况,评估红氧化铁的性能和质量,并形成检验报告。
4. 安全注意事项•在操作过程中,严禁直接接触试剂,应采取适当的防护措施。
•对于可燃或有毒的试剂,应在通风良好的环境中操作,并采取相应的安全措施。
•操作过程中,尽量避免产生气溶胶,以免对操作者和实验环境造成污染和危害。
5. 结论本文档详细描述了红氧化铁检验的操作规程,包括样品制备、溶液处理、滴定等步骤。
通过规范的检验操作,可确保红氧化铁的质量评估准确可靠,为相关领域的产品生产和应用提供参考依据。
在进行检验时,务必遵守安全注意事项,确保操作人员的人身安全和实验室环境的安全。
2020版《中国药典》铁盐检验操作规程

一、目的:制订详尽的工作程序,规范检验操作,保证检验数据的准确性。
二、范围:本标准适用于样品铁盐的测定。
三、职责:1、 检验员:严格按操作规程操作,认真、及时、准确地填写检验记录;2、 化验室负责人:监督检查检验员执行本操作规程。
四、内容:1、原理:该发系利用硫氰酸盐在酸性溶液中与供试品溶液中的三价铁盐生成红的可溶性硫氰酸铁的配位化合物,与一定量标准铁溶液用同法处理后进行比色。
2、试剂:2.1稀盐酸(含HCl 为9.5%~10.5%):取盐酸234ml,加水稀释至1000ml 。
2.2过硫酸铵(AR )2.3 30%硫氰酸铵溶液:取硫氰酸铁铵30g ,加水溶解使成100ml 。
2.4标准铁溶液:称取硫酸铁铵[FeNH 4(SO 4)2·12H 2O]0.863g ,置1000ml 量瓶中,加水溶解后,加硫酸2.5ml ,用水稀释至刻度,摇匀,作为贮备液。
临用前,精密量取贮备液10ml ,置100ml 量瓶中,加水稀释至刻度,摇匀,即得(每1ml 相当于10ug 的Fe )。
3、仪器:纳氏比色管(50ml )、刻度吸管(5ml ,A 级) 4、操作过程:4.1除另有规定外,取各品种项下规定量的供试品,加水溶解使成25ml ,移置50ml 纳氏比色管中,加稀盐酸4ml 与过硫酸铵50mg ,用水稀释使成35ml 后,加30%硫氰酸铵溶液3ml ,再加水适量稀释成50ml ,摇匀;如显色,立即与标准铁溶液一定量制成的对照溶液(取该品种项下规定量的标准铁溶液,置50ml 纳氏比色管中,加水使成25ml ,加稀盐酸4ml 与过硫酸铵50mg ,用水稀释使成35ml ,加30%硫氰酸铵溶液3ml ,再加水适量稀释成50ml ,摇匀)比较,即得。
3.2如供试管与对照管色调不一致时,可分别移至分液漏斗中,各加正丁醇20ml 提取,俟分层后,将正丁醇层移置 50ml 纳氏比色管中,再用正丁醇稀释至25ml ,比较即得。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
红氧化铁
Hong Yanghuatie
Red Ferric Oxide
Fe2O3159.69
[1309-37-1] 本品按炽灼至恒重后计算,含Fe2O3不得少于98.0%。
【性状】本品为暗红色粉末,无臭,无味。
本品在水中不溶,在沸盐酸中易溶。
【鉴别】取本品约0.1g,加稀盐酸5ml,煮沸冷却后,溶液显铁盐的鉴别反应(附录Ⅲ)。
【检查】水中可溶物取本品2.0g,加水100ml,置水浴上加热回流2小时,滤过,滤渣用少量水洗涤,合并滤液与洗液,置经105℃恒重的蒸发皿中,蒸干,在105℃干燥至恒重,遗留残渣不得过10mg(0.5%)。
酸中不溶物取本品2.0g,加盐酸25ml,置水浴中加热使溶解,加水100ml,用经105℃恒重的4号垂熔坩埚滤过,滤渣用盐酸溶液(1→100)洗涤至洗液无色,再用水洗涤至洗液不显氯化物的反应,在105℃干燥至恒重,遗留残渣不得过6mg(0.3%)。
炽灼失重取本品约1.0g,精密称定,在800℃炽灼至恒重,减失重量不得过4.0%。
钡盐取本品0.2g,加盐酸5ml,加热使溶解,滴加过氧化氢试
液1滴,冉加10%氢氧化钠溶液20ml,滤过,滤渣用水10ml洗涤,合并滤液与洗液,加硫酸溶液(2→10) 10ml,不得显浑浊。
铅盐取本品2.5g,置100ml具塞锥形瓶中,加0.1mol/L盐酸溶液35ml,搅拌1小时,滤过,滤渣用0.1mol/L盐酸溶液洗涤,合并滤液与洗液置50ml量瓶中,加0.1mol/L盐酸溶液稀释至刻度,摇匀,作为供试品溶液。
照原子吸收分光光度法(附录Ⅳ D),在217.0nm的波长处测定。
另取标准铅溶液2.5ml,置50ml量瓶中,加1mol/L盐酸溶液5ml,加水稀释至刻度,摇匀,同法测定。
供试品溶液的吸光度不得大于对照溶液(0.001%)。
砷盐取本品0.67g,加盐酸7ml,加热使溶解,加水21ml,滴加酸性氯化亚锅试液使黄色褪去,依法检查(附录ⅧJ第一法),应符合规定(0. 0003%)。
【含量测定】取本品约0.15g,精密称定,置具塞锥形瓶中,加盐酸2.5ml,置水浴上加热使溶解,加过氧化氢试液1ml,加热至沸数分钟,加水25ml,放冷,加碘化钾1.5g与盐酸2.5ml,密塞,摇匀,在暗处静置15分钟,用硫代硫酸钠滴定液(0.1mol/L)滴定,至近终点时加淀粉指示液2.5ml,继续滴定至蓝色消失。
每1ml硫代硫酸钠滴定液(0.1mol/L)相当于7. 985mg昀Fe2O3。
【类别】药用辅料,着色剂和包衣材料等,
【贮藏】密封保存。
