探究铁钉生锈的原因的实验报告
铁生锈条件实验报告

一、实验目的本实验旨在探究铁生锈的条件,分析铁生锈的原理,并验证影响铁生锈速度的因素。
二、实验原理铁生锈是铁与氧气和水发生氧化还原反应的过程。
在潮湿的环境中,铁与氧气和水充分接触,铁逐渐被氧化,生成铁锈。
实验中,通过控制变量法,探究不同条件下铁生锈的速度。
三、实验材料1. 实验器材:铁钉、试管、蒸馏水、植物油、干燥剂氯化钙、棉花、剪刀、镊子、秒表等。
2. 实验试剂:无。
四、实验步骤1. 将铁钉清洗干净,用剪刀将棉花剪成适当大小,放入试管底部。
2. 分别设置三个实验组,如下:(1)实验组A:在试管中加入适量蒸馏水,将铁钉完全浸入水中。
(2)实验组B:在试管中加入适量蒸馏水,将铁钉下半部分浸入水中,上半部分浸入植物油中。
(3)实验组C:将干燥剂氯化钙放入试管底部,然后将铁钉放入试管中,塞上棉花,用橡皮塞密封试管。
3. 同时开始计时,观察三个实验组铁钉生锈的情况,记录生锈时间。
五、实验结果与分析1. 实验组A:铁钉在水中生锈速度较快,约需5天时间。
2. 实验组B:铁钉下半部分在水中生锈,上半部分在植物油中未生锈,约需7天时间。
3. 实验组C:铁钉未生锈,试管内氯化钙吸收了水分,保持干燥。
分析:1. 实验组A结果表明,铁钉在水中容易生锈,说明铁与氧气和水充分接触时容易生锈。
2. 实验组B结果表明,铁钉下半部分在水中生锈,而上半部分在植物油中未生锈,说明植物油可以隔绝氧气,减缓铁生锈速度。
3. 实验组C结果表明,干燥剂氯化钙可以吸收水分,保持试管内干燥,从而防止铁生锈。
六、结论1. 铁生锈的条件是铁与氧气和水充分接触。
2. 植物油可以隔绝氧气,减缓铁生锈速度。
3. 保持干燥可以防止铁生锈。
七、实验讨论1. 实验过程中,为何铁钉在水中生锈速度较快?答案:铁钉在水中与氧气和水充分接触,铁逐渐被氧化,生成铁锈。
2. 实验过程中,为何植物油可以减缓铁生锈速度?答案:植物油可以隔绝氧气,使铁钉与氧气接触减少,从而减缓铁生锈速度。
探究铁钉生锈的原因的实验报告

一、实验目的通过本实验,探究铁钉生锈的原因,分析影响铁钉生锈的各种因素,并探讨有效的防锈措施。
二、实验原理铁钉生锈是铁与氧气和水发生化学反应的结果。
在潮湿的空气中,铁钉表面会形成一层氧化膜,即铁锈。
铁锈的生成是一个电化学腐蚀过程,涉及到电子的转移。
三、实验器材1. 铁钉(若干)2. 玻璃瓶(若干)3. 水(蒸馏水)4. 植物油5. 盐(食盐)6. 干燥剂(无水氯化钙)7. 橡皮塞8. 纱布9. 秒表10. 记录本四、实验步骤1. 准备实验材料:将铁钉、玻璃瓶、水、植物油、盐、干燥剂等实验材料准备好。
2. 实验分组:将铁钉分为四组,分别编号为A、B、C、D。
3. 实验组A:将铁钉放入玻璃瓶中,加入蒸馏水,使铁钉完全浸没在水中,密封瓶口。
4. 实验组B:将铁钉放入玻璃瓶中,加入蒸馏水,使铁钉部分浸没在水中,部分裸露在空气中,密封瓶口。
5. 实验组C:将铁钉放入玻璃瓶中,加入蒸馏水,使铁钉完全浸没在水中,滴加少量植物油,密封瓶口。
6. 实验组D:将铁钉放入玻璃瓶中,加入蒸馏水,使铁钉部分浸没在水中,部分裸露在空气中,滴加少量植物油,密封瓶口。
7. 对照组:将铁钉放入玻璃瓶中,加入蒸馏水,使铁钉完全浸没在水中,加入少量盐,密封瓶口。
8. 观察记录:将四个玻璃瓶放置在相同的环境中,每天观察铁钉的生锈情况,并记录数据。
五、实验现象1. 实验组A:铁钉完全浸没在水中,生锈速度较慢。
2. 实验组B:铁钉部分浸没在水中,部分裸露在空气中,生锈速度较快。
3. 实验组C:铁钉完全浸没在水中,滴加植物油,生锈速度较慢。
4. 实验组D:铁钉部分浸没在水中,部分裸露在空气中,滴加植物油,生锈速度较慢。
5. 对照组:铁钉完全浸没在水中,加入盐,生锈速度最快。
六、实验结论1. 铁钉生锈的主要原因是铁与氧气和水发生化学反应。
2. 铁钉部分浸没在水中,部分裸露在空气中时,生锈速度较快。
3. 滴加植物油可以减缓铁钉的生锈速度。
4. 在水中加入食盐可以加快铁钉的生锈速度。
铁钉生锈实验报告

铁钉生锈实验报告一、实验介绍铁钉生锈是我们生活中常见的现象之一,但是你知道铁钉为什么会生锈吗?本次实验旨在通过模拟真实环境中的条件,探究铁钉生锈的原因。
二、实验材料1. 铁钉:我们选择了三个相同材质和规格的铁钉作为实验样品。
2. 水:我们将使用自来水作为实验中的溶液。
三、实验步骤1. 准备工作:将三个铁钉清洁干净,以确保实验结果的准确性。
2. 分组操作:将三个铁钉分为三组,每组的铁钉数量相等。
3. 实验条件设置:- 组一:将铁钉放置于常温且湿度较高的室内环境。
- 组二:将铁钉放置于常温但相对湿度较低的室内环境。
- 组三:将铁钉浸泡在水中。
4. 实验观察与记录:- 每隔一天,观察并记录铁钉表面的变化情况。
- 记录实验进行的天数。
四、实验结果及分析通过实验观察与记录,我们得到了如下结果:在组一,铁钉表面开始出现少量氧化斑点,随着实验天数的增加,这些斑点逐渐扩大并蔓延。
经过五天的观察,铁钉几乎整个表面都被覆盖了。
这是因为常温且湿度较高的环境中,空气中的水分与铁钉表面的氧气反应,形成了铁的氧化物,即生锈的产物。
组二的观察结果显示,铁钉表面的生锈现象相对较少。
在相对湿度较低的环境下,由于水分供应有限,铁钉的氧化速度大大降低,导致生锈现象不明显。
相比之下,组三中浸泡在水中的铁钉表面迅速产生了大量的生锈现象。
水充当了一个催化剂的角色,加速了铁的氧化反应。
五、实验结论通过以上实验结果及分析,我们可以得出以下结论:1. 铁钉在常温且湿度较高的环境下容易生锈,这是由于铁钉与空气中的水分与氧气反应形成铁的氧化物。
2. 相对湿度较低会减缓铁钉的氧化速度,从而降低铁钉生锈的现象。
3. 水对铁钉生锈具有明显的催化作用,浸泡在水中的铁钉会迅速产生大量的生锈现象。
六、实验启示通过这个实验,我们不仅了解到了铁钉生锈的原因,还意识到环境对其生锈速度的影响。
我们可以通过控制环境条件来减缓铁制品的生锈速度,如在潮湿环境中加强通风,保持环境相对湿度的合理范围。
化学实验报告《观察铁钉生锈的过程》(精选五篇)

化学实验报告《观察铁钉生锈的过程》(精选五篇)第一篇:化学实验报告《观察铁钉生锈的过程》1>,生锈,但不严重,水中溶解有一定的空气,金属铁在潮湿的空气中生锈;2>,不生锈,只有水,但是没有空气;3>,生锈,最严重,水和空气都很充足;4>,生锈,较严重,空气中有一定量的水蒸气。
蒸馏水中的铁钉生锈速度最慢。
速度排序:2第二篇:化学实验报告格式例一定量分析实验报告格式(以草酸中h2c2o4含量的测定为例)实验题目:草酸中h2c2o4含量的测定实验目的:学习naoh标准溶液的配制、标定及有关仪器的使用;学习碱式滴定管的使用,练习滴定操作。
实验原理:h2c2o4+2naoh===na2c2o4+2h2o计量点ph值8.4左右,可用酚酞为指示剂。
naoh标准溶液采用间接配制法获得,以邻苯二甲酸氢钾标定:-cook-cooh+naoh===-cook-coona+h2o此反应计量点ph值9.1左右,同样可用酚酞为指示剂。
实验方法:一、naoh标准溶液的配制与标定准确称取0.4~0.5g邻苯二甲酸氢钾三份,分别置于250ml锥形瓶中,加20~30ml蒸馏水溶解,再加1~2滴0.2%酚酞指示剂,用naoh标准溶液滴定至溶液呈微红色,半分钟不褪色即为终点。
二、h2c2o4含量测定准确称取0.5g左右草酸试样,置于小烧杯中,加20ml蒸馏水溶解,然后定量地转入100ml容量瓶中,用蒸馏水稀释至刻度,摇匀。
实验数据记录与处理:一、naoh标准溶液的标定实验编号123备注mkhc8h4o4/g始读数终读数结果vnaoh/ml始读数终读数结果cnaoh/mol·l-1naoh/mol·l-1结果的相对平均偏差二、h2c2o4含量测定实验编号123备注cnaoh/mol·l-1m样/gv样/ml20.0020.0020.00vnaoh/ml始读数终读数结果ωh2c2o4h2c2o4结果的相对平均偏差实验结果与讨论:结论:例二合成实验报告格式实验题目:溴乙烷的合成实验目的:1.学习从醇制备溴乙烷的原理和方法2.巩固蒸馏的操作技术和学习分液漏斗的使用。
铁钉除锈实验报告

一、实验目的通过本次实验,探究铁钉生锈的原因,了解除锈的原理和方法,并验证不同除锈剂对铁钉除锈效果的影响。
二、实验原理铁钉生锈主要是由于铁与空气中的氧气和水发生氧化反应,生成氧化铁(铁锈)。
除锈实验主要基于以下原理:1. 物理除锈:通过摩擦、打磨等方式去除铁锈。
2. 化学除锈:利用酸、碱等化学物质与铁锈发生反应,溶解铁锈。
三、实验材料1. 生锈铁钉:5根2. 除锈剂:钢丝刷、砂纸、稀盐酸、稀硫酸、纯碱溶液、草酸溶液3. 实验工具:剪刀、量筒、滴管、镊子、烧杯、手套、防护眼镜、实验记录表四、实验步骤1. 物理除锈:- 将生锈铁钉用剪刀剪成相同长度。
- 用钢丝刷轻轻刷去铁钉表面的锈层。
- 用砂纸打磨铁钉表面,直至铁钉表面光滑。
2. 化学除锈:- 将生锈铁钉分别放入以下除锈剂中:- 稀盐酸溶液:1:1(体积比)- 稀硫酸溶液:1:1(体积比)- 纯碱溶液:1:1(体积比)- 草酸溶液:1:1(体积比)- 观察铁钉在除锈剂中的变化,记录除锈时间。
- 用清水冲洗铁钉,去除残留的除锈剂。
3. 除锈效果比较:- 将除锈后的铁钉分别用钢丝刷和砂纸进行处理,去除表面的残留物。
- 观察并比较不同除锈剂对铁钉除锈效果的影响。
五、实验结果1. 物理除锈:- 使用钢丝刷和砂纸可以有效去除铁钉表面的锈层,但除锈效果相对较慢。
2. 化学除锈:- 稀盐酸、稀硫酸、纯碱溶液和草酸溶液均能有效地去除铁钉表面的锈层,其中草酸溶液的除锈效果最佳。
- 除锈时间:草酸溶液 < 稀盐酸 = 稀硫酸 = 纯碱溶液。
3. 除锈效果比较:- 草酸溶液除锈后的铁钉表面光滑,锈层去除最为彻底。
- 稀盐酸、稀硫酸和纯碱溶液除锈后的铁钉表面仍有少量锈层。
六、实验结论1. 铁钉生锈的主要原因是铁与空气中的氧气和水发生氧化反应。
2. 物理除锈和化学除锈均能有效去除铁钉表面的锈层,其中草酸溶液的除锈效果最佳。
3. 在实际应用中,可根据具体情况选择合适的除锈方法。
铁钉生锈实验报告范文

一、实验目的通过本实验,探究铁钉生锈的条件及其影响因素,验证铁钉生锈与氧气、水分的关系,并分析铁钉纯度对生锈过程的影响。
二、实验原理铁钉生锈是铁与氧气、水分发生电化学腐蚀的结果。
在潮湿的环境中,铁钉表面会形成微电池,铁作为阳极被氧化,氧气作为阴极被还原,从而产生铁锈。
铁的纯度也会影响生锈速度,纯铁不易生锈。
三、实验材料与仪器1. 实验材料:铁钉、蒸馏水、植物油、食盐、干燥剂、三个透明塑料瓶、滴管2. 实验仪器:天平、温度计、计时器、量筒、显微镜四、实验步骤1. 将三个塑料瓶分别标记为A、B、C。
2. 在A瓶中放入干燥剂,用滴管向瓶中滴入少量蒸馏水,形成湿润的环境。
3. 在B瓶中放入食盐,用滴管向瓶中滴入少量蒸馏水,形成盐水环境。
4. 在C瓶中不加入任何物质,形成干燥环境。
5. 将三个铁钉分别放入三个瓶子中,用瓶盖密封。
6. 在实验开始时记录铁钉的重量,并观察铁钉的生锈情况。
7. 每隔一定时间(如一天、三天、一周、两周)观察铁钉的生锈情况,并记录数据。
8. 利用显微镜观察铁钉表面的微观结构,分析铁钉生锈的原因。
五、实验现象与结果1. 在A瓶中,铁钉逐渐生锈,表面出现红褐色锈斑。
2. 在B瓶中,铁钉生锈速度较快,表面出现大量红褐色锈斑。
3. 在C瓶中,铁钉未发生生锈现象。
4. 利用显微镜观察,发现A、B瓶中铁钉表面的锈斑结构相似,均为氧化铁。
5. 经过两周的实验,A瓶中铁钉的重量减轻,B瓶中铁钉的重量减轻较多。
六、实验分析与结论1. 铁钉生锈的条件是氧气和水分同时存在。
在A、B瓶中,铁钉与氧气、水分充分接触,导致生锈。
2. 盐水环境可以加速铁钉的生锈速度。
B瓶中食盐的存在使得铁钉与水分中的离子相互作用,促进了电化学腐蚀过程。
3. 干燥环境不利于铁钉生锈。
C瓶中干燥剂吸收了瓶内的水分,使得铁钉无法与水分接触,从而未发生生锈。
4. 铁的纯度对生锈速度有一定影响。
本实验中,未观察到纯铁钉的生锈现象,说明纯铁不易生锈。
探究铁钉生锈实验报告
探究铁钉生锈实验报告
九一xxx
一、实验目的
通过对比实验,确定影响铁钉生锈的因素。
二、实验猜想
铁在水与氧气的共同参与下使铁生锈。
三、实验器材
1、三只透明的小玻璃瓶(代替试管)
2、三只经过打磨除锈的铁钉(同一厂家,同一型号)
3、蒸馏水(购得)食用油干燥剂(硅胶)
4、电吹风
四、实验步骤
1、将三个玻璃瓶洗净,用电吹风烘干。
2、向经烘干的,干燥的A瓶内放入一枚铁钉、少量硅胶,并用瓶塞将瓶口
塞住,使其与外部的空气无法接触。
3、在B瓶内装入一定量的蒸馏水,使蒸馏水将铁钉完全浸没。
再向水上滴
加食用油,使其与空气隔绝。
4、在C瓶内装入少量蒸馏水,使铁钉一部分在水里,另一部分裸露在空气,
不封口,使其与外部空气接触。
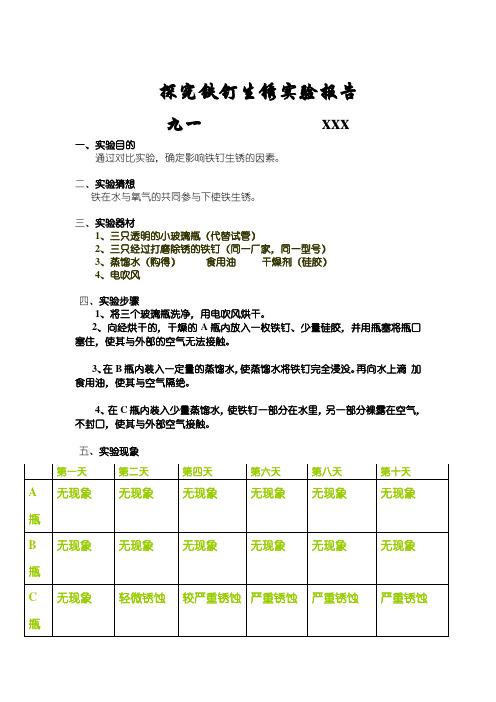
五、实验现象
第一天第二天第四天第六天第八天第十天
A瓶无现象无现象无现象无现象无现象无现象
B瓶无现象无现象无现象无现象无现象无现象
C瓶无现象轻微锈蚀较严重锈蚀严重锈蚀严重锈蚀严重锈蚀
六、实验结论
铁生锈的必要条件是氧气.水同时存在。
破坏其中任意一个即可防止锈蚀。
研究铁生锈实验报告

一、实验目的1. 探究铁生锈的条件和过程。
2. 分析影响铁生锈速度的因素。
3. 探讨铁生锈的防锈措施。
二、实验原理铁生锈是铁与氧气和水发生氧化反应的过程。
铁在潮湿的空气中,由于氧气和水的共同作用,会发生电化学腐蚀,从而生成铁锈。
铁锈的主要成分是氧化铁。
三、实验材料与仪器1. 实验材料:铁钉、蒸馏水、植物油、食盐、氯化钙、试管、烧杯、铁架台、橡皮塞、导管、止水夹、红墨水、稀盐酸。
2. 实验仪器:铁丝网、硬质玻璃管、单孔橡皮塞、乳胶管、止水夹、烧杯。
四、实验步骤1. 准备实验装置:按照实验原理,组装实验装置,并检查装置的气密性。
2. 放置铁钉:将事先经过除锈并在清水中漂洗干净的铁钉放入硬质玻璃管中。
3. 注入溶液:用带导管的橡皮塞塞紧下端,用止水夹夹住下端乳胶管,并从上端向硬质玻璃管中注满食盐水。
4. 密封上端:再用带导管的橡皮塞塞紧上端,并用止水夹夹住上端乳胶管。
5. 观察现象:打开两端止水夹,排净其中的食盐水后,再夹住上端的止水夹,然后把硬质玻璃管下端导管插入烧杯中红墨水液面以下。
6. 记录数据:观察并记录铁钉生锈的情况,以及红墨水在硬质玻璃管中的上升情况。
五、实验结果与分析1. 铁钉生锈现象:实验结果表明,在食盐水中,铁钉生锈速度明显加快,且红墨水在硬质玻璃管中的上升速度也相应加快。
2. 影响因素分析:- 氧气:铁钉在干燥的空气中不生锈,而在潮湿的空气中容易生锈,说明氧气是铁生锈的必要条件。
- 水:铁钉在纯水中不生锈,但在食盐水中生锈速度加快,说明水中的溶解物质(如盐)可以加速铁生锈。
- 电解质:食盐水中含有电解质,可以促进铁的电化学腐蚀,从而加快铁生锈速度。
3. 防锈措施:- 隔绝氧气和水:将铁制品涂上油漆、镀上不易生锈的金属,或将其放置在干燥的环境中,可以隔绝氧气和水,从而防止铁生锈。
- 控制电解质:在水中加入适量的防腐剂,可以抑制铁的电化学腐蚀,从而减缓铁生锈速度。
六、实验结论1. 铁生锈的条件是氧气、水和电解质的存在。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
探究铁钉生锈的原因的实验报告探究影响铁钉生锈的因素的实验报告
一、实验目的
通过对比实验,确定影响铁钉生锈的因素。
二、实验猜想
铁在水与氧气的共同参与下使铁生锈。
三、实验器材
1、三只透明的小玻璃瓶,代替试管,
2、三只经过打磨除锈的铁钉,同一厂家,同一型号,
3、蒸馏水,购得,食用油干燥剂,硅胶,
4、电吹风
四、实验步骤
1、将三个玻璃瓶洗净,用电吹风烘干。
2、向经烘干的,干燥的A瓶内放入一枚铁钉、少量硅胶,并用瓶塞将瓶口
塞住,使其与外部的空气无法接触。
3、在B瓶内装入一定量的蒸馏水,使蒸馏水将铁钉完全浸没。
再向水上滴加食用油,使其与空气隔绝。
4、在C瓶内装入少量蒸馏水,使铁钉一部分在水里,另一部分裸露在空气, 不封口,使其与外部空气接触。
五、实验现象
第一天第二天第四天第六天第八天第十天
A瓶无现象无现象无现象无现象无现象无现象
B瓶无现象无现象无现象无现象无现象无现象
C瓶无现象轻微锈蚀较严重锈蚀严重锈蚀严重锈蚀严重锈蚀六、实验结论
铁生锈的必要条件是氧气.水同时存在。
破坏其中任意一个即可防止锈蚀。
