药品公司组织机构图(可编辑)
集团化管理模式及组织架构

在设计组织架构时,应考虑到各活动(职能)的地域特点、专业特点等;
*
集团化管理与资源优化配置
自建必要的生产线,其它委托制药业务板块进行生产
标提
*
集团架构调整优化总体思路
目前某某集团的业务方向很明确,也很好的在各法人实体间进行了分配,今后集团基于各种目的还会成立其它的法人实体。如果各法人均完全独立运作,有可能会出现集团控制力下降、总体战略不能很好实施、事业重复、经营资源分散、内部竞争等问题。
营销监审中心
法律事务中心
安全保卫中心
*
某某集团组织架构(二级架构)
某某集团
制药业务板块
*
某某集团组织架构(二级架构)
医药流通业务板块
某某集团
江西科研营销
行政管理部
深圳健美医药
医药流通事业部
XX医药公司
经营发展中心
市场拓展中心
采购中心
采购供应部
OTC销售部
专业产品销售部
医疗器械销售部
财务管理部
集团最高决策机构: 董事局 集团日常决策机构: 总裁办公会 董事局负责对集团重大 经营问题进行最终的决 策。包括:集团战略规 划、经营目标、年度预 算、重大投资等。 总裁办公会由集团决策 层人员组成,负责企业 日常经营决策。 专业性强的决策组成临 时专业委员会进行决策。
*
各事业部(部)的核心任务
研发事业部:负责某某集团制药、植物药业GAP业务板块中相关新产品的选择、购买、研究、二次开发、临床试验、中试、工艺改进、证照报批等工作,为集团制药和植物药业业务板块的持续稳定发展提供坚实的基础。 采购部:负责某某集团制药、植物药业业务板块中所有物资(包括原材料、辅料、包装材料、零配件、办公用品等)的采购、仓储与运输,产成品的仓储与运输,保证集团生产经营的正常进行,并降低成本。 制造事业部:负责某某集团制药业务板块所有产品的生产制造工作并接受其它业务板块产品的委托生产,保证集团产品按质按量低成本的生产,为企业发展服务。 OTC营销部:负责某某集团制药业务板块OTC产品、保健品、卫生用口等相关产品的市场营销工作,同时接受植物药业业务板块的委托进行部分饮片、标提的市场营销工作,为集团发展提供充足的现金保证。 处方药营销部:负责某某集团制药业务板块专业产品的市场营销工作,为集团发展提供充足的现金保证。 医药流通事业部:全面负责某某集团医药流通业务的发展与经营,保证医药流通业务在2005年前成为集团的支柱业务之一。 植物药业公司:全面负责某某集团中药材种植、饮片、中药标准提取物、成品、中药材贸易等业务的培育和开展,使植物药业业务在2010年前成为集团支柱业务之一。
GMP制药企业组织机构设置与人员管理课件(1)

一、组织机构的设置
基本原则:
1、机构是因事而设,不能因人而设; 2、一定要设置生产管理部与质量管理部,其他部
门据企业实际情况而定;
3、生产部与质量部一定要分设; 4、质量管理部一定要包括QA、QC两块,一定要直
属企业负责人领导;
5、机构的设置要扁平、简单,职责明确。 6、这一机构的良好运行是顺利完成硬件整改、软
3
一、组织机构的设置
XX有限公司组织机构图
总经理
GMP办公室
综合管理部
生产管理部
质量管理部
物料科 工程设备科 生产科 QA
QC
另外,还应设财务部、销售部、
资料档案室。并对生产、质量管 理细化形成单独的组织机构图
各车间
展通医药科技
4
生产部组织机构示例
生产部经理
工程设备
机修组 电修组 仪修组
物料管理
5立即成立GMP领导小组。领导小组组长一般由企业的最高领导亲自 担任,原因是GMP认证直接关系到企业的生死存亡,Байду номын сангаас且是一项 涉及多个部门配合、资金筹措、生产调度的系统工程。
6、如果是小厂,可将设一综合部,管行政、公关、人力资源等,并 将物料、采购、计划、工程设备归属生产部。具体设置见下图:
展通医药科技
结束语
在保证产品质量的诸多因素中,管理模式被认为是最活跃、影响最大 的最主要的因素。 一个健全的组织机构可以高效组织和发挥全企业的职工的潜能;可以 相互协调、相互促进以及建立必要的监督制度,最大限度地调动全企 业各部门,最终使整个企业的运行获得最好的生产及经营效益。 在生产要素中,人的因素第一。一切工作离不开人,人员素质水平高 低,对实施兽药GMP将起决定性的作用。 人员素质——企业素质——产品质量 ;企业人员素质的总和——体 现出企业的素质——企业的文化精神 企业的管理哲学、价值取向、聘用制度、晋升机制、决策风格、激励 手段、沟通网络都影响人员能力的发挥。同一个人在不同企业文化精 神的影响下,表现出不同的积极性及工作的能力。 所以,人员的素质影响了企业的素质,企业的素质也影响了人的素质。
药事管理组织机构图
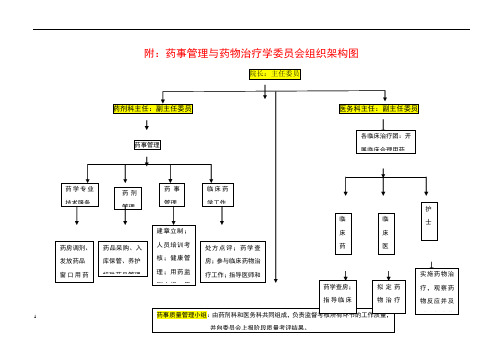
院长:主任委员
v1.0 可编辑可修改
药剂科主任:副主任委员
药事管理
医务科主任:副主任委员
各临床治疗团:开 展临床合理用药
药学专业 技术服务
药剂 管理
药事 管理
临床药 学工作
建章立制;
护
临
临
士
床
床
药房调剂、 发放药品 窗口用药 咨询
药品采购、入 库保管、养护 特
不良事件
v1.0 可编辑可修改
2
v1.0 可编辑可修改
人员培训考 核;健康管 理;用药监 测上报;用 品信息发
处方点评;药学查 房;参与临床药物治 疗工作;指导医师和 患者安全用药。
药 师
药学查房; 指导临床
医 生
拟定药 物治疗
实施药物治 疗,观察药 物反应并及
1
布 药。 事质量管理小组:由药剂科和医务科共同组成,负责监督考合核理所用有药环节的工作质方量案,
药品批发企业GSP内审检查内容:计算机系统

计药品的数量、流向等信息,并可追溯。
审核结果
备注
05801 05802
计算机系统应有支持系统正
常运行的服务器和终端机。
与04001、05701 并查
综合管理部
企业计算机系统应当有安全 稳定的网络环境、固定接入 互联网的方式和安全可靠的 信息平台。
与04001、05701 、05801并查
综合管理部
并查
1、检查公司计算机系统,核实是否按照组织机构建立 了计算机系统的内部局域网;
2、对照公司组织机构图,抽查质量管理、采购、销售 □符合规定 、验收、收货、养护、出库复核等岗位,核实是否能够 □不符合规定
实现实时数据传输,并按照规定的权限实时进行数据查 询。
05804
企业计算机系统应当有药品 经营业务票据生成、打印和 管理功能。
□符合规定 □不符合规定
日备份;
4、检查公司数据备份介质的存放场所,核实是否与服
务器存放于不同场所。
质量管理体系内部检审查核人检查表(计算机系统)
检查时间
员
编号 条款
检查方法 被审核部门
检查内容及结果判定标准
*05701
企业应当建立能够符合经营全 过程管理及质量源自制要求的计 算机系统,实现药品可追溯。
1、检查公司计算机系统管理文件相关要求是否符合本
检查项目的内容;
2、检查公司计算机系统,核实是否与其经营范围和规
**05805
与04001、05701
、05801、05802 、05803、05804
综合管理部
并查
1、检查公司计算机系统,核实公司建立的应用软件和 相关数据库是否符合公司管理实际需要,并符合《规范 》的相关要求; 2、检查公司计算机系统,核实公司计算机系统建立的 质量管理基础数据信息是否符合本检查项目的相关要 求; 3、分别抽查供货单位、购货单位、经营品种、供货单 位销售人员、购货单位采购人员及提货人员等档案资料 至少各3分,核实计算机系统中相对应的经营范围、经 营方式、资质、文件有效期等质量管理基础数据信息, 是否符合本检查项目的内容,并与质量管理档案内容相 符,是否存在超过有效期的情况;
小型公司扁平化管理组织结构及组织结构图(草稿))

小型公司扁平化管理组织结构及组织结构图(草稿))目录:1、小型公司扁平化管理组织结构及组织结构图(草稿))2、财务部组织机构和工作内容 (酒店)公司组织结构、职责及组织结构图职责:一、总经理:1、全面负责、主持公司的日常经营、行政和管理活动,负责检查和绩效考核,努力营造良好的企业发展运营内外部环境。
2、负责和组织实施公司发展规划、年度经营计划,并监督完成。
3、负责对公司重大投资、经营活动决策。
4、负责公司财务管理、预算、决策和利润分配。
5、决定对成绩显著的员工予以奖励、加薪和晋级以及对违纪员工的处分,直至辞退。
6、强化员工管理,建立一支作风优良、纪律严明、训练有素、适应需要的员工队伍。
7、代表公司对外签署有关协议、合同、合约和处理有关事宜。
二、副总经理1、负责单位日常的运营管理,协助总经理对单位的计划,制度进行实施和检查。
2、掌握单位的组织机构,人事制度,各部门日常操作规程以及各项规章制度的落实。
3、向总经理建议任免项目组主管人员人选。
4、掌握控制及处理各种紧急情况的方法及步骤,妥善处理各种突发性事件。
5、主持单位人事培训工作,督导和考核部门的服务质量,以及纪律性符合有关标准。
6、了解和分析单位需求,制度营销计划,负有拓展单位前景的责任。
7、了解和掌握各项目组运营状况。
8、协调各项目组主管工作,定期召开会议,根据总经理的意向指导单位工作方向。
9、当总经理外出,受总经理委托,代理行使总经理权力。
10、综合协调处理企业内部各部门、各种形式、各种类型的日常事务。
三、综合组1、负责人力资源管理工作(1)薪酬管理(2)绩效管理(3)员工培训(4)人员调配2、办公室工作(1)起草各项管理制度(2)负责协议起草、招投标文件起草(3)负责公司文件起草(4)督促、指导各项目组管理规定的制定、执行(5)负责领导交办的临时性工作3、物资采购工作(1)制定物资采购计划(2)执行采购流程(3)建立物资采购台账及物资采购数据录入系统,保证物资采购数据的准确性,可追溯性(4)建立物资采购月报制度,每月向总经理报送数据。
制药工厂现场主文件编写说明

PHARMACEUTICAL INSPECTION CONVENTION PHARMACEUTICAL INSPECTION CO-OPERATION SCHEME药品检查协定和药品检查合作计划组织PE 00841 Annex1 January 2011PE 0084附件一2011年1月1日EXPLANATORY NOTES FOR PHARMACEUTICAL MANUFACTURERS ON THE PREPARATIONOF A SITE MASTER FILE制药工厂现场主文件编写说明PIC/S January 2011Reproduction prohibited for commercial purposesReproduction for internal use is authorizedProvided that the source is acknowledgedEditor/编著: PIC/S Secretariatemail/邮箱: ******************web site/网站: TABLE OF CONTENTS目录1 Document History/文件历史 (2)2 Introduction/简介 (2)3 Purpose/目的 (2)4 Scope/范围 (3)5 Content of Site Master File/现场主文件内容 (3)6 Revision History/修订历史 (3)2 INTRODUCTION 简介2.1 The Site Master File is prepared by the pharmaceutical manufacturer and should contain specific information about the quality management policies and activities of the site, the production and/or quality control of pharmaceutical manufacturing operations carried out at the named site and any closely integrated operations at adjacent and nearby buildings. If only part of a pharmaceutical operation is carried out on the site, a Site Master File need only describe those operations, e.g. analysis, packaging, etc.现场主文件是由制药厂家编写,并包含以下信息:质量管理方针及现场活动、在对在指定现场进行生产或/和对在指定现场的制药生产操作进行的质量控制以及在临近及附近建筑内进行的一体化操作。
集团公司流程图大全(可编辑修改)

用人单位
请假当事人填写 请假单
分厂人事科
当事人工作交 代
存档
16
职 员 及 干 部 请 假 申 请 程 序
用人单位
请假当事人填写 请假单
总经理
集团总裁
人事行政部
科长签审 部长签审 副总签审 请假单 请假单 请假单
终审
终审
签审
2
定 岗 定 编 计 划 报 批 程 序
各单位
依据组织机构图 拟制制定
人事行政 部
定岗定 员方案 组织讨论
总经理
定岗定 员方案 部长签审
部门人员 定编方案
分管副总 签审
部门人员 定编方案
部长签审
副总签审 终审
部门人员 定编方案 发文、存档
3
定 编 外 用 人 需 求 申 请 程 序
用人单位
拟制 用人需求 申请单 经理签审 分管副总签审
移交 登记表 办理结算
辞退、开除,可以退回原用人单位再议。
12
员 工 年 度 、 半 年 度 培 训 计 划 报 批 程 序
基层单位
提供培训需 求意见
人事行政部
搜集整理外部培 训市场信息 编制培训计划 和预算 培训 计划
总经理
科长签审 部长签审 副总签审 培训 计划
终审 培训 计划
实施培训计划
13
集团公司工作流程图大全
黄色部分为标识备注,均可编辑可修改。
组 织 机 构 图 计 划 编 制 报 批 程 序
人事行政部
组织 机构图
总经理
集团总裁
根据决策讨论定稿的组织机构拟制
决策 报批表
组织 机构图 决策 报批表 签审 组织 机构图 决策 报批表
药事管理组织机构PPT课件

五、SFDA药品审评中心
CDE(Center for Drug Evaluation)
六、SFDA药品认证管理中心
CCD(certification Committee for Drugs)
GLP药物非临床研究质量管量规范 GCP药品临床实验管理规范 GMP药品生产质量管理规范 GAP药材生产管理规范 GSP药品经营质量管理规范 GUP药品使用管理规范
二、我国医药行业管理机构的职责
1、我国医药行业管理 机构的建立 SFDA 国家中医药管理局 国家经贸委医药司 2、我国医药行业管理 机构的职责(P15)
第三节
药学教育、科研组织和社会团体
随着改革的深入发展,我国药学教育和药物 科研的机构和体制,发生了较大变化。药物科研 机构处于从事业性组织向企业化过渡阶段。政府 机构改革以来,部分原有职能委托药学社团机构 办理,药学社团的行业管理职能有所加强。
一、药学教育组织
有药学类专业的高校大多为综合性大学,仅 有独立药科大学2所,另有中医药大学和中医学院 23所。96所设置有药学类专业的高校。 药学继续教育主要由设有药学类专业的高校、 中等学校和药学会承担。
二、药学科研组织
我国的药学科研组织有独立的药物研究院、所 以及附设在高等药学院校、大型制药企业、大型医 院中的药物研究所、室两种类型。
县级FDA(派出机构)
三、药品检验机构
国家级、省级、市级、县级 中国药品生物制品检定所 省、自治区、直辖市药品检验所
四、国家药典委员会
(The Pharmacopoeia commission of the
People’s Requblic of China) 性质: 组成: 全体委员会(主任委员、副主任委员等) 专业委员会 常设机构
