第13章 β-二羰基化合物
第14章β-二羰基化合物

的酯在强碱 有α-H的酯在强碱(一般是用乙醇钠)的作用下与另一分子酯 的酯在强碱(一般是用乙醇钠)的作用下与另一分子酯 发生缩合反应,失去一分子醇 生成β-羰基酯 一分子醇, 羰基酯的反应叫做酯 发生缩合反应,失去一分子醇,生成 羰基酯的反应叫做酯 缩合反应,又称为克莱森( 缩合反应,又称为克莱森(Claisen)缩合。 )缩合。
有机化学
上页 下页
重要β 二羰基化合物 重要 –二羰基化合物
O O C 2 H 5 O-C-CH 2 -C-OC 2 H 5
丙二酸二乙酯
O O CH3-C CH2-C-OC2H5
乙酰乙酸乙酯
有机化学
上页
下页
三、 丙二酸酯在有机合成上的应用
一.丙二酸二乙酯的制备 丙二酸二乙酯的制备
O O O O NaCN C H OH CH2-C-OH CH2-C-ONa 2 5 C2H5O-C-CH2-C-OC2H5 OH H2SO4 Cl CN
OH O CH3-C=CH-C-OC H5 2 烯醇式 (7%)
有机化学
上页
下页
二、 β –二羰基化合物碳负离子的反应 二羰基化合物碳负离子的反应
碳负离子是带部分负电荷的碳原子或氧原子, 碳负离子是带部分负电荷的碳原子或氧原子,都具 是带部分负电荷的碳原子或氧原子 亲核性, 有亲核性,在碳原子和氧原子上都有可能发生亲核 反应,主要发生在碳原子上 常见的反应有下列几种: 在碳原子上。 反应,主要发生在碳原子上。常见的反应有下列几种: (1)碳负离子与卤代烷的反应 卤代烷的反应 )碳负离子与卤代烷 羰基化合物的缩合反应 (2)碳负离子和羰基化合物的缩合反应 )碳负离子和羰基化合物 不饱和羰基化合物的共轭加成 (3)碳负离子和 ,β-不饱和羰基化合物的共轭加成 )碳负离子和α, 不饱和 反应
β-二羰基化合物

+
CH2(COOH)2
CH3COOH
②α -H的取代反应
CH2(COOC2H5)2 C2H5ONa CH COOC2H5 CH3Br COOC2H5 CH3 CH COOC2H5 COOC2H5
3.合成应用 ●合成一元酸
例如:以C≤2的醇为原料经丙二酸二乙酯合成2-丁酸
CH3 C COOH COOH
① NaOH,H2O ② H
+
CH3CH2
- CO2
CH3 CH3CH2 CH COOH
③ 合成环状羧酸
例:以丙二酸二乙酯、不超过2个碳的醇及其它无机试剂为原料, 合成
CH3CH2OH CH3CH2OH Na
COOH
C2 H5ONa H2C CH2 Br2 BrCH2CH2Br
分析:(1) 产物为甲基酮,合成时一定要经过酮式分解。
(2) 将TM的结构与丙酮进行比较,确定引入基团 (3) 最后确定合成路线。
注意:当引入基团不同时,通常是先引入活性较高和体积较大
的基团
▲合成一元羧酸
如上述合成的α-丙基乙酰乙酸乙酯中间体进行酸式分解:
O O ① C2H5ONa O O CH3 C CH2 C OC2H5 CH3 C CH C OC2H5 ② CH3CH2CH2Br CH2CH2CH3
O O C2H5 O CH3 C CH2 C OC2H5 O O
O O [ CH C CH C OC H 3 2 5 C2H5OH
CH3 C CH C OC2H5
]
+
再如:
O 2 CH3 CH2 CH2 C OC2H5 ① ② O C2H5ONa H
+
第十四章_β-二羰基化合物
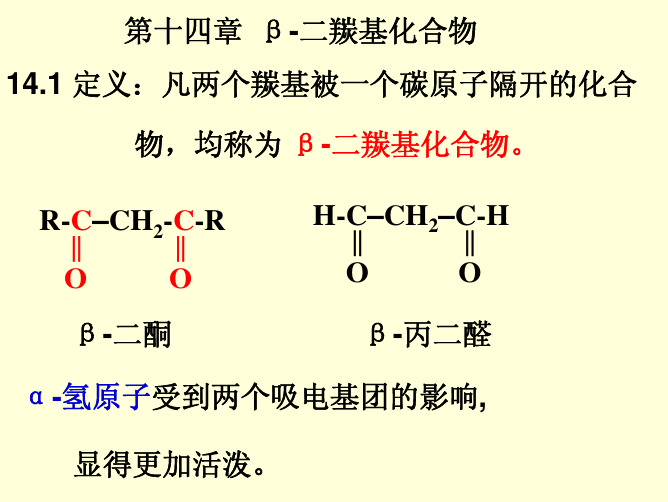
物,均称为 β-二羰基化合物。
R-‖C–CH2-‖C-R
O
O
β-二酮
H-‖C–CH2–C‖-H
O
O
β-丙二醛
α-氢原子受到两个吸电基团的影响,
显得更加活泼。
14.2 命名
HO-‖C–CH2-‖C-OH
O
O
β- 丙二酸
R-‖C–CH2–C‖-OR’
CH3︱CH=CH‖COC2H5 OH O
NaOC2H5 H+
CH3‖C CH-‖COC2H5 OO
Na
+
CH3‖CCH2C‖OC2H5 OO
①5%NaOH CH3COCH2COOH
②H+
CH3COCH3
△,-CO2
?
CH3‖CCH2C‖OC2H540%△NaOH OO
CH3‖COON+a
C2H5OH
CH3‖CO︱CCHH‖O2CCOHC2C2HO①5O5C%2H︱CNHaO2CHH2CCHO3‖OCO︱CCHHH2‖OCCOHN2CaOONa ②H+ , ③△ CH3‖CCH2
O
CH3‖C︱CCHH‖2CCOHC2C2HO5OC酮2式H 分解 OO
C︱H2CH2COOH CH3‖CCH2
O
︱CH2CH2COO酸C2式H分5 解
CH3‖CCH2C‖OC2H5 OO
H2N-OH H+
CH3‖CCH2COOC2H5 N-OH
Na CH3︱C= CH ‖COC2H5 ONa O
CH3︱C = CHC‖OC2H5 OH O
+ H2
CH3‖C-CH-‖COC2H5Na +
课件有机化学第13章 取代酸和二羰基化合物

第十三章 取代酸 和β-二羰基化合物Substituted Carboxylic Acids and β-Dicarbonyl Compounds1CONTENT1 2 3 4 5取代酸的酸性(自学) 羟基酸 羰基酸(氧代酸) β-酮酸酯 β-二羰基化合物的反应213.1 取代酸的酸性(自学)• 有利离解出质子的因素使酸性增强 • 不利离解出质子的因素使酸性减弱O吸电子基O给电子基C OC O提高羧酸根阴离子 稳定性的因素降低羧酸根阴离子 稳定性的因素313.2 羟基酸1. 羟基酸的命名和物理性质(自学)许多羟基酸来自于动植物,常用俗名来表示2-羟基丙酸(乳酸)2-羟基丁二酸(苹果酸)413.2 羟基酸2. 羟基酸的制备• 卤代酸水解CH3CH2CHCOOH Br NaOH/H2O H+ CH3CH2CHCOOH OHCH3 CH3C OH CN CH3 CH3C OH COOH• 羟基腈水解CH3COCH3 HCN H• Reformatsky反应O + BrCH2CO2Et Zn Benzene H2O H+ OH CH2CO2H513.2 羟基酸3. 羟基酸的反应• 氧化反应OHCH3CH2COOHTollens 试剂CH3COCOOHCH3COOH• 脱水反应(1) α-羟基酸OH RCHCOOHOO C R CH O CH R O C OC R CH OH O H H O HO CH R C O6(2) β-羟基酸OH RCHCH2CO2H H+ RCH CHCO2H(3) γ-羟基酸OH RCHCH 2CH2CO2H R O O713.3 羰基酸(氧代酸)CH3COCH2COOH 3-氧代丁酸• 酸性大于羧酸 • α或β-酮酸受热易脱羧RCOCH2COOHNa2Cr2O7/H2SO4RCOCH3RCHCH2COOH OH813.4 β -酮酸酯1. β -酮酸酯的形成Claisen 酯缩合:含α−氢的酯在碱(醇钠)的作 用下,两分子酯发生缩合反应,生成 β −羰基酸 酯同时消去一分子醇O 2 CH3COEt 乙酸乙酯 Ethyl acetate EtONa EtOH H2 O H+OOCH3C CHCOEt + EtOH 乙酰乙酸乙酯 Ethyl acetoacetate9反应机理pKa 24.5CH3CO2Et + EtO CH2CO2Et O − CH3 C OEt + CH2CO2Et CH O−−−+ EtOH O C−3OEtCH3 C CH2CO2Et + EtO O O + − Na EtO − CH C CH3 C CH2CO2Et CHCO2Et + EtOH 3pKa ~11CH2CO2EtOH+CH3 C CH2CO2Et10作业•P283: 13.1(1);•P285: 13.2;•P293: 13.5,13.6;•P297: 13.10,13.11;习题•P306: 3,5(1),(2),6。
第14章_β-二羰基化合物和有机_[1]...
![第14章_β-二羰基化合物和有机_[1]...](https://img.taocdn.com/s3/m/489a41b68762caaedd33d446.png)
不含α-H的酯如草酸二乙酯、甲酸酯、碳酸二乙酯 苯甲酸酯等在酰化反应中可分别引入-COCO2C2H5, -CHO, -COOC2H5, -COPh基团。
2. 酰基化反应
使用草酸酯得到的产物既是β-酮酯,又是α-酮 酯。由于α-酮酯在加热时可脱去羰基,为合成取 代丙二酸酯及相关化合物提供一条方便的途径。
3. 迈克尔加成反应
活泼氢化合物在催化量碱(常用醇钠,季铵碱及 苛性碱等)作用下与α, β-不饱和化合物发生1, 4-加成的反应称为Michael加成反应。
催化量 C2H5ONa + CH2=CHCCH3 C2H5OH O O (H5C2O2C) 2CH CH2CH2CCH3
CH2(CO2C2H5)2
COOC2H5 C2H5ONa PhCH2CO2C2H5 + COOC2H5 COOC2H5 C CO2C2H5 O 178° C
Ph HC
PhCH(COOC2H5)2
Ph HC
COOC2H 5 C CO 2C 2H 5 O
H 3O+
COOH Ph CH C COOH - CO2 O
PhCH2COCOOH
CH 3 O O
2-甲基-1,3-环戊二酮
练习14.2
14.1.2 β-二羰基化合物活泼氢的酸性
• β-二羰基化合物的两个羰基之间的α-氢原子的 酸性,由于其相应阴离子的共振稳定化而大大增 强。 pKa在9~13之间。 在碱的作用下,活性亚甲基上的质子具有酸性,易 脱去形成二羰基碳负离子或烯醇负离子,存在着酮 式和烯醇式的互变异构。
+ NaX
C
OC2H5 + C2H5OH
二烃基乙酰乙酸酯
α-烃基乙酰乙酸乙酯的应用
有机化学二羰基化合物
碳氧双键处于共轭体系,发生了电子的离域,使体
系能量降低而趋于稳定。
:OH
H3C C CH
O C OC2H5
2024/7/26
4
第5页/共53页
影响烯醇式含量的其它因素:
① 活泼亚甲基上连有吸电子基团,烯醇式含 量↑,连有供电子基团,烯醇式含量↓。
O
O
O
O
H3C
C
CH
C OC2H5 > H3C
C
CH2
2+
Hg
+
H
OH CH CH2
O CH3C H
β-二羰基化合物的烯醇式结构稳定性:乙酰乙酸乙酯
实验事实:
① 能与NaHSO3、HCN等发生加成反应; ② 能与羟胺、苯肼反应,生成肟、苯腙等; ③ 能被还原成β-羟基酸酯; ④ 经水解、酸化后,可以脱羧生成丙酮。
O
O
H3C C CH2 C OC2H5
有羰基
O CH3C CH
O COC2H5
Na+
Br(CH2)4Br
O CH3C
C2H5ONa
COCH3
成酮分解
COOC2H5
O CH COC2H5 CH2(CH2)3Br
O
CCH3
2024/7/26
28
第29页/共53页
② 制二酮
2024/7/26
制β-二酮(1,3-二酮)
O CH3C CH
O COC2H5
第11页/共53页
三、丙二酸二乙酯的合成及应用
1、丙二酸二乙酯的制法 2、丙二酸二乙酯在有机合成上的应用
① 制备烃基取代乙酸 ② 制备二元羧酸
2024/7/26
β-二羰基化合物酮式和烯醇式的互变异构
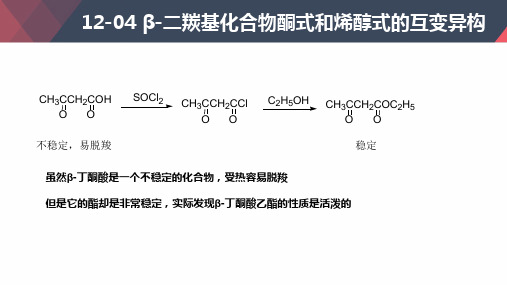
CH3CCH2COH O O 不稳定,易脱羧
SOCl2
CH3CCH2CCl O O
C2 H5OH
CH3CCH2COC2H5 O O 稳定
虽然β-丁酮酸是一个不稳定的化合物,受热容易脱羧 但是它的酯却是非常稳定,实际发现β-丁酮酸乙酯的性质是活泼的
12-04 β -二羰基化合物酮式和烯醇式的互变异构
β-丁酮酸乙酯可以发生一系列的化学反应:
-丁酮酸酯的化学反应: ① 与Na反应生成氢气
② 遇溴水褪色
③ FeCl3溶液显紫红色 ④ 遇到饱和NaHSO3得无色晶体
Байду номын сангаас
12-04 β -二羰基化合物酮式和烯醇式的互变异构
β-丁酮酸乙酯存在互变异构:
产生原因:① CH2解离出H与CH3CO中的O结合,形成烯醇式 ② 烯醇式中由于分子中形成共轭体系,且通过氢键形成六元环
12-04 β -二羰基化合物酮式和烯醇式的互变异构
溶剂对异构体的影响:
在极性溶剂中,烯醇式会很少,因为自身不易形成氢键
在非极性溶剂中,烯醇式含量多,由于有利于烯醇式自身形成氢键
12.5β-二羰基化合物的烃化和酰化反应

12-05 β-二羰基化合物的烃化和酰化反应
2.酰基化反应
β-二羰基化合物的活性亚甲基在碱性条件下还能够发生酰基 化反应,能够用于酰基化反应的试剂是酯、酰卤、酸酐 如:
NaH CH3COCH2COOC2H5 CH3COOCOCH3 CH3COCHCOOC2H5 C CH3 O
CH3
12-05 β-二羰基化合物的烃化和酰化反应
1.烃基化反应
在一般条件下, β-二羰基化合物的烃基化反应均发生在活性的亚甲基 上,但是在强碱条件下如有机锂、氨基钠等作用下, β-二羰基化合物 可以被转化为双负离子,在与1mol的卤代烃反应时,碱性更强的端基 碳负离子将优先发生γ-烃基化 如:
O CH3COCH2COCH3 2 NaNH2 / NH3(l) H2C C C H O C CH3 RX R O H2CC H2 C O CCH2 CH3
12-05 β-二羰基化合物的烃化和酰化反应
1.烃基化反应
能够用于 β-二羰基化合物的烃化的烃基化试剂有磺酸酯、硫酸酯和卤
代烃,其中卤代烃最为普遍。不过,三级卤代烃由于在碱性条件下容易 发生消除反应,不宜被用于烃基化试剂 如:
CH3COCH2COOC2H5 C2H5ONa CH3I CH3COCHCOOC2H5
12-05 β-二羰基化合物的烃化和酰化反应
主讲人:王刚
12-05 β-二羰基化合物的烃化和酰化反应
1.烃基化反应
β-二羰基化合物的烃基化反应是以醇钠为碱在醇溶液中进行
反应为SN2反应 β-二羰基化合物的烃基化反应是有机化学增长碳链的方法之一
X Y R'ONa X Y
RZ
+
H2C
R
CH
(X,Y=NLeabharlann 2, R''CO, R''OCO, CN 等)
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
解:(B)没有烯醇结构。故可以采用①FeCl3溶液、 ② Br2/CCl4溶液鉴别。
P255 习题
2.用简单的化学方法鉴别下列化合物
(1)CH3COCH2COOH与HOOCCH2CH2CH2COOH
含有α-氢的酯都可发生Clainsen缩合反应,但两种不同的都含α-氢的酯缩合 后会产生四种产物。
O O RCH2CCHCOC2H5 R O O O 1.C2H5ONa 2.H+ O O
R'CH2CCHCOC2H5 R' O RCH2COC2H5 + R'CH2COC2H5
RCH2CCHCOC2H5 R' O O
(皂化反应)
CH3 C CH2 C ONa
第二步:后酸(化)
O
O
CH3 C CH2 C ONa
第三步:再加热
O O
H3+O
O
O
CH3 C CH2 C OH
O
CH3 C CH2 C OH
CH3 C CH3 + CO2 (2)乙酰乙酸乙酯类化合物的酸式分解 当用氢氧化钠或氢氧化钾的浓碱溶液(40%的NaOH或KOH)和乙酰 乙酸乙酯类化合物反应时,则发生另一种分解反应,生成两分子羧酸,这 个反应叫乙酰乙酸乙酯类化合物的酸式分解反应。
R'CH2CCHCOC2H5 R
若将一个含α-氢的酯和另一个不含α-氢的酯缩合,控制合适条件可生成主 要产物。 例如,苯甲酰乙酸乙酯可通过苯甲酸乙酯和乙酸乙酯的缩合反 应来制备:
O O O 1.C2H5ONa 2.H+ O C OC2H5 + CH3 C OC2H5 C CH2 C OC2H5
为避免乙酸乙酯的自身缩合,可将苯甲酸乙酯和催化剂(乙醇钠)首 先加入到反应容器中,待达到反应温度时,再将乙酸乙酯慢慢滴加到苯甲 酸乙酯和催化剂的混合溶液中去。
CH3COCH2COOH HOOCCH2CH2CH2COOH
(2) CH3 C O CH2 C O
FeCl3
C O
显色反应 (-)
CH3
CH3 与 CH3
O O CH3CCH2CCH3
=
=
CH3CCH3
=
O
FeCl3
显色反应 (-)
烯醇式结构有一定的稳定性的原因:
1、通过烯醇羟基氢原子构成分子内氢键,形成一个稳定的 六元环状化合物; 2、烯醇式羟基氧原子上的未共用电子对与碳碳双键和碳氧 双键是共轭体系,发生了电子离域,降低了分子的能量。
O O 1.5%NaOH(稀碱) 2.H+/ O CH3 C CH3 + CO2 + C2H5OH
CH3 C CH2 C OC2H5
O
O
CH3 C CH C OC2H5 R
O R' O CH3 C C C OC2H5 R
1.5%NaOH(稀碱) 2.H+/
O CH3 C CH2R + CO2 + C2H5OH
COOC2H5 COOC2H5
1.C2H5ONa 2. H+
?
COOC2H5 COCH2COOC2H5
CH3COOC2H5 +
1.C2H5ONa 2.H+
乙酸乙酯 + 甲酸 乙酯 (2)
CH3COOC2H5 + HCOOC2H5 2.H
+
1.C2H5ONa 2. H+
?
1.C2H5ONa
HCOCH2COOC2H5
?
CH3CHCOOC2H5 CH3CH2CO
(3) 2CH3CH2COOC2H5
1.C2H5ONa 2. H+
13.2.2 乙酰乙酸乙酯在有机合成中的应用
(1)乙酰乙酸乙酯类化合物的酮式分解 用氢氧化钠或氢氧化钾的稀碱溶液(5%的NaOH或KOH)对乙酰乙酸 乙酯类化合物进行水解,首先生成β-酮酸,β-酮酸在加热情况下分解成甲 基酮和二氧化碳,这个反应叫乙酰乙酸乙酯类化合物的酮式分解反应。
1.5%NaOH(稀碱) 2.H+/
O CH3 C CH R + CO2 + C2H5OH R'
从上述反应可知,利用乙酰乙酸乙酯类化合物的酮式分解反应可以制备各 种甲基酮类化合物。 乙酰乙酸乙酯的酮式分解反应过程如下:(共三步) 第一步:先碱(5% NaOH )
O O 5%NaOH O O
CH3 C CH2 C OC2H5
(4)与稀碱作用,再酸化,然后加热分解得到丙酮。
O CH3CCH2COOC2H5 稀OH皂化反应 O CH3CCH2COOH -CO2 脱羧反应P223 O CH3CCH3
怎么证明为烯醇式? A、含有羟基: (1)与Na作用放出H2。 (2)与PCl5作用生成氯代物。
OH CH3C=CHCOOC2H5 PCl5 Cl CH3C=CHCOOC2H5 3-氯-2-丁烯酸乙酯
O
d
+
O
O
d
+
O
O
d
O
CH3C-CH2-CCH3
ÓÓ á Ó ÓÓ± ÓÓ 2,4-Ó ì ÓÓ
CH3C-CH2-C-OC2H5
ÓÓ á Ó ÓÓÓÓ á ÓÓ á ÓÓ b-ÓÓÓ
C2H5OC-CH -C-OC2H5 + 2
ÓÓ á Ó ÓÓÓ ± á ÓÓÓ
β-二羰基化合物的α-H受两个羰基的影响,具有特殊 的活泼性!
13.1 酮-烯醇互变异构
教材P50、P199~200。Kucherov(库切洛夫)反应
O RCH2CR' 酮式
互变异构
OH RCH=CR' 烯醇式
由于分子内的原子(或基团)连接位置不同而产生的异构称 为互变异构。 互变异构,也属于同分异构的一种。
鉴别乙醇、乙醛,可采用的试剂有( B、D )。
A、I2/OH-
(亲核取代反应)
这个反应条件可以适合很多种不同酯的缩合,通常把含有α-氢原子的酯, 在碱催化条件下发生缩合生成β-酮酸酯的反应叫Clainsen(克莱森 ) 酯缩合 反应。
Clainsen 缩合反应机理:(亲核取代反应)
O CH3 C OC2H5 + C2H5OO CH3 C OC2H5 + O
-
B、Cu2++OH-
C、Na
D、饱和NaHSO3
乙酰乙酸乙酯既有羰基的性质,又有羟基和双键的 性质,表明它是由酮式和烯醇式两种互变异构体组成 的:
O CH3CCH2COOC2H5 CH3
OH C=CHCOOC2H5
酮式(92.5%)
b.p.41℃(267Pa)
烯醇式(7.5%)
b.p.33℃(267Pa)
CH3
C O
CH H
C OC2H5 O
CH3-C CH-C-OC 2H5 OH O
共轭体系
六元环
表13-1一些常见羰基化合物烯醇式结构的相对含量
化合物名称 酮式结构
O CH3 C H
O
烯醇式结构
OH CH2 CH
烯醇式含 量
乙醛
极少
OH CH2 C CH3
OH CH2 C OC2H3
OH O CH3 C CH C OC2H5
CH2 C CH3
(互为互变异构体:既有电子的移动,也有原子的移动) 而以下两个结构互为共振杂化体:
O
-
O
-
CH2 C CH3
CH2 C CH3
(共振杂化体:只有电子的移动,没有原子的移动)
13.2 乙酰乙酸乙酯的合成及应用
13.2.1 乙酰乙酸乙酯的合成-Clainsen 缩合反应
13.2.2乙酰乙酸乙酯在有机合成上的应用
OH C=CHCOOC2H5
O O CH C OC2H5
CH3C=CH C
CH3C
互变异构体和共振杂化体最大的区别是后者原子核的相 对位置是不发生相对变化而只存在电子对的转移。前者 是允许原子核的位置发生变化。 书写方法,也不同!
共振杂化体 互变异构体
例如,下列两个结构互为互变异构体:
H
O
OH CH2 C CH3
O CH3-C-CH3
C2H5ONa
O CH3-C-CH2
O-
CH3-C=CH2
O O CH3-C-OC2H5 + CH2-C-CH3
亲核取代反应
O OCH3-C-CH2-C-CH3 OCH2CH3
O O CH3-C-CH2-C-CH3
O
O + H-C-OC2H5
O
NaH
O-CH OC2H5
O O -C-H + C H OH 2 5
O O CH3 C CH2 C OC2H5 1.40%NaOH(浓碱) 2.H+/ O CH3 C OH O + CH3 C OH + C2H5OH
CH3 C CH C OC2H5 + C2H5OH
-
(活泼α -H)
O
O
O H+
(酸化)
O
CH3 C CH C OC2H5
-
CH3 C CH2 C OC2H5
产物有互变异构:
O
O
OH
O
CH3 C CH2 C OC2H5
CH3 C CH C OC2H5
(烯酮式)
讨论: ① Claison酯缩合反应的本质是亲核加成 -消除反 应,最终得到β-二羰基化合物。 ② 酮的酸性一般大于酯,所以在乙醇钠的作用下, 酮更易生成碳负离子。 例如:
O CH2 C OC2H5 + C2H5OH
