药品不良反应分析报告表格
医院药品不良反应的总结分析报告.doc
2014年药品不良反应分析、反馈报告药品不良反应(ADR)监测是合理用药的重要依据,是关系到广大患者用药安全,减少医患纠纷的一项重要工作。
我院2014年共收集上报135例ADR,较2013年的71例增加了90.14%。
现就2014年的ADR报告进行统计、分析,了解ADR的一般规律和特征,为临床合理用药提供依据。
报告人职业和科室分布报告人包括医生和药师,其中医生上报122份,占90.37%;药师上报13份,占9.63%。
ADR报告来自全院18个科室,132例住院患者,3例门诊患者。
详见表1。
表1 2014年ADR上报科室排序科室例数(例)构成比外三病区16 11.85%内一病区15 11.11%内二病区15 11.11%内四病区14 10.37%内三病区12 8.89%临床药学室10 7.41%外一病区8 5.93%儿科病区8 5.83% 中医二病区(肛肠)7 5.19% 中医一病区7 5.19%外四病区 5 3.70% 中医二病区(康复) 5 3.70% ICU综合组 4 2.96%妇产科病区 2 1.48%住院药房 2 1.48%门诊急诊科 2 1.48%外二病区 2 1.48%门诊西药房 1 0.74%合计135 100% 发生ADR的患者性别及年龄分布情况在报告的135例ADR中,男81例,女54例,年龄分布区间为1-95岁,情况详见表2。
表2 患者年龄分布情况年龄例数百分比小于1岁 2 1.48%1-4岁 3 2.22%5-14岁 4 2.96%15-44岁31 22.96%45-64岁38 28.15% 65岁及其以上57 42.22% 总计135 100%用药情况分析用药途径包括静脉给药及口服、皮下注射等。
最常见仍为静脉滴注,占74.85%。
详细统计见表3:表3:给药途径统计排名给药途径一般严重总计例次百分比例次百分比例次静脉滴注116 95.08% 6 4.92% 122口服19 76.0% 6 24.0% 25皮下注射 3 75.0% 1 25.0% 4泵内注射 2 100.0% 0 0.0% 2皮内注射 2 100.0% 0 0.0% 2静脉注射 1 50.0% 1 50.0% 2鞘内给药0 0.0% 2 100.0% 2灌注 1 100.0% 0 0.0% 1肌内注射 1 100.0% 0 0.0% 1阴道给药 1 100.0% 0 0.0% 1鼻饲 1 100.0% 0 0.0% 1总计147 90.18% 16 9.82% 163引起ADR的可疑药物共包含73个品种,可疑药品依据药理作用分类,共包括10种药物;其品种数及上报次数排名统计结果见表4所示:表4 药物类别品种数排名及上报次数排名药物类别品种数构成比(%)上报次数构成比(%)抗感染药物21 28.77 55 33.74中药注射剂7 9.59 41 25.15循环系统药物 5 6.85 9 5.52血液系统药物8 10.96 11 6.75神经系统药物 4 5.48 9 5.52呼吸系统药物 2 2.74 4 2.45消化系统药物 3 4.11 4 2.45镇痛药物 6 8.22 10 6.13内分泌系统药物 6 8.22 7 4.29其他专科用药11 10.87 13 12.90合计73 100.00 163 100.00由表4可见,引起ADR例数最多的为抗感染药物,其所含品种数也最多,排名第二的则为中药注射剂。
药品不良反应报告表范例

药品不良反应/ 事件报告表
新的□严重□一般□医疗卫生机构□生产企业经营企业□个人□编码□□□□□□□□□□□□□□□□□□□单位名称:部门:电话:报告日期:年月日
不良反应
分析
1.用药与不良反应的出现有无合理的时间关系?有√无□
2.反应是否符合该药已知的不良反应类型?是√否□不明□
3.停药或减量后,反应是否消失或减轻?是√否□不明□未停药或未减量□
4.再次使用可疑药品后是否再次出现同样反应?是□否□不明□未再使用√
5.反应是否可用并用药的作用、患者病情的进展、其他治疗的影响来解释?是□否√不明□
报告人职业(医疗机构):医生□药师□护士□其他□报告人职务职称(企业):报告人签名:。
(药店GSP表格)药品不良反应报告表
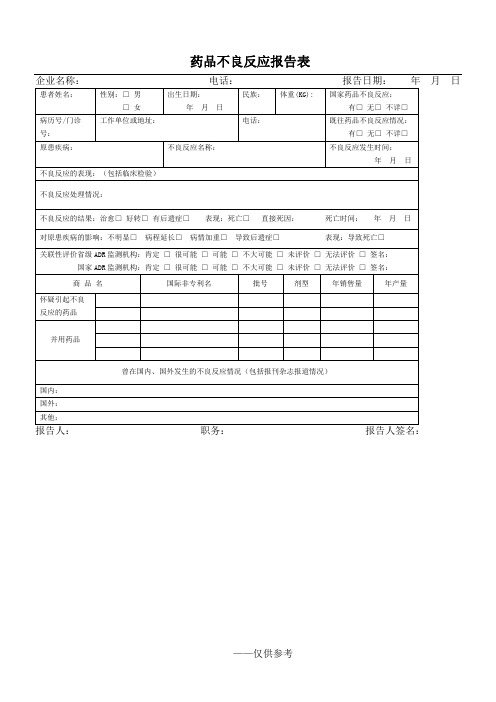
企业名称:电话:报告日期:年月日
患者姓名:性别:□男□女来自出生日期:年月日
民族:
体重(KG):
国家药品不良反应:
有□无□不详□
病历号/门诊号:
工作单位或地址:
电话:
既往药品不良反应情况:
有□无□不详□
原患疾病:
不良反应名称:
不良反应发生时间:
年月日
不良反应的表现:(包括临床检验)
不良反应处理情况:
商品名
国际非专利名
批号
剂型
年销售量
年产量
怀疑引起不良反应的药品
并用药品
曾在国内、国外发生的不良反应情况(包括报刊杂志报道情况)
国内:
国外:
其他:
报告人:职务:报告人签名:
不良反应的结果:治愈□好转□有后遗症□表现:死亡□直接死因:死亡时间:年月日
对原患疾病的影响:不明显□病程延长□病情加重□导致后遗症□表现:导致死亡□
关联性评价省级ADR监测机构:肯定□很可能□可能□不大可能□未评价□无法评价□签名:
国家ADR监测机构:肯定□很可能□可能□不大可能□未评价□无法评价□签名:
药品不良反应报告表格

药品不良反应报告表格一、背景介绍药品安全是一个极其重要的问题,任何时候,都不能忽视对药品不良反应的监测和报告。
药品不良反应是指使用药物后,出现的与治疗目的无关的不良症状或事件。
这些不良反应可能是轻微的,也可能是严重的,甚至可能危及生命。
二、意义和目的药品不良反应报告表格的目的在于收集关于药物使用过程中出现的不良反应信息,以便及时发现和评估药品的安全性,并采取相应的措施来减少不良反应对患者的伤害。
通过报告不良反应,可以提高公众对药物使用风险的认识,增强患者和医生的药物安全意识,为改进药物治疗提供数据支持。
三、报告表格内容药品不良反应报告表格通常包括以下内容:1. 药品信息:包括药品的通用名称、商品名、剂型、规格等。
2. 不良反应信息:详细描述患者使用药物后出现的不良反应症状,如头痛、恶心、呕吐等。
同时,还需要填写发生不良反应的时间、频率和严重程度等。
3. 患者信息:包括患者的姓名、性别、年龄、身体状况等基本信息。
同时,还需要填写患者的病历号码、联系方式等以方便进一步的联系。
4. 医生信息:填写处方医生的姓名、执业医师证号、科室等信息,以便进行进一步的咨询和调查。
5. 报告人信息:填写报告人的姓名、职位、联系方式等,以方便进行后续的沟通和取证。
四、使用流程1. 实施单位(如医院、药店等)需要将药品不良反应报告表格制作成电子版或纸质版,并确保在相关部门和医务人员中进行广泛宣传。
2. 患者或医生在发现药品不良反应后,应填写完整的药品不良反应报告表格,并尽快递交给相关部门或医务人员。
3. 相关部门或医务人员收到报告后,需要及时进行初步评估,并进一步收集相关的信息和数据。
4. 适时组织专家对收集到的药品不良反应报告进行分析和评估,并提出相关的建议和对策。
5. 及时向公众发布药品不良反应信息,并提醒患者和医生注意合理用药和药物安全。
六、总结药品不良反应报告表格是药品安全监测和管理的重要工具,通过收集和分析药品不良反应信息,可以及时发现和解决药品存在的安全问题,进一步提高患者的用药安全性。
药品不良反应报告表范本
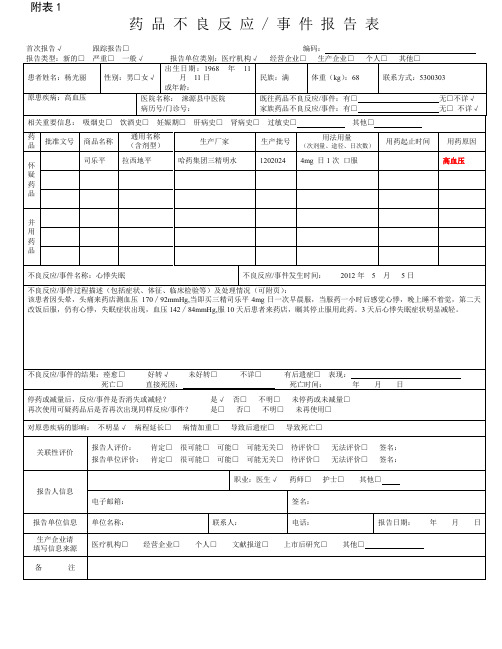
附表1药品不良反应 / 事件报告表首次报告√跟踪报告□编码:报告类型:新的□严重□一般√报告单位类别:医疗机构√经营企业□生产企业□个人□其他□患者姓名:杨光丽性别:男□女√出生日期:1968 年11月11日或年龄:民族:满体重(kg):68 联系方式:5300303原患疾病:高血压医院名称:涞源县中医院病历号/门诊号:既往药品不良反应/事件:有□无□不详√家族药品不良反应/事件:有□无□不详√相关重要信息:吸烟史□饮酒史□妊娠期□肝病史□肾病史□过敏史□其他□药品批准文号商品名称通用名称(含剂型)生产厂家生产批号用法用量(次剂量、途径、日次数)用药起止时间用药原因怀疑药品司乐平拉西地平哈药集团三精明水1202024 4mg 日1次口服高血压并用药品不良反应/事件名称:心悸失眠不良反应/事件发生时间:2012年 5 月5日不良反应/事件过程描述(包括症状、体征、临床检验等)及处理情况(可附页):该患者因头晕,头痛来药店测血压170∕92mmHg,当即买三精司乐平4mg日一次早晨服,当服药一小时后感觉心悸,晚上睡不着觉,第二天改饭后服,仍有心悸,失眠症状出现,血压142∕84mmHg,服10天后患者来药店,瞩其停止服用此药。
3天后心悸失眠症状明显减轻。
不良反应/事件的结果:痊愈□好转√未好转□不详□有后遗症□表现:死亡□直接死因:死亡时间:年月日停药或减量后,反应/事件是否消失或减轻?是√否□不明□未停药或未减量□再次使用可疑药品后是否再次出现同样反应/事件?是□否□不明□未再使用□对原患疾病的影响:不明显√病程延长□病情加重□导致后遗症□导致死亡□关联性评价报告人评价:肯定□很可能□可能□可能无关□待评价□无法评价□签名:报告单位评价:肯定□很可能□可能□可能无关□待评价□无法评价□签名:报告人信息职业:医生√药师□护士□其他□电子邮箱:签名:报告单位信息单位名称:联系人:电话:报告日期:年月日生产企业请填写信息来源医疗机构□经营企业□个人□文献报道□上市后研究□其他□备注严重药品不良反应,是指因使用药品引起以下损害情形之一的反应:1) 导致死亡;2)危及生命;3)致癌、致畸、致出生缺陷;4)导致显着的或者永久的人体伤残或者器官功能的损伤;5)导致住院或者住院时间延长;6)导致其他重要医学事件,如不进行治疗可能出现上述所列情况的。
药品不良反应报告表模板

药品不良反应报告表部分项目填报注意事项一、药品不良反应事件名称及描述1.如果患者出现皮疹伴瘙痒,不要把二者同时列为一个不良反应,应当分类描述为“皮疹;瘙痒",对于皮疹的发生部位、大约形态进行描述;2.如果患者发生多种过敏反应,就不用分类描述,直接描述为“过敏反应"或是“过敏样反应”;不属于过敏反应的其他症状,应当分类描述;3.如果患者出现过敏性休克,就必须描述患者的临床表现(包含呼吸道阻塞、微循环障碍、中枢神经系统症状及皮肤过敏症状)及体征;例如头晕、面色苍白、呼吸困难、胸闷、腹痛、出汗、脉搏增快及血压下降等;此时相应的体征进行描述,如体温、心率、血压、呼吸频率等;还包含不良反应发生前后的症状和体征的动态变化.4.如果患者出现血象异常,要将不良反应发生前后相应指标、实验室检查进行描述;例如患者白细胞降低,此时就需要提供患者入院时(或服药前)白细胞指数,服药后发生不良反应是监测的白细胞指数以及采取措施停药后患者白细胞有所恢复的指数。
5.如果患者出现消化道反应,例如腹泻、呕吐等,请具体描述一哈相关的症状;例如腹泻,一日几次、什么性状;呕血,一日几次、颜色等性状;呕吐,一日几次、内容物是什么。
二、药品不良反应发生后采取的措施及转归1、药品不良反应发生以后,主要采取的治疗措施要进行描述。
例如立即停药,给与抗过敏治疗(过敏反应)、给与升白细胞治疗(白细胞下降)、给与物理降温(高热)等对症治疗。
具体的治疗措施,例如给与地塞米松10mg肌肉注射,要尽量详细描述对症治疗的药物及剂量.2、药品不良反应的转归,要尽量描述采取对症治疗之后患者的转归.有的医疗机构在患者刚刚发生不良反应,采取措施尚未缓解的时候就立即上报,这种是不规范的。
国家规定药品不良反应报告的上报时限。
大家应当按照规定时限完整的对药品不良反应进行上报。
备注:提供一个药品不良反应/事件报告表填写模板(见附表),供大家参考。
附表药品不良反应 / 事件报告表首次报告□跟踪报告□编码:。
药品不良反应报告表、填写示例及填写说明
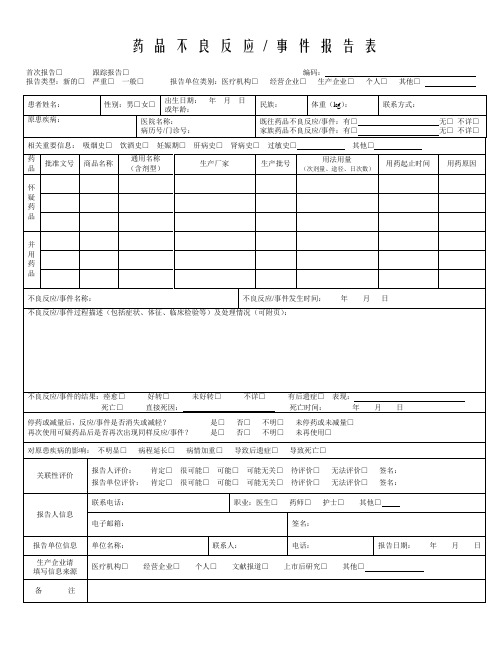
药品不良反应/ 事件报告表首次报告□跟踪报告□编码:报告类型:新的□严重□一般□报告单位类别:医疗机构□经营企业□生产企业□个人□其他□药品不良反应/ 事件报告表示例首次报告□跟踪报告□编码:报告类型:新的□严重□一般□报告单位类别:医疗机构□经营企业□生产企业□个人□其他□《药品不良反应/事件报告表》填写说明1.《药品不良反应/事件报告表》应填写真实事件,报表所列患者信息及怀疑药品信息项目必须真实、完整、准确。
2.《药品不良反应/事件报告表》填写字迹要清晰,其中选择项画“√”,叙述项应准确、简明,不得有缺漏项。
3. 新的□严重□一般□(1)新的药品不良反应:是指药品说明书中未载明的不良反应。
说明书中已有描述,但不良反应发生的性质、程度、后果或者频率与说明书描述不一致或者更严重的,按照新的药品不良反应处理。
根据不良反应/事件损害的严重程度,不良反应/事件可能是新的严重的,也可能是新的一般的。
(2)严重药品不良反应,是指因使用药品引起以下损害情形之一的反应:1) 导致死亡;2)危及生命;3)致癌、致畸、致出生缺陷;4)导致显著的或者永久的人体伤残或者器官功能的损伤;5)导致住院或者住院时间延长;6)导致其他重要医学事件,如不进行治疗可能出现上述所列情况的。
(3)一般:指新的、严重的药品不良反应以外的所有不良反应。
4. 单位名称:必须填写单位的完整全称,如日照市人民医院。
5. 部门:应填写科室的标准全称,如:消化内科、普外三科等。
6. 电话:填写报告部门(即科室)的电话。
7. 报告日期:指上交不良反应/事件报告的时间。
新的或严重的药品不良反应/事件应于发现之日起15日内报告,其中死亡病例须立即报告,其他药品不良反应应30日内报告。
有随访信息的,应当及时报告。
8. 患者姓名:填写患者真实全名。
9. 体重:以千克为单位。
如果不知道准确体重,请做一个最佳的估计。
10. 联系方式:最好填写患者的联系电话,也可填写患者的通信地址。
(药店GSP表格)药品不良反应报告表
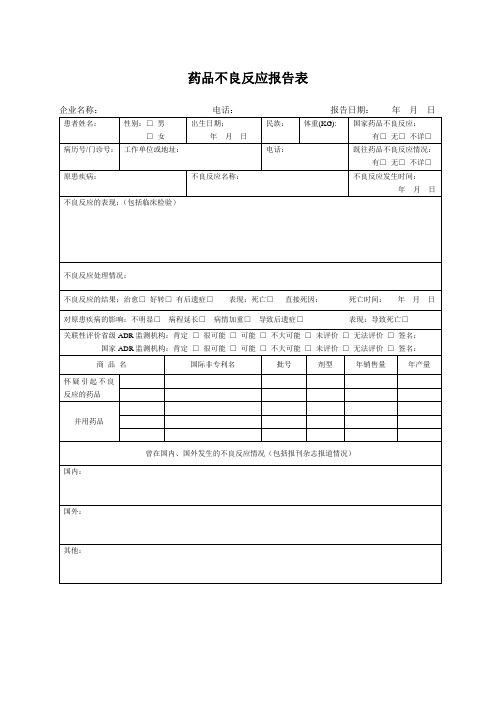
国际非专利名
批号
剂型
年销售量
年产量
怀疑引起不良反应的药品
并用药品
曾在国内、国外发生的不良反应情况(包括报刊杂志报道情况)
国内:
国外:
其他:
不良反应的结果:治愈□好转□有后遗症□表现:死亡□直接死因:死亡时间:年月日
对原患疾病的影响:不明显□病程延长□病情加重□导致后遗症□表现:导致死亡□
关联性评价省级ADR监测机构:肯定□很可能□可能□不大可能□未评价□无法评价□签名:
国家ADR监测机构:肯定□很可能□可能□不大可能□未评价□无法评价□签名:
药品不良反应报告表
企业名称:电话:报告日期:年月日
患者姓名:
性别:□男
□ 女
出生日期:
年月日
民族:
体重(KG):
国家药品不良反应:
有□无□不详□
病历号/门诊号:
工作单位或地址:
电话:
既往药品不良反应情况:
有□无□不详□
原患疾病:不良反应名称:来自不良反应发生时间:年月日
不良反应的表现:(包括临床检验)
不良反应处理情况:
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
药品不良反应分析报告
表格
文件编码(GHTU-UITID-GGBKT-POIU-WUUI-8968)
药品不良反应/事件报告表
报告类型:新的□严重□一般□首次报告□跟踪报告□报告来源:医疗机构□药品经
除非得到允许,报告表中的个人信息将予以保密。
严重药品不良反应/事件是指因使用药品引起以下损害情形之一的反应/事件:
1)导致死亡;
2)危及生命;
3)致癌、致畸、致出生缺陷;
4)导致显着的或永久的人体伤残或器官功能的损伤;
5)导致住院或住院时间延长
6)其他有意义的重要医学事件。
如,尽管事件不会立即危及生命或导致死亡和/或需住院,但为了预防出现任一上述所列情况可能需要进行治疗,通常也被认为是严重的。
关联性评价说明:
肯定:用药及反应发生时间顺序合理;停药以后反应停止,或迅速减轻或好转;再次使用,反应再现,并可能加重(即激发试验阳性),同时有文献资料佐证,并已排除原患疾病等其他混杂因素影响。
很可能:无重复用药史,余同“肯定”,或虽然有合并用药,但基本可排除合并用药导致反应发生的可能性。
可能:用药与反应发生时间关系密切,同时有文献资料佐证;但引发ADR/ADE的药品不止一种,或原患疾病病情进展因素不能排除。
可能无关:ADR/ADE与用药时间相关性不密切,反应表现与已知该药的ADR/ADE不吻合,原患疾病发展同样可能有类似的临床表现。
待评价:报表内容填写不齐全,等待补充后再评价,或因果关系难以定论,缺乏文献佐证。
无法评价:报表缺项太多,因果关系难以定论,资料又无法补充。
其他说明
合并用药:指发生此药品不良反应/事件时患者除怀疑药品外得其他用药情况,其中也包括患者自行购买的药品或中草药等。
报告的处理
所有的报告将会录入数据库,专业人员会分析药品和不良反应之间的关系。
我们会考虑风险是否普遍或严重,然后决定我们是否需要采取行动,例如在药品说明书中加入警示信息,更新药
品如何安全使用的信息,如,限制使用剂量或在某些特定人群中限制使用。
极少数情况下,我们会把产品撤市,只有当我们认为产品的风险大于效益时。
