色谱参数的测试及计算
中药色谱分析试验讲义试验一高效液相色谱操作及其参数的测定一

《中药色谱分析》实验讲义实验一高效液相色谱操作及其参数的测定一、目的要求:1.熟悉高效液相色谱仪的原理和基本方法2.熟悉使用高效液相色谱仪基本操作方法二、实验提要:以高压液体为流动相的液相色谱分析法称高效液相色谱法(HPLC)。
其基本方法是用高压泵将具有一定极性的单一溶剂或不同比例的混合溶剂泵入装有填充剂的色谱柱,经进样阀注入的样品被流动相带入色谱柱内进行分离后依次进入检测器,由记录仪、积分仪或数据处理系统记录色信号或进行数据处理而得到分析结果。
由于高效液相色谱法具有分离效能高、选择性好、灵敏度高、分析速度快、适用范围广(样品不需气化,只需制成溶液即可)、色谱柱可反复使用的特点,在《中国药典》中有50种中成药的定量分析采用该法,已成为中药制剂含量测定最常用的分析方法。
高效液相色谱法按固定相不同可分为液-液色谱法和液-固色谱法;按色谱原理不同可分为分配色谱法(液-液色谱)和吸附色谱法(液-固色谱)等。
目前,化学键合相色谱应用最为广泛,它是在液-液色谱法的基础上发展起来的。
将固定液的官能团键合在载体上,形成的固定相称为化学键合相,不易流失是其特点,一般认为有分配与吸附两种功能,常以分配作用为主。
C18(ODS)为最常使用的化学键合相。
根据固定相与流动相极性的不同,液-液色谱法又可分为正相色谱法和反相色谱法,当流动相的极性小于固定相的极性时称正相色谱法,主要用于极性物质的分离分析;当流动相的极性大于固定相的极性时称反相色谱法,主要用于非极性物质或中等极性物质的分离分析。
在中药制剂分析中,大多采用反相键合相色谱法。
三、实验内容1.高效液相色谱系统组成:(一)高压输液系统由贮液罐、脱气装置、高压输液泵、过滤器、梯度洗脱装置等组成。
1.贮液罐由玻璃、不锈钢或氟塑料等耐腐蚀材料制成。
贮液罐的放置位置要高于泵体,以保持输液静压差,使用过程应密闭,以防止因蒸发引起流动相组成改变,还可防止气体进入。
2.流动相流动相常用甲醇-水或乙腈-水为底剂的溶剂系统。
液相色谱计算公式

液相色谱计算公式
液相色谱(Liquid Chromatography,简称LC)的计算公式包括保留时间和保留率的计算公式。
1.保留时间(Retention Time)的计算公式:
保留时间是指化合物在液相色谱柱中停留的时间,它是液相色谱中最常用的性能参数之一。
保留时间(t_R)的计算公式为:
t_R = t_m - t_0
其中,t_m表示化合物在色谱柱中出现的时间,称为终点时间(即化合物在色谱柱中运行的总时间);
t_0表示无保留物(即溶剂前端)出现的时间,称为起点时间(即样品注入柱后到出现第一个色谱峰的时间)。
2.保留率(Retention Factor)的计算公式:
保留率是指化合物在色谱柱中停留时间与无保留物停留时间之比,用于评估化合物在液相色谱中的保留能力。
保留率(k)的计算公式为:
k = (t_R - t_0) / t_0
其中,t_R表示化合物的保留时间,t_0表示无保留物的保留时间。
在实际的液相色谱分析中,需要根据所使用的色谱柱、流动相组
成和流速等参数来选择适当的计算公式和相应的数值,以获得准确的
结果。
另外,液相色谱还有其他常用的计算公式,如峰面积的计算公式、分离度的计算公式等,这些公式可以用于进一步量化和评估色谱分离
效果和样品组成。
3种色谱参数的详细说明

3种色谱参数的详细说明
1、色谱柱柱效参数:
色谱柱的柱效通常是用理论塔板数或有效理论塔板数来衡量,而它们的大小又与区域宽度有直接关系。
区域宽度:这个色谱流出曲线上的一个重要参数,它的大小反映色谱柱与所选色谱条件的好坏,从色谱分离的角度着眼,希望区域宽度越窄越好,通常度量色谱区域宽度有三种方法:标准偏差,峰宽以及半峰宽。
2、色谱的分离参数:
塔板数和塔板高度:色谱分析的前提是待测组分的分离,而无论柱效参数还是选择性参数均反映不出分离效能的高低,为此引入了一个衡量色谱柱综合分离能力的指标-分离度。
分离度又称分辨率,它是以组分的分离情况来制定的,当两组分色谱峰之间的距离足够大,两峰不互相重叠,即保留值有足够的差别,且峰形较窄时,才可以仍为两组分达到了较好的分离,因此色谱图上相邻两峰的保留时间之差与峰宽均值的比值称为分离度,其定义式为:
式中tR1,tR2分别组分1.2的保留时间;W1,W2分别为组分1.2的峰宽,分离度作为两相邻色谱峰分离程度的量度,其值也大,表明两组分的分离情况越好,对于等面积的两色谱峰,当R=1时,两峰有5%的重合,两峰的分开程度为95%,而当R=1.5时,两峰的分离程度达99.7%,可认为两峰完全分离,如图所示,因此R=1.5可作为两峰完全分离的标志。
不同分离度时两峰分离情况
用色谱图上得到的信息,利用定义式可直接计算分离度,但并不能提现出影响分离度的因素,其影响因素将在色谱方程式中做具体阐述。
3、相平衡参数:
在色谱分离过程中,混合物中的两个组分要达到完全分离,其中重要的一点是两组分色谱峰间的距离必须足够大,也就是说两组分保留值的差别要足够大。
以上关于色谱的三种参数介绍,更多内容后期会更新,如果需要可以关注或者查
阅更多资料。
色谱参数的测试及计算

色谱参数的测试及计算(色谱理论验证性实验)一、目的要求1. 通过本实验基本色谱参数的测试与计算,定量地了解溶质组分在色谱柱过程中热力学和动力学作用的量度。
2. 理解各色谱参数的意义及其相互关系。
3. 通过本实验进一步掌握柱效、柱选择性、分离能力、保留值等性质,使之能选择出最佳色谱操作条件,得到可靠的定性,定量结果。
二、测定意义通过试验,了解色谱中的各个基本参数, 从色谱图中学会参数的获得及各基本参数计算。
在规定的色谱条件下,测定惰性组分的死时间(t M )及被测组分的保留时间(t R )、半高峰宽(W 1/2)、及峰高(H )等参数,便可计算出基本色谱参数值。
1 调整保留时间:用公式计算出2 相对保留值:计算出(正庚烷, 正已烷);( 乙酸正丁酯, 正已烷);( 正辛烷, 正已烷)的相对保留值,以正已烷作标准。
3 容量因子:计算出正已烷;正庚烷;乙酸正丁酯;正辛烷的K ’,以其中K ’=2-5的组分进行计算。
4 理论塔板数:以其中K ’=2-5的组分进行计算。
MR R t t t -=,,,()()(),()()()R i g i N i is R S g s N s t V V t V V α===MRM M R t t t t t K ,,=-=222/1)(16)(54.5Wt W t n R R ==5 有效塔板数:以其中K ’=2-5的组分进行计算。
当K ’足够大时理论塔板数与有效塔板数是否近似相等。
6 分离度:计算出较难分离二组分的分离度。
7 分离数:计算出任意二相邻正构烷烃峰之间的TZ 值(即二峰间可容纳的峰数)。
8 保留指数:计算出任意二相邻正构烷烃峰之间的I 值三、方法原理 “塔板理论”:把色谱柱看作一个有若干层塔板的分馏塔,通过物质在每层塔板中进行平衡的物理模型过程,导引出一个描述色谱流出曲线的数学表达式:式中 c ——色谱流出曲线上任意一点样品的浓度;n ——理论塔板数;m ——溶质的质量;V R ——溶质的保留体积,即从进样到色谱峰极大点出现时通入色谱柱中载气的体积;Wt t W W t t R R R R R 122/12/112)(2-≈+-=2,22/1,)(16)(54.5Wt W t n R R eff==11k R k αα+⎫=⎪+⎝⎭]lg lg lg lg [100,)(,)(,)(,)(Z R n Z R z R X R t t t t Z --+=I +X 1)1(2/1)(2/1)()1(--=++Z Z Z Z R W W t t TZV——在色谱流出曲线上任意一点的保留体积。
μgc检测限的计算方法

μgc检测限的计算方法
μGC(微型气相色谱)是一种高效气相色谱(GC)的变种,通常用于分析样品中的挥发性有机化合物(VOCs)。
μGC检测限的计算涉及到仪器灵敏度、信噪比等因素。
以下是计算μGC检测限的一般步骤:
1. 峰高和峰面积的测量:首先,在无样品和有样品的条件下进行μGC分析。
记录相关峰的高度(peak height)和峰面积(peak area)。
2. 信噪比计算:计算信噪比(Signal-to-Noise Ratio,SNR)。
信噪比是峰高或峰面积与背景噪声之比。
一般来说,SNR可通过以下公式计算:
SNR=峰高噪声
或
SNR=峰面积噪声
这里的“噪声”是在没有目标化合物存在的情况下记录的背景峰的高度或面积。
3. 检测限的计算:μGC检测限通常被定义为信噪比为3:1或者10:1时的目标化合物浓度。
根据具体的信噪比定义,可以使用以下公式计算检测限:
Detection Limit=噪声3 或 10Detection Limit=3 或 10噪声
其中,“噪声”是在没有目标化合物存在的条件下记录的背景峰的高度或面积。
需要注意的是,μGC检测限的计算可能还会受到一些其他因素的影响,例如仪器的灵敏度、分辨率等。
因此,在具体的分析中,最好参考仪器的文档或制造商的建议。
高效液相色谱实验

高效液相色谱实验The document was prepared on January 2, 2021高效液相色谱实验I. 色谱柱的评价请在实验前预习基础分析化学实验第二版137-140页.目的(1)了解高效液相色谱仪的工作原理;(2)学习评价液相色谱反相柱的方法.原理高效液相色谱是色谱法的一个重要分支.它采用高压输液泵和小颗粒的填料,与经典的液相色谱相比,具有很高的柱效和分离能力.色谱柱是色谱仪的心脏,也是需要经常更换和选用的部件,因此,评价色谱柱是十分重要的.而且对色谱柱的评价也可以检查整个色谱仪的工作状况是否正常.评价色谱柱的性能参数主要有:(1) 柱效理论塔板数n式中t r 为测试物的保留时间,W 1/2为色谱峰的半峰宽.(2) 容量因子k’式中t 0为死时间,通常用已知在色谱柱上不保留的物质的出峰时间作死时间.(3)相对保留值选择因子α式中k 1’和k 2’分别为相邻两峰的容量因子,而且规定峰1的保留时间小于峰2的.(4)分离度R s式中t r1、t r2分别为相邻两峰的保留时间,W b1、W b2分别为两峰的底宽.对于高斯峰来讲,W b =2.为达到好的分离,我们希望n 、α和R s 值尽可能大.一般的分离如α=,R s =,需n 达到2000.柱压一般为104 kPa 或更小一些.本实验采用多核芳烃作测试物,尿嘧啶为死时间标记物,评价反相色谱柱.仪器和试剂Waters 510高效液相色谱仪由Waters 510高压输液泵,Rheodyne 7725i 进样器,440检测器和记录仪组成色谱柱:5 cm × mm ., YWG-C 18H 37 ODS,10 μm流动相:甲醇-水80+20样品I : 含尿嘧啶 mg ·mL -1、萘 mg ·mL -1、联苯 mg ·mL -1、菲 mg ·mL -1的甲醇混合溶液;样品I I :尿嘧啶的甲醇溶液;萘的甲醇溶液;联苯的甲醇溶液;菲的甲醇溶液.溶液浓度约为·mL -1;实验内容(1) 准备流动相.将色谱纯甲醇和色谱纯水按比例配制200mL 溶液,混合均匀并经超声波脱气后加入到仪器储液瓶中.(2) 检查电路连接和液路连接正确以后,接通高压泵、检测器和记录仪的电源.设定操作条件为:流速 mL ·min -1,压力上限2′104 kPa 约3000 psi,检22/1r )/(54.5W t n =00r /)('t t t k -=12'/'αk k =)/()(2b2b1r1r2s W W t t R +-=测波长254 nm 该仪器检测波长已固定,灵敏度 AUFS,记录仪走纸速度 cm ·min -1,记录灵敏度为5 mV.开启记录仪走纸开关记录基线.并调节基线到合适位置一般为距右10%处.(3) 待基线平稳后建议观察检测器的读数显示,将进样阀手柄拨到“Load ”的位置,使用专用的液相色谱微量注射器取5μL 样品注入色谱仪进样口,然后将手柄拨到“Inject ”位置,同时按一下检测器的标记按钮,同时计时,记录色谱图.(4) 重复3的实验两次.(5) 用同样方法进纯样品的甲醇溶液,确定出峰顺序.(6) 根据三次实验所得结果计算色谱峰的保留时间、半峰宽,然后计算色谱柱参数n 、k’,以及相邻两峰的α、R s(7) 将流速降为0,待压力降为0后关机.思考题1. 高效液相色谱与气相色谱相比有什么相同点和不同点2. 如何保护色谱柱延长使用寿命高效液相色谱实验II固相萃取水样中的多核芳烃并以内标法测定其含量目的(1) 学习固相萃取法处理样品;(2) 用内标法定量.原理固相萃取法是色谱法的一个重要的应用.在此方法中,使一定体积的样品溶液通过装有固体吸附剂的小柱,样品中与吸附剂有强作用的组分被完全吸附;然后,用强洗脱溶剂将被吸附的组分洗脱出来,定容成小体积被测样品溶液.使用固相萃取法,可以使样品中的组分得到浓缩,同时可初步除去对感兴趣组分有干扰的成分,从而提高了分析的灵敏度.固相萃取不仅可用于色谱分析中的样品预处理,而且可用于红外光谱、质谱、核磁共振、紫外和原子吸收等各种分析方法的样品预处理.C18固相萃取小柱具有疏水作用,对非极性的组分有吸附作用,因此可以从水中将多核芳烃萃取出来,完成浓缩样品的作用.固相萃取小柱还有其他类型,如极性、离子交换等.内标法的原理是,设在V mL 样品中含有W i g 待测组分i,加入W S g 内标物S,混匀后进样,得组分i 及内标物S 的峰面积分别为A i 及A S .由于峰面积正比于通过检测器的物质量,所以有:W i =f i A iW S =f S A S式中f i 、f S 分别为组分i 和内标S 的校正因子.两式相除,得所以,组分i 的体积浓度为:S Si S i i W A A f f W ⋅⋅=V W A A f V W A A f f VW SS i i S S i S i i '⋅⋅=⋅⋅=fi’可用已知被测物i和内标物浓度的样品进样分析得到.内标法是一种相对测量方法,因此,进样量不必准确,操作条件稍有变化对结果没有什么影响.仪器和试剂Waters 510高效液相色谱仪由Waters 510高压输液泵,Rheodyne 7725i进样器和440检测器组成色谱柱:5 cm× mm ., YWG-C18H37ODS,10 μm流动相:甲醇-水80+20 流速: mL·min-1检测波长:254 nmC18固相萃取小柱:2支25 mL移液管:1支50 mL医用注射器:1支10 mL医用注射器:2支2 mL容量瓶:2个样品I:内标标准样,含萘 mg·mL-1、联苯 mg·mL-1、菲 mg·mL-1的甲醇溶液.样品II:内标物溶液.含联苯 mg·mL-1的甲醇溶液.样品III:含萘、菲的被测水样.实验内容(1)固相萃取小柱预处理:用10 mL注射器将2 mL甲醇压过小柱,再将2 mL 纯水压过小柱.(2)用移液管取25 mL水样,用50 mL注射器压过小柱,这时水样中的萘和菲被吸附在小柱上.在小柱下端承接一2 mL的容量瓶,将约 mL甲醇用10 mL 注射器压过小柱到容量瓶中,加入一定量内标联苯溶液,定容摇匀,得到浓缩的样品.(3)按“实验I”中的步骤,进样分析内标标准样和浓缩样品各三次.(4)取平均结果,计算峰面积A s和A i;根据内标标准样的浓度计算f i’,再计算出浓缩样品中的萘和菲的浓度,进而计算出原水样中的浓度mg·mL-1.思考题1.内标法与外标法各有哪些特点本实验为什么采用内标法为好2.为什么要对色谱分析中的样品进行预处理简单列出三个以上的原因.。
色谱分析(中国药科大学)第2章色谱法的基本参数及理论
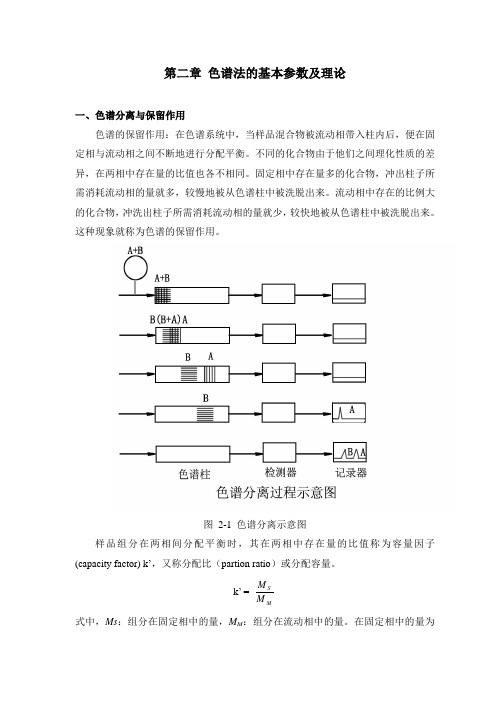
第二章 色谱法的基本参数及理论一、色谱分离与保留作用色谱的保留作用:在色谱系统中,当样品混合物被流动相带入柱内后,便在固定相与流动相之间不断地进行分配平衡。
不同的化合物由于他们之间理化性质的差异,在两相中存在量的比值也各不相同。
固定相中存在量多的化合物,冲出柱子所需消耗流动相的量就多,较慢地被从色谱柱中被洗脱出来。
流动相中存在的比例大的化合物,冲洗出柱子所需消耗流动相的量就少,较快地被从色谱柱中被洗脱出来。
这种现象就称为色谱的保留作用。
图 2-1 色谱分离示意图样品组分在两相间分配平衡时,其在两相中存在量的比值称为容量因子(capacity factor) k ’,又称分配比(partion ratio )或分配容量。
k ’ = MS M M 式中,Ms :组分在固定相中的量,M M :组分在流动相中的量。
在固定相中的量为零的化合物,其k ’=0,这些组分被称为在该色谱条件下的非保留物质。
容量因子(分配比)可通过实验计算:k ’ =MR t t ' 。
即k ’为组分在固定相中消耗的时间与其在流动相中消耗的时间之比。
样品组分在两相中分配平衡时,其在固定相和流动相中的浓度比称为分配系数(partion factor ),分配系数以K 表示。
其公式如下:Ms c c K ==组分在流动相中的浓度组分在固定相中的浓度 K =m m S S V M V M // = k ’· S m V V 式中,Ms/Vs 为样品组分在固定相中的浓度,M m /V m 为样品组分在流动相中的浓度。
分配系数大的组分保留时间长(色谱的保留作用强),分配系数小的组分保留时间短(色谱的保留作用弱)。
K = k ’· Sm V V = k ’· β 式中β = Sm V V 称为相比率,即色谱柱中流动相体积与固定相体积之比。
例在毛细管GC 中壁涂空心柱的相比为:β = 固定相体积(柱中)流动相体积(柱中) = dfrl l r ⋅ππ22 = df r 2式中r为毛细管柱横截面的半径,d f为柱内壁固定液的膜厚。
方法确证实验实例1(气相色谱法)

检验方法标准修订细则1 标准曲线的绘制标准曲线的浓度点(包括试剂空白)至少应作: 光谱法(包括分光光度法, 原子吸收、原则荧光、ICP/MS法)为5个点, 色谱法和电化学法为4个。
每个浓度至少测定3次, 以3次测定值的均值与对应的浓度绘制标准曲线, 计算回归方程和相关系数。
相关系数的要求: 石墨炉原子吸收法应在0.99以上, 其它方法应在0.999以上。
在规定的采样体积和分析条件下, 标准曲线的测定范围应包括相应污染物0.5~5倍的标准限值。
2 检出限、测定下限、测定上限、测定范围测试方法: 连续测定10次以上空白溶液(或接近空白浓度的溶液), 计算响应值的平均值和标准差, 以3倍标准差所对应的待测物浓度为检出限。
以10倍标准差所对应的待测物浓度为测定下限。
分光光度法习惯用与0.01吸光度相对应的浓度值为检出限。
测定下限至测定上限之间的浓度范围作为测定范围。
3 精密度测试测试方法: 按方法的测定上限浓度c , 配制0.1c、0.5c、0.9c 的标准溶液浓度, 各浓度标准溶液按方法操作步骤平行测定6次, 计算相对标准偏差(RSD)。
要求:RSD<10%.4 准确度的测试测试方法: 样品加标回收法。
在现场样品中, 加入高、中、低3个浓度的标准溶液(高、中、低3个浓度分别为污染物限值浓度的0.5倍、2倍、4倍), 然后测定样品溶液和加标溶液, 至少各测定3次, 由平均值计算加标回收率。
实验时应注意: 加标后的浓度应在测定方法的线性范围之内。
要求: 平均加标回收率应在90%-110%之间。
附件2新方法确认实验报告示例1(气相色谱法)《居住区大气中苯、甲苯、二甲苯卫生标准检验方法* 一次热解析法》方法确认报告为证实本实验室能够正确掌握《居住区大气中苯、甲苯、二甲苯卫生标准检验方法一次热解析法》, 根据我国《实验室资质认定评审准则》 5.3条款“检测和校准方法”的要求和本中心制定的检测方法和方法确认程序(BJCDC/CX21: 2007)中的规定, 首次使用该方法之前对本实验室的检测能力进行了确认, 结果如下。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
色谱参数的测试及计算(色谱理论验证性实验)一、目的要求1. 通过本实验基本色谱参数的测试与计算,定量地了解溶质组分在色谱柱过程中热力学和动力学作用的量度。
2. 理解各色谱参数的意义及其相互关系。
3. 通过本实验进一步掌握柱效、柱选择性、分离能力、保留值等性质,使之能选择出最佳色谱操作条件,得到可靠的定性,定量结果。
二、测定意义通过试验,了解色谱中的各个基本参数, 从色谱图中学会参数的获得及各基本参数计算。
在规定的色谱条件下,测定惰性组分的死时间(t M )及被测组分的保留时间(t R )、半高峰宽(W 1/2)、及峰高(H )等参数,便可计算出基本色谱参数值。
1 调整保留时间:用公式计算出2 相对保留值:计算出(正庚烷, 正已烷);( 乙酸正丁酯, 正已烷);( 正辛烷, 正已烷)的相对保留值,以正已烷作标准。
3 容量因子:计算出正已烷;正庚烷;乙酸正丁酯;正辛烷的K ’,以其中K ’=2-5的组分进行计算。
4 理论塔板数:以其中K ’=2-5的组分进行计算。
MR R t t t -=,,,()()(),()()()R i g i N i is R S g s N s t V V t V V α===MRM M R t t t t t K ,,=-=222/1)(16)(54.5Wt W t n R R ==5 有效塔板数:以其中K ’=2-5的组分进行计算。
当K ’足够大时理论塔板数与有效塔板数是否近似相等。
6 分离度:计算出较难分离二组分的分离度。
7 分离数:计算出任意二相邻正构烷烃峰之间的TZ 值(即二峰间可容纳的峰数)。
8 保留指数:计算出任意二相邻正构烷烃峰之间的I 值三、方法原理 “塔板理论”:把色谱柱看作一个有若干层塔板的分馏塔,通过物质在每层塔板中进行平衡的物理模型过程,导引出一个描述色谱流出曲线的数学表达式:式中 c ——色谱流出曲线上任意一点样品的浓度;n ——理论塔板数;m ——溶质的质量;V R ——溶质的保留体积,即从进样到色谱峰极大点出现时通入色谱柱中载气的体积;Wt t W W t t R R R R R 122/12/112)(2-≈+-=2,22/1,)(16)(54.5Wt W t n R R eff==11k R k αα+⎫=⎪+⎝⎭]lg lg lg lg [100,)(,)(,)(,)(Z R n Z R z R X R t t t t Z --+=I +X 1)1(2/1)(2/1)()1(--=++Z Z Z Z R W W t t TZV——在色谱流出曲线上任意一点的保留体积。
四、仪器与试剂仪器气相色谱仪一套,邻苯二甲酸二壬酯与吐温混合固定液填充柱(DNP柱)1m×3mm;微量注射器(5—10μl)一支试剂甲烷,正己烷,正庚烷,正辛烷,乙酸正丁酯,混合样。
五、实验步骤1.联结好仪器系统,检查并排除故障至正常工作状态2 .色谱条件TD=120°C,TC=100°C,Ti =120°C;载气H2流速40 ml/min;进样量:空气50μl,乙酸正丁酯+n-C06+n-C07 +n-C08混合样1μl;纯样进0.4μl。
信号衰减视灵敏度而定。
3.色谱条件 Tj=120℃,Tc=100℃,Td=120℃;载气:N2流速30m1/min,H2流速40ml/min,空气流速350m1/min记录仪灵敏度10mV/25cm,纸速10mm/min;甲烷,乙酸正丁酯+n-C06n-C07+n-C08混合样4µ1,信号衰减视灵敏度状况而定。
4.测试待仪器开启运行至基线平稳后,取纯净CH4样品10µ1注入GC仪器系统(如信号过大则可以适当减少进样量),计时,准确记录保留时间(t M)。
重复进样5-10次,至t M值绝大多数重复为止。
取其平均值,为本实验的t M值[t M (甲烷)]。
再取四种混合组分的样品溶液4µl注入仪器系统,得到较理想谱图后,再重复进样3- 5次,取其平均保留时间为本实验各组分的保留时间[t R (乙酸正丁脂),t R (正已烷)、t R (正庚烷)、t R (正辛烷)]。
5.测试结果在仪器操作条件稳定无误的情况下,应得到分离状况良好的色谱图六、数据处理1、记录甲烷的t R值和四组分混合样的各保留值(平均值)。
令t n-1=t R(正己烷); t n=t R(正庚烷);t n+1=t R (正辛烷);t i=t R (乙酸正丁酯).2.测量并记录各组分的半高峰宽W h/23.各基本参数计算:2和峰宽W值(1)调整保留时间:以t 'R = t R-t M关系计算出t'n-1、 t'n、t'n+1及t'i;(2)相对保留值(r i,s):按r i,s=t 'R(i)/ t M的关系,计算出γ正庚垸,正已垸,γ乙酸正丁酯,正已烷,γ正辛烷,正已垸(以正已烷作标准物时)(3)容量因子:根据K=t 'R/t M的关系,计算出K' (正己烷)K' (正庚烷),K'(乙酸正丁脂),K'(正辛烷)值(4)理论塔板数:以其中K'=2—5的某组分为代表,根据n=5.54(t R/W h/2)2或n=16(t R/W)2的关系计算出柱效率(每米柱长所具有的理论塔板数) (5)有效塔板数:n eff=5.54(t'R/W h/2)2或n eff=16(t'R/W)2的关系计算出有效塔板数(仍可用K'=2—5的组分)。
当K'值足够大时,n≈n eff(6)分离度:可根据R=2(t R2-t R1)/(W1+W2)关系,计算出四种组分中较难分离的二组分间的分离度;(7)分离数:可根据TZ=(t R(Z+1)-t R(Z))/( W h/2(Z)+W h/2(Z+1))的关系,计算出任意二相邻正构烷烃峰之间的TZ值(即二峰间可容纳的峰数)(8)保留指数:是色谱定性的重要指标,准确测量十分重要。
只要严格保证色谱条件的一致性(同文献Sandtler保留指数的色潜条件比较),该指数可作为未知物可靠的定性指标。
保留指数计算可按I=100[(log t 'R(і)-log t 'R(z))/ (log t 'R(z+1)-log t 'R(Z))+z]的关系计算出任意二相邻正构烷烃伺某组分的I值。
如载气流速不非常稳定时,可用V'R(i), V'R(z), V'R(z+1),代替上述的t 'R(і)、 t 'R(z)) 和t 'R(z+1),这样可以使I值测量更准确些。
例在上述条件下测得以下实验数据:乙酸正丁酯 t 'R(乙酸正丁脂)= 3.10min log3.10=0.4914正庚烷 t 'R(正庚烷)=1.74min logl.74=0.2405正辛烷 t 'R (正辛烷)=3.73min log3.73=0.5722试计算乙酸正丁酯的保留指数。
解因z=7,所以I(乙酸正丁脂)=100[(0.0914-0.2405)/(0.5722-0.2405]=75.6+700.0=775.6七、问题讨论1.色谱定性尚有一些色谱参数可以用,如tR ,t 'R , V'R, r'i,s等,为什么说用I值最可靠?因为采用保留值定性要求两次进样条件完全一致,这是比较困难的,r'i,s 要求温度一定,且需要标准物质。
保留指数定性的重现性最佳,当固定液和柱温一定时,定性可不需要标准物质。
一般讲只要色谱柱(固定液)和柱温相同,就可以利用文献或手册发表的保留指数来定性。
2.关于t M值的测量:从t M定义看,t M值的测量规定为惰性组分从进样开始至柱后流出浓度极大点所对应的时间,即该惰性组分不能与固定相发生任何作用(溶解或吸附)便流出色谱柱。
实际上不存在这种州想的惰性组分,或多或少在柱中有保留作用,因此直接测量而得到的t M值,相对说不那么准确,特别是数值小的t M,会引入一定的误差(而数值大的误差往往可以略而不计)。
因t M射值是诸色谱参数的基淮数据,故有许多人研究它的准确计算方法。
如利用三个同系物的保留值来推算死时间,其三个同系物的碳数必须符合如下条件,C n-C(n-i)=C(n+i)-C n (5—1) 又根据同系物的碳原子.数与调整保留时间的对数呈线性关系而推导出来的方程式,即C n=mlog t'n +q= mlog (t n-t M )+q (5—2) 式中, C n——同系物中的碳原子数;t n——具有C n同系物的保留时间;t'n——C n同系物的调整保留时间;m、q——方程式中常数。
三个同系物(正己烷,正庚烷,正辛烷)的t 'R值可分别设定为[t(n-i)-t M]、[t n-t M]、[t(n+i)-t M],把它们代入(3—1—2)式;则得:C(n-i)= mlog (t(n-i)-t M )+q (5—3)C n=mlog(t n-t M )+q (5—4)C(n+i)= mlog (t(n+i)-t M )+q (5—5)将(3—1—4)式减去(3—1—3)式,(3—1—5)式减去(3—1—4)式得:C n-C(n-i)= mlog [(t n-t M )/(t(n-i)-t M )] (5—6)C(n+i)-C n = mlog [(t(n+i)-t M )/(t n-t M )] (5—7)又因为存在(3—1—1)式的关系,所以得:(t n-t M )/(t(n-i)-t M ) =(t(n+i)-t M )/(t n-t M) (5—8)整理(3—1—8)式,得到最终结果:t M=(t(n+i)+t(n-i)-2t n)/ (t(n+i)+t(n-i)-2t n) (5—9)式中i=1,2,3...;t n-i——第一个同系物的保留时间(正己烷),t n ——第二个同系物的保留时间(正庚烷),t n+i——第三个同系物的保留时间(正辛烷)。
X. Guardino等人的验证认为(5—9)式准确可靠,并提出i值愈大则计算出来的t M值愈准确。
请同学们根据本实验测得的t n-i、t n、t n+i值,试计算出t M与甲烷组分实测值的比较值,分析其误差。
八、注意事项1.色谱基本参数的测定,要严格控制操作条件的稳定性, 否则易产生误差。
2.为了保护色谱柱,要求载气首先打开,然后开机,结束时先关机,后关载气;严格按照要求的顺序开启和关闭色谱仪。
九、思考题1.色谱基本参数测量与计算的关键问题是什么?2.K'值及W h/2值的大小与色谱柱过程的哪些因素有关?其原因何在?控制哪些操作条件可以得到适宜K'值和W h/2值?。
