人工合成有机化合物汇总.
人工合成有机化合物
[已知]
催化剂(PdCl2、CuCl2)
2CH2=CH2+O2
2CH3CHO
CH =CH +O 催化剂(Pd-H3PO4-Cu/Al2O3 2 22
)
CH3COOH
乙烯 (C2H4)
催化剂 ① H2O
乙醇 (C2H6O)
② O2 催化剂
③O2 催化剂
O2 催化剂
乙醛 (C2H4O)
O2 催化剂
催化剂
7、
C12H22O11
(麦芽糖)
+
H2O
稀硫酸 水浴加热
2C6H12O6
(葡萄糖)
酒化酶
C6H12O6
(葡萄糖)
2C2H5OH+2CO2↑ (酒精)
第三单元
人工合成有机化合物
——简单有机物的合成
我们世界上每年合成的近百万个新化 合物中约70%以上是有机化合物。
①近几百年来,有机化学家已 经设计和合成了数百万种有机 化合物,极大地丰富了物质世界
③ CH≡CH
H2 催化剂
CH2=CH2
HCl 催化剂
CH3-CH2Cl
或 CH≡CH
HCl 催化剂
CH2=CHCl
H2 催化剂
CH3-CH2Cl
习题讲解
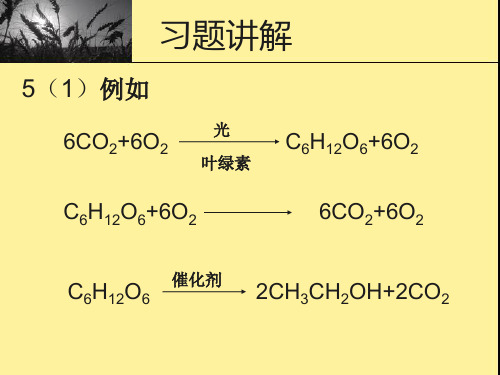
5(1)例如Байду номын сангаас
6CO2+6O2
光 叶绿素
C6H12O6+6O2
C6H12O6+6O2
6CO2+6O2
C6H12O6 催化剂 2CH3CH2OH+2CO2
5.(2)植物吸收太阳光,经过光合作用,把光 能(太阳能)转化成化学能储存起来。这是燃 烧的相反过程,生成的葡萄糖一部分储存起来 ,一部分转化为淀粉或纤维素,成为生物质能
人工合成尿素的化学方程式

人工合成尿素的化学方程式尿素是一种常见的有机化合物,化学式为(NH₂)₂CO。
它是由氨气和二氧化碳在催化剂存在下进行反应合成的。
尿素的合成方法有几种不同的途径,下面我将详细介绍两种常见的方法。
1.湿法尿素合成法湿法尿素合成法是将氨气和二氧化碳在高温高压条件下进行反应合成尿素。
首先,将氨气和二氧化碳通过压缩机分别加压,然后将氨气和二氧化碳分别输送到反应釜中。
在反应釜中,应加入催化剂,一般是金属铁、钴、锌等催化剂。
金属铁是常用的催化剂之一。
反应开始时,由于在高温高压条件下,氨气和二氧化碳发生反应生成碳酸铵。
该反应为一个可逆反应,其反应方程式为:2NH₃ + CO₂ → (NH₄)₂CO₃此时,产物是碳酸铵,不断向前方向进行反应。
随着反应的进行,反应达到一定程度时,生成的碳酸铵继续与氨气反应生成尿素,并释放出水分。
该反应方程式为:(NH₄)₂CO₃ → 2NH₂CONH₂ + H₂O反应釜中不断破碎生成的尿素和碳酸铵颗粒,以保持反应进行。
当反应达到平衡时,产物中的尿素被蒸馏出来,纯度可以达到99%以上。
剩余的废液经过处理,可以回收和再利用。
2.氨法尿素合成法氨法尿素合成法是将氨气和二氧化碳在催化剂存在下进行氨法反应,然后将生成的尿素经过蒸馏和结晶处理,得到纯度较高的尿素产品。
首先,在反应器中加入催化剂,催化剂可以是铷溴化物、钾溴酸盐等,以促使反应的进行。
然后,将氨气和二氧化碳通过压缩机分别加压,并加热至适当的温度。
然后,将氨气和二氧化碳通过管道输送到反应器中。
在反应器中,氨气和二氧化碳发生氨法反应生成尿素。
该反应是一个多步反应过程,具体的反应机理还不太清楚。
反应过程中,氨气和二氧化碳生成碳酸铵,然后经过一系列反应逐步转化为尿素。
氨法尿素合成法相对于湿法尿素合成法来说,反应条件较为温和,且催化剂的种类较多,因此具有更广泛的应用范围。
总结起来,人工合成尿素的化学方程式可以归纳为以下两个步骤:1.湿法尿素合成法:2NH₃ + CO₂ → (NH₄)₂CO₃(NH₄)₂CO₃ → 2NH₂CONH₂ + H₂O2.氨法尿素合成法:NH₃ + CO₂ → NH₂CONH₂尿素是一种非常重要的有机化合物,在农业、医药、化工等领域均有广泛的应用。
人工合成有机化合物_1-课件

;C能与
答案 CH3CH2COOH HOCH2CH2CHO或
CH3OOCCH3
CH3CH2OOCH
•
9、有时候读书是一种巧妙地避开思考 的方法 。2021/2/272021/2/27Saturday, February 27, 2021
•
10、阅读一切好书如同和过去最杰出 的人谈 话。2021/2/272021/2/272021/2/272/27/2021 4:15:52 PM
-CH2-CH2-,而不是-CH2-。
有机物的合成
1. 有机合成的概念:利用简单、易得的原料,通 过有机反应,生成具有特定结构和功能的有机 化合物的过程。
2.有机合成的关键:合成有机物要依据被合成 物质的组成和结构特点,精心设计并选择合理 的合成方法和合成路线。
3.有机合成的一般思路:可由原料出发,正向 思维;也可由目标产物出发,逆向思维;也可 由原料和目标产物同时出发,双向思维。
4.有机合成遵循的原则
(1)合成路线的简约性。
(2)实际生产的可操作性。
(3)还要综合考虑原料来源、反应物利用率、 反应速率、设备和技术条件、是否有污染物排 放、生产成本等问题来选择最佳的合成路线。
【例1】已知,有机化合物A只由C、H两种元素 组成且能使溴水褪色,其产量可以用来衡量 一个国家石油化工发展水平。A、B、C、D、 E有如下关系:
2.要利求用:率 在实际生速产率中,还要综合考虑原料
的污染物
、反生应产成物本
设备和技术条件、是否有
能量 、反应排原放子、、
降低
消耗,提高 利用率等问题来选
择最佳合成路线。
笃学二 有机高分子的合成
1.有机高分子化合物
(1) 概 念 : 相 对几万分乃至子几百万质 量 高 达 的有机化合物。简称高聚物或高分子。
有机化合物的制备方法

有机化合物的制备方法有机化合物是由碳元素以及其他元素(如氢、氧、氮等)组成的化合物。
它们在许多领域中起着重要的作用,包括药物、合成材料、染料等。
为了满足不同需求,研究人员开发了各种方法来制备有机化合物。
下面将介绍一些常见的有机化合物制备方法。
1.烷烃制备烷烃是最简单的有机化合物,由碳和氢原子组成。
常用的方法是碳氢化合物的脱氢反应,如烃类的裂解反应。
在高温和适当的条件下,如催化剂的作用下,长链碳氢化合物可以裂解为较短的链烷烃。
此外,烷烃还可以通过碳氢化合物的加氢反应得到,将氢气加入到烃类化合物中,通过催化剂的作用,将氢原子与碳原子相结合,生成烷烃。
2.醇的合成醇是由羟基和碳链组成的有机化合物。
醇可以通过多种方法合成,如水合反应、酸催化反应和还原反应。
在水合反应中,烯烃经过水加成反应生成醇。
在酸催化反应中,烃类化合物在酸催化剂的存在下与水反应生成醇。
还原反应是将醛或酮还原为相应的醇,常使用还原剂如氢气或金属氨基醇。
3.酯的制备酯是由羧酸和醇反应生成的有机化合物。
酯的制备方法主要有酸酯化反应和酯交换反应。
在酸酯化反应中,羧酸和醇在酸催化剂的存在下反应生成酯。
酯交换反应是指将已有的酯与醇反应生成新的酯,此反应通常在酯交换剂的存在下进行。
4.醚的合成醚是由两个有机基团通过氧原子连接而成的有机化合物。
醚的制备方法主要有醇缩合反应和醚交换反应。
醇缩合反应是指醇分子中的羟基与另一个醇分子中的氢原子发生反应,生成醚。
醚交换反应是指将已有的醚与醇反应生成新的醚,此反应通常在醇或醚的存在下进行。
5.脂肪酸的制备脂肪酸是由碳链和羧基组成的有机化合物。
脂肪酸的制备方法主要有化学氧化法和酶法。
化学氧化法是指使用化学氧化剂,如酸性高锰酸钾或过氧化氢将烃类氧化为脂肪酸。
酶法是指使用酶催化酯水解反应,将酯类水解为脂肪酸。
虽然以上只是介绍了几种常见的有机化合物制备方法,但实际上,制备有机化合物的方法是非常多样的。
根据具体的化学反应和要求,化学家可以选择不同的方法来合成所需的有机化合物。
人工有机合成化合物

实际生产过程中应遵循的原则
1.原料来源 2.反应物利用率
3.反应速率
4.设备和技术条件
5.是否有污染物排放
6.生产成本
有机合成的思维结构
合成目标
审题
新旧知识
设计合成路线
分析
突破
思维求异 解法求优
确定方法
推断过程和方向
结构简式
准确表达 反应类型 化学方程式
思考题
若有甲酸(HCOOH)、乙酸(CH3COOH)、甲醇 (CH3OH)和乙醇(CH3CH2OH)在一定条件下于同
一反应体系中发生酯化反应,则理论上能生成几种酯?
有机高分子的合成
天然高分子:淀粉、纤维素和蛋白质等 有机高分子
合成高分子:合成纤维、塑料、合成橡胶
聚合反应
1、加聚反应:相对分子质量小的化合物分子互 相结合成相对分子质量大的高分 子的反应叫加成聚合反应.简称加 聚反应有机高分子的形成:
催化剂
nCH2=CH2 △, P
◆聚四氟乙烯 单体:
CF2=CF2
◆聚苯乙烯
单体:
CH2=CH C6H5
聚甲基丙烯酸甲酯 (有机玻璃)
单体:
CH2=C COOCH3 CH3
[CH2 CH2]n(聚乙烯)
单体
链节
聚合度
◆ 聚乙烯(PE)产品
单体: CH2=CH2
无毒,化学稳定性好,适合做食品和药物的 包装材料
吹塑成型的聚乙烯薄膜
保鲜膜
◆聚氯乙烯(PVC) 单体: CH2=CHCl
化学稳定性好,耐酸碱腐蚀,使用温度不宜 超过60℃,在低温下会变硬 分为:软质塑料和硬质塑料
乙酸乙酯 (CH3COOC2H5)
合成路线2:
人工合成尿素的化学方程式

人工合成尿素的化学方程式人工合成尿素的化学方程式1. 引言人工合成尿素作为有机化学中的重要合成反应之一,具有重要的工业应用和科学意义。
本文将以人工合成尿素为主题,从其化学方程式、生产工艺以及应用领域等方面进行探讨,旨在深入理解尿素合成的原理和应用意义。
2. 尿素的化学方程式及反应原理在化学领域中,尿素具有化学式CO(NH₂)₂,它是一种有机化合物。
尿素的合成主要通过一系列的化学反应来实现,其中最重要的是氨和二氧化碳的反应。
具体的化学方程式如下:NH₃ + CO₂ → NH₂CONH₂尿素的合成反应主要以两个步骤进行。
氨气与二氧化碳反应生成胺基甲酸酯(NH₂COONH₄),然后胺基甲酸酯分解为尿素和水。
这个反应过程中需要催化剂和适当的温度和压力条件,以促进反应的进行。
3. 尿素的生产工艺人工合成尿素的生产工艺通常采用了德国化学家弗里德里希·维勒于1828年发现的维勒合成法。
这个工艺是通过氨与二氧化碳的反应制备尿素。
具体的生产步骤如下:步骤一:氨合成将天然气或石油发酵产生的甲醇与空气氧化,得到气态一氧化碳和氢气。
然后将气态一氧化碳与水蒸气反应生成氢气和一氧化碳水合物。
将一氧化碳水合物通过催化加热分解为气态氨。
步骤二:尿素合成将步骤一得到的氨与二氧化碳通过合成反应生成胺基甲酸酯。
胺基甲酸酯通过热裂解和结晶处理生成尿素。
4. 尿素的应用领域尿素是一种重要的化工原料,在农业、医药和化妆品等领域具有广泛的应用。
以下是尿素在各个领域的应用:4.1 农业领域尿素是制造氮肥的主要原料之一,可以为作物提供必需的氮元素,促进植物的生长和发育。
尿素还可以用作农田土壤改良剂和作物叶面喷肥剂,提高农作物的产量和质量。
4.2 医药领域尿素具有良好的溶解性和保湿性,常被用于医药制剂和护肤品中。
在某些皮肤病的治疗中,尿素可以作为角质层软化剂,帮助治疗和预防皮肤病症。
4.3 化妆品领域尿素在化妆品中作为一种保湿剂和软化剂广泛应用。
有机化合物分类及常见合成方法详解

有机化合物分类及常见合成方法详解有机化合物是由碳和氢等元素组成的化合物。
基于不同的结构和化学性质,有机化合物可分为苯环化合物、脂肪族化合物、氨基酸、生物碱等多种类型。
本文将详细介绍不同类型有机化合物举例及其常见合成方法。
苯环化合物苯环化合物是指具有苯环基团的有机分子。
苯环基团包含6个碳原子构成的芳香环。
广泛存在于石油和天然气中,其中最常见的是苯、甲苯和萘。
常见苯环化合物如下:1.苯(Benzene):六个碳原子组成的芳香环,以烷基苯为主要衍生物。
2.甲苯(Toluene):一种具有苯环基团的有机化合物,其主要衍生物为二甲苯。
3.萘(Naphthalene):二个苯环相连的化合物,也称作“半苯”。
苯环化合物的合成方法包括单氯代、双氯代、硝基化等方法。
其中,单氯代是将苯环中的一个氢原子替换为氯原子,以亚硫酸钠和氯化铁为催化剂。
双氯代方法是在单氯化合物的基础上,进一步对其进行氯代,将其转化为二氯代化合物。
硝基化是利用硝化酸对化合物进行硝基化反应生成硝基化合物。
脂肪族化合物脂肪族化合物是指由烷基、烯基、炔基等功能基团构成的不含芳香环的有机化合物。
常见的脂肪族化合物包括乙烯(Vinyl)、丙烯(Propene)、丁烯(Butene)等。
脂肪族化合物的合成方法包括烷基化、烯基化、炔基化等方法。
其中,烷基化是将溶液中的烯烃或苯环化合物和烷基化剂在催化剂的作用下反应生成脂肪族化合物。
烯基化是利用乙烯等烯基化合物作为原料,在化学反应中发生合成反应,从而生成脂肪族化合物。
炔基化是将含有炔基的化合物在氢化镍等催化剂的作用下,吸收氢分子生成脂肪族化合物。
氨基酸氨基酸是重要的生物大分子,是蛋白质的构成单元。
氨基酸包括天然氨基酸和人工氨基酸。
其中,天然氨基酸分为20种,可分为两类: 极性和非极性。
常见的氨基酸包括丙氨酸(Alanine)、谷氨酸(Glutamate)、甘氨酸(Glycine)等。
氨基酸的合成方法主要有三种: 工业方法、化学方法、生化方法。
考点16人工合成有机化合物(核心考点归纳)

考点16 人工合成有机化合物【核心考点梳理】一、常见有机化合物的合成以乙烯为原料合成乙酸乙酯(1)常规合成路线根据所学知识,常用的合成路线为此过程中发生反应的化学方程式及反应类型: ①CH 2===CH 2+H 2O ――→催化剂CH 3CH 2OH ,加成反应。
②2CH 3CH 2OH +O 2――→催化剂△2CH 3CHO +2H 2O ,氧化反应。
③2CH 3CHO +O 2――→催化剂2CH 3COOH ,氧化反应。
④CH 3COOH +C 2H 5OHCH 3COOC 2H 5+H 2O ,酯化反应或取代反应。
【典型例题】 例1.(2022·浙江高一月考)以乙烯为有机原料制备乙酸乙酯的合成路线中,最后一步化学反应的反应类型是( )A .氧化反应B .取代反应C .加成反应D .水解反应【答案】B【详解】以乙烯为原料制备乙酸乙酯的反应中,最后一步是乙醇与乙酸的酯化反应,该反应也属于取代反应,B 项正确。
例2.(2023春·高一课时练习)某高聚物的结构式如图:,其单体的结构简式为 A . B . C .和CH 3CH=CH 2 D . 和CH 2=CH 2【答案】D 【解析】由高聚物的结构可知,主链可含有6个C 原子,没有其他杂原子,其中含有1个C=C双键,为二烯烃和烯烃的加聚反应产物,按如图所示断键,其中双键中1个C-C断裂,再恢复原来的双键,CH=CH,答案选D。
故单体为,22例3.(2023·全国·高一专题练习)下列各组原料适合合成聚氯乙烯单体的是A.乙烷、氯气B.乙烯、氯气C.乙烯、氯化氢D.乙炔、氯化氢【答案】D【分析】聚氯乙烯的单体是氯乙烯(CH2=CHCl) ,据此分析解答。
【解析】A.乙烷和氯气发生取代反应,得到多种氯代烷和氯化氢的混合物,得不到CH2=CHCl,故A不选;B.乙烯和氯气发生加成反应,得到1,2-二氯乙烷,得不到CH2=CHCl,故B不选;C.乙烯和氯化氢发生加成反应,得到一氯乙烷,得不到CH2=CHCl,故C不选;D.乙炔和氯化氢按照物质的量1:1发生加成反应,得到CH2=CHCl,故D选;故选D。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第16页
苏教版•高中化学•必修2
二、加聚反应 加聚反应的全称是加成聚合反应。从微观上来看,它是小分子化
合物断开不饱和键的一部分而转变为原子团 (又叫做结构单元 ),这种原
子团相互结合形成高分子化合物;从宏观上来看它就是小分子化合物相 互化合为高分子化合物 (注意:一般不叫做化合反应 )。因此,在加聚反
三大合成材料是指 ______ 、 ________ 和 ________ ,它们都是有机
高分子。有机高分子是由________________通过______反应制得的。 2.加聚反应 含有 ______________________ 的相对分子质量小的化合物分子在 一定条件下,互相结合成________________________的反应。如:
答案:方案Ⅱ CH3CH2Cl的产率高且不污染环境
第11页
苏教版•高中化学•必修2
第12页
苏教版•高中化学•必修2
第13页
苏教版•高中化学•必修2
核心解读——————————————————— 一、有机合成的基本方法
解答有机合成题的方法较多,基本方法有:
①顺合成法:采用正向思维从已知原料入手,找出合成所需直接 或间接中间产物,逐步推向待合成物,其思维程序是从原料到中间产物 再到产品。 ②逆合成法:采用逆向思维,从产品的组成、结构、性质入手, 找出中间产物,逐步推向已知原料,其思维程序从产品到中间产物再到 原料。
____________________________。 其单体为________,链节为________,聚合度为____。
第7页
苏教版•高中化学•必修2
4.缩聚反应 单体间相互反应形成 ________ 的同时还生成了 ________ 化合物的
反应。例如:
第8页
苏教版•高中化学•必修2
自我校对
以上三种合成路线,从理论上看都能在一定反应条件下实现。在 实际生产中,还要考虑原料______、反应物________、反应______、设 备和技术______、是否有____________、生产______等问题来选择最佳 的合成路线。
第5页
苏教版•高中化学•必修2
二、有机高分子的合成 1.三大合成材料
应的过程中,具有下列重要的、需要理清的关系。
1.小分子与结构单元之间的关系 小分子与由其转化成的结构单元之间,组成元素以及原子数目相 同、式量相同,结构不同。例如:
第17页
苏教版•高中化学化学•必修2
2.结构单元与高分子之间的关系 高分子与结构单元之间,组成元素相同,高分子的原子数目和式
第6页
苏教版•高中化学•必修2
日常生活中常见的腈纶、有机玻璃、合成橡胶、聚四氟乙烯都是 通过______反应得到的。
3.有机高分子的链节与单体
将形成高分子化合物的小分子物质称为 ______,将高分子化合物 中不断重复的基本结构单元称为______,链节的数目称为________。
乙烯发生加聚反应的化学方程式为
第9页
苏教版•高中化学•必修2
第10页
苏教版•高中化学•必修2
做一做 · 自我测评 ——————————————— 1.工业制备纯净的 CH3CH2Cl 有以下两种方案,请指出哪种方案 合理,为什么? 光 方案Ⅰ: CH3CH3+ Cl2――→CH3CH2Cl+ HCl 催化剂 方案Ⅱ: CH2===CH2+ HCl ――→ CH3CH2Cl 合理方案: ______________, 原因是 ______________________________ 。
第14页
苏教版•高中化学•必修2
③综合比较法:采用综合思维的方法,将正向或逆向推导出的多 种合成途径进行比较,从而得到最佳的合成路线。
如:由乙烯合成乙酸乙酯,①顺合成法:
第15页
苏教版•高中化学•必修2
O2 ③综合比较法: 由乙烯制备乙酸还有两种途径, CH2===CH2 ――→ 催化剂 O2 O2 CH3CHO ――→ CH3COOH 或 CH2===CH2 ――→ CH3COOH,把上述 催化剂 催化剂 各途径进行综合比较 (原料及利用率、反应速率、设备和技术条件、成 本、污染等问题 ),从而得出合适的合成途径。
第三单元
人工合成有机化合物
第1页
苏教版•高中化学•必修2
课标定位:①掌握高分子化合物的链节和单体,能根据高分子判 断单体,根据单体写出高分子化合物。②了解常见高分子材料的合成反
应。③知道有机物合成的路线和方法,高分子材料的独特功能及合成的
发展方向。
第2页
苏教版•高中化学•必修2
第3页
苏教版•高中化学•必修2
一 、 1. 有 机 化 学 反 应
起始原料
合成 方 法 和 路线
催化剂 2.CH2===CH2+ H2O ――→ CH3CH2OH Cu 2CH3CH2OH+ O2――→2CH3CHO+ 2H2O △ 催化剂 2CH3CHO+ O2 ――→ 2CH3COOH 浓 H2SO4 CH3CH2OH+ CH3COOH ――→ CH3COOCH2CH3+ H2O △ 利用率 速率 条件 污染物排放 成本 来源
填一填·知识清单——————————————— 一、简单有机物的合成
1.合成有机物化合物的思路
合成有机物要依据被合成物质的组成和结构特点,选择合适的 _______和______,精心设计并选择合理的_______________。 2.以乙烯为原料合成乙酸乙酯的三种合成路线
第4页
苏教版•高中化学•必修2
量都是结构单元的整倍数(n倍)。例如
第19页
苏教版•高中化学•必修2
3.单体的推断方法 凡链节主碳链全部为单键的高聚物,以主链上的两个 C 原子为基
本单元,将两半键闭合即得单体。如:
第20页
苏教版•高中化学•必修2
第21页
苏教版•高中化学•必修2
合成路线(1)转化的反应方程式为 ________________________________; ________________________________; ________________________________;
________________________________。
