环境化学及实验
环境化学实验1

活性炭吸附实验1.实验目的①了解活性炭的吸附工艺及性能②掌握用实验方法(含间歇法、连续流法)确定活性炭吸附处理污水的设计参数的方法。
2.实验装置及材料(1)间歇式活性炭吸附装置间歇式吸附用用三角烧杯,在烧杯内放入活性炭和水样进行振荡。
(2)连续式活性炭吸附装置连续式吸附采用有机玻璃柱D25mm×1000mm,柱内500~750mm高烘干的活性炭,上、下两端均用单孔橡皮塞封牢。
各柱下端设取样口。
装置具体结构如图4—10所示。
(3)间歇与连续流实验所需的实验器材①振荡器(1台)。
②有机玻璃柱(3根D25mm×1000mm)③活性炭。
④三角烧瓶(2个,500mL)⑤COD测定装置。
⑥配水及投配系统。
⑦酸度计(1台)。
⑧温度计(1只)。
⑨漏斗(6个)。
⑩定量滤纸。
3.实验步骤(1)间歇式吸附实验①将活性炭放在蒸馏水中浸泡24h,然后在10 5℃烘箱内烘24h,再将烘干的活性炭研碎成能通过270目的筛子(0.053mm孔眼)的粉状活性炭。
②测定预先配制的废水水温、pH值和COD。
③在5个三角烧瓶中分别加入100mg、200mg、300mg、400mg、500mg粉状活性炭。
④在每个烧瓶中分别加入同体积的废水进行搅拌。
一般规定,烧瓶中废水COD(mg/L)与活性炭浓度(mg/L)比值为0.5—5.0。
⑤将上述5个三角烧瓶放在振荡器上振荡,当达到吸附平衡时即可停止。
(振荡时间一般为30min以上)。
⑥过滤各三角烧瓶中废水,并测定COD值,上述原始资料和测定结果记入表4—11。
(2)连续流吸附实验①配制水样或取自实际废水,使原水样中含COD约l00mg/L,测出具体的COD,pH 值、水温等数值。
②打开进水阀门,使原水进入活性炭柱,并控制为3个不同的流量(建议滤速分别为5 m/h,l 0 m/h,15 m/h)③运行稳定5min后测定各活性炭出水COD值。
④连续运行2—3h,每隔30min取样测定各活性炭柱出水COD值一次。
环境化学-环境化学实验
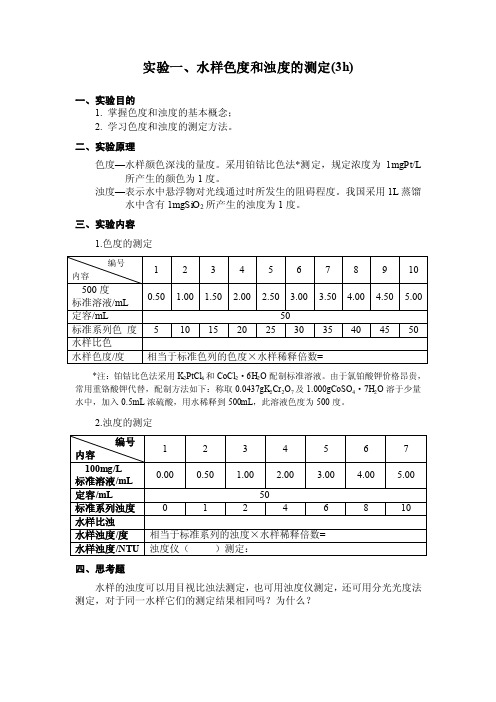
实验一、水样色度和浊度的测定(3h)一、实验目的1. 掌握色度和浊度的基本概念;2. 学习色度和浊度的测定方法。
二、实验原理色度—水样颜色深浅的量度。
采用铂钴比色法*测定,规定浓度为1mgPt/L 所产生的颜色为1度。
浊度—表示水中悬浮物对光线通过时所发生的阻碍程度。
我国采用1L蒸馏水中含有1mgSiO2所产生的浊度为1度。
三、实验内容1.色度的测定编号1 2 3 4 5 6 7 8 9 10 内容500度0.50 1.00 1.50 2.00 2.50 3.00 3.50 4.00 4.50 5.00 标准溶液/mL定容/mL 50标准系列色度 5 10 15 20 25 30 35 40 45 50 水样比色水样色度/度相当于标准色列的色度×水样稀释倍数=*注:铂钴比色法采用K2PtCl6和CoCl2·6H2O配制标准溶液。
由于氯铂酸钾价格昂贵,常用重铬酸钾代替,配制方法如下:称取0.0437gK2Cr2O7及1.000gCoSO4·7H2O溶于少量水中,加入0.5mL浓硫酸,用水稀释到500mL,此溶液色度为500度。
2.浊度的测定编号1 2 3 4 5 6 7内容100mg/L0.00 0.50 1.00 2.00 3.00 4.00 5.00 标准溶液/mL定容/mL 50标准系列浊度0 1 2 4 6 8 10水样比浊水样浊度/度相当于标准系列的浊度×水样稀释倍数=水样浊度/NTU 浊度仪()测定:四、思考题水样的浊度可以用目视比浊法测定,也可用浊度仪测定,还可用分光光度法测定,对于同一水样它们的测定结果相同吗?为什么?实验二、水样酸度和碱度的测定(3h)一、目的和要求1. 掌握酸度和碱度的基本概念;2. 学习酸度和碱度的测定方法。
二、实验原理酸度—指水中含有能与强碱发生中和作用的物质的总和。
①OH- + H+ = H2O (pHeq=7.0)②OH- + H2CO3 = HCO3- + H2O(pHeq=8.3)③OH-+ HCO3- = CO32- + H2O(pHeq=10.8)(甲基橙为指示剂—无机酸度①;酚酞为指示剂—CO2酸度①②)碱度—指水中含有能与强酸发生中和作用的物质的总和。
环境化学及实验

《环境化学》教学大纲课程编号:097007课程名称:环境化学(Environment Chemistry)课程类型:专业课学时/学分:32/2先修课程:无机化学、分析化学、有机化学和物理化学适用专业:化学开课系或教研室:化学与化工系一、课程的性质和任务1.课程性质:本课程为化学专业本科生开设的一门专业课程,为学生提供必要的环境化学的知识。
本课程的先修课程是无机化学、分析化学和有机化学。
2. 课程任务:本课程使学生重点掌握大气环境化学、水环境化学、土壤环境化学、生物体内污染物质的运动过程及毒性、典型污染在环境各圈层中的转归与效应等基本原理、基本知识和环境化学相关交叉学科的知识,掌握受污染环境的修复的基本知识和基本技能,了解绿色化学的基本原理和在现实中的典型应用。
二、课程教学的基本要求本课的教学环节包括:课堂讲授、学生自学、习题、答疑、期末考试。
通过上述环节,要求学生了解和掌握各类污染物质在大气、水、土壤以及生物机体内的迁移转化过程,产生效应的基本原理和防治的基本方法。
本课程课堂讲授32学时(具体按当年教学计划而定),考核方式为可采取闭卷考试、开卷考试、撰写课程论文的形式进行。
总评成绩:考试占90%、平时作业占10%三、课程教学内容(一)结论环境问题,环境化学;环境污染物的类别,环境效应及其影响因素,环境污染物在环境各圈的迁移转化过程简介。
(二)大气环境化学※1.大气温度层结,辐射逆温层,气绝热过程和干绝热递减率,大气稳定度,影响大气污染物迁移的因素;※2.光化学反应基础,大气中重要自由基的来源,氮氧化物的转化,碳氢化合物的转化※3.光化学烟雾型污染,酸性降水,大气颗粒物,温室气体和温室效应,臭氧层的形成与耗损。
(三)水环境化学1.天然水的基本特征2.水中污染物的分布与存在形态,水中无机污染物的迁移转化※3.颗粒物与水之间的迁移,水中颗粒物的聚集,溶解和沉淀,氧化-还原,配合作用※4.水中有机污染物的迁移的分配作用,挥发作用,水解作用,光解作用,生物降解作用。
环境化学实验指导书环科环工学时

实验一不同水域水碱度的分析实验项目性质:设计性实验所属课程名称:环境化学及实验实验计划学时: 4学时水的碱度是指水中所含能与强酸定量作用的物质总量。
水中碱度的来源是多种多样的。
地表水的碱度,基本上是碳酸盐、重碳酸盐及氢氧化物含量的函数,所以总碱度被当作这些成分浓度的总和。
当水中具有硼酸盐、磷酸盐或硅酸盐等时,则总碱度的测定值也包含它们所起的作用。
废水及其他复杂体系的水体中,还具有有机碱类、金属水解性盐类等,均为碱度组成成分。
在这些情况下,碱度就成为一种水的综合性特性指标,代表能被强酸滴定的物质的总和。
碱度的测定值因使用的终点pH值不同而有很大的差异,只有当试样中的化学成分已知时,才干解释为具体的物质。
对于天然水和未污染的地表水,可直接用酸滴定至pH为8.3时消耗的量,为酚酞碱度。
以酸滴定至pH为4.4-4.5时消耗的量,为甲基橙碱度。
通过计算,可以求出相应的碳酸盐、重碳酸盐和氢氧根离子的含量;对于废水、污水,则由于组分复杂,这种计算无实际意义,往往需要根据水中物质的组分拟定其与酸作用达成终点时的pH值。
然后,用酸滴定以便获得分析者感爱好的参数,并做出解释。
1.方法的选择用标准酸滴定水中碱度是各种方法的基础。
有两种常用的方法,即酸碱指示剂滴定法和电位滴定法。
电位滴定法根据电位滴定曲线在终点时的突跃,拟定特定pH值下的碱度,他不受水样浊度、色度的影响,合用范围较广。
用指示剂判断滴定终点的方法简便快速、合用于控制性实验及例行分析。
二法均可根据需要和条件选用。
2.样品保存样品采集后应在4℃保存,分析前不应打开瓶塞,不能过滤、稀释或浓缩。
样品应用于采集后的当天进行分析,特别是当样品中具有可水解盐类或具有可氧化态阳离子时,应及时分析。
实验目的:1.了解不同水域水碱度的意义2. 熟悉设计实验的过程3. 掌握滴定法测定水碱度的方法实验环节:1.实验用水分别为:湖泊水、景观用水、绿化灌溉用水、浑河水、锅炉水、雨水、自来水等,根据季节特点和实际情况,选取2-3种。
环境化学实验

环境化学实验环境安全与工程系2009.3实验一空气中挥发性有机物的污染前言挥发性有机化合物(Volatile Organic Compounds)是指沸点在50~260℃之间、室温下饱和蒸气压超过1 mmHg的易挥发性化合物,是室内外空气中普遍存在且组成复杂的一类有机污染物。
它主要来自有机化工原料的加工和使用过程,木材、烟草等有机物的不完全燃烧过程,汽车尾气的排放。
此外,植物的自然排放物也会产生VOCs。
随着工业迅速发展,建筑物结构发生了较大变化,使得新型建材、保温材料及室内装璜材料被广泛使用;同时各种化妆品、除臭剂、杀虫剂和品种繁多的洗涤剂也大量应用于家庭。
其中有机化合物有的可直接挥发,有的可在长期降解过程中释放出低分子有机化合物,由此造成环境空气有机物的污染。
由于VOCs的成分复杂,其毒性、刺激性、致癌作用等对人体健康造成较大的影响。
因此,研究环境中VOCs的存在、来源、分布规律、迁移转化及其对人体健康的影响一直受到人们的重视,并成为国内外研究的热点。
一、实验目的1.了解VOCs的成分、特点。
2.了解气相色谱法测定环境中VOCs的原理,掌握其基本操作。
二、实验原理将空气中苯、甲苯、乙苯、二甲苯等挥发性有机化合物吸附在活性炭采样管上,用二硫化碳洗脱后,经色谱柱分离,火焰离子化检测器测定,以保留时间定性,峰高(或峰面积)外标法定量。
本法检出限:苯1.25ng;甲苯1.00ng;二甲苯(包括邻、间、对)及乙苯均为2.50ng。
当采样体积为100L时,最低检出浓度苯为0.005mg/m3;甲苯为0.004 mg/m3;二甲苯(包括邻、间、对)及乙苯均为0.010 mg/m3。
三、仪器与试剂1. 仪器(1) 容量瓶:5 mL、100 mL。
(2) 移液管:1 mL、5 mL、10 mL、15 mL及20 ml。
(3) 微量注射器:10 μL。
(4) 带火焰离子化检测器(FID)气相色谱仪。
(5) 空气采样器:流量范围0.0~1.0 L/min。
环境化学实验报告空气中氮氧化物日变化曲线doc精选全文完整版

可编辑修改精选全文完整版实验一空气中氮氧化物的日变化曲线大气中氮氧化物(NO x)主要包括一氧化氮和二氧化氮,主要来自天然过程,如生物源、闪电均可产生NO x。
NO x的人为源绝大部分来自化石燃料的燃烧过程,包括汽车及一切内燃机所排放的尾气,也有一部分来自生产和使用硝酸的化工厂、钢铁厂、金属冶炼厂等排放的废气,其中以工业窑炉、氮肥生产和汽车排放的NO x量最多。
城市大气中2/3的NO x来自汽车尾气等的排放,交通干线空气中NO x的浓度与汽车流量密切相关,而汽车流量往往随时间而变化,因此,交通干线空气中NO x的浓度也随时间而变化。
NO x对呼吸道和呼吸器官有刺激作用,是导致支气管哮喘等呼吸道疾病不断增加的原因之一。
二氧化氮、二氧化硫、悬浮颗粒物共存时,对人体健康的危害不仅比单独NO x严重得多,而且大于各污染物的影响之和,即产生协同作用。
大气中的NO x能与有机物发生光化学反应,产生光化学烟雾。
NO x能转化成硝酸和硝酸盐,通过降水对水和土壤环境等造成危害。
一、实验目的1.掌握氮氧化物测定的基本原理和方法;2.绘制城市交通干线空气中氮氧化物的日变化曲线。
二、实验原理在测定NO x时。
先用三氧化铬将一氧化氮等低价氮氧化物氧化成二氧化氮;二氧化氮被吸收在溶液中形成亚硝酸,与对氨基苯磺酸发生重氮化反应,再与盐酸萘乙二胺偶合,生成玫瑰红色偶氮染料,用比色法测定。
方法的检出限为0.01 /ml(按与吸光度0.01相应得亚硝酸盐含量计)。
线性范围为0.03~1.6/ml。
当采样体积6L时,NO x (以二氧化氮计)的最低检出浓度为0.01mg/m3。
盐酸萘乙二胺盐比色法的有关反应式如下:主要反应方程式为:采集并测定1天内不同时间短交通干线空气中氮氧化物的浓度,可绘制空气中氮氧化物浓度随时间的变化曲线。
三、仪器与试剂1.仪器(1) 大气采样器:流量范围0. 0--1. 0 L/min。
(2) 分光光度计。
(3) 棕色多孔玻板吸收管。
环境化学实验报告简版

环境化学实验报告简版第一篇:环境化学实验报告简版环境化学实验实验1水溶液中染料浓度的测定一实验目的:熟悉染料浓度的测定原理、方法和分光光度计的使用。
二实验原理:各种染料均有一定的吸光波长,而且在一定浓度范围内吸光值与浓度之间成线性关系,根据这一原理作出标准曲线,测定未知溶液的染料浓度。
三实验仪器与试剂仪器722S分光光度计、恒温振荡器、离心机试剂刚果红,亚甲基蓝,C.P.级。
四实验步骤标准曲线的绘制分别称取2.500g上述染料于1000ml容量瓶中,用水稀释至刻度,配成2500 g/ml的上述染料标准溶液。
准确吸取该溶液0.2、0.4、0.6、0.8、1.0ml分别于50ml比色管中,用水稀释至刻度,在494nm(刚果红)、572nm(亚甲基蓝)处测定吸光度。
未知溶液的浓度测定吸取一定量的未知溶液或其稀释液,在相应的波长下测定其吸光度。
五实验计算标准曲线中的吸光度对浓度作图并回归成线性方程,计算方差。
2对照标准曲线或线性方程确定未知样浓度。
六实验结果与讨论讨论浓度测定的过程及其注意事项;注意标准曲线回归方程的方差。
实验2活性炭吸附法处理色度废水一实验目的测定活性炭的吸附等温线二实验原理吸附法是处理废水常用的方法,吸附剂的吸附能力常用吸附量G 表示,在一定温度下它与溶液中吸附溶质的平衡浓度有关。
G(mg/g)= x/m,x为吸附溶质的质量(g),m为吸附剂的质量(g)。
关于吸附等温线有H、Freundlich、Langmiur等类型:H型: G = kcFreundlich型:G = kc1/n,lgG = lgk + 1/n lgc,k、n为常数。
Langmiur型:G = G0c/(A+c),1/G = 1/ G0 +(A/ G0)(1/c),A 为常数,G0 为表面上吸附饱和时的最大吸附量。
三实验仪器与试剂仪器722S分光光度计、恒温振荡器、离心机试剂活性炭:粉末状活性炭0.076mm(200目),将活性炭过筛,取小于0.076mm筛孔以下的样品,水洗后105-110︒C烘干3h。
环境化学环境化学实验方案

实验一水体富营养化程度的评价富营养化(eutrophication)是指在人类活动的影响下,生物所需的氮、磷等营养物质大量进入湖泊、河口、海湾等缓流水体,引起藻类及其他浮游生物迅速繁殖,水体溶解氧量下降,水质恶化,鱼类及其他生物大量死亡的现象。
在自然条件下,湖泊也会从贫营养状态过渡到富营养状态,沉积物不断增多,先变为沼泽,后变为陆地。
这种自然过程非常缓慢,常需几千年甚至上万年。
而人为排放含营养物质的工业废水和生活污水所引起的水体富营养化现象,可以在短期内出现。
水体富营养化后,即使切断外界营养物质的来源,也很难自净和恢复到正常水平。
水体富养化严重时,湖泊可被某些繁生植物及其残骸淤塞,成为沼泽甚至干地。
局部海区可变成“死海”,或出现“赤潮”现象。
植物营养物质的来源广、数量大,有生活污水、农业面源、工业废水、垃圾等。
每人每天带进污水中的氮约50 g。
生活污水中的磷主要来源于洗涤废水,而施入农田的化肥有50%~80%流入江河、湖海和地下水体中。
一、实验目的1. 掌握总磷、叶绿素-a及初级生产率的测定原理及方法。
2. 评价水体的富营养化状况。
二、仪器设备及试剂1. 仪器(1) 可见分光光度计。
(2) 移液管:1mL、2mL、10mL。
(3) 容量瓶:100mL、250mL。
(4) 锥型瓶:250mL。
(5) 比色管:25mL。
(6) BOD瓶:250mL。
(7) 具塞小试管:10mL。
(8) 玻璃纤维滤膜、剪刀、玻棒、夹子(9) 多功能水质检测仪2. 试剂(1) 过硫酸铵(固体)。
(2) 浓硫酸。
(3) 1 mol/L硫酸溶液。
(4) 2 mol/L盐酸溶液。
(5) 6 mol/L氢氧化钠溶液。
(6) 1%酚酞:1g酚酞溶于90mL乙醇中,加水至100mL。
(7) 丙酮:水(9:1)溶液。
(8) 酒石酸锑钾溶液:将4.4g K(SbO)C4H4O6 ·1/2H2O溶于200mL蒸馏水中,用棕色瓶在4℃时保存。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
《环境化学》教学大纲
课程编号:097104
课程名称:环境化学(Environment Chemistry)
课程类型:专业课
学时/学分:32/2
先修课程:无机化学、分析化学和有机化学、物理化学
适用专业:化学工程与工艺
开课系或教研室:应用化学教研室
一、课程的性质和任务
1.课程性质:本课程为化学工程与工艺专业本科生开设的一门专业课程,为学生提供必要的环境化学的知识。
本课程的先修课程是无机化学、分析化学和有机化学。
2. 课程任务:本课程使学生重点掌握大气环境化学、水环境化学、土壤环境化学、生物体内污染物质的运动过程及毒性、典型污染在环境各圈层中的转归与效应等基本原理、基本知识和环境化学相关交叉学科的知识,掌握受污染环境的修复的基本知识和基本技能,了解绿色化学的基本原理和在现实中的典型应用。
二、课程教学的基本要求
本课的教学环节包括:课堂讲授、学生自学、习题、答疑、期末考试。
通过上述环节,要求学生了解和掌握各类污染物质在大气、水、土壤以及生物机体内的迁移转化过程,产生效应的基本原理和防治的基本方法。
本课程课堂讲授32学时(具体按当年教学计划而定),考核方式为可采取闭卷考试、开卷考试、撰写课程论文的形式进行。
总评成绩:考试占90%、平时作业占10%
三、课程教学内容
(一)结论(2学时)
环境问题,环境化学;环境污染物的类别,环境效应及其影响因素,环境污染物在环境各圈的迁移转化过程简介。
(二)大气环境化学(6学时)
※1.大气温度层结,辐射逆温层,气绝热过程和干绝热递减率,大气稳定度,影响大气污染物迁移的因素;
※2.光化学反应基础,大气中重要自由基的来源,氮氧化物的转化,碳氢化合物的转化
※3.光化学烟雾型污染,酸性降水,大气颗粒物,温室气体和温室效应,臭氧层的形成与耗损。
(三)水环境化学(8学时)
1.天然水的基本特征
2.水中污染物的分布与存在形态,水中无机污染物的迁移转化
※3.颗粒物与水之间的迁移,水中颗粒物的聚集,溶解和沉淀,氧化-还原,配合作用
※4.水中有机污染物的迁移的分配作用,挥发作用,水解作用,光解作用,生物降解作用
(四)土壤环境化学(6学时)
1.土壤组成,土壤的粒级分组与质地分组
※2.土壤吸附性,土壤酸碱性,土壤的氧化还原性
※3.污染物在土壤-植物体系中的迁移,植物对重金属污染产生耐性的几种机制;土壤中农药的迁移,典型农药在土壤中的迁移转化
(五)生物体内污染物质的运动过程及毒性(4学时)
1.生物膜的结构,物质通过生物的方式
※2.污染物质在机体内的吸收、分布、排泄、蓄积;污染物质的生物富集,生物放大,生物积累
4.污染物质生物转化中的酶,若干重要辅酶的功能,生物氧化中的氢传递过程
※5.耗氧有机污染物质的微生物降解,有毒有机污染物质生物转化类型,有毒有机污染物质的微生物降解,氮及硫的微生物转化,重金属元素的微生物转化,污染物质的生物转化速率
※6.毒物,毒物的毒性,毒物的联合作用,毒作用的过程,毒作用的生物化学机制。
(六)典型污染物在环境各圈层中的转归与效应(2学时)
※1.汞,砷
※2.有机卤代物,多环芳烃,表面活性剂
(七)受污染环境的修复(3学时)
植物修复技术;化学氧化技术;电动力学修复;地下水修复的可渗透格栅技术;表面活性剂及共溶淋洗技术。
(八)绿色化学的基本原理与应用(1学时)
绿色化学的基本原理;绿色化学的应用
五、教材及教学参考书
教材:《环境化学》第二版主编:戴树桂
出版社:高等教育出版社,2008;
参考书:《环境化学》主编:王晓蓉
出版社:高等教育出版社,1993;
《环境化学》主编:陶秀成
出版社:高等教育出版社,2002
《环境化学》主编:Manahan S E. 陈甫华等译,戴树桂校
出版社:南开大学出版社,1993;
执笔:唐复明
审定:薛兆民
日期:2011年04月
《环境科学与工程基础实验》实验大纲
课程编号:096112
课程名称:环境科学与工程基础实验(Experiment of Environment science and Engineering)
课程类型:专业课
学时/学分48/3
适用专业:化学工程与工艺
开课系或教研室:应用化学教研室
一、实验教学的目的和要求
环境科学与工程基础实验是一门综合性非常强的实验学科,它所涉及的理论知识和实验技能的范围非常广泛。
本门实验课的目的是:使学生掌握必要的环境科学与工程实验的基本实验技能,并加深对环境化学有关理论的理解和认识,同时了解环境科学与工程领域当前新的研究动态和研究方法。
本门实验课程要求是:在掌握基本化学实验技能的基础上,通过系统学习环境化学的理论知识和实验方法,培养和锻炼学生在环境化学领域基本实验技能。
三、单项实验的内容和要求
实验一空气中氮氧化的日变化曲线
实验类型:综合性实验
实验学时8
每组人数:8
实验目的与教学要求:
1.了解空气中氮氧化物的主要类型、来源及其环境应。
2.了解空气中氮氧化物测定方法。
3.掌握盐酸萘乙二胺分光光度法测定空气中氮氧化物总量,NO,NO2的原理及操作方法。
掌握空气氮氧化物测定的基本原理和操作方法。
4.掌握大气采样器的使用,进一步熟悉分光光度计的使用。
5.绘制学校周边主要交通干线空气中氮氧化物的日变化曲线,并分析其与车流量的关系。
教学方法:
教师分配任务,讲解重点要点,明确要求。
学生以小组为单位制定方案,经教师批准后实施,教师现场指导。
实验内容提要:
本实验测定氮氧化物总量(NO+NO2),空气样品首先通过三氧化铬氧化管将一氧化氮氧化为二氧化氮,然后进入吸收液,二氧化氮在水溶液中反应部分生成亚硝酸,亚硝酸与对氨基苯磺酸发生重氮化反应,再与盐酸萘乙二胺发生偶合反应生成玫瑰红色染料,在540nm 处进行比色测定,用亚硝酸钠配制标准溶液,绘制标准曲线。
采集并测定1天内不同时段交通干线中氮氧化物的浓度,并绘制氮氧化物浓度的时间变化曲线。
实验二水体自净程度指标的测定
实验类型:综合实验
实验学时:8
每组人数:4
实验目的与教学要求:
1. 复习理论课内容,水体中氮的形态的转化。
2. 掌握纳氏试剂分光光度法测定氨氮的原理及操作过程。
3.掌握盐酸萘乙二胺分光光度法测测定亚硝盐的原理及操作方法。
4. 掌握紫外分光光度法测定硝酸根的原理和操作方法。
5. 了解三态氮测定对环境化学研究的意义和作用,根据三态氮的相对含量分析水体自净程度。
教学方法:
教师讲解要点及注意事项,学生分组实验,教师指导。
实验内容提要:
1.氨氮的测定:水样蒸馏预处理,标准系列溶液配制、显色,取适量水样蒸馏液显色,在
425nm处测定吸光度,计算回归方程,计算水样中氨氮的浓度。
2.亚硝酸盐氮的测定:在pH为2.0-2.5的范围内,亚硝酸与对氨基苯磺酸发生重氮化反
应,再与盐酸萘乙二胺发生偶合反应生成玫瑰红色染料,在540nm处进行比色测定,用标准曲线法定量。
3. 硝酸盐氮的测定:紫外分光光度法,利用硝酸根对220nm光的吸收定量测定硝酸盐氮,有机物的影响可通过220nm的吸光度减去275nm处吸光度的2倍消除,用标准曲线法定量。
实验三水体富营养化程度的评价
实验类型:综合实验
实验学时:4
每组人数:4
实验目的与教学要求:
1.复习水体富营养化的概念,了解水体富营养化产生的原因及其评价指标。
2. 掌握总磷、叶绿素-a的测定原理及操作方法。
3. 评价水体富营养化状况。
教学方法:
教师讲解要点及注意事项,学生分组实验,教师指导。
实验内容提要:
1.总磷的测定:水样在酸性介质中用过硫酸钾氧化,将各种形态的磷转化为磷酸盐,用磷
钼蓝分光光度法测定。
2.叶绿素-a的测定:用丙酮萃取分光光度法测定。
实验四土壤、活性炭对苯酚的吸附作用
实验类型:综合实验
实验学时:4
每组人数:8
实验目的与教学要求:
1.了解土壤、活性炭的环境化学意义及其在水体自净中的作用。
2.掌握4-氨基安替比林分光光度法测定苯酚的原理和操作方法。
3.绘制两种土壤、活性炭对苯酚的吸附等温线,求出吸附常数,比较它们对苯酚的吸附能
力。
教学方法:
教师讲解要点及注意事项,学生分组实验,教师指导。
实验内容提要:
试验土壤、活性炭对一系列不同浓度的苯酚的吸附情况,计算平衡衡浓度和吸附量,绘制等温吸附线,分析吸附性能。
用4-氨基安替比林分光光度法测定苯酚。
四、使用教材及参考书
教材:《环境化学实验》主编:董德明,朱利中
出版社:高等教育出版社2008年
五、考核办法和成绩评定标准
本实验是环境化学课程内实验,实验成绩记入平时成绩。
每个实验根据表现(10%)、操作技能(40%)和实验报告(50%)计算成绩,不做实验则该次实验成绩为0,最后成绩以总平均成绩计。
实验成绩按30%比例计入课程总成绩。
实验成绩不及格者,不能参加课程理论考试。
执笔:唐复明
审定:薛兆民
日期:2011年04月。
