有机物分子共线共面问题
有机物共线共面问题的判断技巧

有机物共线共面问题的判断技巧一、共线与共面基本概念在有机化学中,共线与共面问题是指分子中的原子或基团是否处于同一平面或直线上。
共线问题主要涉及碳碳三键和苯环中的原子共线问题,而共面问题则更加复杂,涉及到多种因素。
二、判断原则和方法判断有机物分子中的原子是否共面或共线,需要遵循以下原则和方法:1.烷烃分子中C原子周围最多有3个H原子与其共平面。
2.含有苯环的有机物分子中,与苯环直接相连的原子一定与苯环共平面。
3.含有碳碳双键或碳碳叁键的有机物分子中,与双键或叁键碳原子直接相连的原子一定与双键或叁键共平面。
4.含有-C=O的有机物分子中,与氧原子直接相连的原子与C=O共平面。
5.某些取代基中有苯环、碳碳双键或碳碳叁键等结构时,可能影响到整个分子中的原子共平面。
6.利用空间几何关系,判断原子是否共平面或共直线。
三、常见有机物的共线与共面问题实例分析1.丙炔中的C≡C键和甲基中的C-C键的C原子周围最多有2个H原子与其共平面。
2.苯酚分子中的苯环上的所有原子共平面,-OH基处于该平面上,故该分子最多有14个原子共平面。
3.氯乙烯和苯乙烯中的双键碳原子周围最多有4个H原子与其共平面。
4.甲醛分子中的C=O双键和C原子周围最多有2个H原子与其共平面。
5.含有苯环的有机物分子中,如果苯环上含有甲基等取代基,则取代基中的H原子最多有3个与其共平面。
6.含有-CN基的有机物分子中,与氮原子直接相连的原子可能为2个或3个与其共平面。
7.含有-CH=CH-结构的有机物分子中,如果存在π-π共轭,则与碳碳双键碳原子直接相连的原子可能为4个与其共平面。
8.含有-C≡C-结构的有机物分子中,如果存在π-π共轭,则与碳碳叁键碳原子直接相连的原子可能为2个与其共直线。
9.含有-OH基的有机物分子中,如果存在氢键,则与氧原子直接相连的原子可能为3个与其共直线。
10.含有苯环的有机物分子中,如果存在硝基等取代基,则硝基中的氮原子的直线结构可能会影响整个分子中的原子共直线。
有机物分子中原子的共面共线问题

有机物分子中原子的共面共线问题有机分子中原子的共面共线是中学有机化学教学的一个难点。
此类题目的解题思维方法如下:原子共面共线问题思维的基础:甲烷的正四面体结构;乙烯、苯的平面结构;乙炔的直线结构。
1、甲烷的正四面体结构在甲烷分子中,一个碳原子和任意个氢原子可确定一个平面。
当甲烷分子中某氢原子被其他原子或原子团取代时,该代替原子的共面问题,可将它看作是原来氢原子位置。
丙烷其结构式可写成如图2所示,丙烷分子中最多原子可能共面。
2、乙烯的平面结构乙烯分子中的所有原子都在同一平面内,键角为120°。
当乙烯分子中某氢原子被其他原子或原子团取代时,则代替该氢原子的原子一定在乙烯的平面内。
CH3CH=CH2 原子一定共面,最多原子可能共面。
3.苯的平面结构苯分子所有原子在同一平面内,键角为120°。
当苯分子中的一个氢原子被其他原子或原子团取代时,代替该氢原子的原子一定在苯分子所在平面内。
甲苯如右下图所示,甲苯分子中最多有可能是个原子共面。
4.乙炔的直线结构乙炔分子中的2个碳原子和2个氢原子一定在一条直线上,键角为180°。
当乙炔分子中的一个氢原子被其他原子或原子团取代时,代替该氢原子的原子一定和乙炔分子的其他原子共线。
丙炔如图所示,丙炔分子中有个原子共线。
巩固练习:1、描述CH3-CH=CH-C≡C-CF3分子结构下列叙述中,正确的是A.6个碳原子有可能都在一条直线上B.6个碳原子不可能都在一条直线上C.6个碳原子有可能都在一个平面上D.6个碳原子不可能都在一个平面上2、甲烷分子中的4个氢原子全部被苯基取代,可得如图所示的分子,对该分子的描述不正确的是()A.分子式为C25H20B.分子中所有原子有可能处于同一平面C.该化合物分子中所有原子不可能处于同一平面D.分子中所有原子一定处于同一平面3、盆烯是近年合成的一种有机物,它的分子结构可简化表示为(其中C、H原子已略去),下列关于盆烯的说法中错误的是()A.盆烯是苯的一种同分异构体B.盆烯分子中所有的碳原子不可能在同一平面上C.盆烯是乙烯的一种同系物D.盆烯在一定条件下可以发生加成反应4、某烃的结构简式为CH3―CH2―CH=C(C2H5)―C≡CH分子中含有四面体结构的碳原子(即饱和碳原子)数为a,在同一直线上的碳原子数量最多为b,一定在同一平面内的碳原子数为c,则a、b、c分别为()A.4、3、5 B.4、3、6 C.2、5、4 D.4、6、45、观察以下有机物结构:CH3 CH2CH3(1) C = CH H (2) H—C≡C—CH2CH3 (3) —C≡C—CH=CF2思考:最多有几个碳原子共面、、最多有几个碳原子共线、、有几个不饱和碳原子、、不饱和度及其应用不饱和度又称为“缺氢指数”,用希腊字母Ω来表示,顾名思义,它是反映有机物分子不饱和程度的量化标志。
有机物分子中原子的共面共线问题
有机物分子中原子的共面共线问题有机分子中原子的共面共线是中学有机化学教学的一个难点。
此类题目的解题思维方法如下:原子共面共线问题思维的基础:甲烷的正四面体结构;乙烯、苯的平面结构;乙炔的直线结构。
1、甲烷的正四面体结构在甲烷分子中,一个碳原子和任意个氢原子可确定一个平面。
当甲烷分子中某氢原子被其他原子或原子团取代时,该代替原子的共面问题,可将它看作是原来氢原子位置。
丙烷其结构式可写成如图2所示,丙烷分子中最多原子可能共面。
2、乙烯的平面结构乙烯分子中的所有原子都在同一平面内,键角为120°。
当乙烯分子中某氢原子被其他原子或原子团取代时,则代替该氢原子的原子一定在乙烯的平面内。
CH3CH=CH2 原子一定共面,最多原子可能共面。
3.苯的平面结构苯分子所有原子在同一平面内,键角为120°。
当苯分子中的一个氢原子被其他原子或原子团取代时,代替该氢原子的原子一定在苯分子所在平面内。
甲苯如右下图所示,甲苯分子中最多有可能是个原子共面。
4.乙炔的直线结构乙炔分子中的2个碳原子和2个氢原子一定在一条直线上,键角为180°。
当乙炔分子中的一个氢原子被其他原子或原子团取代时,代替该氢原子的原子一定和乙炔分子的其他原子共线。
丙炔如图所示,丙炔分子中有个原子共线。
巩固练习:1、描述CH3-CH=CH-C≡C-CF3分子结构下列叙述中,正确的是A.6个碳原子有可能都在一条直线上B.6个碳原子不可能都在一条直线上C.6个碳原子有可能都在一个平面上D.6个碳原子不可能都在一个平面上2、甲烷分子中的4个氢原子全部被苯基取代,可得如图所示的分子,对该分子的描述不正确的是()A.分子式为C25H20B.分子中所有原子有可能处于同一平面C.该化合物分子中所有原子不可能处于同一平面D.分子中所有原子一定处于同一平面3、盆烯是近年合成的一种有机物,它的分子结构可简化表示为(其中C、H原子已略去),下列关于盆烯的说法中错误的是()A.盆烯是苯的一种同分异构体B.盆烯分子中所有的碳原子不可能在同一平面上C.盆烯是乙烯的一种同系物D.盆烯在一定条件下可以发生加成反应4、某烃的结构简式为CH3―CH2―CH=C(C2H5)―C≡CH分子中含有四面体结构的碳原子(即饱和碳原子)数为a,在同一直线上的碳原子数量最多为b,一定在同一平面内的碳原子数为c,则a、b、c分别为()A.4、3、5 B.4、3、6 C.2、5、4 D.4、6、45、观察以下有机物结构:CH3 CH2CH3(1) C = CH H (2) H—C≡C—CH2CH3 (3) CH=CF2思考:最多有几个碳原子共面、、最多有几个碳原子共线、、有几个不饱和碳原子、、不饱和度及其应用不饱和度又称为“缺氢指数”,用希腊字母Ω来表示,顾名思义,它是反映有机物分子不饱和程度的量化标志。
专题有机物分子共面共线问题的判断pptx

烯烃分子共面共线实例
在烯烃分子中,与双键C原子直接相连的原子和双键C原子共面,双键C原子与其相邻的C原子以及与双键C原子相连的原子共线。
总结词
例如,在丁烯分子中,CH2=CH-CH2-CH3,由于与双键C原子直接相连的原子为H、H、CH3,因此这些原子与双键C原子共面。同样,由于双键C原子与其相邻的C原子相连,因此这些原子也共面。此外,与双键C原子相连的原子为H、H、CH3、H,因此这些原子也共面。
总结词
详细描述
炔烃分子共面共线实例
在芳香烃分子中,与苯环直接相连的原子和苯环共面,与苯环直接相连的碳原子所连接的其他碳原子及其氢原子也共面。
总结词
例如,在甲苯分子中,由于与苯环直接相连的原子为碳和氢,因此这些原子与苯环共面。同样,由于与苯环直接相连的碳原子所连接的其他碳原子及其氢原子也与苯环直接相连,因此这些碳氢原子也共面。
通过观察有机物分子的结构形式,判断不饱和度是否会影响共面。
运用常见共面结构单元法
如苯环、双键、碳碳三键等,根据其结构特征判断是否共面。
运用等电子原理
对于碳碳单键,如果成键原子所含电子数相同,则它们共面。
01
02
03
直接观察法
运用碳碳三键的直线性
运用等电子原理
共线问题判断方法
有机物分子共面共线问题的实例展示
xx年xx月xx日
专题有机物分子共面共线问题的判断
有机物分子共面共线问题的判断方法有机物分子共面共线问题的实例展示有机物分子共面共线问题在合成中的应用有机物分子共面共线问题在实验中的验证有机物分子共面共线问题相关习题解析
contents
目录
有机物分子共面共线问题的判断方法
01
共面问题判断方法
有机分子共线共面问题
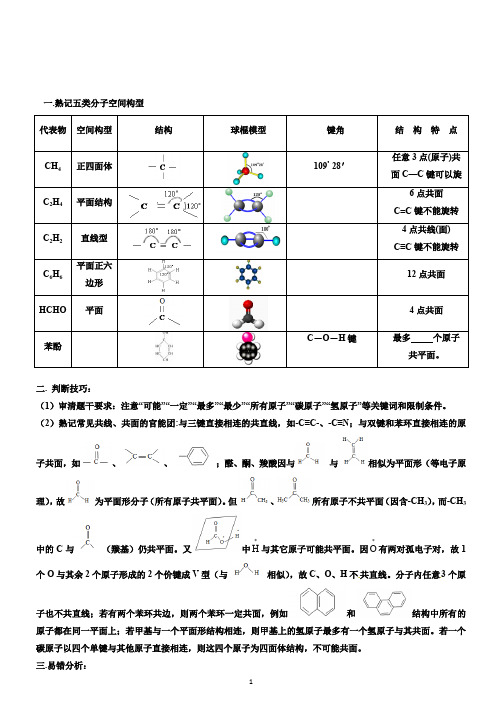
一.熟记五类分子空间构型二. 判断技巧:(1)审清题干要求:注意“可能”“一定”“最多”“最少”“所有原子”“碳原子”“氢原子”等关键词和限制条件。
(2)熟记常见共线、共面的官能团:与三键直接相连的共直线,如-C≡C -、-C≡N ;与双键和苯环直接相连的原子共面,如、、;醛、酮、羧酸因与 与相似为平面形(等电子原理),故为平面形分子(所有原子共平面)。
但、所有原子不共平面(因含-CH 3),而-CH 3中的C 与(羰基)仍共平面。
又中*H 与其它原子可能共平面。
因*O 有两对孤电子对,故1个O 与其余2个原子形成的2个价键成V 型(与相似),故C 、O 、H 不共直线。
分子内任意3个原子也不共直线;若有两个苯环共边,则两个苯环一定共面,例如和结构中所有的原子都在同一平面上;若甲基与一个平面形结构相连,则甲基上的氢原子最多有一个氢原子与其共面。
若一个碳原子以四个单键与其他原子直接相连,则这四个原子为四面体结构,不可能共面。
三.易错分析:(1)苯与环己烷:苯()中所有原子共平面,而环己烷()中所有原子不共面。
(2)庚烷中碳碳单键经过旋转,所有的碳原子有可能共面。
(3)以碳原子和化学键为立足点,若碳原子周围都是单键,那么该碳原子与其周围的原子就不共面,。
如CH3Cl。
(4)若两个平面形结构的基团之间以单键相连,这个单键可以旋转,则两个平面可能共面,但不是“一定”共面,如联苯(5)碳原子以单键与其他原子结合时位于四面体中心,且与另两个原子共面;碳碳单键可旋转,碳碳单键不可旋转;CH2Cl2没有同分异构体,说明CH4是正四面体结构;的二元卤代物没有同分异构体,说明苯环上的碳与碳之间的化学键都一样,整个分子中的原子共面。
四、结构不同的基团连接后原子共面分析1.直线与平面连接:直线结构中如果有2个原子(或者一个共价键)与一个平面结构共用,则直线在这个平面上。
如CH2=CH-C≡CH,其空间结构为,中间两个碳原子既在乙烯平面上,又在乙炔直线上,所以直线在平面上,所有原子共平面。
高中必读-有机物分子共线-共面问题大全
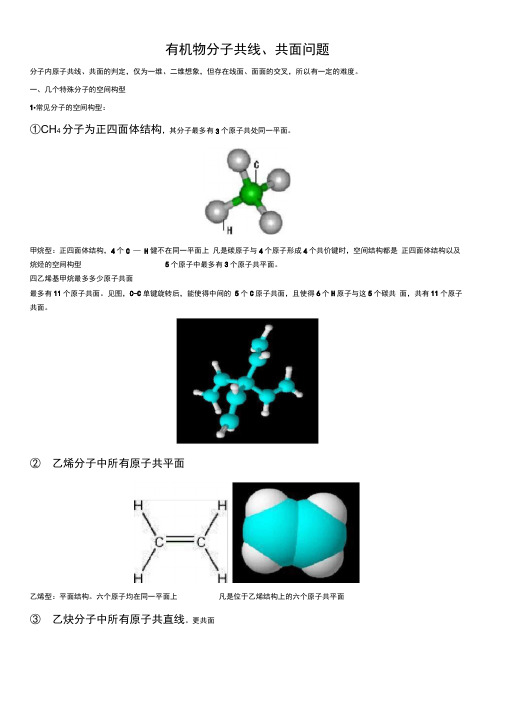
有机物分子共线、共面问题分子内原子共线、共面的判定,仅为一维、二维想象,但存在线面、面面的交叉,所以有一定的难度。
一、几个特殊分子的空间构型1•常见分子的空间构型:①CH4分子为正四面体结构,其分子最多有3个原子共处同一平面。
甲烷型:正四面体结构,4个C —H健不在同一平面上凡是碳原子与4个原子形成4个共价键时,空间结构都是正四面体结构以及烷烃的空间构型5个原子中最多有3个原子共平面。
四乙烯基甲烷最多多少原子共面最多有11个原子共面。
见图,C-C单键旋转后,能使得中间的5个C原子共面,且使得6个H原子与这5个碳共面,共有11个原子共面。
②乙烯分子中所有原子共平面乙烯型:平面结构。
六个原子均在同一平面上凡是位于乙烯结构上的六个原子共平面③乙炔分子中所有原子共直线。
更共面(1) 熟记四类空间构型中学有机化学空间结构问题的基石是甲烷、乙烯、乙炔和苯的分子结构。
(2) 理解三键三角三键:C — C 键可以旋转,而 C=C 键、gC 键不能旋转。
三角:甲烷中的C — H 键之间的夹角为109° 28'乙烯和苯环中的 C — H 键之间的夹角为120°,乙炔中的C — H 键 之间的夹角为180°2•单键的转动思想有机物分子中的单键,包括碳碳单键、碳氢单键、碳氧单键等可转动。
、结构不同的基团连接后原子共面分析IEI 球盟櫃显 II 忧侧腔型 乙映分子的模型乙炔型:直线型结构。
四个原子在同一条直线上④ 苯分子中所有原子共平面。
凡是位于乙炔结构上的四个原子共直线。
H H A % cue Hie CIH<总CIC H H*解CIC冬^HIC CIH*帕cue本型:平面正六边形结构。
六个碳原子和六个氢原子共平面⑤H — CHO 分子中所有原子共平面。
凡是位于苯环上的12个原子共平面。
1直线与平面连接: 直线结构中如果有 2个原子(或者一个共价键)与一个平面结构共用,则直线在这个平面于这个平面上。
专题有机物分子共面共线问题的判断

专题有机物分子共面共线问题的判断xx年xx月xx日CATALOGUE目录•有机物分子共面共线问题的判断方法•有机物分子共面共线问题的实例展示•有机物分子共面共线问题在合成中的应用•有机物分子共面共线问题的进阶判断方法•有机物分子共面共线问题的总结与展望01有机物分子共面共线问题的判断方法1 2 3通过观察有机物分子的结构形式,判断不饱和键和双键的位置,确定分子构型。
直接观察法运用价层电子对互斥理论,判断分子构型是否符合价层电子对互斥理论,从而确定分子是否共面。
运用价层电子对互斥理论根据分子的对称性来判断分子是否共面,如果分子具有对称性,则分子一定不共面。
根据分子对称性判断根据碳碳单键的旋转自由度判断由于碳碳单键可以自由旋转,因此如果两个碳碳单键之间夹角为180度,则两个碳碳单键上的原子一定共线。
根据分子对称性判断如果分子具有对称性,则分子一定不共线。
根据分子轨道理论判断利用分子轨道理论分析分子的轨道结构,判断分子是否共线。
02有机物分子共面共线问题的实例展示在烯烃分子中,与双键C原子直接相连的原子和双键C原子共面,双键C原子与其相邻的C原子以及与双键C原子相连的原子共线。
总结词例如,在丁烯分子中,由于双键C原子与其相邻的C原子以及与双键C原子相连的原子共线,因此与双键C原子直接相连的四个原子(包括双键C原子)必然共面。
详细描述烯烃分子共面共线实例总结词在炔烃分子中,与三键C原子直接相连的原子和三键C原子共面,三键C原子与其相邻的C原子以及与三键C原子相连的原子共线。
详细描述例如,在丙炔分子中,由于三键C原子与其相邻的C原子以及与三键C原子相连的原子共线,因此与三键C原子直接相连的两个原子(包括三键C原子)必然共面。
炔烃分子共面共线实例总结词在芳香烃分子中,苯环上的所有原子共面,与苯环直接相连的原子和苯环上任意两个碳原子共线。
详细描述例如,在甲苯分子中,由于苯环上的所有原子共面,因此与苯环直接相连的四个原子(包括苯环上的四个碳原子)必然共面。
有机物分子共线共面问题大全

有机物分子共线.共面问题分子内原子共线.共面的剖断,仅为一维.二维想象,但消失线面.面面的交叉,所以有必定的难度.一.几个特别分子的空间构型1.罕有分子的空间构型:①CH4分子为正四面体构造,其分子最多有3个原子共处统一平面.甲烷型:正四面体构造,4个C—H健不在统一平面上凡是碳原子与4个原子形成4个共价键时,空间构造都是正四面体构造以及烷烃的空间构型5个原子中最多有3个原子共平面.四乙烯基甲烷最多若干原子共面最多有11个原子共面.见图,C-C单键扭转后,能使得中央的5个C原子共面,且使得6个H原子与这5个碳共面,共有11个原子共面.②乙烯分子中所有原子共平面.乙烯型:平面构造.六个原子均在统一平面上凡是位于乙烯构造上的六个原子共平面③乙炔分子中所有原子共直线.更共面乙炔型:直线型构造.四个原子在统一条直线上凡是位于乙炔构造上的四个原子共直线.④苯分子中所有原子共平面.苯型:平面正六边形构造.六个碳原子和六个氢原子共平面凡是位于苯环上的12个原子共平面.⑤H—CHO分子中所有原子共平面.(1)熟记四类空间构型中学有机化学空间构造问题的基石是甲烷.乙烯.乙炔和苯的分子构造.(2)懂得三键三角三键:C—C键可以扭转,而C=C键.C≡C键不克不及扭转.三角:甲烷中的C—H键之间的夹角为109°28′,乙烯和苯环中的C—H键之间的夹角为120°,乙炔中的C—H键之间的夹角为180°.2.单键的迁移转变思惟有机物分子中的单键,包含碳碳单键.碳氢单键.碳氧单键等可迁移转变.二.构造不合的基团衔接后原子共面剖析1.直线与平面衔接:直线构造中假如有2个原子(或者一个共价键)与一个平面构造共用,则直线在这个平面上.如CH2=CH-C≡CH,其空间构造为,中央两个碳原子既在乙烯平面上,又在乙炔直线上,所以直线在平面上,所有原子共平面.2.平面与平面衔接:假如两个平面构造经由过程单键相连,则因为单键的扭转性,两个平面不必定重合,但可能重合.如苯乙烯分子中共平面原子至少12个,最多16个.同理可剖析萘分子中10个碳原子,8个氢原子18原子共面和蒽分子中14个碳原子,10个氢原子,共24个原子共面问题.再如:其构造简式可写成起码6个碳原子(因双键与双键之间的碳碳单键可以迁移转变)6个原子,最多10个碳原子共面.16个原子再如:中11个碳原子,萘环上的6个氢原子共17个原子共面.亚甲基上的两个氢原子分离位于平面的两侧(甲烷型①C ②C ③C组成三角形).3.平面与立体衔接:假如甲基与平面构造经由过程单键相连,则因为单键的扭转性,甲基的一个氢原子可能临时处于这个平面上.如丙烯分子中,共面原子至少6个,最多7个.甲苯中的7个碳原子(苯环上的6个碳原子和甲基上的一个碳原子),5个氢原子(苯环上的5个氢原子)这12个原子必定共面.此外甲基上1个氢原子(①H,②C,③C组成三角形)也可以转到这个平面上,其余两个氢原子散布在平面两侧.故甲苯分子中起码12个,最多有可能是13个原子共面.4.直线.平面与立体衔接:如图所示的大分子中共平面原子至少12个,最多19个.剖析时要留意两点:①不雅察大分子的构造,先找出甲烷.乙烯.乙炔和苯分子的“影子”,再将甲烷“正四面体”.乙烯“平面型”.乙炔“直线形”和苯“平面型”等分子构型常识迁徙过来即可;②苯环以单键衔接在6号不饱和碳原子上,不管单键若何扭转,8号和9号碳原子老是处于乙烯平面上.不要疏忽8号碳原子对位上的9号碳原子,三.比较重要的是须要记住-------共线必共面以下几个根本纪律:单键是可扭转的,是造成有机物原子不在统一平面上最重要的原因1. 构造中每消失一个饱和碳原子,则全部分子不再共面.2. 构造中每消失一个碳碳双键,至少有6个原子共面;3. 构造中每消失一个碳碳三键,至少有4个原子共线;4. 构造中每消失一个苯环,至少有12个原子共面5.正四面体构造:甲烷 平面构造:乙烯.苯.萘( ).蒽 .甲醛( ) 直线构造:乙炔 与饱和碳(CH 4型)直接相连的原子既不共线也不共面.与 或 或 或 直接相连的原子共面. 与—C≡C—直接相连的原子共线.碳碳单键可随意率性扭转,而双键或三键均不克不及扭转.例题:1.丙烷中最多有3个碳原子共面,最多有5个原子共面.2.① 丙烯中有3个C 原子共面和3个H 原子必定共面.丙烯中至少有3个C 原子共面和3个H 原子共面.丙烯中最多有3个C 原子共面和4个H 原子共面.丙烯中可能有3个C 原子共面和4个H 原子共面.②2,3—二甲基—2—丁烯至少有6个原子共面,最多有10个原子共面. ③右上图的二烯烃至少有6个C 原子共面,最多有10个C 原子共面. 至少有6个原子共面,最多有16个原子共面. 3.甲苯有12个原子必定共面,最多有13个原子共面.4.丙炔有4个原子必定共线,最多有5个原子共面.5.①下图该有机物有4个原子必定在一条直线上,至少有8个原子共面,最多有9 O H —C —HC=C CH 3 ╲ CH 3 ╱ H 3C ╱ ╲ H 3C C=C ╲ CH 3 ╱ ╱ H 3C C=C CH 3 ╲ CH 3 ╱H 3C ╱ H 3C ╲ ╲ ╱ ╱ ╲ C=C个原子共面.CH3-CH2—CH=C(C2H5)-C≡CH中含四面体构造的碳原子数为4,在统一向线上的碳原子数最多为3,必定在统一平面内的碳原子数为6,起码共面的原子数为8,最多共面的原子数为12.③CH3--CH=CH-C≡C-CH3分子中,处于统一平面上的原子数最多可能是20个.【演习】1.下列有机分子中,所有的原子不成能处于统一平面的是(D )构造中消失饱和碳原子,则全部分子不再共面22=CH-CH=CH2C. -CH=CH22=C-CH=CH2CH32.描写CH3-CH=CH-C≡C-CF3分子构造的下列论述中,准确的是(B)C.6个碳原子一建都在统一平面上D.6个碳原子不成能都在统一平面上该分子构造中至少可以有8个原子在统一个平面?最多可以有10个原子在统一个平面?3.甲烷分子中四个氢原子都可以被代替.若甲烷分子中的四个氢被苯基代替,则可得到的分子如下图,对该分子的描写,不准确的是( B )25H20(中间碳原子甲烷型)(提醒:有可能两个苯和一个中间碳原子,共一个平面.)4.六苯乙烷为白色固体,其构造暗示如图:下列有关说法中不准确的是( C )A.它是一种芬芳烃,易溶于乙醚中B.它的分子式为C38H30,长短极性分子C.它的一氯代物只有一种D.在统一平面上的原子最多有14个温习进程中除了对球棍模子.比例模子增强熟悉外,还要留意不合分子构造之间的接洽之处.温习中要留意将有机物构造跟无机物构造接洽起来,如高考中经常考到的水分子.水合氢离子.氨分子.铵离子.甲烷分子.白磷分子等之间都可找到接洽.请看下图:。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
有机物分子共线、共面问题
分子内原子共线、共面的判定,仅为一维、二维想象,但存在线面、面面的交叉,所以有一定的难度。
一、几个特殊分子的空间构型
1.常见分子的空间构型:
①CH4分子为正四面体结构,其分子最多有3个原子共处同一平面。
甲烷型:正四面体结构,4个C—H健不在同一平面上凡是碳原子与4个原子形成4个共价键时,空间结构都是正四面体结构以及烷烃的空间构型5个原子中最多有3个原子共平面。
四乙烯基甲烷最多多少原子共面
最多有11个原子共面。
见图,C-C单键旋转后,能使得中间的5个C原子共面,且使得6个H原子与这5个碳共面,共有11个原子共面。
②乙烯分子中所有原子共平面。
乙烯型:平面结构。
六个原子均在同一平面上凡是位于乙烯结构上的六个原子共平面
③乙炔分子中所有原子共直线。
更共面
乙炔型:直线型结构。
四个原子在同一条直线上凡是位于乙炔结构上的四个原子共直线。
④苯分子中所有原子共平面。
苯型:平面正六边形结构。
六个碳原子和六个氢原子共平面凡是位于苯环上的12个原子共平面。
⑤H—CHO分子中所有原子共平面。
(1)熟记四类空间构型
中学有机化学空间结构问题的基石是甲烷、乙烯、乙炔和苯的分子结构。
(2)理解三键三角
三键:C—C键可以旋转,而C=C键、C≡C键不能旋转。
三角:甲烷中的C—H键之间的夹角为109°28′,乙烯和苯环中的C—H键之间的夹角为120°,乙炔中的C—H 键之间的夹角为180°。
2.单键的转动思想
1.直线与平面连接:直线结构中如果有2个原子(或者一个共价键)与一个平面结构共用,则直线在这个平面上。
如CH2=CH-C≡CH,
其空间结构为,中间两个碳原子既在乙烯平面上,又在乙炔直线上,所以直线在平面上,所有原子共平面。
2.平面与平面连接:如果两个平面结构通过单键相连,则由于单键的旋转性,两个平面不一定重合,但可能重合。
如苯乙烯分
子中共平面原子至少8个,最多16个。
同理可分析萘分子中10个碳原子,8个氢原子18原子共面
和蒽分子中14个碳原子,10个氢原子,共24个原子共面问题。
再如:其结构简式可写成最少6个碳原子(因双键与双键之间的碳碳单键可以转动)6个原子,最多10个碳原子共面。
16个原子
再如:中11个碳原子,萘环上的6个氢原子共17个原子共面。
亚甲基上的两个氢原子分别位于平面的两侧(甲烷型①C ②C ③C构成三角形)。
3.平面与立体连接:如果甲基与平面结构通过单键相连,则由于单键的旋转性,甲基的一个氢原子可能暂时处于这个平面上。
如
丙烯分子中,共面原子至少6个,最多7个。
甲苯中的7个碳原子(苯环上的6个碳原子和甲基上的一个碳原子),5个氢原子(苯环上的5个氢原子)这12个原子一定共面。
此外甲基上1个氢原子(①H,②C,③C构成三角形)也可以转到这个平面上,其余两个氢原子分布在平面两侧。
故甲苯分子中最少12个,最多有可能是13个原子共面。
4.直线、平面与立体连接:如图所示的大分子中共平面原子至少12个,最多19个。
分析时要注意两点:①观察大分子的结构,先找出甲烷、乙烯、乙炔和苯分子的“影子”,再将甲烷“正四面体”、乙烯“平面型”、乙炔“直线形”和苯“平面型”等分子构型知识迁移过来即可;②苯环以单键连接在6号不饱和碳原子上,不管单键如何旋转,8号和9号碳原子总是处于乙烯平面上。
不要忽视8号碳原子对位上的9号碳原子,
三、比较重要的是需要记住-------共线必共面
以下几个基本规律:单键是可旋转的,是造成有机物原子不在同一平面上最主要的原因
1. 结构中每出现一个饱和碳原子,则整个分子不再共面。
2. 结构中每出现一个碳碳双键,至少有6个原子共面;
3. 结构中每出现一个碳碳三键,至少有4个原子共线;
4. 结构中每出现一个苯环,至少有12个原子共面 5. 正四面体结构:甲烷 平面结构:乙烯、苯、萘( )、蒽 、
甲醛( ) O H —C —H
与饱和碳(CH 4型)直接相连的原子既不共线也不共面。
与 或 或 或 直接相连的原子共面。
与—C≡C—直接相连的原子共线。
碳碳单键可任意旋转,而双键或三键均不能旋转。
例题:
1、丙烷中最多有 3 个碳原子共面,最多有 5 个原子共面。
2、① 丙烯中有 3 个C 原子共面和 3 个H 原子一定共面。
丙烯中至少有 3 个C 原子共面和 3 个H 原子共面。
丙烯中最多有 3 个C 原子共面和 4 个H 原子共面。
丙烯中可能有 3 个C 原子共面和 4 个H 原子共面。
╲
╱ ╱ ╲ C=C
②2,3—二甲基—2—丁烯至少有 6 个原子共面,最多有 10 个原子共面。
③右上图的二烯烃至少有 6 个C 原子共面,最多有 10 个C 原子共面。
至少有 6 个原子共面,最多有 16 个原子共面。
3、甲苯有 12 个原子一定共面,最多有 13 个原子共面。
4、丙炔有 4 个原子一定共线,最多有 5 个原子共面。
C=C CH 3
╲ CH 3 ╱ H 3C ╱ ╲ H 3C C=C
╲ CH 3
╱ ╱ H 3C C=C CH 3
╲
CH 3 ╱ H 3C ╱ H 3C ╲
5、①下图该有机物有 4 个原子一定在一条直线上,至少有 8 个原子共面,最多有 9 个原子共面。
CH3-CH2—CH=C(C2H5)-C≡CH中含四面体结构的碳原子数为4 ,
在同一直线上的碳原子数最多为 3 ,一定在同一平面内的碳原子数为 6 ,
最少共面的原子数为 8 ,最多共面的原子数为 12 。
③CH3--CH=CH-C≡C-CH3分子中,处于同一平面上的原子数最多可能是 20 个。
【练习】
1、下列有机分子中,所有的原子不可能处于同一平面的是( D )结构中出现饱和碳原子,则整个分子不再共面
A.CH2=CH-CN B.CH2=CH-CH=CH2
C. -CH=CH2=C-CH=CH2
CH3
2、描述CH3-CH=CH-C≡C-CF3分子结构的下列叙述中,正确的是(B)
都在一条直线上
C.6个碳原子一定都在同一平面上D.6个碳原子不可能都在同一平面上
该分子结构中至少可以有 8 个原子在同一个平面最多可以有10 个原子在同一个平面
3、甲烷分子中四个氢原子都可以被取代。
若甲烷分子中的四个氢被苯基取代,则可得到的分子如下图,对该分子的描述,不正确的是( B )
A.分子式为C25H20
B.所有碳原子都在同一平面上(中心碳原子甲烷型)
C.此物质属于芳香烃
D.此分子最多有13个碳原子在一个平面上
(提示:有可能两个苯和一个中心碳原子,共一个平面。
)
4、六苯乙烷为白色固体,其结构表示如图:
下列有关说法中不正确的是( C )
A.它是一种芳香烃,易溶于乙醚中
B.它的分子式为C38H30,是非极性分子
C.它的一氯代物只有一种
D.在同一平面上的原子最多有14个。
