化工原理-第十章
化工原理第10章
第10章习题解答1 在操作条件下,以纯净的氯苯为萃取剂,在单级接触萃取器中,萃取含丙酮的水溶液。
丙酮-水-氯苯三元混合液的平衡数据见本题附表。
试求:⑴在直角三角形坐标系下,绘制此三元体系的相图,其中应包括溶解度曲线、联接线和辅助曲线;⑵若近似地将前五组数据中B与S视为不互溶,试在X-Y直角坐标图上标绘分配曲线;⑶若丙酮水溶液质量比分数为0.4,并且m B/m S=2.0,在X-Y直角坐标图上求丙酮在萃余相中的浓度;⑷求当水层中丙酮浓度为45%(质量%,下同)时,水与氯苯的组成以及与该水层成平衡时的氯苯层的组成;⑸由0.12kg氯苯和0.08kg水所构成的混合液中,尚需加入多少kg丙酮即可成为三元均相混合液;⑹预处理含丙酮35%的原料液800kg,并要求达到萃取平衡时,萃取相中丙酮浓度为30%,试确定萃取剂(氯苯)的用量;⑺求条件⑹下的萃取相和萃余相的量,并计算萃余相中丙酮的组成;⑻若将条件⑹时的萃取相中的溶剂全部回收,求可得萃取液的量及组成。
解:⑴依平衡数据绘出溶解度曲线如附图1-1所示,图中各点代号与数据的对应关系注于附表1-1中。
联结互成平衡的两液层组成点得E1R1、E2R2、E2R2……等平衡联结线。
由E1、E2、E3……各点作平行于AB边的直线,再由R1、R2、R3……各点作平行于AS边的直线,两组线分别相交于点G、H、I、J、K,连接P、G、H、I、J、K即得辅助曲线。
⑵将前五组数据转换为质量比浓度,其结果列于附表1-2中,并在X-Y直角坐标图上标绘分配曲线,如图1-2。
附表1-2⑶由X F=0.4,在图1-2上,自点X F作斜率为-m B/m S=-2.0的直线与分配曲线相交于点T,点T的横坐标即为丙酮在萃余相中的浓度X R=0.25。
图1-1 图1-2⑷水层中各组分的浓度由所绘制的溶解度曲线如图1-3,在AB边上确定组分A的浓度为45%的点F,由点F绘直线FW平行于三角形底边BS,则FW线上各点表示A的组成均为45%。
西北大学化工原理 第十章第一节 气液传质设备-板式塔

工作录像
西北大学化工原理课件
五、板式塔的不正常操作现象
1. 夹带液泛
液沫夹带使塔板上液层厚度增加,相当于板间距的减小, 因此夹带量将进一步增加,这样可能会产生恶性循环破坏塔的 正常操作。 夹带液泛经常因气速过高引起,塔板上开始出现恶性循环 工作录像 的气速成为液泛气速。
2. 溢流液泛
因降液管通过液体能力限制而引起的液泛称为溢流液泛。 通常是由于液量过大引起。 工作录像
① 结构:
动画演示
② 特点与应用:
工作录像1 工作录像2
弹性大、操作稳定可靠;但结构复杂,成本高,压降大。
西北大学化工原理课件
2. 浮阀塔
① 结构:
动画演示 工作录像
② 特点与应用: 结构上较泡罩简单,操作 弹性大,可有效防止漏液,生 产能力大。
动画演示
西北大学化工原理课件
3. 筛板塔
① 结构: 由筛孔、溢流堰和降 液管等主要部分组成。 制作:wang 单位:西北大学 盗版投诉邮箱: iquygnaw@
西北大学化工原理课件
八、塔板类型
评价塔设备性能的指标
① 生产能力大 即:单位塔截面能处理的气液负荷高; ② 塔板效率高 ③ 板压降低,两相流动阻力小 ④ 操作弹性大 即:上、下操作极限通过的气量之比大; ⑤ 满足工业对生产设备的一般要求 结构简单、造价低、安装维修方便等。
西北大学化工原理课件
1. 泡罩塔板
西北大学化工原理课件
2. 塔板负荷性能图
由五条线组成,分别为: 1——过量液沫夹带线 2——(溢流)液泛线 3——液相上限线 4——漏液线 5——液相下限线 操作液气比下两相流量的关系
A B C
OLeabharlann 塔板负荷性能图① OA线(低L/V):塔的生产能力由1线控制; ② OB线(中L/V):塔的生产能力由2线控制; ③ OC线(高L/V):塔的生产能力由3线控制;
化工原理第10章_蒸馏
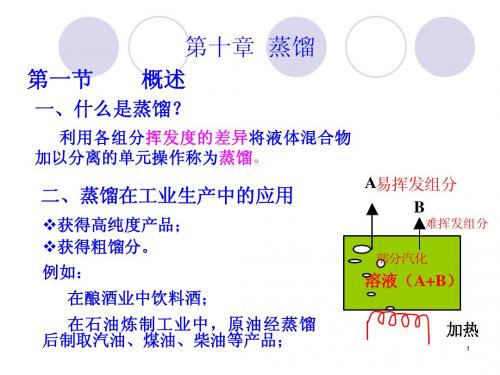
t f x
t g y
?
对理想物系,汽相满足:P 0 P pB x 0 0 p A pB
0 p A pB p 0 x pB (1 x ) A
pA pA p0 x A y P P P
F xF 高温 高压
P t
L xW
26
思考:在操作压力、原料相同的条件下(F=W1,x1=xF ),若平衡蒸馏的操作温 度与简单蒸馏的最终温度相同(t=t2)。则简单蒸馏与平衡蒸馏相比: 分离效果孰好(比较xD、 yD )? 产品量孰大(比较WD、 V ) ?
答:由图上的得:简单蒸馏分离效果好; 由杠杆原理作图得简单蒸馏产量小, 或如下计算也可得此结论。 简: W1 W2 W D
y f x
-----理想物系的x-y相平衡关系
pA p0 x y A P P
P p A pB
0 p 0 x pB (1 x) A
p0 x A y 0 0 0 p A x pB (1 x ) pA x (1 x ) 0 pB
p0 A 令 0 ----相对挥发度 pB
W1,x1
dW y
W x
加热
x2
W2
WD, xD
ydW d (Wx) Wdx xdW
( y x )dW Wdx
dW dx W y x
x1 dx W1 ln x2 y x W2
3个未知数
x 对理想物系 y 1 ( 1) x
22
一、简单蒸馏
原料液中易挥发组分的摩尔数
t B
W1 x1 x 2 WD x D x2
(完整版)化工原理各章节知识点总结

(完整版)化工原理各章节知识点总结第一章流体流动质点含有大量分子的流体微团,其尺寸远小于设备尺寸,但比起分子自由程却要大得多。
连续性假定假定流体是由大量质点组成的、彼此间没有间隙、完全充满所占空间的连续介质。
拉格朗日法选定一个流体质点,对其跟踪观察,描述其运动参数(如位移、速度等)与时间的关系。
欧拉法在固定空间位置上观察流体质点的运动情况,如空间各点的速度、压强、密度等,即直接描述各有关运动参数在空间各点的分布情况和随时间的变化。
定态流动流场中各点流体的速度u 、压强p 不随时间而变化。
轨线与流线轨线是同一流体质点在不同时间的位置连线,是拉格朗日法考察的结果。
流线是同一瞬间不同质点在速度方向上的连线,是欧拉法考察的结果。
系统与控制体系统是采用拉格朗日法考察流体的。
控制体是采用欧拉法考察流体的。
理想流体与实际流体的区别理想流体粘度为零,而实际流体粘度不为零。
粘性的物理本质分子间的引力和分子的热运动。
通常液体的粘度随温度增加而减小,因为液体分子间距离较小,以分子间的引力为主。
气体的粘度随温度上升而增大,因为气体分子间距离较大,以分子的热运动为主。
总势能流体的压强能与位能之和。
可压缩流体与不可压缩流体的区别流体的密度是否与压强有关。
有关的称为可压缩流体,无关的称为不可压缩流体。
伯努利方程的物理意义流体流动中的位能、压强能、动能之和保持不变。
平均流速流体的平均流速是以体积流量相同为原则的。
动能校正因子实际动能之平均值与平均速度之动能的比值。
均匀分布同一横截面上流体速度相同。
均匀流段各流线都是平行的直线并与截面垂直,在定态流动条件下该截面上的流体没有加速度, 故沿该截面势能分布应服从静力学原理。
层流与湍流的本质区别是否存在流体速度u、压强p的脉动性,即是否存在流体质点的脉动性。
稳定性与定态性稳定性是指系统对外界扰动的反应。
定态性是指有关运动参数随时间的变化情况。
边界层流动流体受固体壁面阻滞而造成速度梯度的区域。
夏清《化工原理》(第2版)(下册)章节题库-第10章 干 燥【圣才出品】

章节题库第10章干燥一、选择题1.对于一定干球温度的空气,当其湿度越大,湿球温度就()。
A.越低B.越高C.不变D.不确定【答案】B【解析】湿球温度可反映空气的状态,空气湿度越高,湿球温度越接近干球温度。
2.对于恒速干燥阶段,下列描述错误的是()。
A.干燥速度与物料种类有关B.干燥速度与气体的流向有关C.干燥速度与气体的流速有关D.干燥速度与气体的性质有关【答案】A【解析】恒速干燥阶段主要除去的是非结合水,干燥速率主要取决于空气的状态,与物料自身结构关系不大。
3.对流干燥过程,恒速干燥阶段,液体的蒸发速率与()有关;降速干燥阶段,液体的蒸发速率与()有关。
A.被干燥固体性质B.干燥介质的流量C.干燥介质的流量、性质D.都有关【答案】CA【解析】恒速干燥阶段与空气的流动状况有关,与物料自身结构关系不大(表面汽化控制阶段);而降速干燥阶段蒸发速率与物料自身的特性有关(物料内部扩散控制阶段)。
4.用相对湿度100%的空气干燥湿物料,干燥推动力为(),此时干球t、湿球和露点温度的关系为();若将此空气预热后,干燥推动力为(),此时干球t、湿球和露点温度的关系为()。
A.0B.>0C.D.【答案】ADBC【解析】相对湿度为100%,干燥过程无推动力。
预热后,相对湿度减小,w d t t t >>,推动力大于零。
5.在恒速干燥阶段中,在给定的空气条件下,对干燥速率正确的判断是:A.干燥速率随物料种类不同而有极大的差异B.干燥速率随物料种类不同而有极小的差异C.各种不同物料的干燥速率实质上是相同的D.不一定【答案】B【解析】恒速干燥阶段,速率主要取决于空气状态,与物料自身结构关系不大。
二、填空题在总压为101.33kPa下,将饱和空气的温度从t1降至t2,则该空气的下列状态参数变化的趋势是:相对湿度φ,湿度H,露点t4。
【答案】不变降低降低【解析】因为是饱和空气,温度降低,相对湿度不变,但由于有冷凝水出现导致湿度减小,露点随湿度的降低而降低。
柴诚敬《化工原理》笔记和课后习题(含考研真题)详解(10-12章)【圣才出品】

量分数。
b.对于萃取剂 S 与原溶剂 B 互不相溶的物系,溶质在两液相中的分配关系与吸收中的
类 似,即 Y KX
式中 Y——萃取相 E 中溶质 A 的质量比组成;X——萃余相 R 中溶质 A 的质量比组成;K—
e MR r ME
结合三角形相似定理可得
e xA zA MR m xA yA RE
3 / 96
圣才电子书
及
十万种考研考证电子书、题库视频学习平台
r zA yA ME m xA yA RE
式中 ——线段 的长度,m。
③若向 A、B 二元混合液 F 中加入纯溶剂 S,则三元混合液的总组成点 M 必位干 SF 的
④过 M 点分别作三个边的垂线 MN、ML 及 MJ,则垂直线段
及 分别代表 A、
B 及 S 的组成。由图可知,M 点的质量分数为:
和
(2)杠杆规则
如图 10-3 所示,将质量为 r,组成为 xA、xR、xS 的混合液 R 与质量为 e,组成为 yA、yB、
ys 的混合液 E 相混合,得到一个质量为 m,组成为 zA、zB、zS 的新混合液 M,其在三角形坐
连线上,具体位置由杠杆规则确定,即
MF S MS F
2.三角形相图 (1)根据萃取操作中各组分的互溶性,可将三元物系分为以下三种情况,即 ①溶质 A 完全溶于 B 及 s,B 与 S 不互溶; ②溶质 A 完全溶于 B 及 S,B 与 S 部分互溶; ③溶质 A 完全溶于 B,A 与 s 及 B 与 S 部分互溶。 (2)溶解度曲线及联结线 ①设溶质 A 可完全溶于 B 及 S,但 B 与 S 为部分互溶,一定温度下的平衡相图如图 l0-4 所示,图中曲线 R0R1R2RiRnKEnEiE2E1E 0 称为溶解度曲线。 ②溶解度曲线将三角形相图分为两个区域 曲线以内的区域为两相区,曲线以外的区域为均相区。位于两相区内的混合物分成两个 互相平衡的液相,称为共轭相,连接两共轭相组成坐标的直线称为联结线,显然萃取操作只 能在两相区内进行。 ③若组分 B 与组分 S 完全不互溶,则点 R。与 E。分别与三角形顶点 B 及顶点 S 相重合。
化工原理第10章-3
1.0 a
xD R’ + 1
若已知蒸馏釜的汽化能力 υ (kmol/s), 则精馏一釜料液所需时间为
τ=
V
xD R终+ 1 0 x We x W' x D 1.0
υ
回流比保持恒定的间歇精馏 已知F、 馏出液的平均组成, 已知 、xF、最终釜液组成 xWe 和馏出液的平均组成,确定适宜的回流 比和所需的理论板数。 比和所需的理论板数。 回流比与理论板数的确定 塔板数一定时, 塔板数一定时,任意时刻的 xD 与 xW 之间存在着相互制约的关系。 之间存在着相互制约的关系。 随过程的进行,操作线将平行下移, 随过程的进行,操作线将平行下移, 即操作线的起点和截距均在变。 即操作线的起点和截距均在变。 首先假设一最初的馏出液组成 xD始, 始 由设定的 xD始 与料液组成 xF 求出所需 始 的最小回流比。 的最小回流比。
V
L
D, xD
理论板数的确定
恒定 xD,终了时刻xW 最低,分离程度(xD-xW)最大,故所需理论板数应 以终了时刻为准。设终了时刻釜液组成为 xWe,可用图解法求理论板数。
理论板数的确定 根据 xD 与 xWe 按下式计算最小回流比
Rmin = xD − yWe yWe − xWe
1.0 a
y We xD Rmin + 1 0 x We x D 1.0
yn +1 = W W xn − xW V0 V0
1.0 a
因 xn=xW 时 yn+1=0,提馏段操作线 的终点在 x 轴上的 g 点(xW ,0) a 点出发绘梯级至 g 点得理论板数。 较之间接精馏,直接加热精馏所需 的理论板数稍有增加。因为直接加 热蒸汽的稀释作用,使得塔内物料 分离程度增加,当达到相同的馏出 液组成及回收率时需更多塔板。
化工原理第十章-蒸馏
2、泡点、露点方程:
汽相压力不高时,可视为理想气体,满足道 尔顿分压定律。
pA pA0 xA fA (t)xA ; pB pB0 xB fB (t)xB
p pA pB pA0 xA pB0 xB pA0 xA pB0 (1 xA )
xA
p pB0 pA0 pB0
p fB(t) fA(t) fB(t)
5)冷凝器及再沸器热负荷及设计计算。
2024/9/29
全塔物料衡算
F D W FxF DxD WxW
F, xF
F、D、W——kmol/h
xF、xD、xW——摩尔分率
塔顶采出率 塔底采出率
D xF xW F xD xW
W 1 D
F
F
2024/9/29
D, xD W, xW
塔顶易挥发组分回收率 塔底难挥发组分回收率
混合液中组分数
双组分 多组分
间歇 按操作方式
连续
2024/9/29
五 与吸收、萃取旳比较
单元操作 分离根据
操作难易 合用性
蒸馏
挥发性旳差别 操作简便,操 适于多种
作费用在于加 浓度混合
热、冷却
物旳分离
吸收 萃取
溶解度旳差别
需加入分离剂,仅适于低
操作费用在于 浓气体、
解吸
液体混合
物旳分离
2024/9/29
V L D Vyn1 Lxn DxD
LD
yn1
V
xn
V
xD
L
D
L D xn L D xD
令
R
L D
——回流比
yn1
R R1
xn
xD R1
——精馏段操作线方程
化工原理第十章 蒸馏小结 PPT
●教学基本要求● 掌握双组分溶液的汽液相平衡;双组分连 续精馏的计算和分析。了解间歇精馏、特别 精馏和多组分精馏。掌握板式塔的结构和设 计。 学习本章重点应掌握的内容: (1)蒸馏操作的依据; (2)双组分物系的汽液相平衡; (3)精馏原理; (4)精馏操作线方程推导、意义与应用;
②在y x图上,两条操作线皆与对角线重合; ③全回流时所需理论板数最少,
lg[( xD ) ( xW )]
Nmin
1 xD 1 xW
lg
④多用于设备开车,调试及科学研究。
● 最小回流比Rmin:
Rmin
xD yq
yq xq
式中:xq、yq为q线与具有最小回流比操作线交
点坐标。
①影响Rmin的因素有:物系的相平衡曲线、 分离要求;
液具有负偏差,这种系统会出现最低蒸汽压和 相应的最高恒沸点,如硝酸—水溶液。
注意:不管是正偏差依然负偏差溶液,在恒 沸组成时,其溶液两相的组成皆相同,故无法用 一般蒸馏方法加以分离。
二、蒸馏过程 1、简单蒸馏 (1)流程:如下图所示,为一间歇操作过程。
10-4
(2)特点
●间歇操作过程;
●不稳定过程,随着蒸馏的进行,釜内液体中易 挥发组分的组成逐渐降低,与之相平衡的汽相中, 易挥发组分的组成亦随之降低,釜液温度不断升 高;
●侧线出料和多股进料
侧线出料和多股进料可将塔分成若干段,
各段分别有相应的操作线,各股进料亦分别
有相应的q线方程和q线。各段的操作线方程
通过每段的物料衡算推导出。
●加设中间再沸器或中间冷凝器的情况
从用能的角度来考虑,加设中间再沸器可 降低高温热源的能量热耗,而加设中间冷凝器, 则能够节约低温冷剂的消耗量。但不管是加 设中间再沸器依然中间冷凝器对分离都是不 利的。
化工原理 第十章 课件 陈敏恒
9.2双组分溶液的气液平衡
第九章
蒸馏
Distillation
1
化工原理
9.2双组分溶液的气液平衡
9.2双组分溶液的气液相平衡
9.2.1双组分理想物系的气液平衡 9.2.2双组分非理想物系的气液平衡
2
化工原理
9.2双组分溶液的气液平衡
9.2.1 双组分理想物系的气液平衡
3
化工原理
9.2双组分溶液的气液平衡
一、相律
在物理化学中,我们学习过相律,即:
F C 2
式中F――自由度数; C ――独立组分数; Φ ――相数。 对双组分的气液相平衡,由相律知其自由度数为2。
4
化工原理
9.2双组分溶液的气液平衡
二、双组分理想物系的液相组成-温度 关系——泡点方程
理想物系,遵循拉乌尔定律:
pA pA xA
挥发度与相对挥发度 挥发度: v A
pA xA
7
vB
pB xB
化工原理
9.2双组分溶液的气液平衡
相对挥发度:
vA vB
pA
yA xA
pB xB
xA yB xB
对双组分溶液,气相遵循道尔顿分压定律,则:
y
x
1 1 x
上式称为气液相平衡方程。α 越大,分离越容易。
0
p B p B x B p B 1 x A
0 0
pA0、 pB0为溶液温度下纯组分A和B的饱和蒸气压
可查有关手册或由下面安托因方程求得:
lg p A
0
B C T
5
化工原理
9.2双组分溶液的气液平衡
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
满足理想气体状态方程、道尔顿分压定律
P pA pB
1.理想溶液
yA
pA P
yB
pB P
在全部浓度范围内都服从拉乌尔定律的溶液称为理想溶液。
只有物性和结构相似,且分子大小也相近的物系才符 合拉乌尔定律,如苯-甲苯、甲醇-乙醇、烃类同系 物组成的溶液等等。
二元物系的汽液相平衡
§10.2 二元物系的汽液相平衡
二.蒸馏在工业生产中的应用
例如: 在酿酒业中饮料酒; 在石油炼制工业中,原油经蒸馏后制 取汽油、煤油、柴油等产品; 在合成材料工业中
概述(Introduction)
三. 蒸馏的分类
二元蒸馏 根据被蒸馏的混合物的组分数,可分为:多元蒸馏
连续蒸馏 根据操作过程是否连续,可分为:间歇蒸馏
常压蒸馏 根据操作压力,可分为加压蒸馏
浓度高
重组分
部分 冷凝
部分 汽化
汽相 液相 汽相 液相
概述(Introduction)
沸点低的组分 沸点高的组分
易挥发组分(轻组分),以A表示。 难挥发组分(重组分),以B表示。
原料液
加热器
Q
塔顶产品 yA
闪 蒸
xA 罐
塔底产品
yA xA
或
yA xA
yB xB
概述(Introduction)
概述(Introduction)
蒸馏
概述(Introduction) 依据
一.什么是蒸馏?
利用各组分挥发度的差异将液体混合物 加以分离的单元操作称为蒸馏。
A 易挥发组分
B 难挥发组分
部分汽化
溶液(A+B)
加热
混合 液体 A+B
部分 汽化
挥发性高组分 汽相易挥发组分 浓度高
轻组分
液相
挥发性低组分 难挥发组分
t f x, P 在一定的压力下 t f x
t gy, P
t gy
t, P, y
A
B
t, x 溶液(A+B)
加热
pA Py f x, t 在一定的温度下 pA f x
pB P1 y gx, t
pB gx
§10.2 二元物系的汽液相平衡
一. 理想物系的汽液相平衡
汽相为理想气体、液相为理想溶液的体系,称为 。
p
0 A
pB0
P fB t fAt fB t
泡点方程(bubblepoint equation)
yA
p
0 A
P
P pB0 pA0 pB0
fAt
P
P fB t fAt fB t
露点方程(dewpoint equation)
【例10.1】 分离苯—甲苯溶液的某蒸馏塔塔顶设有 一部分冷凝器和一全凝器,其操作压强为101.3kPa。 现测得全凝器出口馏出液中苯的含量为92.3%(摩尔 分数)。设离开部分冷凝器的汽、液相组成互为平衡 组成,试求部分冷凝器馏出液的组成及温度。苯-甲 苯溶液可视为理想溶液,纯组分的蒸汽压为
第十章 蒸 馏 Chapter 10 Distillation
时间安排表
9.24 吸收…… 蒸馏概述
9.26 汽液相平衡 简单蒸馏和平衡蒸 馏(闪蒸),精馏
10.8
精馏原理,全塔板 效率,板式塔精馏 过程的基本计算式
10.10
双组分连续精馏塔 的计算
10.15 理论板数的求法
10.17 传质设备
答疑时间:单周星期四下午2:30~5:00;双周星期五晚7:30~9:00 网上答疑:信箱meiguiyi9@
1345 83.8 219.5
1.645
p
0 B
44 .20 k Pa
【例10.1】
p0A P
p pB0 p0A pB0
113.6 101.3 44.20 101.3 113.6 44.20
0.923
假设正确,即部分冷凝器的馏出 液温度为83.8℃,其组成可如下 求得
p
A
pB
p
0 A
x
A
------拉乌尔(Raoult)定律
p
0 B
x
B
t f x
t gy pA f x
pB gx
纯组分B pB0
p
A
pB
p
0 A
x
A
pB0 x B
P
纯组分A pA0
A pA0
B
At 加热
pA
0
xA (xB)
1
§10.2 二元物系的汽液相平衡
在一定的温度下 pA f x pB g x
P
P pB0
p
0 A
pB0
即
0.923
pA0 101.3
101.3 pB0 pA0 pB0
部分冷凝器
y1,V
全 凝
xA
器
L
xD=0.923
y1
x1
例10-1 附图
设=83.8℃
log pA0
6.031 1211 83.8 220.8
2.055
p
0 A
113
.6k Pa
log
pB0
6.080
y
pA
p
0 A
x
程进行推算:
P
p
0 A
P
P
P
p
0 B
p
0 A
p
0 B
ln p0 A B T C
§10.2 二元物系的汽液相平衡
在一定的温度下 pA f x pB g x
理想物系
p
A
pB
p
0 A
x
A
p
0 B
x
B
拉乌尔定律
在一定的压力下 t f x
t gy
理想物系
xA
P pB0
苯 甲苯
log
p
0 A
6.031
t
1211 220.8
log
p
0 B
6.080
t
1345 219.5
式中p 的单位为kPa, 温度t 的单位为℃。
部分冷凝器 y1,V
全 凝
xA
器
L
xD=0.923
y1
x1
例10-1 附图
【例10.1】
解:对全凝器有
yA xD 0.923
由露点方程
yA
p
0 A
规整填料 塑料 丝网波纹填料
散装填料塑料 鲍尔环填料
级式接触:气、液两相逐级接触传质, 两相的组成呈阶跃变化。 如板式塔。
DJ 塔盘 新型塔板、填料
二元物系汽液相平衡时,所涉及的变量有:
温度t、压力P、汽相组成y、液相组成x等4个。
自由度数 F C 2
222 2
变量个数 方程个数
方程个数 2
减压蒸馏
简单蒸馏 根据操作方式,可分为:平衡蒸馏
精馏
概述(Introduction)
本章要讨论的问题
汽液相平衡; 精馏原理; 双组分连续精馏塔的计算:
➢ 物料恒算:操作线方程; ➢ 操作回流比的确定; ➢ 理论塔板数的计算;
其他类型精馏塔的特点。
气液两相的接触方式
连续接触(也称微分接触):气、液 两相的浓度呈连续变化。如填料塔。
理想物系
p
A
pB
p
0 A
x
A
p
0 B
x
B
拉乌尔定律
在一定的压力下 t f x
t gy
? 理想物系
理想物系的 t-x(y)相平衡关系:
对理想物系,汽相满足:P pA pB
p
0 A
x
A
pB0
p
0 A
、
pB0
仅与温度
t
有关,可采用
实测数据或用安托因(Antoine)方
