最新ACS患者的抗血小板治疗
急性冠脉综合征非血运重建患者抗血小板治疗中国专家共识
服用阿司匹林和(或)氯吡格雷时,不推荐常规服用质子泵抑制剂(PPI)以预防胃肠道不良反应,对于高胃肠道风险的患者可考虑更换其他抑酸药如组胺H2受体拮抗剂;对于有消化道溃疡需要服用PPI的ACS患者,建议由心内科、消化内科以及普内科医师共同评估,制定治疗方案。
2005年CPACS (中国急性冠脉综合征临床路径研究) 63%ACS患者接受了单纯药物治疗
63%
PCI或CABG
52%
PCI或 CABG
单纯药物 治疗
3级医院
单纯药物治疗
80%
PCI或CABG
2级医院
入组2,823ACS患者
入组1731ACS患者
入组1092ACS患者
Ruilin G, et al. Heart published online 11 Oct 2007; doi:10.1136/hrt.2007.119750
ACS的病理生理基础
2、急性血栓形成 男性68%首发AMI和心脏猝死 出现在冠脉狭窄<50%的病例。 女性50%首发AMI和心脏猝死
ACS的病理生理基础
一旦斑块破裂,便激活血小板和凝血系统,在破裂斑块的基础上形成富含血小板的止血血栓。 当损伤严重,则在血小板血栓的基础上形成以纤维蛋白和红细胞为主的闭塞性血栓—红色血栓,冠脉血流完全中断,ECG一般表现为ST段抬高。 当损伤较轻,形成的血栓为非闭塞性,以血小板为主—白色血栓。形成白色血栓时,冠脉血流没有完全中断,可以冲击血栓而栓塞末梢小动脉,表现为UA或NSTEMI。
氯吡格雷及其治疗建议
NSTEACS患者中不准备进行早期(5d内)诊断性冠脉造影或冠状动脉旁路移植术(CABG)的患者,立即给予氯吡格雷负荷剂量300mg,继以75mg/d。除非有高出血风险,建议持续应用12个月。 ST段抬高心肌梗死(STEMI)患者无论是否采用纤溶治疗,应该给予氯吡格雷75mg/d,至少持续14d,并且建议长期治疗,如1年。如患者<75岁给予负荷剂量300mg(75岁以上和出血高危的患者不用负荷剂量)。 正在服用氯吡格雷,拟行择期CABG的患者,建议术前停用氯吡格雷至少5d,除非急诊手术。
ACS抗血小板治疗

新型ADP受体拮抗剂
如cangrelor,可在手术过程中快速逆转抗血 小板作用,降低围手术期血栓风险。
抗血小板治疗的个体化方案研究
根据患者的基因型、危险因素和临床 特征制定个体化的抗血小板治疗方案 ,以提高治疗效果并降低不良反应。
研究不同患者对不同抗血小板药物的 反应差异,为临床提供更精确的治疗 选择。
防止血栓形成
血小板在血栓形成过程中起关键作用,通过抗血小板治疗 可有效抑制血小板聚集,预防血栓形成,从而降低心肌梗 死、中风等严重心血管事件的发生率。
改善患者预后
及时、规范的抗血小板治疗有助于改善ACS患者的临床预 后,提高患者的生活质量和生存率。
临床实践中的注意事项与挑战
01 02
出血风险
抗血小板治疗会增加出血风险,特别是消化道出血、脑出血等严重出血 事件。医生需根据患者情况谨慎评估抗血小板治疗的利弊,选择合适的 药物和剂量。
01
02
03
抑制血小板活化
抗血小板药物通过抑制血 小板表面的受体或酶,阻 止血小板活化,从而降低 血栓形成的风险。
抑制血小板聚集
抗血小板药物可以抑制血 小板之间的聚集反应,防 止血栓形成和血管阻塞。
增加血小板溶解
某些抗血小板药物可以促 进血小板溶解,从而降低 血小板数量和活性,减少 血栓形成的风险。
ACS的分类与临床表现
NSTEMI/UA
非ST段抬高型心肌梗死和不稳定型心绞痛的病理生理机制相似,冠状动脉存在 不稳定的粥样斑块,但没有完全闭塞,心电图表现为非ST段抬高。临床表现为 阵发性胸痛、呼吸困难、心悸等。
STEMI
ST段抬高型心肌梗死是由于冠状动脉完全闭塞导致心肌缺血坏死,心电图表现 为ST段抬高。临床表现为持续剧烈胸痛、心力衰竭、心律失常甚至心脏骤停。
急性冠脉综合征ACS-PCI后的DAPT双联抗血小板治疗策略(全文)

急性冠脉综合征ACS-PCI后的DAPT双联抗血小板治疗策略(全文)双联抗血小板治疗(dual antiplatelet therapy,DAPT)和经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI)均被证实为治疗急性冠脉综合征(acute coronary syndrome,ACS)的有效临床手段。
现阶段对置入药物洗脱支架(drug eluting stents,DES)后DAPT的使用时间指南建议为12个月,以减少晚期或超晚期的支架内血栓的形成,对于高危ACS患者则建议延长DAPT使用时间。
研究发现,新一代DES由于改良了血管愈合和再内皮化的特性,疗效优于早期DES,临床应用比例逐渐增加。
应用光学相干断层成像术(OCT)对二代和三代DES置入后血管进行观察研究,结果发现87%支架术后3个月内新生内膜完全覆盖支架,提示新一代DES置入后可能不必延长DAPT应用时间[1-3]。
这些发现引发有关ACS患者DAPT使用时长的讨论。
PCI后双联抗血小板治疗的必要性2005 ACC/AHA/SCAI PCI指南[4]指出:支架较PTCA显著降低了血管再狭窄(BENESTENT II:PTCA31%vs. 支架17%;STRESS:PTCA42%vs. 支架32%)。
DES可对冠脉病变局部提供缓慢和长期高浓度的药物释放,抑制细胞过度增生和抗血管重塑,进一步降低了支架内再狭窄率:裸支架36%vs. 西罗莫司洗脱支架9%;裸支架27%vs. 紫杉醇洗脱支架8%。
DES的应用,在进一步降低了支架内再狭窄率的同时,由于药物及涂层本身抑制了支架表面的内皮化,从而增加了支架植入术后晚期血栓形成的风险。
通过观察停用氯吡格雷后晚期缺血事件的发生率,发现停用DAPT增加DES晚期血栓形成,增加了死亡或非致死性心肌梗死的发生率[5]。
晚期和超晚期支架血栓的主要危险因素为过早停用抗血小板药物[6]。
ACS患者抗血小板治疗策略

抗血小板治疗药物的演变
1988年FDA批准用于临床的抗血小板药物 单用疗效有限,增加剂量会增加出血危险
阿司匹林
第一个噻吩吡啶类
1991年FDA批准 严重不良反应:中性粒细胞减少、血栓性血小板减少性紫癜
噻氯匹定
氯吡格雷
1998年FDA批准 疗效、安全性被广泛证实
ESC2014 心肌血运重建指南对PCI术后DAPT治疗,维持剂量及时间的推荐
ESC 2014 《心肌血运重建指南》推荐
择期PCI 术前建议服用氯比格雷600mg或更大剂量的负荷剂量,75mg/日维持剂量 对于支架置入术后的抗血小板治疗,药物洗脱支架(DES)置入术后应给予双
联抗血小板治疗6 个月 接受第二代DES 置入后的高危出血风险患者应接受双重抗血小板治疗3 个月 而对于存在高缺血和低出血风险的患者,或许可以给予双重抗血小板治疗6 个
② 发病12h后接受PCI的患者,参照直接PCI用药; ③ 接受溶栓的PCI患者,溶栓后24h内口服300mg负荷剂量,24h后口服300-600mg
负荷剂量,维持剂量75mg/d,至少12个月; ④ 未接受再灌注治疗的患者,口服氯吡格雷75mg/d,至少12个月。
新进展:ESC 2014 心肌血运重建指南
血风险)
Ferreiro JL, Sibbing D, Angiolillo DJ.Thromb Haemost. 2010;103:1128-35.
抗血小板策略调整需基于缺血与出血风险的平衡
平衡策略
缺血
• 对于心脑血管事件高危患 者,如ACS、近期行PCI 者,建议继续双抗治疗
• 过早停用抗血小板药物者 临床结局更差
小结
合并CKD患者同时增加ACS患者缺血及出血风险 无禁忌征的情况下,CKD患者应该接受与其他患者相同的一线
急性冠脉综合征(ACS)的抗血小板 双联抗血小板 实用总结全

急性冠脉综合征(ACS)的抗血小板双联抗血小板实用总结急性冠脉综合征(ACS):冠脉不稳定斑块破裂或糜烂继发新鲜血栓致急性缺血综合征,包括:STEMI和非ST段抬高型心肌梗死(NSTEMI)、不稳定性心绞痛(UA),NSTEMI与UA合称NSTE-ACS o基本治疗抗血小板、抗缺血。
无论ACS是否血运重建史,接受长期DAPT(双联抗血小板)是获益的。
-:非血运重建ACS者的DAPT(双联抗血小板)建议:(目前尚缺乏ACS患者P2Y12受体抑制剂单独使用临床证据)1 :接受单纯药物治疗者建议DAPT至少12个月。
2 :既往有心梗病史且存在高缺血风险者,若12个月内耐受DAPT 且无出血并发症,可阿司匹林基础上予替格瑞洛60mgbid延长方案,最长36个月。
3 :处于高出血风险(如PREQSE-DAPT>25分或符合ARC-HBR 标准)者至少1个月DAPT o4 :P2Y12受体抑制剂建议用替格瑞洛而非氯毗格雷,除非出血风险大于潜在缺血获益。
因替格瑞洛疗效优于氯叱格雷且不增加主要出血事件。
对于未计划血运重建且无高出血风险可予P2Y12负荷量预治疗。
(注:ACS为急性冠状动脉综合征;DAPT为双联抗血小板治疗;ARC-HBR为学术研究联合会高出血风险工作组)二:ACS者接受PCI术后DAPT的建议:1:PCI术前均阿司匹林150~300mg负荷剂量联合P2Y12受体抑制剂负荷剂量预治疗:P2Y12受体抑制剂首选替格瑞洛(负荷剂量18Omg,维持剂量90mgbid),当替格瑞洛不可及、无法耐受或有禁忌证时,用氯叱格雷(负荷剂量300〜600mg,维持齐(]量75mgqd)o①替格瑞洛与氯叱格雷相比作用更强、起效更快。
PQ术前服用替格瑞洛后1年的MACE(心血管事件)发生率低于氯叱格雷组且主要出血风险无差异。
院前启用替格瑞洛较院内启用降低术后24h和30d 内支架血栓形成发生率。
在排除主动脉夹层/脑出血后,对低危出血风险者尽早予替格瑞洛预治疗。
(完整版)ACS抗血小板与抗凝治疗新进展

---------------------------------------------------------------最新资料推荐------------------------------------------------------ ACS抗血小板与抗凝治疗新进展急性冠脉综合征抗血小板与抗凝治疗新进展急性冠脉综合征(ACS) 是以冠状动脉粥样硬化斑块破裂或糜烂,继发斑块表面血栓形成和/或远端血栓栓塞,造成完全或不完全心肌缺血为特征的一组疾病。
根据心电图表现, ACS 分为 STE-ACS和 NSTE-ACS。
STE-ACS 反映了冠状动脉急性完全闭塞,血栓成分以纤维蛋白和红细胞为主,即红血栓。
NSTE-ACS 反映了冠状动脉非完全闭塞,血栓成分以血小板为主,即白血栓。
无论 STE-ACS 还是 NSTE-ACS,血栓形成和/或血栓栓塞都是最主要的病理生理机制,因此,抗栓在 ACS 的治疗中占据极为重要的地位。
血小板活化与凝血系统激活是血栓形成和/或血栓栓塞过程中具有决定性作用的两个关键环节,两者在体内紧密联系,凝血系统激活后产生的凝血酶,是一个强有力的血小板活化因子,血小板活化后又将促进凝血过程。
抗栓治疗应针对凝血系统和血小板两个环节,分别称为抗凝治疗和抗血小板治疗。
全球每年有 1700 万人死于心血管疾病, ACS 患者住院期间及远期死亡率分别为 6%和 12%。
1/ 8大量的研究证明,抗凝和抗血小板药物的联合使用一方面可以降低 ACS 患者血栓事件的发生率,改善预后;但另一方面,各种出血并发症的发生率增加同样威胁患者的生命。
因此,平衡血栓与出血风险是 ACS 患者抗血小板与抗凝治疗的重点及难点,尤其在高危患者和某些特殊人群如高龄、肾功能不全等。
一、抗血小板治疗首先,无论 STE-ACS 还是 NSTE-ACS,急性期双联(甚至多联)抗血小板治疗是必须的。
抗血小板药物主要有阿司匹林、氯吡格雷、血小板膜糖蛋白Ⅱ b/Ⅲa(GPⅡ b/Ⅲa)受体拮抗剂和西洛他唑等。
胸痛中心NSTE-ACS用药治疗规范

NSTEMI/UA患者的药物治疗规范一、抗血小板治疗1、阿司匹林:所有无阿司匹林禁忌证患者初始口服负荷剂量100~300mg,并长期100mg/d维持2、P2Yi2受体拮抗剂:在阿司匹林基础上加1种P2Yi2受体拮抗剂,并维持至少12个月,除非存在禁忌(如出血风险较高)氯毗格雷:负荷剂量600mg,维持剂量75mg、1次/天3、需早期行PCI治疗时,首选氯毗格雷4、对缺血风险高(如再次心梗发作、冠脉多支病变、糖尿病、肾功能不全),出血风险低的患者,可考虑在阿司匹林基础上加用P2Y12受体拮抗剂治疗>1年二、抗缺血治疗1、β受体阻滞剂:早期:除禁忌症外,患者尽量在发病24小时内服用β受体阻滞剂(建议口服美托洛尔,若耐受可改为长效控释制剂)。
美托洛尔:25-50mgq6-12h,2~3天以后转换为琥珀酸美托洛尔每日一次给药;若耐受则滴定至每日给药200mg o长期:β受体阻滞剂可改善心肌梗死患者生存率,应结合患者的临床情况采用最大耐受剂量长期治疗。
2、硝酸酯类:用于有胸痛或心肌缺血表现的患者。
对于无禁忌的NSTE-ACS患者应立即舌下含服硝酸甘油0.3∙0.6mg,每5min重复一次,总量不超过1.5mg.同时评估必要时予静脉用药,起始剂量5-10ug∕min,每3-5min以5-10ug/min剂量递熠,一般不超过200ug/min,收缩压不低于IlOmmHg,病情稳定后改为口服。
不能用于近期使用西地那非或伐地那非(<24h),以及他达月阳E(<48h)的患者。
3、钙离子通道阻滞剂:CCB用于NSTE-ACS缓解心绞痛症状或控制血压。
在应用β受体阻滞剂和硝酸酯类药物后患者仍存在心绞痛或难以控制的高血压,可加用长效的二氢毗咤类CCB e若患者不能耐受β受体阻滞剂,应予非二氢毗碇类CCB与硝酸酯类合用。
非二氢毗咤类CCB不宜与β受体阻滞剂合用,不宜用于左心室功能不全的NSTE-ACS的患者。
4、血管紧张素转换酶抑制剂(ACEI):除非不能耐受,所有NSTE-ACS的患者均应接受ACEI的治疗。
ACS患者双联抗血小板和抗凝治疗流程图
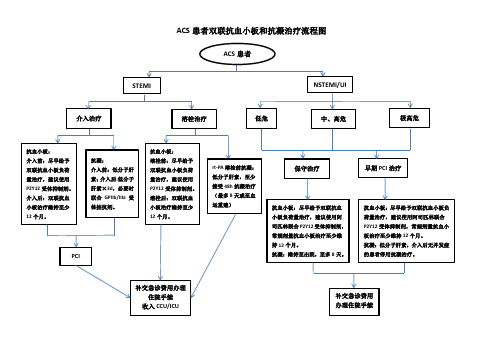
抗血小板: 溶栓前:尽早给予 双联抗血小板负荷 量治疗,建议使用 P2Y12 受体抑制剂。 溶栓后:双联抗血 小板治疗维持至少 12 个月。 rt-PA 溶栓前抗凝: 低分子肝素,至少 接受 48h 抗凝治疗 (最多 8 天或至血 运重建) 抗血小板:尽早给予双联抗血 小板负荷量治疗,建议使用阿 司匹林联合 P2Y12 受体抑制剂, 常规剂量抗血小板治疗至少维 持 12 个月。 抗凝:维持至出院,至多 8 天。 抗血小板:尽早给予双联抗血小板负 荷量治疗,建议使用阿司匹林联合 P2Y12 受体抑制剂,常规剂量抗血小 板治疗至少维持 12 个月。 抗凝:低分子肝素,介入后无并发症 的患者停用抗凝治疗。
ACS 患者双联抗血小板和抗凝治疗流程图
ACS 患者
STEMI
NSTEMI/UI
介入治疗
ห้องสมุดไป่ตู้
溶栓治疗
低危
中、高危
极高危
抗血小板: 介入前:尽早给予 双联抗血小板负荷 量治疗,建议使用 P2Y12 受体抑制剂。 介入后:双联抗血 小板治疗维持至少 12 个月。 抗凝: 介入前:低分子肝 素; 介入后:低分子 肝素×3d,必要时 联合 GPIIb/IIIa 受 体拮抗剂。
保守治疗
早期 PCI 治疗
PCI
补交急诊费用办理 住院手续 收入 CCU/ICU
补交急诊费用 办理住院手续
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
NSTE-ACS患者的抗血小板治疗
死亡、心梗和卒中
双重抗血小板治疗(波立维+ASA) 显著降低UA/NSTEMI药物治疗患者的
死亡/心梗/卒中发生率
CURE研究: 12,563 例病人, 不鼓励GP IIb/IIIa & 早期侵入性治疗
0.14
安慰剂 + ASA
(11.4%)
0.12
PTCA=percutaneous transluminal coronary angioplasty.
Fox KAA et al. Circulation. 2004;110:1202-1208.
波立维300/75mg+ASA显著降低采用不同 治疗策略的UA/NSTEMI患者1年终点事件发生率
* 主要终点事件:死亡/MI/卒中
什么时间用?
PCI前3-24小时波立维 300mg负荷剂量给 予越早,受益越大
10
无波立维负荷剂量
9
8.3%
8
提前3-6小时给予负荷剂量 7.9%
38.6 % RRR
7
p = 0.05
6
5.8%
5
提前6-24 小时给予负荷剂量
58.8 % RRR
p = 0.0028
4
提前15-24 小时给予负荷剂量3.5%
. Montalescot G et al. J Am Coll Cardiol 2006; 48:931-938
高负荷剂量600mg明显降低主要终点事件率 ARMYDA-2 Trial
• 255例SA / NSTE-ACAS病人,随机分组, PCI 术前4-8小时分别给 300mg 或600mg 波立维负荷剂量;比较30天死亡/MI/靶血管重建,
死亡、心梗及靶血管血运重建%
14% 12% 10%
8% 6% 4% 2% 0%
p = 0.041
4%
600mg
12%
300mg
Patti G. et al, Circulation. 2005; 111:2099-2106
Meta分析结果显示:高负荷剂量的临床效果更好
Study研究项目
评价终点:1个月内的心血管死亡 / MI
538
0.1 0.2 0.5 1 2
5 10
高负荷剂量更好
0.00
30
0
0
波立维 + ASA†
95% CI, 0.69–0.96
100
200
300
随访天数
对计划择期CABG且正在服用波立维的患者,应在CABG前5填内暂停5-7天波立维
* PCI was also referred to as PTCA. † Other standard therapies were used as appropriate.
Total (95% CI)
502
Total events: 14 (High loading), 35 (Standard loading)
G. Biondi Zoccai et al. 2007
N0A//1100 15/129 3/60 N0A/1/31838 N0A/2/020 1/35 16/146
高Hi负gh荷lo剂ad量ing
n/N
Sta标nd准ard负l荷oa剂din量g
n/N
PeOto ROR
95% CI
Muller et al ARMYDA-2 CLEAR PLATELETS Gurbel et al ISAR-CHOICE ALBION Cuisset et al
N0A//1100 5/126 1/60 N0A//5252 N0A//4040 2/68 6/146
0.020
事 件 0.015 发 生 率
0.010
0.005
Placebo+ ASA 2.1%
34%
RRR
RR= 0.66 p=0.003
Clopidogrel+ASA 1.4%
0.0
0
2
4
6
8 10 12 14 16 18 20 22 24
随机分组后时间 (小时)
Yusuf S. Circulation 2003;107:966
ACS患者的抗血小板治疗
STEMI患者院内死亡率高于NSTEMI患者, 而NSTEMI患者出院后的死亡率高于STEMI患者
死亡(%)
死亡(%)
院内死亡
(天)
NSTEMI患者应更 重视强化抗栓治疗
从出院至6个月的死亡率
Keith A A Fox, et al. BMJ. 2006 November 25; 333(7578): 1091.
药物治疗患者
PCI* 和/或 CABG
0.20
0.20
Cumulative Hazard Rate
0.15
0.15
安慰剂 + ASA†
安慰剂 +
0.10
ASA†
0.10
18% 相对危险下降
0.05
0.00
0
波立维l + ASA†
100
20
随访天数0
20%
0.05
相对危险下降
95% CI, 0.69–0.92
Fox et al. Circulation 2004; 110(10):1202-8.
多大负荷剂量?
高负荷剂量波立维提供更快、 更强血小板抑制作用
103 名 NSTE ACS患者随机接受300, 600 or 900 mg波立维治疗
比较最大血小板抑制 (5 µM A负荷剂量在服药2小时后即达到300mg5小时后的血小板抑制率
600~900 mg负荷剂量达到同等血小板抑制的时间
300 mg LD 600 mg LD 900 mg LD
30
20
10
300 mg负荷剂量达到血小板最大抑制的时间
0 123456
时间 (小时)
P < 0.05 vs. 300 mg LD
0.10
波立维 + ASA
0.08
(9.3%)
0.06
RRR 20%, p<0.001
0.04
0.02
0.0
0
3
6
9
12
随访时间 (月)
NEJM 2001; 345: 494
什么时间用?
双重抗血小板治疗:
波立维负荷剂量300mg+ASA
24小时内即显现减少严重缺血事件
0.025
* 随机分组后24小时内的CV死亡/MI/卒中/严重缺血事件发生率
3
死亡/心梗/UTVR(%)
2
1
0
0
7
14
21
28
随机化后天数
UTVR: 紧急目标血管血运重建
Steinhubl S, et al. JAMA, 2002 288 2411 – 2420, JACC 2006; 47:939-943
CURE 的后续分析:
双重抗血小板治疗(波立维+ASA) 对采用药物治疗和对采用介入治疗的患者一样有效
