黑龙江省2021年高考理综化学真题试卷(新课标Ⅰ)
高考全国Ⅰ2021理综试题及答案(新课标全国卷1)

2021 年全国卷1理综第一卷(选择题共126分)可能用到的相对原子质量:H 1 C 12 N 14 O 16 Cl 35.5 K 39Cr 52 Fe 56 Cu 64 Br 80 Ag 108 I 127一、选择题:此题共13小题,每题6分。
在每题给出的四个选项中,只有一项为哪一项符合题目要求的。
1.以下表达错误的选项是A.DNA与ATP中所含元素的种类一样B.一个tRNA分子中只有一个反密码子C.T2噬菌体的核酸由脱氧核糖苷酸组成D.控制细菌性状的基因位于拟核和线粒体中的DNA上2.以下关于植物生长素的表达,错误的选项是A.植物幼嫩叶片中的色氨酸可转变为生长素B.成熟茎韧皮部中的生长素可以进展非极性运输C.幼嫩细胞和成熟细胞对生长素的敏感程度一样D.豌豆幼苗切段中乙烯的合成受生长素浓度的影响3.某同学给安康实验兔静脉滴注0.9%的NaCl溶液(生理盐水)20 mL后,会出现的现象是A.输入的溶液会从血浆进入组织液B.细胞内液和细胞外液分别增加10 mLC.细胞内液Na+的增加远大于细胞外液Na+的增加D.输入的Na+中50%进入细胞内液,50%分布在细胞外液4.以下关于初生演替中草本阶段和灌木阶段的表达,正确的选项是A.草本阶段与灌木阶段群落的丰富度一样B.草本阶段比灌木阶段的群落空间构造复杂C.草本阶段比灌木阶段的群落自我调节才能强D.草本阶段为灌木阶段的群落形成创造了适宜环境5.人或动物PrP基因编码一种蛋白(PrP°),该蛋白无致病性。
PrP°的空间构造改变后成为PrP°°(朊粒),就具有了致病性。
PrP°°可以诱导更多的PrP°转变为PrP°°,实现朊粒的增殖,可以引起疯牛病。
据此判断,以下表达正确的选项是A.朊粒侵入机体后可整合到宿主的基因组中B.朊粒的增殖方式与肺炎双球菌的增殖方式一样C.蛋白质空间构造的改变可以使其功能发生变化D.PrP°转变为PrP°°的过程属于遗传信息的翻译过程6.抗维生素D佝偻病为X染色体显性遗传病,短指为常染色体显性遗传病,红绿色盲为X染色体隐性遗传病,白化病为常染色体隐性遗传病。
黑龙江省2021年高考理综-化学二模考试试卷(I)卷

黑龙江省2021年高考理综-化学二模考试试卷(I)卷姓名:________ 班级:________ 成绩:________一、单选题 (共7题;共14分)1. (2分) (2016高三上·岐山期中) 下列叙述正确的是()A . 含有最低价元素的化合物不一定具有很强的还原性B . 元素的单质一定是由氧化或还原该元素的化合物制得C . 阳离子只能得电子被还原,阴离子只能失电子被氧化D . 在化学反应中,得电子越多的氧化剂,其氧化性就越强2. (2分)(2018·佛山模拟) 化合物结构简式如图,下列说法正确的是()A . a、b、c均属于芳香烃B . a、b、c 均能与钠反应产生氢气C . a、b、c苯环上的二氯代物均有6种D . a、b、c中所有碳原子不可能存在于同一平面中3. (2分) (2018高二上·衡阳期中) 下列物质灼烧时,透过蓝色钴玻璃能看到紫色火焰的是()A . NaClB . K2SO4C . CaCl2D . CuSO44. (2分) x、y为短周期元素,x原子K、L、M各电子层的电子数之比为1:4:1,它比y原子多3个电子,下列叙述正确的是()A . x离子半径大于y离子半径B . x单质在空气中燃烧可生成两种化合物C . x、y形成的化合物与浓硫酸共热可在烧瓶中进行D . 电解x、y形成的化合物的水溶液可得到y单质5. (2分)(2016·六安模拟) 锌溴液流电池是一种新型电化学储能装置(如图),电解液为溴化锌水溶液,电解液在电解质储罐和电池间不断循环.下列说法不正确的是()A . 充电时电极a连接电源的负极B . 放电时负极的电极反应式为Zn﹣2e﹣=Zn2+C . 放电时左侧电解质储罐中的离子总浓度增大D . 阳离子交换膜可阻止Br2与Zn直接发生反应6. (2分)下列各装置不能达到实验目的是()A . 利用①吸收多余的氨气B . 装置②可用于除去Cl2中的HClC . 装置③可用于干燥氨气D . 装置④可用于排空气法收集H2、CO2、Cl2、HCl等气体7. (2分)下列说法正确的是()A . 相同温度下,1 mol•L﹣1氨水与0.5 mol•L﹣1氨水中c(OH﹣)之比是2:1B . 物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合:c(CH3COO﹣)+2c(OH﹣)═2c(H+)+c(CH3COOH)C . 向0.2 mol•L﹣1 NaHCO3溶液中加入等体积0.1 mol•L﹣1 NaOH溶液:c(CO32﹣)>c(HCO3﹣)>c(OH ﹣)>c(H+)D . CH3COOH是弱电解质,NH3•H2O是弱电解质,故CH3COONH4也是弱电解质二、实验题 (共1题;共8分)8. (8分)(2018·韶关模拟) 某学习小组在实验室中利用下图装置(夹持装置略去)测定某铁硫化物(FexSy)的组成,并探究反应后D装置所得溶液中含硫化合物的组成。
黑龙江省2021年高考理综-化学三模考试试卷(I)卷

黑龙江省2021年高考理综-化学三模考试试卷(I)卷姓名:________ 班级:________ 成绩:________一、单选题 (共7题;共14分)1. (2分)下列叙述中,正确的是()A . 常温下铝和浓硫酸、浓硝酸不反应B . 两份相同质量的铝粉,分别与足量的稀硫酸和氢氧化钠溶液反应,产生的氢气前者多C . 合金的熔点一般比组成它的各成分的熔点都高D . 工业上常利用铝热反应冶炼难熔的金属,如钒2. (2分) (2019高三上·南昌期末) 增塑剂DCHP可由环己醇制得。
DCHP和环己醇的结构简式如图所示,下列说法错误的是()环己醇DCHPA . DCHP的分子式为C20H26O4B . 环己醇分子中所有碳原子不可能共平面C . DCHP的一氯取代物有5种D . DCHP通过取代反应可以得到环己醇3. (2分) (2016高一下·乐清月考) 用NA表示阿伏伽德罗常数,下列叙述正确的是()A . 标准状况下,22.4 L H2O含有的分子数为1 NAB . 常温常压下,1.06 g Na2CO3含有的Na+离子数为0.02 NAC . 通常状况下,1 NA 个CO2分子占有的体积为22.4 LD . 物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl﹣个数为1NA4. (2分) (2018高二上·临县期中) 甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下转化关系:。
下列有关物质的推断错误的是()A . 若甲为焦炭,则丁可能是O2B . 若甲为SO2 ,则丁可能是氨水C . 若甲为Fe,则丁可能是盐酸D . 若甲为NaOH溶液,则丁可能是CO25. (2分)下列实验方法使用不合理的是()A . 用结晶法从水溶液中获得氯化铁晶体B . 用纸上层析法检验氯化铁溶液中是否混有少量氯化铜C . 为准确测定盐酸与NaOH溶液反应的中和热,所用酸和碱的物质的量必需相等D . 用AgNO3溶液、稀硝酸鉴别亚硝酸钠和食盐6. (2分) (2016高二上·温州期中) 如图所示,下列说法正确的是()A . 该装置中能量转化方式为电能转化为化学能B . 电子从锌片流出,经导线流向铜片C . 工作一段时间之后,溶液颜色逐渐变蓝D . 锌片发生还原反应7. (2分)可以证明乙酸是弱酸的事实是()A . 乙酸和水能任意比例混溶B . 1mol•L﹣1的醋酸水溶液能使紫色石蕊试液变红色C . 醋酸能与碳酸钠溶液反应生成CO2气体D . 醋酸溶液中存在醋酸分子二、填空题 (共2题;共19分)8. (9分) (2018高三下·温州开学考) 工业生产硝酸铵的流程如下图所示:(1)硝酸铵的水溶液呈________(填“酸性”、“中性”或“碱性”);其水溶液中各离子的浓度大小顺序为:________。
黑龙江省2020-2021年高三上学期理综-化学期末考试试卷(I)卷

黑龙江省2020-2021年高三上学期理综-化学期末考试试卷(I)卷姓名:________ 班级:________ 成绩:________一、单选题 (共7题;共14分)1. (2分) (2019高一下·长春期中) 实验室可以按如图所示的装置干燥、贮存气体M,多余的气体可用水吸收,则M是()A . 氯气B . 氨气C . 氢气D . 二氧化氮2. (2分) (2016高二上·溧水期中) 下列对某未知溶液中离子的检验方法及其结论一定正确的是()A . 取溶液进行焰色反应显黄色,一定含有Na+B . 滴加BaCl2溶液,产生白色沉淀,证明有SO42﹣C . 滴加KSCN溶液,变为血红色,溶液中含Fe2+D . 加入稀盐酸产生无色气体,一定含有CO32﹣3. (2分)(2018·郑州模拟) 已知草酸晶体(H2C2O4·2H2O)的熔点为101℃,170℃分解。
下列选用的装置和药品能达到实验目的的是()A . AB . BC . CD . D4. (2分)下列各项内容中,排列顺序不正确的是()A . 微粒半径:S2﹣>K+>Na+B . 氢化物的沸点:HI>HBr>HFC . 固体的热稳定性:Na2CO3>CaCO3>NaHCO3D . 相同物质的量浓度的下列溶液中NH4+的浓度:(NH4)2Fe(SO4)2>NH4Cl>NH4HCO35. (2分)(2018·西宁模拟) 25℃时,将浓度均为0.1mol/L、体积不同的HA溶液与BOH 溶液混合,保持溶液的总体积为100 mL,溶液的体积与混合液pH 的关系如图所示。
下列说法正确的是()A . V1表示HA 溶液的体积,V2表示BOH 溶液的体积B . Ka(HA) 和Kb(BOH) 的数量级相等,均为10-6C . y点时,c(B+)=c(A-)=c(OH-)=c(H+)D . x、y、z 所示三点时水的电离程度:y>x=z6. (2分) (2016高一下·襄阳期中) 某锂电池的电池总反应为4Li+2SOCl2=4LiCl+S+SO2 ,下列有关说法正确的是()A . 锂电极作电池负极,放电过程中发生还原反应B . 1 mol SOCl2发生电极反应转移的电子数为4 molC . 电池的正极反应为2SOCl2+2e﹣=4Cl﹣+S+SO2D . 组装该电池必须在无水、无氧的条件下进行7. (2分)已知维生素A的结构简式可用如图所示键线式表示,有关它的叙述正确的是()A . 维生素A分子中含有一个苯环B . 维生素A不能使酸性KMnO4溶液褪色C . 维生素A能与金属钠反应产生H2D . 维生素A属于烯烃二、实验题 (共1题;共6分)8. (6分) (2018高三上·重庆月考) 某一化工厂以废铁屑为原料制备FeCl3溶液,用作印刷电路铜板腐蚀剂,并对溶液B进行电解处理的实验流程如图:(1)试剂a应选用________(填写名称);(2)步骤Ⅰ用到的主要玻璃仪器有漏斗、________(填写仪器名称);(3)写出步骤Ⅱ中主要反应的化学方程式________;(4)实验室制取气体E的离子方程式是________,欲对气体E进行干燥和吸收,需选用下列装置中的________(填写序号);(5)如何用化学方法检验气体E?________。
全国高考历年考题精选专题19 物质结构与性质(选修)-2021年高考化学试题分项版解析(解析版)

——碳及其化合物广泛存在于自然界中,回答下列问题:)碳有多种同素异形体,其中石墨烯与金刚石的晶体结构如图所示:石墨烯晶体)问中的晶体结构,石墨烯晶体相对简单,使用均分法即可得解。
金刚石晶体结构复杂,这里说明一下。
大家看一下晶体结构示意图(我找了一幅图并处理了一下)→→=Cl非金属性越强,电负性越大,则四种元素中电负性最大的是)氧元素有氧气和臭氧两种单质,由于的熔点高于的物质,均与CaF2中的化学试卷键为离子键,因此“低”)。
【正确答案】(1)bd(2)Al3++3CaF2= 3Ca2++AlF63-(3)角形或V形;sp3。
(4)172;低。
【解析】(1)a、Ca2+与F‾间既有静电引力作用,也有静电排斥作用,错误;b、离子所带电荷相同,F-的离子半径小于Cl-,所以CaF2晶体的晶格能大,则CaF2的熔点高于CaCl2,正确;c、晶体构型还与离子的大小有关,所以阴阳离子比为2:1的物质,不一定与CaF2晶体构型相同,错误;d、CaF2中的化学试卷键为离子键,CaF2在熔融状态下发生电离,因此CaF2在熔融状态下能导电,正确。
(2)CaF2难溶于[水],但可溶于含Al3+的溶液中,生成了AlF63-,所以离子方程式为:Al3++3CaF2=3Ca2++ AlF63-。
(3)OF2分子中O与2个F原子形成2个σ键,O原子还有2对孤对电子,所以O原子的杂化方式为sp3,空间构型为角形或V形。
(4)根据焓变的含义可得:242kJ·mol-1+3×159kJ·mol-1—6×E Cl—F =-313kJ·mol-1,解得Cl-F键的平均键能E Cl—F =172 kJ·mol-1;组成和结构相似的分子晶体,相对分子质量越大,范德华力越大,所以ClF3的熔、沸点比BrF3的低。
【考点定位】本题以CaF2为情景,考查了物质的结构、离子半径比较、离子方程式的书写、中心原子的杂化方式和分子的构型、键能的计算、熔点的比较。
黑龙江省2021年高三上学期理综-化学期末考试试卷(I)卷

黑龙江省2021年高三上学期理综-化学期末考试试卷(I)卷姓名:________ 班级:________ 成绩:________一、单选题 (共7题;共7分)1. (1分) (2018高一上·广安期末) 过滤后的食盐水仍含有可溶性的CaCl2、MgCl2、Na2SO4等杂质,通过如下几个实验步骤,可制得纯净的食盐水:①加入稍过量的Na2CO3溶液;②加入稍过量的NaOH溶液;③加入稍过量的BaCl2 溶液;④滴入稀盐酸至无气泡产生;⑤过滤正确的操作顺序()A . ①②③⑤④B . ③②①⑤④C . ②③①④⑤D . ③⑤②①④2. (1分) (2018高二上·林州期中) 4-乙烯基苯酚()常出现在肉香和海鲜香精的配方中,在其同分异构体中,含有苯环且能发生银镜反应的有()A . 3种B . 4种C . 5种D . 6种3. (1分) (2018高二上·丰台月考) 设阿伏伽德罗常数为NA ,则下列说法正确的是()A . 15g甲基(-CH3)所含有的电子数是10NAB . 常温常压下,4g氦气所含有的原子数目为NAC . 标准状况下,1L戊烷充分燃烧后生成的气态产物的分子数为(5/22.4)NAD . 常温常压下,1mol丙烷所含有的共价键数为12NA4. (1分) (2018高二上·承德期末) 下列实验装置(夹持装置略去)选择正确且能达到相应实验目的的是()A . 测定中和热B . 测定反应速率C . 实现化学能转化为电能D . 测定食醋浓度5. (1分) (2015高二下·揭阳期中) X、Y、Z、W是原子序数依次增大的四种短周期元素,甲、乙、丙、戊是由其中的两种或三种元素组成的化合物,丁是由Z元素形成的单质.已知:甲+丙→丁+己,甲+乙→戊+丁;25℃时0.01mol•L﹣1己溶液的pH为12.下列说法不正确的是()A . 1.0L0.1mol•L﹣1戊溶液中阴离子总的物质的量大于0.1molB . 将足量甲加入到酚酞试液中,溶液先变红后褪色C . X与W构成的化合物、戊、己均为离子化合物D . W的简单离子半径大于Z的简单离子半径6. (1分) (2018高二下·六安开学考) 如图所示,将铁棒和石墨棒插入盛有饱和NaCl溶液的U型管中。
2021年高考全国乙卷理综化学试题及参考答案
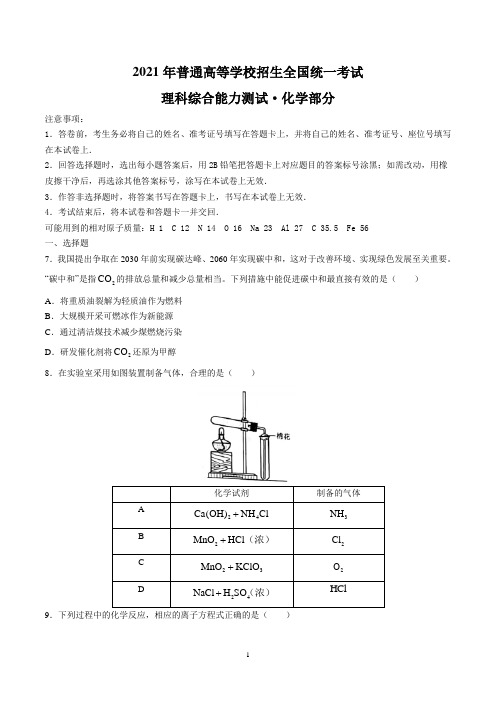
2021年普通高等学校招生全国统一考试理科综合能力测试·化学部分注意事项:1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上,并将自己的姓名、准考证号、座位号填写在本试卷上.2.回答选择题时,选出每小题答案后,用2B 铅笔把答题卡上对应题目的答案标号涂黑;如需改动,用橡皮擦干净后,再选涂其他答案标号,涂写在本试卷上无效.3.作答非选择题时,将答案书写在答题卡上,书写在本试卷上无效. 4.考试结束后,将本试卷和答题卡一并交回.可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Al 27 C 35.5 Fe 56 一、选择题7.我国提出争取在2030年前实现碳达峰、2060年实现碳中和,这对于改善环境、实现绿色发展至关重要。
“碳中和”是指2CO 的排放总量和减少总量相当。
下列措施中能促进碳中和最直接有效的是( ) A .将重质油裂解为轻质油作为燃料 B .大规模开采可燃冰作为新能源 C .通过清洁煤技术减少煤燃烧污染 D .研发催化剂将2CO 还原为甲醇8.在实验室采用如图装置制备气体,合理的是( )化学试剂制备的气体A 24Ca(OH)NH Cl + 3NHB 2MnO HCl +(浓) 2ClC 23MnO KClO + 2OD24NaCl H SO +(浓) HCl9.下列过程中的化学反应,相应的离子方程式正确的是( )A .用碳酸钠溶液处理水垢中的硫酸钙:223434CO CaSO CaCO SO --+=+ B .过量铁粉加入稀硝酸中:332Fe 4H NO Fe NO 2H O +-+++=+↑+C .硫酸铝溶液中滴加少量氢氧化钾溶液:322Al4OH AlO 2H O +--+=+D .氯化铜溶液中通入硫化氢:22Cu S CuS +-+=↓10.一种活性物质的结构简式为,下列有关该物质的叙述正确的是( )A .能发生取代反应,不能发生加成反应B .既是乙醇的同系物也是乙酸的同系物C .与互为同分异构体D .1mol 该物质与碳酸钠反应得244g CO11.我国嫦娥五号探测器带回1.731kg 的月球土壤,经分析发现其构成与地球土壤类似。
黑龙江省2021年高考化学试卷(新高考I)

黑龙江省2021年高考化学试卷(新高考I)姓名:________ 班级:________ 成绩:________一、选择题 (共10题;共20分)1. (2分) (2018高二下·浙江期中) 下列仪器可直接加热的是()A .B .C .D .2. (2分) (2016高一上·普宁期中) 下列生产、生活中的事例不属于氧化还原反应的是()A . 金属冶炼B . 燃放鞭炮C . 食物腐败D . 点制豆腐3. (2分) (2017高一下·赣州期中) 元素性质呈周期性变化的决定因素是()A . 元素原子核外电子层排布呈周期性变化B . 元素相对原子质量依次递增C . 元素原子半径大小呈周期性变化D . 元素的最高正化合价呈周期性变化4. (2分)最近,科学家研制是一种新的分子,它具有类似足球状结构,化学式为C60 ,下列说法正确的是()A . C60是一种新型化合物B . C60和金刚石都是碳的单质C . C60含离子键D . C60中含极性共价键5. (2分)现有烧杯、试管、量筒、带铁圈铁夹的铁架台、酒精灯、集气瓶、玻璃片、水槽、药匙、带导管的橡皮塞、天平,仅有这些仪器(所需化学药品可任选),不能完成的实验是()A . 制取氧气B . 制取二氧化碳C . 粗盐提纯D . 用氯化钠晶体配制100g 5%的氯化钠溶液6. (2分) (2016高二下·德州期中) 维生素C的结构简式为,丁香油酚的结构简式为:,下列关于两者的说法正确的是()A . 均含酯基B . 均含碳碳双键C . 均含醇羟基和酚羟基D . 均为芳香化合物7. (2分)下列物质中含有共价键的离子化合物是()A . CaF2B . KOHC . CO2D . CH48. (2分) (2019高一上·南山期中) 现有三组液体混合物:①乙醇与水②汽油与水③碘的水溶液,分离以上各混合液的正确方法依次是()A . 蒸馏、分液、萃取B . 萃取、蒸馏、分液C . 分液、蒸馏、萃取D . 蒸馏、萃取、分液9. (2分)(2018·三明模拟) 战国时《周礼》中记载沿海古人“煤饼烧蛎房成灰”(“蛎房”即牡蛎壳),并把这种灰称为“蜃”。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
黑龙江省2021年高考理综化学真题试卷(新课标Ⅰ)姓名:________ 班级:________ 成绩:________一、选择题 (共7题;共42分)1. (6分) (2018高二下·河口期中) 已知正四面体形分子E和直线型分子G反应,生成四面体形分子L和直线型分子M。
(组成E分子的元素的原子序数小于10,组成G分子的元素为第三周期的元素。
)如下图,则下列判断中正确的是()A . 常温常压下,L是一种液态有机物B . E中化学键是极性键C . G有漂白性D . 上述反应的类型是加成反应2. (6分) (2016高二下·海口期末) 丙烯醇(CH2=CH—CH2OH)可发生的化学反应有()①加成②氧化③酯化④加聚⑤取代A . 只有①②③B . 只有①②③④C . ①②③④⑤D . 只有①③④3. (6分) (2016高一上·长春期中) 下列分离或提纯物质的方法正确的是()A . 用蒸馏的方法制取蒸馏水B . 用过滤的方法除去NaCl溶液中含有的少量Na2SO4C . 用溶解、过滤的方法提纯含有少量BaSO4的BaCO3D . 用加热、蒸发的方法可以除去NaCl中CaCl2、MgCl2等杂质4. (6分) (2017高二上·南充期中) 有机物A和B分子中都有2个碳原子,室温下A为气体,B为液体.A 在催化剂作用下与水反应生成一种含氧化合物C,加氢还原C则生成B.则三种物质是()A . A是CH2=CH2 , B是CH3CHO,C是CH3CH2OHB . A是CH3CHO,B是CH2=CH2 , C是CH3CH2OHC . A是CH≡CH,B是CH3CH2OH,C是CH3CHOD . A是CH3CH2OH,B是CH3﹣CH3 , C是CH≡CH5. (6分) (2019高三上·吕梁期末) 已知A,B,D,E均为中学化学中的常见物质,它们之间的转化关系如图所示(部分产物略去),则下列有关物质的推断错误的是()A . 若A是铁,则E可能为稀硝酸B . 若A是CuO,E是碳,则B为COC . 若A是NaOH溶液,E是CO2 ,则B为NaHCO3D . 若A是AlCl3溶液,E可能是氨水6. (6分) (2015高二上·邢台月考) 下列有关原电池和金属腐蚀的说法错误的是()A . 普通锌锰干电池碳棒是负极,锌片是正极B . 盛水的铁器,在空气与水交界处更容易锈蚀C . 为防止金属的腐蚀可在金属表面涂油漆、油脂D . 用盐酸与锌反应制取氢气,含有杂质的锌比纯锌产生氢气速度快7. (6分)(2018·河西模拟) 常温下,向20mL0.lmol/LCH3COOH溶液中逐滴加入0.1mol/L的NaOH溶液,溶液中水电离出的c(OH-)在此滴定过程变化如下图所示,下列说法正确的是()A . a~e点,a点时水的电离受抑制最强B . b、d两点溶液的pH相同C . c点所示溶液中c(OH-)=c(CH3COOH)+c(H+)D . d点所示浴液中c(Na+)>c(CH3COOH)>c(CH3COO-)二、非选择题 (共3题;共43分)8. (14.0分) (2018高一上·惠州期末) 硫酸铜的制备实验是化学实验教学中一个必做实验,某学习小组设计了如下两个实验方案:(1)实验一:因铜不能与稀硫酸反应,实验中用铜和浓硫酸加热使之完全反应,将溶液通过蒸发、结晶等操作得到硫酸铜晶体。
根据上述实验和反应,比较浓硫酸与稀硫酸的性质,浓硫酸具有________。
(2)该反应的化学方程式为________。
(3)实验二:以空气为氧化剂的一步氧化法,将空气或氧气直接通入到铜粉与稀硫酸的混合物中,其反应原理为2Cu + O2 + 2H2SO4 = 2CuSO4 + 2H2O ,但反应速率太慢,当升高温度到80~90℃,反应仍然缓慢。
如在铜粉和稀硫酸的混合物中加入少量Fe2(SO4)3溶液,则速率明显加快。
Fe2(SO4)3的作用是________。
(4)得到的混合液可以用下列四种物质中的调节溶液的pH =2~4,使Fe3+ 形成Fe(OH)3沉淀而除去:A . NaOHB . CuOC . CuCO3D . Fe(5)请根据以上内容,对这两个实验方案进行评价,填下表:实验(一)实验(二)主要优点操作简便⑴原料充分转化为产品⑵没有有害气体排放主要缺点________________________________9. (15.0分) (2018高一下·宿迁期末) 近年来甲醇用途日益广泛,越来越引起商家的关注,工业上甲醇的合成途径多种多样。
现有实验室中模拟甲醇合成反应,在2 L密闭容器内,400 ℃时反应:CO(g)+2H2(g) CH3OH(g) △H<0,体系中n(CO)随时间的变化如表:时间(s)01235n(CO)(mol)0.0200.0110.0080.0070.007(1)上图中表示CH3OH的变化的曲线是________。
(2)用H2表示从0~2s内该反应的平均速率v(H2) =________。
(3)能说明该反应已达到平衡状态的是________。
a.v(CH3OH) =2v(H2)b.容器内压强保持不变c.2v逆(CO) = v正(H2)d.容器内密度保持不变(4)已知常温常压下1g液态甲醇燃烧生成CO2气体和液态水放出22.68kJ的热量,则该反应的热化学方程式为:________。
CH3OH与O2的反应可将化学能转化为电能,其工作原理如图所示,图中CH3OH从________(填A 或B)通入,b极的电极反应式是________。
10. (14.0分)(2018·哈尔滨模拟) 以高纯H2为燃料的质子交换膜燃料电池具有能量效率高、无污染等优点,但燃料中若混有CO将显著缩短电池寿命。
(1)以甲醇为原料制取高纯H2是重要研究方向。
甲醇水蒸气重整制氢主要发生以下两个反应:主反应:CH3OH(g)+H2O(g) CO2(g)+3H2(g) △H=+49 kJ•mol-1副反应:H2(g)+CO2(g) CO(g)+H2O(g) △H=+41 kJ•mol-1①甲醇在催化剂作用下裂解可得到H2和CO,则该反应的化学方程式为________,既能加快反应速率又能提高CH3OH平衡转化率的一种措施是________。
②分析适当增大水醇比(nH2O∶nCH3OH)对甲醇水蒸气重整制氢的好处________。
③某温度下,将nH2O∶nCH3OH =1∶1的原料气充入恒容密闭容器中,初始压强为p1,反应达到平衡时总压强为p2,则平衡时甲醇的转化率为________。
(忽略副反应)(2)工业常用CH4 与水蒸气在一定条件下来制取H2,其原理为:CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH=+203kJ·mol-1①该反应的逆反应速率表达式为; V逆=k·c(CO)·c3(H2),k为速率常数,在某温度下,测得实验数据如表:0.05C1 4.8c2C119.2c20.158.1由上述数据可得该温度下,上述反应的逆反应速率常数k 为________L3·mol-3·min-1。
②在体积为3L的密闭容器中通入物质的量均为3mol 的CH4和水蒸气,在一定条件下发生上述反应,测得平衡时H2的体积分数与温度及压强的关系如图所示,则压强Pl________P2(填“大于”或“小于”)温度T3________T4(填“大于”或“小于”);压强为P1时,在N点; v正________v逆(填“大于”或“小于”或“等于”)。
求N 点对应温度下该反应的平衡常数 K=________。
三、选考题 (共2题;共30分)11. (15.0分) (2018高二下·揭阳期末) 目前半导体生产展开了一场“铜芯片”革命——在硅芯片上用铜代替铝布线,古老的金属铜在现代科技应用上取得了突破,用黄铜矿(主要成分为CuFeS2)生产粗铜,其反应原理如下:(1)基态硫原子的外围电子排布式为________,硫元素与氧元素相比,第一电离能较大的元素是________(填元素符号)。
(2)反应①、②中均生成有相同的气体分子,该分子的中心原子杂化类型是________,其立体结构是________。
(3)某学生用硫酸铜溶液与氨水做了一组实验:CuSO4溶液蓝色沉淀沉淀溶解,得到深蓝色透明溶液,写出蓝色沉淀溶于氨水的离子方程式________;深蓝色透明溶液中的阳离子(不考虑H+)内存在的全部化学键类型有________。
(4)铜是第四周期最重要的过渡元素之一,其单质及化合物具有广泛用途,铜晶体中铜原子堆积模型为________;铜的某种氧化物晶胞结构如图所示,若该晶体的密度为d g/cm3,阿伏加德罗常数的值为NA,则该晶胞中铜原子与氧原子之间的距离为________pm(用含d和NA的式子表示)。
12. (15.0分) (2016高二下·襄阳期中) 回答下列问题(1)键线式表示的分子式为________;名称是________.中含有的官能团的名称为________.(2)戊基有________种结构,请写出其中的核磁共振氢谱有二个吸收峰的结构简式________.(3)糖类、油脂、蛋白质都是人体必需的营养物质:Ⅰ.下列物质中①葡萄糖②麦芽糖③蔗糖④纤维素⑤淀粉,互为同分异构体的是________;具有还原性,能发生银镜反应的是________.(填序号)Ⅱ.油脂在酸性环境下的水解产物为________(写名称).参考答案一、选择题 (共7题;共42分)1-1、2-1、3-1、4-1、5-1、6-1、7-1、二、非选择题 (共3题;共43分)8-1、8-2、8-3、8-4、8-5、9-1、9-2、9-3、9-4、10-1、10-2、三、选考题 (共2题;共30分) 11-1、11-2、11-3、11-4、12-1、12-2、12-3、。
