化工分离过程课后答案刘家祺
化学分离工程课后答案刘嘉琪

化学分离工程课后答案刘嘉琪1、关于前胡,说法正确的有(多选)()*A是伞形科前胡属植物(正确答案)B药理药效作用主要有祛痰、镇咳、平喘、抗炎、解痉、镇静等(正确答案)C可与皂荚、藜芦等药物一起放在药中煎煮D不溶乙醚等有机溶剂2、香豆素衍生物最常见的羟基取代位置是()[单选题] *AC7位(正确答案)BC5位CC3位DC6位3、所有游离香豆素均可溶于热的氢氧化钠水溶液,是由于其结构中存在()[单选题] * A异戊烯基B酮基C内酯环(正确答案)D酚羟基对位活泼氢4、牛蒡子属于()[单选题] *A香豆素类B木脂内酯(正确答案)C苯丙酸类D黄酮类5、临床用于上呼吸道抗菌消炎的是()[单选题] *A穿心莲内酯(正确答案)B青蒿素C莪术醇D薄荷脑6、E何首乌(正确答案)下列不含蒽醌类成分的中药是()* A丹参(正确答案)B决明子C芦荟D紫草(正确答案)7、具有暖脾胃、散风寒、通血脉作用的是()[单选题] * A穿心莲内酯B青蒿素C莪术醇D桂皮醛(正确答案)8、E与水任意比例相溶(正确答案)不耐热成分不宜采用的提取方法是()* A浸渍法B渗漉法C煮法(正确答案)D回流提取法(正确答案)9、挥发油可析出结晶的温度是()[单选题] *A0~-20℃(正确答案)B0~10℃C0~20℃D0~15℃10、羟基蒽醌类化合物中,大黄素型和茜草素型主要区别于()[单选题] * A羟基位置B羟基数目C羟基在不同苯环上的分布(正确答案)D羟基数目11、挥发油的溶解性难溶于()[单选题] *A水(正确答案)B乙醇C石油醚D乙醚12、二萜的异戊二烯单位有()[单选题] *A5个B6个C3个(正确答案)D4个13、由两个苯环通过三碳链相互连接成的具有6C-3C-6C基本骨架的一系列化合物是()[单选题] *A苷类B黄酮类(正确答案)C醌类D生物碱类14、纸色谱是分配色谱中的一种,它是以滤纸为(),以纸上所含的水分为固定相的分配色谱。
化工分离工程:第三章习题答案(刘家祺版)

第三章 多组分精馏和特殊精馏3-7.(P163) 在一精馏塔中分离苯(B),甲苯(T),二甲苯(X)和异丙苯(C)四元混合物。
进料量200mol/h ,进料组成z B =0.2,z T =0.3,z X =0.1,z C =0.4 (mol)。
塔顶采用全凝器,饱和液体回流。
相对挥发度数据为:BT α=2.25,TT α=1.0,XT α=0.33,CT α=0.21。
规定异丙苯在釜液中的回收率为99.8%,甲苯在馏出液中的回收率为99.5%。
求最少理论板数和全回流操作下的组分分配。
解:根据题意顶甲苯(T)为轻关键组分,异丙苯(C)为重关键组分, 则苯(B)为轻组分,二甲苯(X)为中间组分。
以重关键组分计算相对挥发度。
71.1021.025.2==BC α762.421.00.1==TC α 5714.121.033.0==XC α 1=CC α由分离要求计算关键组分在塔顶釜的分配。
h kmol W C /84.79998.04.0200=⨯⨯=hkmol D C /16.084.795.0200=-⨯=h kmol D T /7.59995.03.0200=⨯⨯= h kmol W T /3.07.593.0200=-⨯=所以37.7762.4lg 3.084.7916.07.59lg[lg ]lg[=⨯=⋅=TCTCCTm W W D D N α 由HH NmiH i i W D W D ⋅=α与ii i W D F +=求出非关键组分的分布苯: 437.7108.784.7916.071.10⨯=⨯=B B W D ∴B W =0,B D =200⨯0.2=40Kmol/h二甲苯:056.084.7916.05714.137.7=⨯=X X W D ,X D +X W =200⨯0.1=20求得X D =1.06,X W =18.94,。
化工分离过程课件陈洪钫,刘家祺编第一章绪论

1.2.2 速率分离过程
膜分离 热扩散
速率分离:
在某种推动力(浓度差、压 力差、温度差、电位差等)的 作用下,有时在选择性膜的 配合下,利用各组分扩散速 率的差异实现组分的分离。
微孔过滤(MF):
目的:溶液脱离子,气体脱离子
进料
颗粒、纤维
(液体和气体)
溶剂、水、 气体
推动力:压力差(~100kPa) 传递机理:筛分 膜类型:多孔膜
超滤(UF):
目的:溶液脱大分子,大分子溶液脱小分子,大 分子分级。
进料
胶体大分子
溶剂、水
推动力:压力差(100~1000kPa) 传递机理:筛分 膜类型:非对称性膜
反渗透(RO):
目的:溶剂脱溶质,含小分子溶质溶液浓缩。
进料
溶质、盐 溶剂、水
推动力:压力差(1000~10000kPa) 传递机理:优先吸附毛细管流动溶解、扩散模型 膜类型:非对称性膜或复合膜
本课程的任务和内容
■地位:专业基础课 ■前期课程:
物理化学、化工原理、化工热力学 ■重点: 1.基本概念的理解
2.讨论各种分离方法的特征 3.对设计、分析能力的训练 4.提高解决问题能力
一般化工生产过程:
煤
石油
化
天然气
工 原
反应
分离
产 品
生物物质
料
第一章 绪论
第一节 分离过程在化工生产中的重要性
(蒸汽压)化装置主
(MSA);有较大差 蒸塔顶产
加入热量 别
物中回收
L
(ESA)
乙烷及较
轻的烃。
萃
取
MSA
或 L或V 共
沸
精
馏
化工分离过程_课后答案

1. 计算在 0.1013MPa 和 378.47K 下苯(1)- 甲苯 (2)- 对二 甲苯 (3) 三元 系,当 x 1 =0.3125,x 2 =0.2978,x 3 =0.3897 时的 K 值。汽相为理想气体,液相为非 理想溶液。并与完全理想系的 K 值比较。已知三个二元系的 Wilson 方程参数。
8.314
378.47
=0.629 同理: 13 0.838
23 1.010
; 31 on 方程 ln i 1 ln ij x j
j
k
ki xk : kj x j
j
1 0.9184 ; 2 0.9718 ; 3 0.9930
组分 Kmol/h 9
N2
1.0
C1
54.4
C2
67.6
C3 141.1
C4
54.7
C5
56.0
C6
33.3
2
合计
2
习题6附图
2
塔顶产物 塔底产物
www.khd课后a答w案网.com
NVU = Nxu+Nau = 20 附加变量:总理论板数。
7. 附图为热藕合精馏系统,进料为三组分混合物,采出三个产品。确定该系统:
K1 2.0 4 8 ; K2 0.858 ; K3 0.377 解 2:在 T=378.47K 下
苯:
ln P1s 20.7936 2788.5 /(378.47 52.36) ; P1s =207.48Kpa
甲苯: ln P2s 20.9065 3096.52 /(378.47 53.67) ; P2s =86.93Kpa
相平衡组成关系式C个
1个平衡温度等式
1个平衡压力等式 共2C+3个
15春西交《化工分离过程》在线作业 答案

15春西交《化工分离过程》在线作业答案1.对于绝热闪蒸过程,当进料的流量组成及热状态给定之后,经自由度分析,只剩下一个自由度由闪蒸罐确定,则还应该确定的一个条件是任意选定其中之一。
3.当两个难挥发组分为关键组分时,则以塔釜往上为起点逐板计算。
4.下列关于吸附过程的描述中,不能分离液体混合物。
5.逆流填料吸收塔,当吸收因数A<1且填料为无穷高时,气液两相将在塔底达到平衡。
6.下列关于吸附剂的描述中,外表面积比内表面积大是不正确的。
7.吸附等温线是指不同温度下平衡吸附量与吸附质分压或浓度的关系曲线。
8.吸收操作中,若要提高关键组分的相对吸收率应采用增加液汽比的措施。
9.简单精馏塔是仅有一股进料且无侧线出料和中间换热设备的分离装置。
10.气液两相处于相平衡时,两相间各组分的逸度相等。
11.汽液相平衡K值越大,说明该组分越易挥发。
13.液相双分子吸附中,U型吸附是指在吸附过程中吸附剂始终优先吸附一个组分的曲线。
15.___提出了等价于化学位的物理量是蒸馏。
16.设计变量数就是指可调节的操作参数个数。
1.易于吸收组分是吸收中吸收因子大的组分,而非小的组分。
答案:错误。
2.∑Kixi>1说明计算的压力偏低,而非偏高。
答案:错误。
3.精馏塔的塔板上液相浓度越高,蒸汽相浓度越低,而非相反。
答案:正确。
4.超滤是通过膜的筛选作用将混合物进行分离的,而非溶解扩散作用。
答案:错误。
5.塔釜液溶剂浓度可以当作塔板上的溶剂浓度,因为溶剂浓度在再沸器中并不会发生骤降。
答案:错误。
6.分离因子可以用于判断任意一个过程分离的难易程度,答案:正确。
正确答案:B7.若要提高关键组分的相对吸收率,需要采用的措施并不是增加塔板数。
8.加大回流量并不能解决萃取塔塔顶产品不合格的问题。
9.并非所有有偏差的物系都是恒沸物系,因此这个说法是错误的。
10.膜分离是一种利用外界能量或化学位差作为推动力,通过天然或人工合成膜对混合物进行分离、提纯和富集的方法,因此这个说法是正确的。
大学化工分离工程教案第7章习题和解答

⼤学化⼯分离⼯程教案第7章习题和解答7.1.1 最⼩分离功分离的最⼩功表⽰了分离过程耗能的最低限。
最⼩分离功的⼤⼩标志着物质分离的难易程度,实际分离过程能耗应尽量接近最⼩功。
图 7-1 连续稳定分离系统由热⼒学第⼀定律:(7-1)和热⼒学第⼆定律(对于等温可逆过程):(7-2)得到等温下稳定流动的分离过程所需最⼩功的表达式:( 7-3 )即或表⽰为⾃由能的形式:( 7-4 )或表⽰为逸度的形式:( 7-7 )⼀、分离理想⽓体混合物对于理想⽓体混合物:(7-8)对于由混合物分离成纯组分的情况:( 7-9 )在等摩尔进料下,⽆因次最⼩功的最⼤值是 0.6931 。
对于分离产品不是纯组分的情况:过程的最⼩分离功等于原料分离成纯组分的最⼩分离功减去产品分离成纯组分所需的分离功。
[例7-1]⼆、分离低压下的液体混合物( 7-10 )对于⼆元液体混合物分离成纯组分液体产品的情况:( 7-11 )可见,除温度以外,最⼩功仅决定于进料组成和性质,活度系数⼤于 1 的混合物⽐活度系数⼩于 1 的混合物需较⼩的分离功。
当进料中两组分不互溶时,—W min,T =0 。
[例7-2][例7-3]7.1.2 ⾮等温分离和有效能当分离过程的产品温度和进料温度不同时,不能⽤⾃由能增量计算最⼩功,⽽应根据有效能来计算。
有效能定义:有效能是温度、压⼒和组成的函数。
稳态下的有效能平衡⽅程:( 7-18 )等当功:( 7-19 )系统的净功(总功):( 7-20 )过程可逆时,可得最⼩分离功:( 7-21a )该式表明,稳态过程最⼩分离功等于物流的有效能增量。
7.1.3 热⼒学效率和净功消耗分离过程的热⼒学效率:系统有效能的改变与过程所消耗的净功之⽐。
(7-22)普通精馏操作(图 7-2)过程所消耗的净功:图 7-2 普通精馏塔(7-23)实际分离过程,热⼒学效率必定⼩于 1 。
试求20 ℃、 101.3kPa 条件下,将 lkmol 含苯 44% (摩尔)的苯-甲苯溶液分离成纯组分产品所需的最⼩分离功。
化工分离过程课件陈洪钫,刘家祺编第四章多组分多级分离严格计算

MESH方程全塔的个 数:N(2C+3)!
二、变量分析
G1、UN
总变N 量 V:数
3 股进料 Q、Gj、U j
串级
NVN[( 3C+2) +3]-2+1N( 3C+9) -1
设计变N量 i N数 x+N : a
N x:
Na:串级单元数 1
进料 N(C + 2) 侧采单元数( 2 N-1)
压力 N
N-1级:AN-1xi,N-2 +BN-1xi,N-1+CN-1xi,N DN-1
N级:ANxi,N-1+BNxi,N DN
BA12
C1 B2
C2
xi,1 xi,2
D1 D2
Aj Bj Cj
xi, j
萃取精馏:被萃取组分在塔釜回收率高, 从釜计算。
共沸精馏:共沸物在塔顶能准确估计, 从顶开始
习题:
P148 2题
返回
第三节 三对角矩阵法
将MESH方程分成三组:
1.修正M方程 用三对角线矩阵求 表解 示 xi, ,j
2.S方程 求解 Tj;yi,j
3. H方程 求解V( j Lj)
适用于:
操作型计算
Newton-Raphson法:松弛法;等…
返回
第二节 逐板计算法
讨论:1.恒摩尔流
2.用相对挥发度或相平衡常数表示平衡关系
方法:交替使用操作线、平衡线方程
模型塔:
V1 L0 DxLK,D FL
ziF V
L
N -1
N
化工分离过程_课后参考答案 刘家祺
分离工程习题第一章 1. 列出5种使用ESA 和5种使用MSA 的分离操作。
答:属于ESA 分离操作的有精馏、萃取精馏、吸收蒸出、再沸蒸出、共沸精馏。
属于MSA 分离操作的有萃取精馏、液-液萃取、液-液萃取(双溶剂)、吸收、吸附。
5.海水的渗透压由下式近似计算:π=RTC/M,式中C 为溶解盐的浓度,g/cm 3;M 为离子状态的各种溶剂的平均分子量。
若从含盐0.035 g/cm 3的海水中制取纯水,M=31.5,操作温度为298K 。
问反渗透膜两侧的最小压差应为多少kPa?答:渗透压π=RTC/M=8.314×298×0.035/31.5=2.753kPa 。
所以反渗透膜两侧的最小压差应为2.753kPa 。
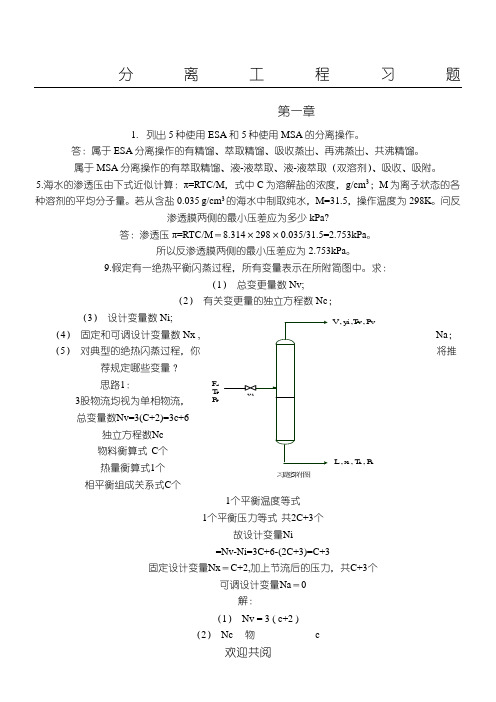
9.假定有一绝热平衡闪蒸过程,所有变量表示在所附简图中。
求:(1) 总变更量数Nv;(2) 有关变更量的独立方程数Nc ;(3) 设计变量数Ni; (4) 固定和可调设计变量数Nx , Na ; (5) 对典型的绝热闪蒸过程,你将推荐规定哪些变量? 思路1:3股物流均视为单相物流, 总变量数Nv=3(C+2)=3c+6独立方程数Nc 物料衡算式 C 个 热量衡算式1个 相平衡组成关系式C 个1个平衡温度等式 1个平衡压力等式 共2C+3个故设计变量Ni =Nv-Ni=3C+6-(2C+3)=C+3固定设计变量Nx =C+2,加上节流后的压力,共C+3个可调设计变量Na =0解:(1) Nv = 3 ( c+2 ) (2) Nc 物 cV -2F z iT F P FV , y i ,T v , P vL , x i , T L , P L习题5附图能 1 相 c 内在(P ,T) 2 Nc = 2c+3 (3) Ni = Nv – Nc = c+3 (4) Nxu = ( c+2 )+1 = c+3 (5) Nau = c+3 – ( c+3 ) = 0思路2:输出的两股物流看成是相平衡物流,所以总变量数Nv=2(C+2) 独立方程数Nc :物料衡算式 C 个 ,热量衡算式1个 ,共 C+1个设计变量数 Ni=Nv-Ni=2C+4-(C+1)=C+3固定设计变量Nx:有 C+2个加上节流后的压力共C+3个可调设计变量Na :有011.满足下列要求而设计再沸汽提塔见附图,求:(1) 设计变更量数是多少? (2) 如果有,请指出哪些附加变量需要规定?解: N x u 进料 c+2压力 9 c+11=7+11=18N a u 串级单元 1 传热 1 合计 2 N V U = N x u +N a u = 20附加变量:总理论板数。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
化工分离过程课后答案刘家祺文件编码(008-TTIG-UTITD-GKBTT-PUUTI-WYTUI-8256)分离工程习题第一章1.列出5种使用ESA和5种使用MSA的分离操作。
答:属于ESA分离操作的有精馏、萃取精馏、吸收蒸出、再沸蒸出、共沸精馏。
属于MSA分离操作的有萃取精馏、液-液萃取、液-液萃取(双溶剂)、吸收、吸附。
5.海水的渗透压由下式近似计算:π=RTC/M,式中C为溶解盐的浓度,g/cm3;M 为离子状态的各种溶剂的平均分子量。
若从含盐 g/cm3的海水中制取纯水,M=,操作温度为298K。
问反渗透膜两侧的最小压差应为多少kPa答:渗透压π=RTC/M=×298×=。
所以反渗透膜两侧的最小压差应为。
9.假定有一绝热平衡闪蒸过程,所有变量表示在所附简图中。
求:(1)总变更量数Nv;(2)有关变更量的独立方程数Nc;(3)设计变量数Ni;(4)固定和可调设计变量数Nx , Na;(5)对典型的绝热闪蒸过程,你将推荐规定哪些变量思路1:3股物流均视为单相物流,总变量数Nv=3(C+2)=3c+6F z iT FP FV , y i ,T v , P vL , x i , T L , P L习题5附图独立方程数Nc物料衡算式 C个热量衡算式1个相平衡组成关系式C个1个平衡温度等式1个平衡压力等式共2C+3个故设计变量Ni=Nv-Ni=3C+6-(2C+3)=C+3固定设计变量Nx=C+2,加上节流后的压力,共C+3个可调设计变量Na=0解:(1)Nv = 3 ( c+2 )(2)Nc 物 c能 1相 c内在(P,T) 2Nc = 2c+3(3)Ni = Nv – Nc = c+3(4)Nxu = ( c+2 )+1 = c+3(5)Nau = c+3 – ( c+3 ) = 0思路2:输出的两股物流看成是相平衡物流,所以总变量数Nv=2(C+2)独立方程数Nc:物料衡算式 C个,热量衡算式1个 ,共 C+1个设计变量数 Ni=Nv-Ni=2C+4-(C+1)=C+3固定设计变量Nx:有 C+2个加上节流后的压力共C+3个可调设计变量Na:有011.满足下列要求而设计再沸汽提塔见附图,求:(1)设计变更量数是多少(2)如果有,请指出哪些附加变量需要规定解: Nxu 进料 c+2压力 9c+11=7+11=18Nau 串级单元 1传热 1合计 2N V U = Nxu+Nau = 20附加变量:总理论板数。
16.采用单个精馏塔分离一个三组分混合物为三个产品(见附图),试问图中所注设计变量能否使问题有唯一解如果不,你认为还应规定哪个(些)设计变量解: NXU进料 c+2压力 40+1+1c+44 = 47N a u 3+1+1+2 = 7进料,顶产物底产物习题6附图N v u = 54设计变量:回流比,馏出液流率。
第二章4.一液体混合物的组成为:苯;甲苯;对二甲苯(摩尔分率)。
分别用平衡常数法和相对挥发度法计算该物系在100kPa 式的平衡温度和汽相组成。
假设为完全理想系。
解1:(1)平衡常数法: 设T=368K用安托尼公式得:kPa P s 24.1561= ;kPa P s 28.632= ;kPa P s 88.263= 由式(2-36)得:562.11=K ;633.02=K ;269.03=K781.01=y ;158.02=y ;067.03=y ;006.1=∑i y 由于∑i y >,表明所设温度偏高。
由题意知液相中含量最大的是苯,由式(2-62)得: 553.11'1==∑iy K K 可得K T 78.367'= 重复上述步骤:553.1'1=K ;6284.0'2=K ;2667.0'3=K 7765.0'1=y ;1511.0'2=y ;066675.0'3=y ;0003.1=∑i y 在温度为时,存在与之平衡的汽相,组成为:苯、甲苯、对二甲苯。
(2)用相对挥发度法:设温度为368K ,取对二甲苯为相对组分。
计算相对挥发度的: 5.807 13=α ; 2.353 23=α ;000.133=α解2:(1)平衡常数法。
假设为完全理想系。
设t=95℃苯: 96.11)36.5215.27395/(5.27887936.20ln 1=-+-=s P ; 甲苯: 06.11)67.5315.27395/(52.30969065.20ln 2=-+-=s P ; 对二甲苯:204.10)84.5715.27395/(65.33469891.20ln 3=-+-=s P ;569.11010569.15511=⨯==PP K s ;6358.022==PP K s选苯为参考组分:552.1011.1569.112==K ;解得T 2=℃05.11ln 2=s P ;Pa P s 4210281.6⨯= 19.10ln 3=s P ;Pa P s 43106654.2⨯=2K = 3K =故泡点温度为℃,且776.05.0552.11=⨯=y ;157.025.06281.02=⨯=y ;067.025.02665.03=⨯=y(2)相对挥发度法设t=95℃,同上求得1K =,2K =,3K =807.513=α,353.223=α,133=α故泡点温度为95℃,且776.074.35.0807.51=⨯=y ;157.074.325.0353.22=⨯=y ;067.074.325.013=⨯=y11.组成为60%(mol)苯,25%甲苯和15%对二甲苯的100kmol 液体混合物,在和100℃下闪蒸。
试计算液体和气体产物的量和组成。
假设该物系为理想溶液。
用安托尼方程计算蒸气压。
解:在373K 下苯: ()36.5251.27887936.20ln 1--=T P S kPa P S 315.1791= 甲苯: )67.5352.30969065.20ln 2--=T P S kPa P S 834.732= 对二甲苯:()84.5765.3346981.20ln 3--=T P S kPa P S 895.313= 计算混合组分的泡点T B T B = 计算混合组分的露点T D T D = 此时:x 1=,x 2=,x 3=,L=; y 1=,y 2=,y 3=,V=。
12.用图中所示系统冷却反应器出来的物料,并从较重烃中分离轻质气体。
计算离开闪蒸罐的蒸汽组成和流率。
从反应器出来的物料温度811K ,组成如下表。
闪蒸罐操作条件下各组分的K 值:氢-80;甲烷-10;苯;甲苯组分流率,mol/h解:以氢为1,甲烷为2,苯为3,甲苯为4。
总进料量为F=460kmol/h ,4348.01=z ,4348.02=z ,1087.03=z ,0217.04=z又K1=80,K2=10,K3=,K4= 由式(2-72)试差可得:Ψ=, 由式(2-68)计算得: y1=,y2=,y3=,y4=;V=h 。
14.在下,对组成为45%(摩尔)正己烷,25%正庚烷及30%正辛烷的混合物。
⑴求泡点和露点温度⑵将此混合物在下进行闪蒸,使进料的50%汽化。
求闪蒸温度,两相的组成。
解:⑴因为各组分都是烷烃,所以汽、液相均可看成理想溶液,K I 只取决于温度和压力,可使用烃类的P-T-K 图。
泡点温度计算得:T B =86℃。
露点温度计算得:T D =100℃。
⑵由式(2-76)求T 的初值为93℃,查图求K I所以闪蒸温度为93℃。
由式(2-77)、(2-68)计算得:x C6=,x C7=,x C8=y C6=,y C7=,y C8=所以液相中含正己烷%,正庚烷%,正辛烷%; 汽相中含正己烷%,正庚烷%,正辛烷%。
第三章12.在压力下氯仿(1)-甲醇(2)系统的NRTL 参数为: 12τ=mol ,12τ=mol ,12α=。
试确定共沸温度和共沸组成。
安托尼方程(S P :Pa ;T :K)氯仿:)(16.4679.26968660.20ln 1--=T P S甲醇:)(29.3455.36264803.23ln 2--=T P S 解:设T 为℃ 则)(16.4665.32679.26968660.20ln 1--=S P S P 1= S P 2=由)(ij ij ij G τα-=exp ,ij α=ji α)(121212exp τα-=G =)(9665.83.0exp ⨯-=)(212121exp τα-=G =)(8365.03.0exp ⨯= =⎥⎦⎤⎢⎣⎡+-⨯+⨯-+⨯--211221221]06788.01[06788.09665.8]2852.11[2852.18365.01x x x x x )()()()( =⎥⎦⎤⎢⎣⎡-+---21212193212.016086.02852.02852.13817.11)()()(x x x =⎥⎦⎤⎢⎣⎡-+⨯-++-⨯211211221]12852.1[2852.18365.006788.0106788.09665.8)()(x x x x x =⎥⎦⎤⎢⎣⎡--+-2121212852.02852.107507.193212.0104131.0)()(x x x 1ln γ-2ln γ=S S P P 21ln =6.645951.76990ln=求得1x = 1γ= 2γ==8971.06.6459568.02092.11.7699032.0⨯⨯+⨯⨯= 设T 为60℃则)(16.4615.33379.26968660.20ln 1--=S PS P 1= S P 2=1ln γ-2ln γ=S S P P 21ln =9.845999.95721ln= 设T 为56℃则)(16.4615.32979.26968660.20ln 1--=S PS P 1= S P 2=1ln γ-2ln γ=S S P P 21ln =3.717592.83815ln= 当1ln γ-2ln γ=时求得1x = 1γ= 2γ==9500.03.7175970.01099.12.8381530.0⨯⨯+⨯⨯= 某1、2两组分构成二元系,活度系数方程为221ln Ax =γ,212ln Ax =γ,端值常数与温度的关系:A=⨯ (T ,K)蒸汽压方程为T P S40500826.16ln 1-=T P S 40503526.16ln 2-= (P :kPa :T :K)假设汽相是理想气体,试问时①系统是否形成共沸物②共沸温度是多少 解:设T 为350K则A=⨯⨯35040500826.16ln 1-=S P ;∴SP 1= kPa35040503526.16ln 2-=S P ;SP 2= kPa因为在恒沸点由1221112==S SP P γγα得SS P P 1221=γγ解得:1x =2x =∴210513.03009.0ln ⨯=γ;1γ=229487.03009.0ln ⨯=γ;2γ=P=∑Si i i P x γ=⨯⨯⨯⨯75.99≠ kPa设T 为340K则A=⨯⨯34040500826.16ln 1-=SP ;SP 1= kPa34040503526.16ln 2-=S P ;SP 2= kPa由)(12121ln x A P P S S -=;)(1213434.08458.847695.64ln x -=解得:1x =2x ==∴211069.03434.0ln ⨯=γ;1γ=228931.03434.0ln ⨯=γ;2γ=P=∑Si i i P x γ=⨯⨯⨯⨯75.99≠ kPa设T 为352K则A=⨯⨯35240500826.16ln 1-=SP ;SP 1= kPa35240503526.16ln 2-=S P ;SP 2= kPa由)(12121ln x A P PS S -=;)(1212924.03473.1272143.97ln x -=∴1x =2x ==∴210383.02924.0ln ⨯=γ;1γ=229617.02924.0ln ⨯=γ;2γ=P=∑Si i i P x γ=⨯⨯⨯⨯75.99≈ kPa说明系统形成共沸物,其共沸温度为352K 。
