初中化学中的常见的酸的性质
中考化学考点常见酸的主要性质和用途

中考化学考点常见酸的主要性质和用途酸是化学中重要的一类物质,常见的酸有无机酸和有机酸,它们在日常生活和工业生产中都有广泛的应用。
下面将介绍一些常见酸的主要性质和用途。
1.硫酸(H2SO4):硫酸是常用的无机酸之一、它是一种无色、稠密的液体,具有强酸性,具有极强的腐蚀作用。
硫酸广泛用于电池、化肥、制药、纺织等行业。
此外,硫酸还用于水处理、金属清洗和催化反应等。
2.盐酸(HCl):盐酸是无机酸中最常见的一种。
盐酸是一种无色、具有刺激性气味的液体,具有强酸性。
盐酸广泛应用于金属清洗、水处理、酸洗和制备氯化物等。
3.硝酸(HNO3):硝酸是一种强氧化性的无机酸。
它通常是无色或黄色的液体,具有刺激性气味。
硝酸用于制造爆炸品、合成化合物和制造肥料。
此外,硝酸还用于金属清洗、催化剂和溶剂等。
4.醋酸(CH3COOH):醋酸是一种有机酸,也是最常见的有机酸之一、醋酸是无色、具有刺激性气味的液体。
醋酸主要用于食品加工、制药、染料和溶剂等。
5.氯化氢(HCl):氯化氢是无机酸之一、它是一种无色气体,具有刺激性气味和强酸性。
氯化氢主要用于金属清洗、水处理、合成氯化物和酸洗等。
6.磷酸(H3PO4):磷酸是一种无色液体,具有强酸性。
磷酸主要用于制药、农业和食品加工等。
磷酸也用于制备肥料和清洗金属等。
7.碳酸(H2CO3):碳酸是无色液体,具有中等酸性。
碳酸主要用于制备饮料、食品加工和药品制造等。
除了上述常见酸之外,还有许多酸是由特定物质产生的,如植物中的柠檬酸、苹果酸等。
这些酸主要用于食品加工、药物制造和化妆品等。
总的来说,酸有以下几个主要的性质和用途:1.酸具有酸味和酸性。
它可以与碱发生中和反应,产生相应的盐和水。
2.酸具有腐蚀性。
酸可以腐蚀金属和有机物,导致其破坏或腐蚀。
3.酸具有氧化性。
一些酸具有强氧化性,可以促使其他物质发生氧化反应。
酸在日常生活和工业生产中有广泛的应用,如:1.食品加工:醋酸用于制造醋和腌制食品,柠檬酸用于调味品和果汁的调味。
酸的性质和分类

酸的性质和分类酸是化学中常见的物质之一,它具有一些独特的性质和特点。
本文将详细介绍酸的性质和分类,并探讨它们在日常生活和工业中的重要应用。
一、酸的性质1.酸味和腐蚀性:酸通常呈酸味,且具有腐蚀性,可以腐蚀或侵蚀许多物质,如金属和皮肤等。
这是由于酸能够释放出氢离子(H+),与其他物质发生反应。
2.酸性溶液的导电性:酸性溶液中含有大量的离子,这些离子能够导电。
酸能够在水中产生杂质离子,如H+离子和对于它们有强烈吸引力的阴离子。
3.酸和金属的反应:酸能够与金属发生反应并产生氢气。
例如,硫酸可以与锌反应生成硫酸锌和氢气。
4.酸和碱的中和反应:酸可以与碱进行中和反应,产生盐和水。
这是因为酸中的氢离子与碱中的氢氧根离子(OH-)结合形成水。
二、酸的分类按照性质和来源的不同,酸可以分为以下几类:1.无机酸:无机酸是指由无机物质形成的酸,如硫酸(H2SO4)、盐酸(HCl)和硝酸(HNO3)等。
它们广泛应用于化肥、化学工业、冶金工业等领域。
2.有机酸:有机酸是指含有碳元素的酸,如乙酸(CH3COOH)、柠檬酸(C6H8O7)和醋酸(C2H4O2)等。
有机酸主要存在于植物和动物体内,并且在食品加工、医药和化妆品等行业有重要应用。
3.单质酸:单质酸是指由单质原子形成的酸,如二氧化碳(CO2)和一氧化碳(CO)等。
尽管它们不是典型的酸,但在某些条件下能够表现出酸性。
4.超强酸:超强酸是指具有极强酸性的酸。
它们通常是有机物质和无机物质的混合物,如三氟化硼(BF3·HF)和三氯化铁(FeCl3)等。
超强酸在有机合成和石油化工等领域具有重要作用。
三、酸的应用1.食品加工:柠檬酸和苹果酸等有机酸可以用作食品酸味剂和防腐剂,提供食物的酸味并延长其保鲜时间。
2.医药制造:许多药物的制造过程中需要使用酸来催化或调节反应,例如合成维生素C和抗生素等。
3.化学工业:酸在化学工业中具有广泛应用,其中硫酸是一种重要的原料,广泛用于生产肥料、玻璃、纺织品等。
酸的化学性质-九年级化学人教版下册

黄色溶液
滴加少量CuSO4溶液
相互交换成分 酸入水、沿器壁、勤搅拌
4、与碱反应,生成 和
口服含氢氧化铝的药物治疗胃酸过多。
4、与碱反应,生成 和
氢氧原子按2:1的个数比(H2O)脱去
2Fe O +6 H SO == 2Fe (SO ) + 6H O 2H2SO4 (浓) + C == CO2 ↑ + 2H2O + 2SO2 ↑
干冰
二氧化碳 CO2
草木灰
碳酸钾(主要成分)
K2CO3
写出镁与稀盐酸反应的化学方程式 A.
B.
(25)镁和稀硫酸:Mg+H2SO4 MgSO4+H2↑(固体逐渐溶解,有气泡产生)
置换反应
16.金刚石和石墨都是碳的单质,石墨在一定条件下可以转化为金刚石并需要吸收能量。已知12 g石墨或金刚石完全燃烧时放出的热
2.与活泼金属反应,生成 盐 和 氢气 钡会发生反应,氢氧化钡和碳酸钾会发生反应,碳酸钾和硫酸会发生反应,氧化钙和水会转化成氢氧化钙,氢氧化钙和二氧化碳会转
化成碳酸钙,碳酸钙高温会生成氧化钙,符合题意,故D正确。故选D。 答案:B
B
除去NaCl溶液中少量Na2CO3
适量澄清石灰水,过滤
【详解】A. 反应达到平衡状态时,正逆反应速率相等,4V正(O2)=5V逆(NO),说明消耗氧气的速率和生成氧气的速率相等,故A
酸的化学性质通性
1.与酸碱指示剂反应
【解析】A、盐酸和氢氧化钠会发生反应,氢氧化钠和碳酸钠不会发生反应,不符合题意,故A错误;B、盐酸和氢氧化钡会发生反应
,氢氧化钡和碳酸钠会发生反应,碳酸钠和盐酸会发生反应,过氧化氢会转化成水,水会转化成氧气,氧气不会转化成过氧化氢,不
初中化学人教第十单元 常见的酸和碱 知识点整理(全面,带答案)
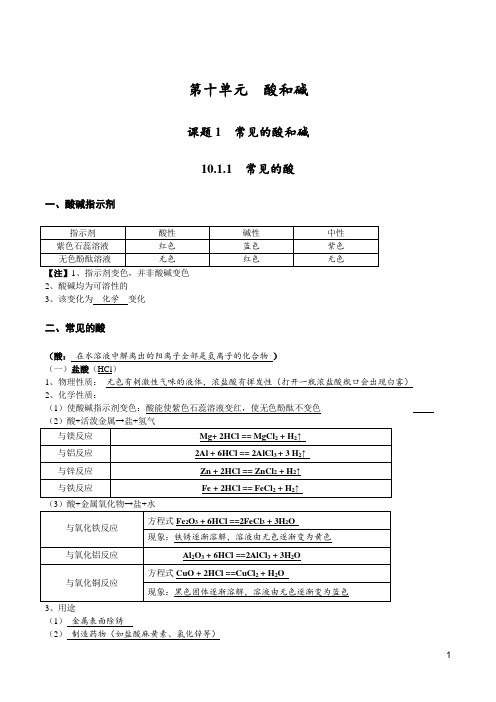
第十单元酸和碱课题1 常见的酸和碱10.1.1 常见的酸一、酸碱指示剂2、酸碱均为可溶性的3、该变化为化学变化二、常见的酸(酸:在水溶液中解离出的阳离子全部是氢离子的化合物)(一)盐酸(HCl)1、物理性质:无色有刺激性气味的液体,浓盐酸有挥发性(打开一瓶浓盐酸瓶口会出现白雾)2、化学性质:(1)使酸碱指示剂变色:酸能使紫色石蕊溶液变红,使无色酚酞不变色(1)金属表面除锈(2)制造药物(如盐酸麻黄素、氯化锌等)(3)人体胃液中的含有盐酸,可帮助消化(二)硫酸(H2SO4)1、浓硫酸(1)物理性质:无色粘稠油状液体,无气味,浓硫酸具有吸水性(2)化学性质:腐蚀性(3)浓硫酸的稀释:将浓硫酸沿着烧杯壁慢慢注入水中,并用玻璃棒不断搅拌(4)浓硫酸的事故处理:先用大量的水冲洗,再涂3%-5%的碳酸氢钠溶液。
2、稀硫酸的化学性质(1)使酸碱指示剂变色:酸能使紫色石蕊溶液变红,使无色酚酞不变色3、用途(1)用于生产化肥、农药、火药、燃料以及冶炼金属、精炼石油(2)金属除锈(3)汽车铅酸蓄电池中含有硫酸(4)浓硫酸在实验室常用作干燥剂三、酸的通性1、酸能与指示剂作用2、酸能与活泼金属反应3、酸能与金属氧化物反应4、酸能与碱反应5、酸能与盐反应注:酸溶液具有相似化学性质的原因:酸溶液中都含有H+四、复分解反应1、定义:两种化合物相互交换成分生成另外两种化合物的反应。
2、表达式:AB+CD=AD+CB3、反应前后各元素化合价不变(“变”或“不变”),属于基本反应类型。
4、10.1.2 常见的碱一、氢氧化钠(NaOH)1、俗称:烧碱、火碱、苛性钠2、物理性质:白色固体,易溶于水,溶解时放出大量的热。
3、化学性质(1)与酸碱指示剂反应:碱溶液能使紫色石蕊溶液变蓝,使无色酚酞变红、事故处理:先用大量的水冲洗,再涂上硼酸溶液5、制取:Ca(OH)2 + Na2CO3 == CaCO3↓+ 2NaOH (化学方程式)6、密封保存的原因:(1)NaOH固体容易吸收空气中的水分发生潮解。
常见的50种酸

常见的50种酸一、引言酸是一种普遍存在于我们生活中的物质,它可以被用于食品加工、化学实验、药品制造等领域。
本文将会介绍常见的50种酸,包括它们的化学性质、应用领域以及注意事项。
二、无机酸1. 硫酸硫酸是一种无色透明的液体,具有强烈的腐蚀性。
它在工业上被广泛应用于制造肥料、化学品和合成纤维等领域。
2. 盐酸盐酸是一种气味刺激的无色液体,具有强烈的腐蚀性。
它在工业上被广泛应用于金属清洗和电镀等领域。
3. 氢氟酸氢氟酸是一种无色液体,具有极强的腐蚀性和毒性。
它在工业上被广泛应用于玻璃刻蚀和半导体制造等领域。
4. 硝酸硝酸是一种无色透明的液体,具有强烈的氧化性和腐蚀性。
它在工业上被广泛应用于制造炸药、肥料和化学品等领域。
5. 磷酸磷酸是一种无色透明的液体,具有强烈的腐蚀性。
它在工业上被广泛应用于制造肥料、食品添加剂和清洗剂等领域。
6. 碳酸碳酸是一种白色粉末或结晶体,具有中等强度的腐蚀性。
它在工业上被广泛应用于制造玻璃、陶瓷和洗涤剂等领域。
7. 氢氧化钠氢氧化钠是一种白色固体,具有强烈的碱性。
它在工业上被广泛应用于制造肥皂、纸张和合成纤维等领域。
8. 氢氧化铝氢氧化铝是一种白色凝胶状固体,具有弱碱性。
它在工业上被广泛应用于制造陶瓷、电解铝和防火材料等领域。
9. 氯酸氯酸是一种无色液体,具有强烈的氧化性和腐蚀性。
它在工业上被广泛应用于制造漂白剂、消毒剂和清洗剂等领域。
10. 硫酸铜硫酸铜是一种蓝色晶体,具有强烈的氧化性和腐蚀性。
它在工业上被广泛应用于制造电池、催化剂和染料等领域。
三、有机酸11. 乙酸乙酸是一种无色液体,具有刺激性气味。
它在食品加工、药品制造和染料生产等领域被广泛应用。
12. 氨基乙酸氨基乙酸是一种无色透明的液体,具有中等强度的腐蚀性。
它在工业上被广泛应用于制造塑料、橡胶和染料等领域。
13. 丁二酸丁二酸是一种无色透明的液体,具有低毒性和低挥发性。
它在工业上被广泛应用于制造塑料、纤维和树脂等领域。
初中化学知识点归纳常见化合物的性质和用途

初中化学知识点归纳常见化合物的性质和用途化学是一门研究物质的性质、组成、结构以及转化过程的科学。
在初中化学学习中,我们学习了很多常见的化合物,并对它们的性质和用途进行了总结。
本文将围绕这一主题展开,分别介绍常见化合物的性质和用途。
一、酸(Acid)酸是常见的化合物之一,常见的酸有硫酸、盐酸、硝酸等。
具有以下性质和用途:1. 酸的性质:- 酸味酸涩;- 酸能与碱发生酸碱中和反应,产生盐和水;- 酸具有导电性。
2. 酸的用途:- 许多酸被用于工业生产,如硫酸用于制造肥料和纺织品;- 酸被广泛用于实验室中,用于分析和调节溶液的pH值。
二、碱(Base)碱是另一个常见的化合物,常见的碱有氢氧化钠、氢氧化钾等。
具有以下性质和用途:- 碱具有苦味;- 碱能与酸发生酸碱中和反应,产生盐和水;- 碱具有腐蚀性。
2. 碱的用途:- 许多碱被用于清洁剂和肥皂的制造;- 碱也常被用于调节溶液的pH值。
三、盐(Salt)盐是由酸和碱中和而成的化合物,在我们的日常生活中非常常见。
具有以下性质和用途:1. 盐的性质:- 盐的味道通常是咸的;- 盐可以导电。
2. 盐的用途:- 盐被用于调味料,提高食物的口感;- 盐在化工产业中被广泛用作原料。
四、水(Water)水是生命之源,也是最常见的一种化合物。
具有以下性质和用途:- 水是无色、无味的液体;- 水具有良好的流动性和溶解性;- 水具有很高的比热容,可以吸收和释放热量。
2. 水的用途:- 水是人类生活和工业生产的基本需求;- 水被用于灌溉农田、发电和制造产品。
五、氧化物(Oxide)氧化物是氧与其他元素形成的化合物,常见的氧化物有二氧化碳、氧化铁等。
具有以下性质和用途:1. 氧化物的性质:- 不同的氧化物具有不同的性质,有些是固体,有些是气体;- 氧化物可以与水反应,形成酸或碱。
2. 氧化物的用途:- 二氧化碳被用于制造饮料和激发消防器材;- 氧化铁被用于制造磁铁和染料。
总结:通过对常见化合物的性质和用途进行归纳,我们可以更好地理解化学知识。
常见酸的性质

解。
几乎所有的硫化物也都可被硝酸溶解,但应先加入盐酸,使硫以H2S的形式挥发出去,以免单质硫将试样裹包,影响分解。
③硫酸(H2SO4)除钙、锶、钡、铅外,其它金属的硫酸盐都溶于水。
热的浓硫酸具有很强的氧化性和脱水性,常用于分解铁、钴、镍等金属和铝、铍、锑、锰、钍、铀、钛等金属合金以及分解土壤等样品中的有机物等。
硫酸的沸点较高(338℃),当硝酸、盐酸、氢氟酸等低沸点酸的阴离子对测定有干扰时,常加硫酸并蒸发至冒白烟(SO3)来驱除。
硫酸能将物质里的H、O元素以2:1脱去。
④磷酸(H3PO4)磷酸根具有很强的配位能力,因此,几乎90%的矿石都能溶于磷酸。
包括许多其它酸不溶的铬铁矿、钛铁矿、铌铁矿、金红石等,对于含有高碳、高铬、高钨的合金也能很好的溶解。
单独使用磷酸溶解时,一般应控制在500~600℃、5min以内。
若温度过高、时间过长,会析出焦磷酸盐难溶物、生成聚硅磷酸粘结于器皿底部,同时也腐蚀了玻璃。
⑤高氯酸(HClO4)热的、浓高氯酸具有很强的氧化性,能迅速溶解钢铁和各种铝合金。
能将Cr、V、S等元素氧化成最高价态。
高氯酸的沸点为203℃,蒸发至冒烟时,可驱除低沸点的酸,残渣易性质:仅知存在于某些溶剂中。
很不稳定,45℃分解,很易快速分解为硫酸、硫、硫化氢、多硫化氢和二氧化硫(混合物)。
硫代硫酸可看成是硫酸分子中的一个氧原子被硫原子所代替的产物。
两个硫原子的平均氧化数为+2。
其中一个硫原子氧化数为+6,另一个硫原子氧化数为-2,因此硫代硫酸及其盐类具有一定的还原性。
硫代硫酸根酸离子在碱性条件下很稳定,有很强的络合能力。
硫代硫酸可在低温(-78℃)下,在乙醚等有机溶剂(-78℃)或无溶剂(10℃以下)中用干燥的氯化氢处理(酸化)无水硫代硫酸钠而得(不能在水溶液中!);或者在0℃和无水条件下,在乙醚中使三氯化硫与硫化氢反应而制得。
由于它很不稳定,故仅用其盐。
主要用作还原剂、定影剂和络合剂等。
对于初中生,只要求掌握盐酸、硝酸、硫酸的一些简单的化学性质,比如酸的通性:使紫色石蕊试液变红、能和碱生成盐和水、能和碱性氧化物生成盐和水。
酸的化学性质及方程式

酸的化学性质及方程式
能释放出质子的物质总称为酸,不同的酸溶液中含有相同的氢离子,所以酸具有相似的化学性质;有不同的化学性质是因为能电离出不同的酸根离子。
一、常见酸的化学性质有:
1.酸溶液能跟酸碱指示剂起反应,例如紫色石蕊试液遇酸变红。
2.酸能跟多种活泼金属起反应,通常生成盐和氢气,例如H2SO4 (稀)+Zn—ZnS04+H2。
3.酸能跟金属氧化物反应生成盐和水,6HCl+Fe2Q3
=2FeCl3+3H20。
4.酸能跟碱起中和反应生成盐和水,例如6HCl+Fe2Q3
=2FeCl3+3H20。
5.酸能跟盐反应生成新酸和新盐,例如Na2 SiO3 + 2
HCl=2NaCl+H2SiO3。
6.有些含氧酸易分解,一般生成酸性氧化物和水。
例如H2SO3—h2o+sO2。
二、酸的化学性质相关例题:
下列关于H2SO4H2SO4性质描述中,不属于酸的通性的是()
A.使紫色石蕊溶液变红
B.与NaOH发生中和反应
C.浓硫酸滴到白纸上使纸变黑
D.与 Mg反应放出氢气
答案:C
解析:各种酸溶液都显酸性,都能使紫色石蕊试液变红色,A不符合题意;各种酸均能与氢氧化钠溶液发生中和反应生成盐和水,B不符合题意;浓硫酸使白纸炭化变黑只有浓硫酸才具有,其他酸溶液无此性质,C符合题意;大部分稀酸的溶液能与活泼金属(如镁)发生置换反应生成盐和氢气,D不符合题意。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
初中化学中的常见的酸的性质酸(初中只要知道以下内容就可以了,一般的注意化学反应主要是置换和复分解反应的拓展,尤其是活学活用溶解性表或者是口诀)通性:
(1)跟指示剂反应紫色石蕊试液遇酸变红色无色酚酞试液遇酸不变色
(2)跟活泼金属(金属活动性顺序表中比氢强的金属)发生
置换反应
(3) 跟碱性氧化物反应酸+ 碱性氧化物→ 盐+水
(4)跟某些盐反应酸+ 盐→ 新酸+ 新盐
(5)跟碱发生中和反应酸+ 碱→ 盐+ 水(3、4、5为复分解反应)酸的PH<7常见的酸(只要知道盐酸和硫酸的性质,硝酸高中才要接触)
浓盐酸和浓硫酸的性质
(1)浓盐酸具有挥发性,打开盛有浓盐酸的试剂瓶,会观察到瓶口有白雾出现,这是由挥发出的氯化氢气体与空气中的水蒸气液化成小液滴的缘故。
(2)○1浓硫酸具有吸水性,故可作干燥剂,可以干燥H2、O2、CO2、CO等气体,但不可以干燥NH3、H2S等气体,因为硫酸可以与它们发生反应。
○2浓硫酸具有脱水性,能将纸张、木材、布料、皮肤等有机化合物中的氢、氧元素以水的组成比脱去而生成黑色的炭。
○3因浓硫酸具有强烈的腐蚀
性,如果不慎将浓硫酸沾在皮肤或衣服上,应立即用水冲洗,然后涂上3%-5%的碳酸氢钠溶液。
○4浓硫酸的稀释。
由于浓硫酸溶于水时放出大量的热,因而在稀释浓硫酸时,一定要把浓硫酸沿着器壁慢慢地注入水里,并不断搅动,使产生的热量迅速地扩散。
切不可把水倒进浓硫酸里。
2、几种常见的酸(1)盐酸(HCl)物理性质:无色液体,易挥发,有刺激性气味,在空气中形成白雾。
(盐酸越浓越易挥发)化学性质:○1跟指示剂的反应:使紫色石蕊试液变红;遇无色酚酞试液不变色。
○2跟金属反应:2HCl+Zn=ZnCl2+H2↑ ○3跟金属氧化物的反应:Fe2O3 +6HCl = 2FeCl3+ 3H2O○4跟碱反应:HCl + NaOH = NaCl + H2O○5跟某些盐的反应:HCl + AgNO3 = AgCl↓+ HNO3(2)硫酸(H2SO4)物理性质:无色液体,无挥发性,无气味,粘稠油状。
化学性质:
○1跟指示剂的反应:使紫色石蕊试液变红;遇无色酚酞试液不变色。
○2跟金属反应:H2SO4+Zn=ZnSO4+H2↑
○3跟金属氧化物的反应:Fe2O3+ 3H2SO4= Fe2(SO4)3 + 3H2O
○4跟碱反应:H2SO4 + Cu(OH)2=CuSO4+ 2H2O
○5跟某些盐的反应:H2SO4+ BaCl2=BaSO4↓+2HCl。
