微生物菌种使用记录
微生物实验用菌种管理规程(含表格)

微生物实验用菌种管理规程(ISO13485-2016/YYT0287-2017)1.0目的规范微生物学检定用菌种的管理,最大限度降低变异率,确保菌种的溯源性与稳定性,从而确保微生物学检验结果的准确可靠。
2.0适用范围适用于微生物实验用菌种管理,包括菌种的申购、传代、使用及销毁等。
3.0引用/参考文件ChP2015实用药品微生物检验检测技术指南4.0职责质量控制实验室负责菌种的申购、传代、使用、销毁等工作,QA负责监控和参与OOS调查。
5.0程序5.1术语和定义5.1.1标准菌株由中国药品生物制品检定所医学微生物菌种保藏管理中心或者其他经认可的机构提供的冷冻干燥菌。
5.1.2传代菌株用标准菌种制备的采用特定保存方法长期固定保存的菌种,用于传代及制备工作用菌种,3代后的传代菌株在需要时可以作为工作菌株使用。
5.1.3工作菌株用标准菌种或传代用菌种接种至普通琼脂斜面培养后,作为日常工作使用的菌种。
5.1.4菌种的代将菌种接种至一新鲜培养基上或培养基内,每萌发一次即称为一代,从菌种保藏中心获得的冷冻干燥菌种为第0代。
5.2菌种来源5.2.1标准菌株由中国药品生物制品检定所医学菌种保藏中心(CMCC)或者其他经认可的机构提供的冷冻干燥菌种。
5.2.2质量控制实验室涉及到的菌种种类、代码、保存方法及保存条件如下。
菌种名称菌种代码保存方法保存温度保存期限TSA斜面2~8℃1个月金黄色葡萄球菌CMCC(B)26003冷冻干燥管-20℃1年TSA斜面2~8℃1个月铜绿假单胞菌CMCC(B)10104冷冻干燥管-20℃1年TSA斜面2~8℃1个月枯草芽孢杆菌CMCC(B)63501冷冻干燥管-20℃1年SDA斜面2~8℃3个月白色念珠菌CMCC(F)98001冷冻干燥管-20℃1年SDA斜面2~8℃3个月黑曲霉菌CMCC(F)98003冷冻干燥管-20℃1年TSA斜面2~8℃1个月生孢梭菌CMCC(B)64941冷冻干燥管-20℃1年5.3菌种的申购、验收、保存5.3.1菌种的申购5.3.1.1微生物室QC依据菌种的库存及菌种的使用情况,提出采购申请,申请需明确菌种的名称,标准编号以及申购数量等信息。
菌种记录表格
操作人
数量
编号
有效期
保存
方法
数量
编号
有效期
保存
方法
分离与纯化过程
附表3:《检定菌种使用登记台账》
记录名称
检定菌种保存、领用登记台账
代码
页次
1
共1页
收到日期
名称及编号
数量
接收人
移交人
领用日期
用途
数量
发放人
领用人
附表4:《检定菌种观察记录》
记录名称
检定菌种观察记录
代码
页次
1
共1页
日期
冰箱温度(℃)
塞子是否松动
是否霉变
处理措施
观察人
附表5:《检定菌种鉴定记录》
记录名称
检定菌种鉴定记录
代码
页次
1
共1页
菌种名称及编号
鉴定原因
开始鉴定日期
鉴定人
复核人
年月日
鉴定项目
菌落形态
革兰染色
显微镜下形态
典型生化反应特征
鉴定结论
日期:年月日
附表6:《检定菌种使用登记台账》
记录名称
检定菌种使用登记台账
代码
页次
1
共1页
领用日期
名称及编号
数量
使用人
制备菌悬液浓度
(CFU/ml)
用于检验的
产品批号
记录名称
废弃菌种(物品)销毁处理记录
代码
页次
1
共1页
日期
被处理菌种(物品)名称
销毁原因
处理方式
批准人
操作人
监督人
备注:废弃菌种要标明编号、数量(支)
微 生 物 检 验 原 始 记 录
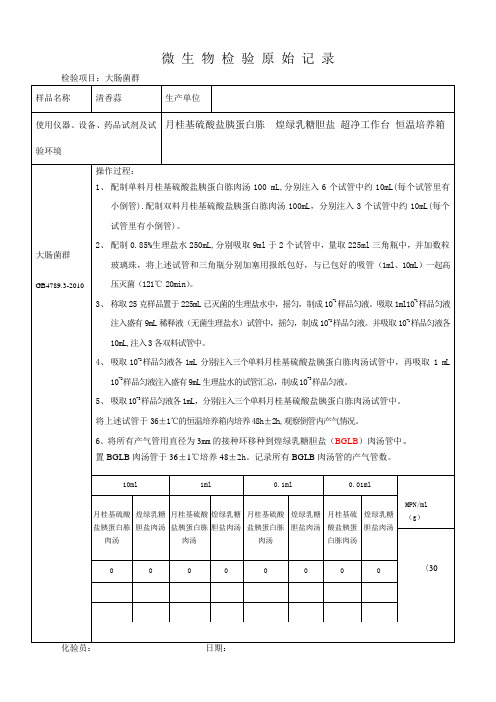
微生物检验原始记录检验项目:大肠菌群样品名称清香蒜生产单位使用仪器、设备、药品试剂及试验环境月桂基硫酸盐胰蛋白胨煌绿乳糖胆盐超净工作台恒温培养箱大肠菌群GB4789.3-2010操作过程:1、配制单料月桂基硫酸盐胰蛋白胨肉汤100 mL,分别注入6个试管中约10mL(每个试管里有小倒管).配制双料月桂基硫酸盐胰蛋白胨肉汤100mL,分别注入3个试管中约10mL(每个试管里有小倒管)。
2、配制0.85%生理盐水250mL,分别吸取9ml于2个试管中,量取225ml三角瓶中,并加数粒玻璃珠,将上述试管和三角瓶分别加塞用报纸包好,与已包好的吸管(1ml、10mL)一起高压灭菌(121℃ 20min)。
3、称取25克样品置于225mL已灭菌的生理盐水中,摇匀,制成10-1样品匀液。
吸取1ml10-1样品匀液注入盛有9mL稀释液(无菌生理盐水)试管中,摇匀,制成10-2样品匀液。
并吸取10-1样品匀液各10mL,注入3各双料试管中。
4、吸取10-2样品匀液各1mL分别注入三个单料月桂基硫酸盐胰蛋白胨肉汤试管中,再吸取1 mL10-2样品匀液注入盛有9mL生理盐水的试管汇总,制成10-3样品匀液。
5、吸取10-3样品匀液各1mL,分别注入三个单料月桂基硫酸盐胰蛋白胨肉汤试管中。
将上述试管于36±1℃的恒温培养箱内培养48h±2h,观察倒管内产气情况。
6、将所有产气管用直径为3mm的接种环移种到煌绿乳糖胆盐(BGLB)肉汤管中。
置BGLB肉汤管于36±1℃培养48±2h。
记录所有BGLB肉汤管的产气管数。
10ml 1ml 0.1ml 0.01ml月桂基硫酸盐胰蛋白胨肉汤煌绿乳糖胆盐肉汤月桂基硫酸盐胰蛋白胨肉汤煌绿乳糖胆盐肉汤月桂基硫酸盐胰蛋白胨肉汤煌绿乳糖胆盐肉汤月桂基硫酸盐胰蛋白胨肉汤煌绿乳糖胆盐肉汤MPN/ml(g)〈300 0 0 0 0 0 0 0化验员:日期:。
检定菌种领用、使用记录
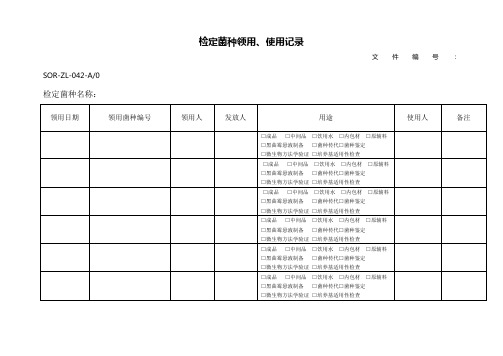
□成品 □中间品 □饮用水 □内包材 □原辅料
□黑曲霉悬液制备 □菌种传代□菌种鉴定
□微生物方法学验证 □培养基适用性检查
□微生物方法学验证 □培养基适用性检查
□成品 □中间品 □饮用水 □内包材 □原辅料
□黑曲霉悬液制备 □菌种传代□菌种鉴定
□微生物方法学验证 □培养基适用性检查
□成品 □中间品 □饮用水 □内包材 □原辅料
□黑曲霉悬液制备 □菌种传代□菌种鉴定
□微生物方法学验证 □培养基适用性检查
□成品 □中间品 □饮用水 □内包材 □原辅料
检定菌种领用、使用记录
文件编号:SOR-ZL-042-A/0
检定菌种名称:
领用日期
领用菌种编号
领用人
发放人
用途
使用人
备注
□成品 □中间品 □饮用水 □内包材 □原辅料 □黑曲霉悬液制备 □菌种传代□菌种鉴定 □微生物方法学验证 □培养基适用性检查
□成品 □中间品 □饮用水 □内包材 □原辅料
□黑曲霉悬液制备 □菌种传代□菌种鉴定
菌种管理记录模板

传代接种
接种
接种
培养基名称
代数
日期
支数
序列号
批号
操作者 保管者 使用日期 使用批号菌株功能试验销日期操作者购进日期
菌种名称
菌种管理记录
标准菌种来源
菌种批号
ATCC
购进菌种 数量 ( 支 )
代数
销毁日期
领用人
保管人
传代接种 日期
代数
纸片 纸片编号
支数
培养基名称
批号
贮存温 度
操作者
保管者
使用日期
使用者
复核者
销毁日期
接种 支数
接种序列 号
培养基名称
批号
操作者 保管者 使用日期 使用批号
菌株功能试验
销毁日期
操作者
菌种计数记录

(2)在预灌装的直径90mm□胰酪大豆胨琼脂培养基□沙氏葡萄糖琼脂培养基上均匀涂布,在℃培养下培养天进行计数。
(3)加入到装有硫乙醇酸盐流体培养基的试管中,在℃培养下培养天进行计数。
(2)在预灌装的直径90mm沙氏葡萄糖琼脂培养基上均匀涂布,在℃培养下培养天进行计数。
4.实验结果
菌悬液平板计数结果
培养温度/时间
℃年月日时分~年月日时分
稀释倍数
平皿号
10-4
10-5
10-6
10-7
10-8
1
2
3
4
平均
标准规定
□每1ml菌悬液中菌落数不大于100cfu.
□每1ml菌悬液中菌落数小于100cfu.
□
结果
cfu/ml
结果判定
□符合规定□不符合规定
检验人/日期: 复核人/日期:
3.2□接种黑曲霉至沙氏葡萄糖琼脂斜面培养基上,在℃培养天增菌培养,再取新鲜培养物操作;□直接取黑曲霉新鲜培养物,之后操作:
加入0.9%无菌氯化钠溶液ml,将孢子洗脱,用0.9%无菌氯化钠溶液将黑曲霉作稀释,每个稀释级取ml菌悬液,
(1)放入直径90mm的无菌玻璃平皿中,注入约ml℃的沙氏葡萄糖琼脂培养基,混匀凝固,在℃培养下培养天进行计数。
菌种名称
来 源
批 号
代 次
检验日期
年 月 日
判定日期
年 月 日
1.实验材料
硫乙醇酸盐流体培养基
批号:来源:胰酪大源自胨液体培养基批号:来源:
胰酪大豆胨琼脂培养基
批号:
检定菌灭活记录范文

检定菌灭活记录范文菌灭活是指通过使用物理或化学手段,成功地消灭细菌的过程。
检定菌灭活记录是指记录菌灭活的过程和结果,以确保菌灭活操作的有效性和可靠性。
以下是一份1200字以上的检定菌灭活记录样本:实验目的:本实验旨在检定菌灭活操作的有效性,以确保在实际应用中能够成功地灭活细菌。
实验材料:1.菌株:使用大肠杆菌作为实验对象。
2.配制好的菌液:使用LB培养基培养得到的大肠杆菌菌液。
3.菌灭活剂:使用酒精和紫外线作为菌灭活剂。
实验步骤:1.菌株培养:将大肠杆菌菌株接种到含有LB培养基的琼脂平板上,进行培养,使菌株生长至指定密度。
2.菌液配制:从琼脂平板上挑取菌落,转移到含有LB培养基的离心管中,经培养,使菌株生长至指定浓度。
在此过程中,严格控制培养条件,确保菌株的生长状态一致性。
3.菌液分装:将培养好的菌液分装到多个离心管中,使每个离心管中的菌液量保持一致。
4.菌灭活剂处理:a.酒精处理:将一部分分装好的菌液加入含有70%酒精的离心管中,轻轻摇匀。
b.紫外线处理:将另一部分分装好的菌液暴露于紫外线灯下,暴露时间为10分钟。
c.对照组:将剩余的菌液分装到离心管中,作为对照组。
5.菌液培养:将各组的菌液分别接种到含有LB培养基的琼脂平板上,进行培养,培养时间为24小时。
6.菌落计数:计算各组菌落的数量,以评估菌灭活效果。
实验结果:在菌液培养后,对照组的琼脂平板上出现了大量的菌落,菌落数较多。
而经过酒精处理的菌液所培养的琼脂平板上,菌落数量明显减少。
经紫外线处理的菌液所培养的琼脂平板上,几乎没有菌落生长。
讨论与结论:通过本实验的菌灭活操作,成功地使用酒精和紫外线灭活了大肠杆菌。
酒精处理能够有效地减少菌落的数量,但并不能完全灭活细菌。
而紫外线处理的菌液几乎没有出现菌落生长,表明紫外线对细菌有较好的灭活效果。
因此,在实际应用中,可以根据灭菌要求选择合适的菌灭活剂和操作方式,以确保菌液的安全性。
总结:菌灭活操作是一项重要的实验步骤,能够有效地减少菌落的数量,确保实验或应用中的细菌的安全性。
菌种记录表格
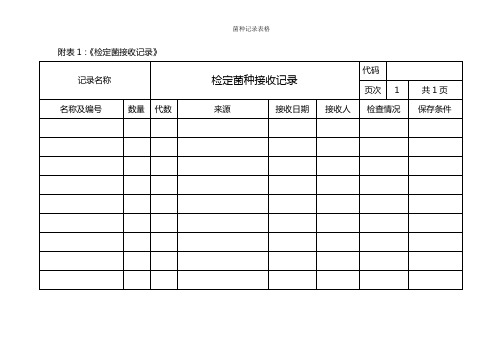
检定菌种使用登记台账
代码
页次
1
共1页
领用日期
名称及编号
数量
使用人
制备菌悬液浓度
(CFU/ml)
用于检验的
产品批号
记录名称废弃菌种(物品)销源自处理记录代码页次1
共1页
日期
被处理菌种(物品)名称
销毁原因
处理方式
批准人
操作人
监督人
备注:废弃菌种要标明编号、数量(支)
附表7:《废弃菌种(物品)销毁记录
传代用菌种
工作用菌种
操作人
数量
编号
有效期
保存
方法
数量
编号
有效期
保存
方法
分离与纯化过程
纯度
检查结果
操作人: 复核人:
附表3:《检定菌种使用登记台账》
记录名称
检定菌种保存、领用登记台账
代码
页次
1
共1页
收到日期
名称及编号
数量
接收人
移交人
领用日期
用途
数量
发放人
领用人
附表4:《检定菌种观察记录》
记录名称
检定菌种观察记录
附表1:《检定菌接收记录》
记录名称
检定菌种接收记录
代码
页次
1
共1页
名称及编号
数量
代数
来源
接收日期
接收人
检查情况
保存条件
附表2:《检定菌种传代、分离、保存记录》
记录名称
检定菌种传代、分离记录
代 码
页次
1
共1页
名称及编号
购进(领取)日期
年 月 日
来源
传代前菌种保存方法
