二肽基肽酶-4抑制剂类治疗药物
达格列净联合二甲双胍治疗肥胖2型糖尿病的临床效果

达格列净联合二甲双胍治疗肥胖2型糖尿病的临床效果1. 引言1.1 研究背景疲劳肥胖症是一种常见的慢性代谢性疾病,其主要病因包括饮食结构不均衡、缺乏运动以及遗传因素等。
在糖尿病患者中,肥胖症更是一个极为严重的问题,因为肥胖会进一步加重糖尿病患者的胰岛素抵抗和血糖控制困难,增加心血管疾病等并发症的风险。
如何有效地治疗肥胖2型糖尿病成为了临床医生和研究者们共同关注的焦点。
在当前的临床实践中,达格列净和二甲双胍被广泛应用于治疗2型糖尿病患者。
达格列净是一种新型的二肽基肽酶4抑制剂,可以通过抑制二肽基肽酶4的活性,延缓胰岛素素的降解,降低血糖水平。
而二甲双胍则是一种口服降糖药物,主要作用是减少肝葡萄糖生成,提高胰岛素敏感性,降低血糖水平。
本文旨在探讨达格列净联合二甲双胍治疗肥胖2型糖尿病的临床效果,为临床实践提供更多的参考和指导。
通过深入研究药物的药理作用、临床试验设计和结果、副作用及安全性以及长期治疗效果观察,我们希望可以为改善肥胖2型糖尿病患者的治疗效果提供更多的依据和支持。
1.2 研究目的"研究目的"部分的内容如下:本研究的目的是评估达格列净联合二甲双胍治疗肥胖2型糖尿病的临床效果,并探讨其可能的机制。
肥胖2型糖尿病是一种常见的代谢性疾病,临床治疗存在一定的挑战性,达格列净和二甲双胍作为常用的口服降糖药物,具有不同的药理作用,联合应用可能会产生协同效应,从而达到更好的治疗效果。
本研究旨在通过系统的临床试验设计和数据分析,评估达格列净联合二甲双胍对肥胖2型糖尿病患者的降糖和减重效果,探讨其对胰岛素抵抗、胰岛素分泌和脂肪代谢的影响,为临床医生提供更为全面的治疗建议。
通过本研究的结果,希望为肥胖2型糖尿病患者的个性化治疗提供依据,提高治疗效果和生活质量。
2. 正文2.1 达格列净联合二甲双胍的药理作用达格列净是一种二肽基肽酶-4(DPP-4)抑制剂,其作用机制是通过抑制DPP-4酶的活性,延长胰岛素释放肽-1(GLP-1)和胰高血糖素(GIP)在肠道内的降解,进而增加GLP-1和GIP在体内的浓度,促进胰岛素分泌和抑制胰高血糖素的释放,降低血糖水平,减少胰岛素阻力。
达格列净片的功能主治

达格列净片的功能主治1. 功能概述达格列净片是一种口服降糖药物,主要用于治疗2型糖尿病。
它属于二肽基肽酶-4(DPP-4)抑制剂类药物。
达格列净片通过抑制DPP-4酶的活性,能够增加胰岛素分泌和降低胰岛素分解,有效控制血糖水平。
2. 主治疾病达格列净片主要用于治疗2型糖尿病,以下是它的主要主治疾病:•2型糖尿病:达格列净片能够有效控制血糖水平,降低空腹血糖和餐后血糖,改善胰岛细胞功能,减少胰岛素抵抗,从而有效治疗2型糖尿病。
3. 使用方法达格列净片的使用方法如下:•用药剂型:达格列净片为口服药物,一般为片剂形式。
•剂量:根据医生的指导,每天口服1-2次。
常见剂量为100mg/日或50mg/日。
•用药时间:达格列净片可以在餐前、餐中或餐后口服,具体用药时间应根据医生的建议。
4. 注意事项在使用达格列净片时,需要注意以下事项:•孕妇和哺乳期妇女应在医生指导下使用。
•对达格列净片成分过敏者、儿童和青少年、严重肾功能不全患者应避免使用。
•在使用期间,应定期检测血糖水平以及肝功能和肾功能。
5. 不良反应达格列净片使用过程中可能出现一些不良反应,包括但不限于:•胃肠道反应:如恶心、呕吐、腹泻、胃痛等。
•上呼吸道感染:如鼻塞、咽痛、咳嗽等。
•血糖下降:在使用达格列净片后,出现血糖过低的症状,如头晕、出汗、心悸等。
•皮肤反应:如皮疹、瘙痒等。
6. 注意事项在使用达格列净片时,需注意以下几点:•严禁饮酒:饮酒会增加低血糖的风险,因此在使用达格列净片期间,应避免饮酒。
•避免重复用药:不要同时使用其他类似的降糖药物,以免增加药物的不良反应风险。
•按时用药:达格列净片需要持续使用才能有效控制血糖水平,应按照医生的指导,按时用药。
7. 结论达格列净片是一种有效治疗2型糖尿病的口服药物,通过抑制DPP-4酶的活性,能够增加胰岛素分泌和降低胰岛素分解,从而有效控制血糖水平。
在使用达格列净片时,需遵循医生的指导,注意剂量和用药时间,并定期检测血糖水平以及肝功能和肾功能,以确保安全有效地治疗2型糖尿病。
高效的DPP4抑制剂安立泽

✓
GLP-1 受体激动剂
✓
!
1、Pan C, et al. Curr Med Res Opin. 2009 Jan;25(1):39-45 2. Nathan DM, et al. Diabetologia. 2009;52:17-30. 3. Stumvoll M, et al. Lancet. 2005;365:1333-46.
• 为DPP-4的高选择性、可逆、具有口服活性 的竞争性抑制剂
• 口服用药后迅速、广泛吸收
• 沙格列汀的代谢主要由CYP3A4/5介导,主要 代谢产物也是DPP4抑制剂,其抑制活性作用 是沙格列汀的二分之一
• 沙格列汀和/或代谢产物经由肾脏(主要途径) 和肝脏途径清除
HO
H2N
N
O
CN
沙格列汀
• 5mg剂量的药效学特性支持每日一次给药,作 用时间长达24小时
肌肉
2型糖尿病的治疗药物与现状
▪ 70%的患者血糖控制未达标1 ▪ 不同降糖药物的作用靶点及副作用2,3
作用靶点
副作用
胰岛素 胰岛素抵抗 体重增加
分泌不足
低血糖症
胃肠道 副作用
胰岛素
✓
!
!
二甲双胍
✓
!
磺脲类药物
✓
!
!
格列奈类药物
✓
!
!
α-葡萄糖苷酶抑制剂
-
-
!
噻唑烷二酮类药物
✓
!
DPP-4 抑制剂
2013AACE糖尿病综合管理方案: DPP-4抑制剂为单药和联合治疗的首选药物之一
A1c<7.5%
生活方式调整
(包括采用医学手段辅助减肥)
A1c≥7.5%
DPP-4抑制剂类药物在2型糖尿病管理中的应用比较与选择

1 前言 2型糖尿病的特点是进展性的胰岛β细胞功能衰
减与胰岛素抵抗。纠正糖代谢失调的药物治疗重点
在于增强高血糖刺激下的胰岛素应答、增强胰岛素
敏感性或通过肠道或尿液改变葡萄糖清除途径。二
肽基肽酶-4(dipeptidyl peptidase-4,DPP-4)抑制剂 (或称作列汀类)能阻断胰高血糖素样肽-1(glucagonlik素分泌并抑制胰高血糖素分泌。此外,DPP-4 抑制剂可延迟胃排空、增强饱腹感、抑制摄食量,
外刊拾贝 Foreign Periodical Pickers
DPP-4抑制剂类药物在2型糖尿病管理中的应用比较与选择
卡西夫·穆尼尔、伊丽莎白·拉莫斯* 著,李艳娇1 译 1. 山西医科大学第二医院内分泌科,山西 太原 030001 [摘要] 二肽基肽酶-4(dipeptidyl-peptidase-4,DPP-4)抑制剂是糖尿病药物治疗领域的突破。目前国内已上市的5种DPP-4抑制剂,包括有西 格列汀、维格列汀、沙格列汀、利格列汀和阿格列汀。本文从疗效、安全性、特殊人群中的应用及降糖外作用等方面对此类药物进行阐 述和差异比较,对DPP-4抑制剂在临床的药物应用选择有重要的指导意义。在获得Expert Opinion on Pharmacotherapy杂志(Taylor & Francis Group)授权同意后,本文对2017年5月发表于该刊上的社论“DPP-4抑制剂类药物在2型糖尿病管理中的应用比较与选择”进行中文编译, 并特邀山东大学齐鲁医院内分泌科陈丽教授对文稿进行点评。 [关键词] 糖尿病;降糖药物;DPP-4抑制剂;差异 [中图分类号] R587.1 [文献标识码] A [文章编号] 1672-2809(2018)13-0009-05
译者简介:李艳娇,女,医学博士,副主任医师,现任中 华医学会糖尿病学分会青年委员。研究方向: 糖尿病微血管病变的基础与临床。电话:03513365522;E-mail:lyjfmpa9836@
二肽基肽酶Ⅳ抑制剂的作用机制与临床应用

二肽基肽酶Ⅳ抑制剂的作用机制与临床应用发布时间:2021-07-22T16:01:57.060Z 来源:《医师在线》2021年16期作者:张巧利通讯作者:刘霞[导读] 临床研究[1]显示,DPP-Ⅳ抑制剂对于 2 型糖尿病患者有着良好的降血糖效果,而且这一作用具有葡萄糖依赖性,因此引起低血糖事件发生的频率很低。
张巧利通讯作者:刘霞重庆市沙坪坝区人民医院?全科医学科重庆市 400000 二肽基肽酶Ⅳ(Dipeptidyl peptidase-Ⅳ, DPP-Ⅳ)抑制剂是一种较新的口服降糖药物。
临床研究[1]显示,DPP-Ⅳ抑制剂对于 2 型糖尿病患者有着良好的降血糖效果,而且这一作用具有葡萄糖依赖性,因此引起低血糖事件发生的频率很低。
同时其在与2型糖尿病发生、发展相关的病理、生理学方面可产生对人体有益的作用,尤其是在改善胰岛 β 细胞功能方面有着值得关注的潜能。
近年来,有更多的相关临床研究,可以更全面的认识DPP-Ⅳ抑制剂。
本文关注于DPP-Ⅳ抑制剂产生降糖作用的生物学机制,作用效果及使用的安全性作如下综述。
1 作用机制DPP-Ⅳ抑制剂主要通过抑制二肽基肽酶Ⅳ,延缓酶对内源性胰高血糖素肽-1(Glucagon like peptide-1, GLP-1)的降解,提高其浓度,延长其生物活性,以发挥降糖作用。
1.1 GLP-1的生物学效应 GLP-1是由肠L细胞产生的促胰岛素分泌肽,参与肠促胰岛素效应,膳食引起的高血糖促进肠GLP-1分泌,胰岛β细胞在此激素的刺激下胰岛素分泌增多。
1.1.1 GLP-1可促进胰岛素的分泌、合成 GLP-1参与葡萄糖依赖性的促进胰岛素分泌的效应,这一效应的强弱与血糖浓度呈正相关,随着血糖的增高,效应越强;反之,效应减弱。
当血糖下降至3.36mmol/L时,GLP-1刺激胰岛素分泌的作用甚至会消失。
因此,DPP-Ⅳ抑制剂,通过GLP-1降糖,可避免严重低血糖的发生。
GLP-1对于胰岛素的作用,不仅可增加其释放,还能促进其生物合成。
5种DPP-4抑制剂分子结构差异及药代动力学特性

5种DPP-4抑制剂分子结构差异及药代动力学特性李春杏;纪立伟【摘要】二肽基肽酶-4(Dipeptidyl peptidase-4,DPP-4)抑制剂是近年上市的治疗2型糖尿病的新型口服降糖药,其作用机制独特,以葡萄糖依赖性促进胰岛B细胞分泌胰岛素,同时抑制胰岛α细胞分泌胰高血糖素,可有效降低血糖,减少低血糖发作,同时不增加体重,被临床广泛应用.本文将对常见的5种DPP-4抑制剂的化学结构、亲和力、选择性差异、药代动力学特性及特殊人群用药逐项进行分析,因为尽管都是口服小分子化合物,但其化学结构、对DPP-4的亲和力、选择性、吸收、分布、代谢和排泄等药代动力学特性各异,以便为临床合理用药提供参考.【期刊名称】《药品评价》【年(卷),期】2019(016)008【总页数】8页(P3-9,16)【关键词】DPP-4抑制剂;化学结构;亲和力;选择性;药代动力学;肾功能不全;肝功能不全【作者】李春杏;纪立伟【作者单位】航天中心医院药剂科,北京 100049;北京医院药学部国家老年医学中心,北京 100730【正文语种】中文【中图分类】R587.1二肽基肽酶-4(DPP-4)也被称之为淋巴细胞表面蛋白CD26,与同源酶DPP-2、DPP-8、DPP-9和成纤维细胞活化蛋白(Fibroblast activation protein,FAP)统称为DPP家族,广泛分布于肝、肺、肾、小肠、淋巴细胞和内皮细胞等部位。
DPP-4是一种由766个氨基酸组成的跨膜丝氨酸蛋白酶,具有切割多肽N末端Xproline二肽的催化活性,可降解各种炎症趋化因子和肽类激素而发挥生物学效应。
DPP-4的主要底物有胰高血糖素样肽-1(Glucagonlike peptide 1, GLP-1)、葡萄糖依赖性胰岛素释放肽(Glucose-dependent insulinotropic polypeptide,GIP)、生长素、血管活性多肽及神经肽。
沙格列汀片saxagliptin用于治疗成人的2型糖尿病
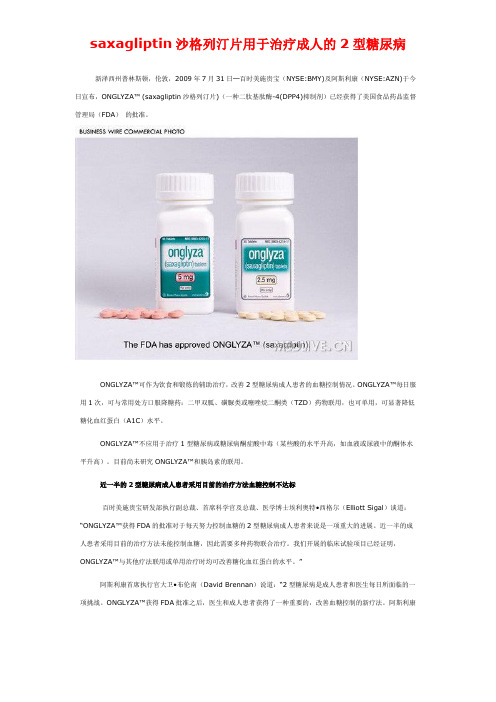
新泽西州普林斯顿,伦敦,2009年7月31日─百时美施贵宝(NYSE:BMY)及阿斯利康(NYSE:AZN)于今日宣布,ONGLYZA™ (saxagliptin沙格列汀片)(一种二肽基肽酶-4(DPP4)抑制剂)已经获得了美国食品药品监督管理局(FDA)的批准。
ONGLYZA™可作为饮食和锻炼的辅助治疗,改善2型糖尿病成人患者的血糖控制情况。
ONGLYZA™每日服用1次,可与常用处方口服降糖药:二甲双胍、磺脲类或噻唑烷二酮类(TZD)药物联用,也可单用,可显著降低糖化血红蛋白(A1C)水平。
ONGLYZA™不应用于治疗1型糖尿病或糖尿病酮症酸中毒(某些酸的水平升高,如血液或尿液中的酮体水平升高)。
目前尚未研究ONGLYZA™和胰岛素的联用。
近一半的2型糖尿病成人患者采用目前的治疗方法血糖控制不达标百时美施贵宝研发部执行副总裁、首席科学官及总裁、医学博士埃利奥特•西格尔(Elliott Sigal)谈道:“ONGLYZA™获得FDA的批准对于每天努力控制血糖的2型糖尿病成人患者来说是一项重大的进展。
近一半的成人患者采用目前的治疗方法未能控制血糖,因此需要多种药物联合治疗。
我们开展的临床试验项目已经证明,ONGLYZA™与其他疗法联用或单用治疗时均可改善糖化血红蛋白的水平。
”阿斯利康首席执行官大卫•布伦南(David Brennan)说道:“2型糖尿病是成人患者和医生每日所面临的一项挑战。
ONGLYZA™获得FDA批准之后,医生和成人患者获得了一种重要的,改善血糖控制的新疗法。
阿斯利康与百时美施贵宝之间开展了密切合作,以期进一步了解如何最好地治疗这种颇具挑战性的疾病,从而帮助成人患者达到治疗目标。
ONGLYZA™正是我们合作的成果。
”ONGLYZA™的获批基于一个临床开发项目,该项目包括约5000名受试者,其中4000多名使用了ONGLYZA™。
在控制饮食和锻炼基础上,该开发项目的组成包括:将ONGLY ZA™加用于其他口服降糖药(包括二甲双胍、磺脲类中的格列苯脲和TZDs)的研究;在初次接受治疗的成人糖尿病患者中,开始便联合使用二甲双胍和ONGLYZA™的研究;以及单药治疗研究。
磷酸西格列汀分子式

磷酸西格列汀分子式1. 简介磷酸西格列汀(Sitagliptin phosphate)是一种口服降糖药物,属于二肽基肽酶-4(DPP-4)抑制剂药物类别。
它通过抑制DPP-4酶的活性,增加胰岛素的分泌,并减少胰高血糖素(GLP-1)的降解,从而帮助调节血糖水平。
磷酸西格列汀的分子式为C16H15F6N5O·H3PO4,其化学结构如下所示:2. 化学性质磷酸西格列汀是一种白色结晶性粉末,无臭,微溶于水。
其化学性质主要包括以下几个方面:•溶解性:磷酸西格列汀在水中的溶解度较低,但在酸性条件下溶解度会增加。
•稳定性:磷酸西格列汀在常温下相对稳定,但在高温、光照和潮湿的条件下易分解。
•酸碱性:磷酸西格列汀是一种弱酸性物质,可以与碱反应生成相应的盐类。
•氧化性:磷酸西格列汀具有一定的氧化性,可以被氧化剂氧化。
3. 合成方法磷酸西格列汀的合成方法一般通过化学合成的方式进行。
以下是一种常用的合成方法:1.首先,将2,4,5-三氟苯甲酸与(2R)-(4-氨基-5-氰基-2-甲基-1-苯乙酰基)-1-苯乙酮反应,生成中间体1。
2.然后,中间体1与N-苯基-N-(1S)-2-氰基-1-苯乙酰胺反应,生成中间体2。
3.接着,中间体2经过合适的处理,生成磷酸西格列汀。
这种合成方法经过多步反应,需要一系列的试剂和条件,但是可以高效地得到纯度较高的磷酸西格列汀。
4. 药理作用磷酸西格列汀主要通过抑制DPP-4酶的活性来发挥药理作用。
DPP-4酶是一种消化酶,它可以降解肽类激素胰高血糖素(GLP-1)和胰岛素释放肽(GIP)。
这两种激素在血糖调节中起到重要的作用,能够增加胰岛素的分泌、抑制胰高血糖素的分泌,并减缓胃肠道的蠕动,从而延长餐后血糖的降低。
磷酸西格列汀能够选择性地抑制DPP-4酶的活性,从而减少GLP-1和GIP的降解,增加它们的半衰期,使其在血液中的浓度增加。
这样一来,GLP-1和GIP能够更好地发挥其调节血糖的作用,从而降低血糖水平。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
编者按/Editorial Journal of Diabetes 9 (2017) 5-7 二肽基肽酶-4抑制剂类治疗药物Dipeptidyl peptidase-4 inhibitor approachesZachary BloomgardenIcahn School of Medicine at Mount Sinai在过去的四十年时间里全世界范围内的糖尿病患者数量已经翻了四番1,国际糖尿病联合会预计全世界成年糖尿病患者的数量将从2015年的4.15亿增加到2040年的6.42亿2。
虽然超过几十年的随访结果已经证实了糖尿病确实就是心血管(cardiovascular,CV)风险的等位症,这个诊断可使患者的死亡率风险急剧上升,与有心肌梗死(myocardial infarction,MI)或者中风病史相似3,4,因此可以得出如下推论,那就是对糖尿病的基本特征(高血糖)进行适当治疗可降低CV风险,为什么会如此推论呢?在包括数十年扩展观察的研究中,基线时没有CV疾病的糖尿病患者必定会有这样的获益,无论是糖尿病前期5、2型糖尿病6还是1型糖尿病患者7。
然而,在基线时就有高CV风险或者潜在CVD的糖尿病患者,观察超过2-5年后,一般来说都不能够证实降糖干预措施具有CV获益8,虽然最近的研究表明确实有一些降糖药物可能与非血糖方面的CV获益有关9。
寻求安全且有效的治疗方法的必要性不能够被过度夸大,我们意识到应该进行在CV并发症发生前的数十年里就开始治疗的长期研究。
随着二肽基肽酶-4抑制剂(dipeptidyl peptidase-4 inhibitors,DPP-4i)使用的日益增多10,在众多的治疗药物中考虑这类药物适合哪些患者非常重要。
在对高CV风险患者进行的研究中,无论是随访时间中位数超过1.5年的阿格列汀研究11、超过2.1年的沙格列汀研究12、还是超过3.0年的西格列汀研究13,都没有发现DPP-4i与复合CV结果风险增加或者减少之间具有相关性,包括CV死亡、非致死性MI以及非致死性中风。
根据这些试验结果发现了一个问题,那就是发生充血性心力衰竭(congestive heart failure,CHF)的风险可能增加,在沙格列汀试验中具有显著性意义,特别是在具有最高CV风险的患者中14,但是在阿格列汀15与西格列汀16试验中都没有影响。
此外,一项meta分析结果显示在低CV风险人群中这些事件并没有增加17。
基于人群的研究结果也显示CHF的风险没有增加。
在一项纳入了1499650名来自几个大型队列研究的糖尿病患者的回顾性分析中18,使用基于肠促胰岛素药物与联用其他口服降糖药物相比,因心脏衰竭住院的风险并没有增加,这与几项针对合并或者不合并CHF病史的患者服用DPP-4i或者使用胰高血糖素样肽-1(glucagon-like peptide-1,GLP-1)受体激动剂治疗后的单独分析结果一致,并且在23205名基于肠促胰岛素治疗的患者与435777名没有CHF病史的对照组患者中这些事件还有略有减少的趋势(危险比为0.82;95%置信区间为0.67-1.00),虽然该研究并没有针对不同的药物进行单独分析。
在另一项纳入218556名患者的比较DPP-4i与磺脲类(SUs)药物的研究中,以及纳入了112888名患者的比较沙格列汀与西格列汀的研究中19;在既往有CV病史的患者中没有发现DPP-4i与CHF住院之间具有相关性,与使用SU治疗的患者相比,没有CV病史且使用DPP-4i治疗的患者因CHF住院的危险比要低41%。
在一项类似的基于人群的研究中,纳入了78553名沙格列汀使用者与298124名西格列汀使用者,除此之外还有144266名吡咯列酮(PGZ)使用者、432351名SU使用者以及247863名长效胰岛素使用者,与使用PGZ或胰岛素的患者相比,使用沙格列汀治疗的患者匹配后的CHF住院倾向风险评分更低,并且与使用SU、PGZ或者胰岛素的患者相比,使用西格列汀治疗的患者评分也更低20;与使用西格列汀治疗的患者相比,使用沙格列汀治疗的患者匹配后的CHF住院倾向风险评分没有增加。
从这些观察结果中衍生出了一个重要的问题,那就是我们是否还能够继续照常使用SUs21,而担心DPP-4i可导致不良CV结果是毫无根据的。
最近有两项调查DPP-4i长期降糖作用的观察性研究。
这个重要的话题很少有人关注。
来自美国医疗保健研究与质量局的疗效对照研究结果表明,只有17%与4%的试验分别在超过1年与2年的时间中比较了成年2型糖尿病患者的治疗效果22。
在一项接受两种药物联合治疗的分析中,有624名糖尿病患者使用西格列汀联合SU、PGZ或二甲双胍进行治疗,与620名只使用后3种药物中的2种等量药物进行联合治疗的患者相比,5年后发现接受包含西格列汀治疗的患者的HbA1c水平要更低一些23。
在一项纳入了1178名糖尿病患者的研究中,他们一开始就处方西格列汀与二甲双胍进行联合治疗,治疗有应答的定义为HbA1c至少下降了0.8%或HbA1c达到了≤7.0%24。
然而,在第1年与第4年分别只有72.2%与35.4%的患者有应答,这意味着除了使用西格列汀还需要升级治疗方案。
该研究还考察了DPP-4i与多种药物联合治疗的效果。
基线HbA1c水平较低的患者联合使用DPP-4i 与钠-葡萄糖共转运体2抑制剂进行治疗可能获益更多25,26。
联合使用DPP-4i与基础胰岛素似乎不但合理而且有效,而基础胰岛素通常是与二甲双胍联用的。
在一项纳入658名患者并且使用了达标治疗方法的研究中,发现与单独使用基础胰岛素治疗的患者相比,无论是联用还是不联用二甲双胍,同时使用西格列汀与甘精胰岛素进行治疗的患者的HbA1c下降得更为显著,而且每日胰岛素剂量也更低,低血糖的发生率也下降了27。
在一项950名使用胰岛素与二甲双胍治疗的糖尿病患者随机联用利拉利汀或安慰剂进行治疗的研究中28,以及一项140名2型糖尿病患者使用胰岛素进行治疗的研究中29,以及另一项比较甘精胰岛素联用西格列汀与预混门冬胰岛素30治疗的研究中30都能够观察到相似的研究结果。
为了使2型糖尿病患者的血糖能够得到控制需要不断地调整治疗方案,将来,我们期望能够制定出一个长期的治疗策略,试验的目的是寻求可以在减少CV同时还能减少微血管终点的最佳治疗方法。
参考文献:1. NCD Risk Factor Collaboration (NCD-RisC). Worldwide trends in diabetes since 1980: A pooled analysis of 751 population-based studies with 4.4 million participants. Lancet. 2016; 387: 1513–30.2. International Diabetes Federation (IDF). IDF Diabetes,7th edn. Brussels, Belgium: International Diabetes Federation, 2015. Available from , accessed 5 July 2016.3. Haffner SM, Lehto S, Rönemaa T, PyöräläK, Laakso M. Mortality from coronary heart disease in subjects with type 2 diabetes and in nondiabetic subjects with and without prior myocardial infarction. N. Engl. J. Med. 1998; 339: 229–34.4. The Emerging Risk Factors Collaboration. Association of cardiometabolic multimorbidity with mortality. JAMA. 2015; 314: 52–60.5. Li G, Zhang P, Wang J et al. Cardiovascular mortality, all-cause mortality, and diabetes incidence after lifestyle intervention for people with impaired glucose tolerance in the Da Qing Diabetes Prevention Study: A 23-year follow-up study. Lancet Diabetes Endocrinol. 2014; 2: 474–80.6. Holman RR, Paul SK, Bethel MA, Matthews DR, Neil HA. 10-year follow-up of intensive glucose control in type 2 diabetes. N. Engl. J. Med. 2008; 359: 1577–89.7. Diabetes Control and Complications Trial (DCCT)/Epidemiology of Diabetes Interventions and Complications (EDIC) Study Research Group. Intensive diabetes treatment and cardiovascular outcomes in type 1 diabetes: The DCCT/EDIC study 30-year follow-up. Diabetes Care. 2016; 39: 686–93.8. Bloomgarden ZT. Glycemic control in diabetes: A tale of three studies. Diabetes Care. 2008; 31: 1913–9.9. Bloomgarden Z. Glycemic control and the heart: It matters how you get there. J. Diabetes. 2016; 8: 453–4.10. Hampp C, Borders-Hemphill V, Moeny DG, Wysowski DK. Use of antidiabetic drugs in the U.S., 2003–2012. Diabetes Care. 2014; 37: 1367–74.11. White WB, Cannon CP, Heller SR et al. Alogliptin after acute coronary syndrome in patients with type 2 diabetes. N. Engl. J. Med. 2013; 369: 1327–35.12. Scirica BM, Bhatt DL, Braunwald E et al. Saxagliptin and cardiovascular outcomes in patients with type 2 diabetes mellitus. N. Engl. J. Med. 2013; 369: 1317–26.13. Green JB, Bethel MA, Armstrong PW et al. Effect of sitagliptin on cardiovascular outcomes in type 2 diabetes. N. Engl. J. Med. 2015; 373: 232–42.14. Scirica BM, Braunwald E, Raz I et al. Heart failure, saxagliptin, and diabetes mellitus: Observations from the SAVOR-TIMI 53 randomized trial. Circulation. 2014; 130: 1579–88.15. Zannad F, Cannon CP, Cushman WC et al. Heart failure and mortality outcomes in patients with type 2 diabetes taking alogliptin versus placebo in EXAMINE: A multicentre, randomised, double-blind trial. Lancet. 2015; 385: 2067–76.16. McGuire DK, Van de Werf F, Armstrong PW et al. Association between sitagliptin use and heart failure hospitalization and related outcomes in type 2 diabetes mellitus: Secondary analysis of a randomized clinical trial. JAMA Cardiol. 2016; 1: 126–35.17. Kongwatcharapong J, Dilokthornsakul P, Nathisuwan S, Phrommintikul A, Chaiyakunapruk N. Effect of dipeptidyl peptidase-4 inhibitors on heart failure: A meta-analysis of randomized clinical trials. Int. J. Cardiol. 2016; 211: 88–95.18. Filion KB, Azoulay L, Platt RW et al. A multicenter observational study of incretin-based drugs and heart failure. N. Engl. J. Med. 2016; 374: 1145–54.19. Fu AZ, Johnston SS, Ghannam A et al. Association between hospitalization for heart failure and dipeptidyl peptidase 4 inhibitors in patients with type 2 diabetes: An observational study. Diabetes Care. 2016; 39: 726–34.20. Toh S, Hampp C, Reichman ME et al. Risk for hospitalized heart failure among new users of saxagliptin, sitagliptin, and other antihyperglycemic drugs: A retrospective cohort study. Ann. Intern. Med. 2016; 164: 705–14.21. Bloomgarden Z. Recent cardiovascular trials: What are the drivers of benefit and adverse effect? J. Diabetes. 2009; 1: 227–9.22. Bolen S, Tseng E, Hutfless S, et al. Diabetes Medications for Adults with Type 2 Diabetes: An Update. Comparative Effectiveness Reviews, No. 173. Report No. 16-EHC013-EF. Rockville (MD): Agency for Healthcare Research and Quality (US); 2016.23. Derosa G, D'Angelo A, Maffioli P. Sitagliptin in type 2 diabetes mellitus: Efficacy after five years of therapy. Pharmacol. Res. 2015; 100: 127–34.24. Ku EJ, Jung KY, Kim YJ et al. Four-year durability of initial combination therapy with sitagliptin and metformin in patients with type 2 diabetes in clinical practice; COSMIC Study. PLoS One. 2015; 10: .e012947725. Rosenstock J, Hansen L, Zee P et al. Dual add-on therapy in type 2 diabetes poorly controlled with metformin monotherapy: A randomized double-blind trial of saxagliptin plus dapagliflozin addition versus single addition of saxagliptin or dapagliflozin to metformin. Diabetes Care. 2015; 38: 376–83.26. Lewis A, DeFronzo RA, Patel S et al. Initial combination of empagliflozin and linagliptin in subjects with type 2 diabetes. Diabetes Care. 2015; 39: 394–402.27. Mathieu C, Shankar RR, Lorber D et al. A randomized clinical trial to evaluate the efficacy and safety of coadministration of sitagliptin with intensively titrated insulin glargine. Diabetes Ther. 2015; 6: 127–42.28. Durán-Garcia S, Lee J, Yki-Jävinen H et al. Efficacyand safety of linagliptin as add-on therapy to basal insulin and metformin in people with type 2 diabetes. Diabet. Med. 2016; 33: 926–33.29. Hong ES, Khang AR, Yoon JW et al. Comparison between sitagliptin as add-on therapy to insulin and insulin dose-increase therapy in uncontrolled Korean type 2 diabetes: CSI study. Diabetes Obes. Metab. 2012; 14: 795–802.30. Cao Y, Gao F, Zhang Q, et al. Efficacy and safety of co-administration of sitagliptin with insulin glargine in type 2 diabetes. J. Diabetes 2016. doi:10.1111/1753-0407.12436中国人群空腹血糖水平与动脉粥样硬化性心血管疾病发病的关系:一项为期8年的随访研究Association of fasting glucose levels with incident atherosclerotic cardiovascular disease: An8-year follow-up study in a Chinese populationFangchao LIU,1 Xueli YANG, 1 Jianxin LI, 1 Jie CAO, 1 Jichun CHEN, 1 Ying LI, 1 Xiaoqing LIU, 2 Liancheng ZHAO, 1 Chong SHEN, 3 Ling YU, 4 Jianfeng HUANG1 and Dongfeng GU11Department of Epidemiology, Fuwai Hospital, State Key Laboratory of Cardiovascular Disease, National Center for Cardiovascular Diseases, Chinese Academy of Medical Sciences and Peking Union Medical College, Beijing, 2Division of Epidemiology, Guangdong Provincial People’s Hospital and Cardiovascular Institute, Guangzhou, 3Department of Epidemiology and Biostatistics, School of Public Health, Nanjing Medical University, Nanjing, and 4Department of Cardiology, Fujian Provincial People’s Hospital, Fuzhou, China摘要背景:识别动脉粥样硬化性心血管疾病高危人群对于疾病预防具有重要的意义。
