【精品】初三化学的所有化学方程式
初三化学的所有化学方程式

初三化学得所有化学方程式化合反应1、镁在空气中燃烧:2Mg + O2 点燃 2MgO2、铁在氧气中燃烧:3Fe + 2O2 点燃 Fe3O43、铝在空气中燃烧:4Al + 3O2 点燃 2Al2O34、氢气在空气中燃烧:2H2 + O2 点燃 2H2O5、红磷在空气中燃烧:4P + 5O2 点燃 2P2O56、硫粉在空气中燃烧: S + O2 点燃 SO27、碳在氧气中充分燃烧:C + O2 点燃 CO28、碳在氧气中不充分燃烧:2C + O2 点燃 2CO9、二氧化碳通过灼热碳层: C + CO2 高温 2CO10、一氧化碳在氧气中燃烧:2CO + O2 点燃 2CO211、二氧化碳与水反应(二氧化碳通入紫色石蕊试液):CO2 + H2O === H2CO312、生石灰溶于水:CaO + H2O === Ca(OH)213、无水硫酸铜作干燥剂:CuSO4 + 5H2O ==== CuSO4·5H2O14、钠在氯气中燃烧:2Na + Cl2点燃 2NaCl分解反应15、实验室用双氧水制氧气:2H2O2 MnO2 2H2O+ O2↑16、加热高锰酸钾:2KMnO4 加热K2MnO4 + MnO2 + O2↑17、水在直流电得作用下分解:2H2O 通电2H2↑+ O2 ↑18、碳酸不稳定而分解:H2CO3 === H2O + CO2↑19、高温煅烧石灰石(二氧化碳工业制法):CaCO3 高温CaO + CO2↑置换反应20、铁与硫酸铜溶液反应:Fe + CuSO4 == FeSO4 + Cu21、锌与稀硫酸反应(实验室制氢气):Zn + H2SO4 == ZnSO4 + H2↑22、镁与稀盐酸反应:Mg+ 2HCl === MgCl2 + H2↑23、氢气还原氧化铜:H2 + CuO 加热 Cu + H2O24、木炭还原氧化铜:C+ 2CuO 高温2Cu + CO2↑25、甲烷在空气中燃烧:CH4 + 2O2 点燃 CO2 + 2H2O26、水蒸气通过灼热碳层:H2O + C 高温 H2 + CO27、焦炭还原氧化铁:3C+ 2Fe2O3 高温4Fe + 3CO2↑其她28、氢氧化钠溶液与硫酸铜溶液反应:2NaOH + CuSO4 == Cu(OH)2↓ + Na2SO429、甲烷在空气中燃烧:CH4 + 2O2 点燃 CO2 + 2H2O30、酒精在空气中燃烧:C2H5OH + 3O2 点燃 2CO2 + 3H2O31、一氧化碳还原氧化铜:CO+ CuO 加热 Cu + CO232、一氧化碳还原氧化铁:3CO+ Fe2O3 高温 2Fe + 3CO233、二氧化碳通过澄清石灰水(检验二氧化碳):Ca(OH)2 + CO2 ==== CaCO3 ↓+ H2O34、氢氧化钠与二氧化碳反应(除去二氧化碳):2NaOH + CO2 ==== Na2CO3 + H2O35、石灰石(或大理石)与稀盐酸反应(二氧化碳得实验室制法):CaCO3 + 2HCl ===CaCl2 + H2O + CO2↑36、碳酸钠与浓盐酸反应(泡沫灭火器得原理): Na2CO3 + 2HCl === 2NaCl + H2O + CO2↑一. 物质与氧气得反应:(1)单质与氧气得反应:1、镁在空气中燃烧:2Mg + O2 点燃 2MgO2、铁在氧气中燃烧:3Fe + 2O2 点燃 Fe3O43、铜在空气中受热:2Cu + O2 加热 2CuO4、铝在空气中燃烧:4Al + 3O2 点燃 2Al2O35、氢气中空气中燃烧:2H2 + O2 点燃 2H2O6、红磷在空气中燃烧:4P + 5O2 点燃 2P2O57、硫粉在空气中燃烧: S + O2 点燃 SO28、碳在氧气中充分燃烧:C + O2 点燃 CO29、碳在氧气中不充分燃烧:2C + O2 点燃 2CO(2)化合物与氧气得反应:10、一氧化碳在氧气中燃烧:2CO + O2 点燃 2CO211、甲烷在空气中燃烧:CH4 + 2O2 点燃 CO2 + 2H2O12、酒精在空气中燃烧:C2H5OH + 3O2 点燃 2CO2 + 3H2O二.几个分解反应:13、水在直流电得作用下分解:2H2O 通电2H2↑+ O2 ↑14、加热碱式碳酸铜:Cu2(OH)2CO3 加热2CuO + H2O + CO2↑15、加热氯酸钾(有少量得二氧化锰):2KClO3 ==== 2KCl + 3O2 ↑16、加热高锰酸钾:2KMnO4 加热K2MnO4 + MnO2 + O2↑17、碳酸不稳定而分解:H2CO3 === H2O + CO2↑18、高温煅烧石灰石:CaCO3 高温CaO + CO2↑三.几个氧化还原反应:19、氢气还原氧化铜:H2 + CuO 加热 Cu + H2O20、木炭还原氧化铜:C+ 2CuO 高温2Cu + CO2↑21、焦炭还原氧化铁:3C+ 2Fe2O3 高温4Fe + 3CO2↑22、焦炭还原四氧化三铁:2C+ Fe3O4 高温3Fe + 2CO2↑23、一氧化碳还原氧化铜:CO+ CuO 加热 Cu + CO224、一氧化碳还原氧化铁:3CO+ Fe2O3 高温 2Fe + 3CO225、一氧化碳还原四氧化三铁:4CO+ Fe3O4 高温 3Fe + 4CO2四.单质、氧化物、酸、碱、盐得相互关系(1)金属单质 + 酸 -------- 盐 + 氢气 (置换反应)26、锌与稀硫酸Zn + H2SO4 = ZnSO4 + H2↑27、铁与稀硫酸Fe + H2SO4 = FeSO4 + H2↑28、镁与稀硫酸Mg + H2SO4 = MgSO4 + H2↑29、铝与稀硫酸2Al +3H2SO4 = Al2(SO4)3 +3H2↑30、锌与稀盐酸Zn + 2HCl === ZnCl2 + H2↑31、铁与稀盐酸Fe + 2HCl === FeCl2 + H2↑32、镁与稀盐酸Mg+ 2HCl === MgCl2 + H2↑33、铝与稀盐酸2Al + 6HCl == 2AlCl3 + 3H2↑(2)金属单质 + 盐(溶液) ------- 另一种金属 + 另一种盐34、铁与硫酸铜溶液反应:Fe + CuSO4 === FeSO4 + Cu35、锌与硫酸铜溶液反应:Zn + CuSO4 === ZnSO4 + Cu36、铜与硝酸汞溶液反应:Cu + Hg(NO3)2 === Cu(NO3)2 + Hg(3)碱性氧化物 +酸 -------- 盐 + 水37、氧化铁与稀盐酸反应:Fe2O3 + 6HCl === 2FeCl3 + 3H2O38、氧化铁与稀硫酸反应:Fe2O3 + 3H2SO4 === Fe2(SO4)3 + 3H2O39、氧化铜与稀盐酸反应:CuO + 2HCl ==== CuCl2 + H2O40、氧化铜与稀硫酸反应:CuO + H2SO4 ==== CuSO4 + H2O41、氧化镁与稀硫酸反应:MgO + H2SO4 ==== MgSO4 + H2O42、氧化钙与稀盐酸反应:CaO + 2HCl ==== CaCl2 + H2O(4)酸性氧化物 +碱 -------- 盐 + 水43.苛性钠暴露在空气中变质:2NaOH + CO2 ==== Na2CO3 + H2O44.苛性钠吸收二氧化硫气体:2NaOH + SO2 ==== Na2SO3 + H2O45.苛性钠吸收三氧化硫气体:2NaOH + SO3 ==== Na2SO4 + H2O46.消石灰放在空气中变质:Ca(OH)2 + CO2 ==== CaCO3 ↓+ H2O47、消石灰吸收二氧化硫:Ca(OH)2 + SO2 ==== CaSO3 ↓+ H2O(5)酸 + 碱 -------- 盐 + 水48.盐酸与烧碱起反应:HCl + NaOH ==== NaCl +H2O49、盐酸与氢氧化钾反应:HCl + KOH ==== KCl +H2O50.盐酸与氢氧化铜反应:2HCl + Cu(OH)2 ==== CuCl2 + 2H2O51、盐酸与氢氧化钙反应:2HCl + Ca(OH)2 ==== CaCl2 + 2H2O52、盐酸与氢氧化铁反应:3HCl + Fe(OH)3 ==== FeCl3 + 3H2O53、氢氧化铝药物治疗胃酸过多:3HCl + Al(OH)3 ==== AlCl3 + 3H2O54、硫酸与烧碱反应:H2SO4 + 2NaOH ==== Na2SO4 + 2H2O55、硫酸与氢氧化钾反应:H2SO4 + 2KOH ==== K2SO4 + 2H2O56、硫酸与氢氧化铜反应:H2SO4 + Cu(OH)2 ==== CuSO4 + 2H2O57、硫酸与氢氧化铁反应:3H2SO4 + 2Fe(OH)3==== Fe2(SO4)3 + 6H2O58、硝酸与烧碱反应:HNO3+ NaOH ==== NaNO3 +H2O(6)酸 + 盐 -------- 另一种酸 + 另一种盐59.大理石与稀盐酸反应:CaCO3 + 2HCl === CaCl2 + H2O + CO2↑60.碳酸钠与稀盐酸反应: Na2CO3 + 2HCl === 2NaCl + H2O + CO2↑61.碳酸镁与稀盐酸反应: MgCO3 + 2HCl === MgCl2 + H2O + CO2↑62.盐酸与硝酸银溶液反应:HCl + AgNO3 === AgCl↓ + HNO363、硫酸与碳酸钠反应:Na2CO3 + H2SO4 === Na2SO4 + H2O + CO2↑64、硫酸与氯化钡溶液反应:H2SO4 + BaCl2 ==== BaSO4 ↓+ 2HCl (7)碱 + 盐 -------- 另一种碱 + 另一种盐65.氢氧化钠与硫酸铜:2NaOH + CuSO4 ==== Cu(OH)2↓ + Na2SO466.氢氧化钠与氯化铁:3NaOH + FeCl3 ==== Fe(OH)3↓ + 3NaCl67.氢氧化钠与氯化镁:2NaOH + MgCl2 ==== Mg(OH)2↓ + 2NaCl68、氢氧化钠与氯化铜:2NaOH + CuCl2 ==== Cu(OH)2↓ + 2NaCl69、氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 === CaCO3↓+ 2NaOH(8)盐 + 盐 ----- 两种新盐70.氯化钠溶液与硝酸银溶液:NaCl + AgNO3 ==== AgCl↓ + NaNO371.硫酸钠与氯化钡:Na2SO4 + BaCl2 ==== BaSO4↓ + 2NaCl五.其它反应:72.二氧化碳溶解于水:CO2 + H2O === H2CO373.生石灰溶于水:CaO + H2O === Ca(OH)274.氧化钠溶于水:Na2O + H2O ==== 2NaOH75.三氧化硫溶于水:SO3 + H2O ==== H2SO476.硫酸铜晶体受热分解:CuSO4·5H2O 加热 CuSO4 + 5H2O77.无水硫酸铜作干燥剂:CuSO4 + 5H2O ==== CuSO4·5H2化学方程式反应现象应用2Mg+O2点燃或Δ2MgO 剧烈燃烧、耀眼白光、生成白色固体、放热、产生大量白烟白色信号弹2Hg+O2点燃或Δ2HgO 银白液体、生成红色固体拉瓦锡实验2Cu+O2点燃或Δ2CuO 红色金属变为黑色固体4Al+3O2点燃或Δ2Al2O3 银白金属变为白色固体3Fe+2O2点燃Fe3O4 剧烈燃烧、火星四射、生成黑色固体、放热 4Fe + 3O2高温2Fe2O3C+O2 点燃CO2 剧烈燃烧、白光、放热、使石灰水变浑浊S+O2 点燃SO2 剧烈燃烧、放热、刺激味气体、空气中淡蓝色火焰、氧气中蓝紫色火焰2H2+O2 点燃2H2O 淡蓝火焰、放热、生成使无水CuSO4变蓝得液体(水) 高能燃料4P+5O2 点燃2P2O5 剧烈燃烧、大量白烟、放热、生成白色固体证明空气中氧气含量CH4+2O2点燃2H2O+CO2 蓝色火焰、放热、生成使石灰水变浑浊气体与使无水CuSO4变蓝得液体(水) 甲烷与天然气得燃烧2C2H2+5O2点燃2H2O+4CO2 蓝色火焰、放热、黑烟、生成使石灰水变浑浊气体与使无水CuSO4变蓝得液体(水) 氧炔焰、焊接切割金属2KClO3MnO2 Δ2KCl +3O2↑ 生成使带火星得木条复燃得气体实验室制备氧气2KMnO4Δ K2MnO4+MnO2+O2↑ 紫色变为黑色、生成使带火星木条复燃得气体实验室制备氧气2HgOΔ2Hg+O2↑ 红色变为银白、生成使带火星木条复燃得气体拉瓦锡实验2H2O通电2H2↑+O2↑ 水通电分解为氢气与氧气电解水Cu2(OH)2CO3Δ2CuO+H2O+CO2↑ 绿色变黑色、试管壁有液体、使石灰水变浑浊气体铜绿加热初三常见化学方程式集。
九年级化学方程式大全

九年级化学方程式大全分解反应水在直流电的作用下分解:2H2O 通电2H2↑+ O2 ↑加热碱式碳酸铜:Cu2(OH)2CO3 加热2CuO + H2O + CO2↑加热氯酸钾(有少量的二氧化锰):2KClO3 ==== 2KCl + 3O2 ↑加热高锰酸钾:2KMnO4 加热K2MnO4 + MnO2 + O2↑碳酸不稳定而分解:H2CO3 === H2O + CO2↑高温煅烧石灰石:CaCO3高温CaO + CO2↑氧化还原反应:氢气还原氧化铜:H2 + CuO 加热 Cu + H2O木炭还原氧化铜:C+ 2CuO高温2Cu + CO2↑焦炭还原氧化铁:3C+ 2Fe2O3 高温4Fe + 3CO2↑焦炭还原四氧化三铁:2C+ Fe3O4 高温3Fe + 2CO2↑一氧化碳还原氧化铜:CO+ CuO 加热 Cu + CO2一氧化碳还原氧化铁:3CO+ Fe2O3 高温 2Fe + 3CO2一氧化碳还原四氧化三铁:4CO+ Fe3O4 高温 3Fe + 4CO2酸与金属氧化物氧化铁和稀盐酸反应:Fe2O3 + 6HCl ==2FeCl3 + 3H2O氧化铁和稀硫酸反应:Fe2O3 + 3H2SO4 == Fe2(SO4)3 + 3H2O氧化铜和稀盐酸反应:CuO + 2HCl ==CuCl2 + H2O氧化铜和稀硫酸反应:CuO + H2SO4 == CuSO4 + H2O金属单质与酸锌和稀硫酸Zn + H2SO4 = ZnSO4 + H2↑铁和稀硫酸Fe + H2SO4 = FeSO4 + H2↑镁和稀硫酸Mg + H2SO4 = MgSO4 + H2↑铝和稀硫酸2Al +3H2SO4 = Al2(SO4)3 +3 H2↑锌和稀盐酸Zn + 2HCl == ZnCl2 + H2↑铁和稀盐酸Fe + 2HCl == FeCl2 + H2↑镁和稀盐酸Mg+ 2HCl == MgCl2 + H2↑铝和稀盐酸2Al + 6HCl == 2AlCl3 + 3 H2↑与氧有关的化学方程式2Mg+O2点燃2MgO 现象:燃烧、放出大量的热、同时放出耀眼的白光S+O2 点燃SO2 现象:空气中是淡蓝色的火焰;纯氧中是蓝紫色的火焰;同时生成有刺激性气味的气体。
九年级化学方程式大全【最全整理】

九年级化学方程式大全【最全整理】物质与氧气的反应(1)单质与氧气的反应:1. 镁在空气中燃烧:2Mg + O2 点燃 2MgO2. 铁在氧气中燃烧:3Fe + 2O2 点燃 Fe3O43. 铜在空气中受热:2Cu + O2 加热 2CuO4. 铝在空气中燃烧:4Al + 3O2 点燃 2Al2O35. 氢气中空气中燃烧:2H2 + O2 点燃 2H2O6. 红磷在空气中燃烧:4P + 5O2 点燃 2P2O57. 硫粉在空气中燃烧: S + O2 点燃 SO28. 碳在氧气中充分燃烧:C + O2 点燃 CO29. 碳在氧气中不充分燃烧:2C + O2 点燃 2CO(2)化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO + O2 点燃 2CO211. 甲烷在空气中燃烧:CH4 + 2O2 点燃 CO2 + 2H2O12. 酒精在空气中燃烧:C2H5OH + 3O2 点燃 2CO2 + 3H2O 几个分解反应13. 水在直流电的作用下分解:2H2O 通电2H2↑+ O2 ↑14. 加热碱式碳酸铜:Cu2(OH)2CO3 加热2CuO + H2O + CO2↑15. 加热氯酸钾(有少量的二氧化锰作催化剂):2KClO3 ==== 2KCl + 3O2 ↑16. 加热高锰酸钾:2KMnO4 加热K2MnO4 + MnO2 + O2↑17. 碳酸不稳定而分解:H2CO3 === H2O + CO2↑18. 高温煅烧石灰石:CaCO3 高温CaO + CO2↑几个氧化还原反应19. 氢气还原氧化铜:H2 + CuO 加热 Cu + H2O20. 木炭还原氧化铜:C+ 2CuO 高温2Cu + CO2↑21. 焦炭还原氧化铁:3C+ 2Fe2O3 高温4Fe + 3CO2↑22. 焦炭还原四氧化三铁:2C+ Fe3O4 高温3Fe + 2CO2↑23. 一氧化碳还原氧化铜:CO+ CuO 加热 Cu + CO224. 一氧化碳还原氧化铁:3CO+ Fe2O3 高温 2Fe + 3CO225. 一氧化碳还原四氧化三铁:4CO+ Fe3O4 高温 3Fe + 4CO2 单质、氧化物、酸、碱、盐的相互关系金属单质 + 酸 -------- 盐 + 氢气 (置换反应)26. 锌和稀硫酸Zn + H2SO4 = ZnSO4 + H2↑27. 铁和稀硫酸Fe + H2SO4 = FeSO4 + H2↑28. 镁和稀硫酸Mg + H2SO4 = MgSO4 + H2↑29. 铝和稀硫酸2Al +3H2SO4 = Al2(SO4)3 +3H2↑30. 锌和稀盐酸Zn + 2HCl === ZnCl2 + H2↑31. 铁和稀盐酸Fe + 2HCl === FeCl2 + H2↑32. 镁和稀盐酸Mg+ 2HCl === MgCl2 + H2↑33. 铝和稀盐酸2Al + 6HCl == 2AlCl3 + 3H2↑。
初三化学方程式大全

初三化学方程式大全一.物质与氧气的反应:(1)单质与氧气的反应:L镁在空气中燃烧:2Mg+02点燃2Mg02.铁在氧气中燃烧:3Fe+202点燃Fe3O43.铜在空气中受热:2Cu+02加热2Cu04.铝在空气中燃烧:4AI+302点燃2AI2O35.氢气中空气中燃烧:2H2+02点燃2H2O6.红磷在空气中燃烧:4P+502点燃2P2O57硫粉在空气中燃烧:S+02点燃S028碳在氧气中充分燃烧:C+02点燃C029碳在氧气中不充分燃烧:2C+02点燃2C0(2)化合物与氧气的反应:10.—氧化碳在氧气中燃烧:2C0+02点燃2CO21L甲烷在空气中燃烧:CH4+202点燃C02+2H2O12酒精在空气中燃烧:C2H5OH+302点燃2CO2+3H2O二.几个分解反应:13.水在直流电的作用下分解:2H2O通电2H2T+02t国登&涅瞬自.Ill+o e u瞿 m o u o起临蕾瞿oo wo u + 02 R u m c o w 票喝WK-^W Z -I一"0 +"OUIAI+寸O U I A I ">I娠吕寸OU S M一肱避艘程蒸晨91一 §+G M R R m o D 湘二艘昔侦南令)旺盈愚莒.3一rxl co+ 0"H+ o n ufxl蒸吕m o u fxl Io m n u一"0¥ + aLL.m唳饱寸 om a LL.+O U寸一抠II IX 1谛S瓯照龄3诵—.捋§m +①LL.fxl卷m o 财LL.+0*-篓崛瓯眼普—.其fxl ou + n u蒸吕o n )+0U -x o ufxl +a LL.m唳饱s m o M - +U "-援川^w 巳限照瑕«质 0M +CULL.寸唳裾m ofxl cu LL."+*一抠¥)«晚照瑕遥.1"§u +n uCN明建O r o "+U 回葵诵晚照瑕长o fxl o"H + n u蒸目o n u+S .回葵诵晚照r w .61四.单质、氧化物、酸、碱、盐的相互关系(1)金属单质+酸------盐+氢气(置换反应) 26.锌和稀硫酸反应:Zn+H2SO4===ZnS04+H2T27.铁和稀硫酸反应:Fe+H2SO4===FeS04+H2T28.镁和稀硫酸反应:Mg+H2SO4===MgS04+H2T29.铝和稀硫酸反应:2AI+3H2SO4===AI2(SO4)3+3H2t30.锌和稀盐酸反应:Zn+2HCI===ZnCI2+H2t31.铁和稀盐酸反应:Fe+2HCI===FeCI2+H2t32.镁和稀盐酸反应:Mg+2HCI===MgCI2+H2T33.铝和稀盐酸反应:2AI+6HCI===2AICI3+3H2T(2)金属单质+盐(溶液)另一种金属+另一种盐ofxl Hm + 8^h h h_U H 9 + m o斜LL.-回底^甜曜曷援^«忘冬+锢--------s s s (m )6h+"(m o N)n uhh hCN (m o N )6H + n u -nu + S ^C Nh h h寸o s n u+C N -回底黑现回盈炬履挞.#n u + 寸 o s a LL.H H H 寸o s n u+ £ .冬+ 锢----®+(寸)ofxl H+ "o e uhh h hd h "+ o e u-ofxl H+ 寸O S 6SR R寸O S "H+06芝-Ofxl H+ 寸o s n uh h h h寸0S 2+ o n u-2 + 3n uh h h h o h" +o n u-02m + m (寸O S )财LL.hh h寸o s "H m+m o斜LL.-ofxl H+Tmoseuh h h h+"(H o )e u-焙^M n-tx lE ^JKZ寸ofxl H+T m o u e uh h h h§ +fxl (H 0)3 -ttg秘任r佃担常宾起粮• 9寸Ofxl H+ 寸0s "e Nh h h h+H o e N "一 长更焙^Ml I l n l e afc •Ln i zO fxl H+m o s z e Nh h h h+ H o e N "一 也r焙^崛门坚举坛坦面•寸寸02 + m o urxl eNh h h h§ +H o e N "一ttg秘任r佃担睡嘿坛坦面• m寸02m + m _%Ll_hh h h2H O OLL.+U H T 回底扳涅M M履离另rxiLn02" + 3e u R R"(Ho)eu+O H "-回底瓠g M M巨离铜.IsOfxl H" + 3n u R R "(H o )n u +U H "-垣景昔«耆铜•oLnCXI H+ sh h h hH 8 + _¥ -回底旺与M w履离铜.6寸2 + G r a zh h h hH o e N+ s一 国胃®誉霸铜• 8寸志 + 铜----®+®(Ln )029+ m (寸O S )财LL.RR 2H O 0LL."+ 寸 o s rxl Hm -回底扳M M M巨离焙以02CXI +寸o s n uh h h h"(H o )n u+ 寸 os fxl H-回监葵源«l w w 9Ln0£" +寸O s ah h h hH 8" +寸O S "H-回底肱M W M巨离焙校OZH"+h h h hH o e N "+1Z 0S 2一 国底詹襄巨离W寸Lno "H m + S 3h h h hm (H O )<+G H m -m o N H+ -_%< hh hm o N 6<+O H -回底揆现聪潮遥巨避铜•"9-"O u + orxl H+"G6IAIH U H D HCXI +O1OU6芝•19一rxl co + 0"H+G e Ncsl hh hD HCXI +m o u fxl eN• 09§u +O "H+ 3e uhh h g hcxi +m o u e u -• 6Ln锢暮—叱 +®ft:—咔----铜 +®( 9)02+m o N e NR RH o e N+8N H一昌®管密od LnD e N m+ -2H O OLL.hh h h+H o e N T抠^喊坍援^崛»・99寸 osfxl eN +一cxl (HO )n ) H H H H寸o s n u +H o e N "一 曜避炬JJ?MV)M M ・Ln 9锢暮—叱+詹拄—咔----铜+®( Z)G H " +-寸O S e sh h h h8^+寸os rxl H-回岛黑佃色节扇巨离W寸9-CN OU + o rxl H+寸0s "e NH H H 寸O S "H+mo u rxl eN -G e N " +-寸o s e mH H H H+ 寸 os CN eN一 M节扇口窝盈焙.IZ.m o N e N+一。
九年级化学方程式大全(最全面)

二、自然界中的水:16.水在直流电的作用下分解(研究水的组成实验):2H2O 通电2H2↑+ O2↑17.生石灰溶于水:CaO + H2O == Ca(OH)218.二氧化碳可溶于水:H2O + CO2==H2CO3三、质量守恒定律:19.镁在空气中燃烧:2Mg + O2点燃2MgO20.铁和硫酸铜溶液反应:Fe + CuSO4 === FeSO4 + Cu21.氢气还原氧化铜:H2 + CuO 加热Cu + H2O22. 镁还原氧化铜:Mg + CuO 加热Cu + MgO四、碳和碳的氧化物:(1)碳的化学性质23. 碳在氧气中充分燃烧:C + O2点燃CO224.木炭还原氧化铜:C+ 2CuO 高温2Cu + CO2↑25.焦炭还原氧化铁:3C+ 2Fe2O3高温4Fe + 3CO2↑(2)煤炉中发生的三个反应:(几个化合反应)26.煤炉的底层:C + O2点燃CO227.煤炉的中层:CO2 + C 高温2CO28.煤炉的上部蓝色火焰的产生:2CO + O2点燃2CO2(3)二氧化碳的制法与性质:29.大理石与稀盐酸反应(实验室制二氧化碳):CaCO3 + 2HCl == CaCl2 + H2O + CO2↑30.碳酸不稳定而分解:H2CO3 == H2O + CO2↑31.二氧化碳可溶于水:H2O + CO2== H2CO332.高温煅烧石灰石(工业制二氧化碳):CaCO3高温CaO + CO2↑ 33.石灰水与二氧化碳反应(鉴别二氧化碳):Ca(OH)2 + CO2 === CaCO3↓+ H2O(4)一氧化碳的性质:34.一氧化碳还原氧化铜:CO+ CuO 加热Cu + CO235.一氧化碳的可燃性:2CO + O2点燃2CO2其它反应:36.碳酸钠与稀盐酸反应(灭火器的原理):Na2CO3 + 2HCl == 2NaCl + H2O + CO2↑五、燃料及其利用:37.甲烷在空气中燃烧:CH4 + 2O2点燃CO2 + 2H2O38.酒精在空气中燃烧:C2H5OH + 3O2点燃2CO2 + 3H2O39.氢气中空气中燃烧:2H2 + O2点燃2H2O六、金属(1)金属与氧气反应:40.镁在空气中燃烧:2Mg + O2点燃2MgO41.铁在氧气中燃烧:3Fe + 2O2点燃Fe3O442. 铜在空气中受热:2Cu + O2加热2CuO43. 铝在空气中形成氧化膜:4Al + 3O2 = 2Al2O3(2)金属单质+ 酸-------- 盐+ 氢气(置换反应)44. 锌和稀硫酸Zn + H2SO4 = ZnSO4 + H2↑45. 铁和稀硫酸Fe + H2SO4 = FeSO4 + H2↑46. 镁和稀硫酸Mg + H2SO4 = MgSO4 + H2↑47. 铝和稀硫酸2Al +3H2SO4 = Al2(SO4)3 +3 H2↑48. 锌和稀盐酸Zn + 2HCl == ZnCl2 + H2↑49. 铁和稀盐酸Fe + 2HCl == FeCl2 + H2↑50. 镁和稀盐酸Mg+ 2HCl == MgCl2 + H2↑51.铝和稀盐酸2Al + 6HCl == 2AlCl3 + 3 H2↑(3)金属单质+ 盐(溶液)------- 新金属+ 新盐52. 铁和硫酸铜溶液反应:Fe + CuSO4 == FeSO4 + Cu53. 锌和硫酸铜溶液反应:Zn + CuSO4 ==ZnSO4 + Cu54. 铜和硝酸汞溶液反应:Cu + Hg(NO3)2 == Cu(NO3)2 + Hg (3)金属铁的治炼原理:55.3CO+ 2Fe2O3高温4Fe + 3CO2↑七、酸、碱、盐1、酸的化学性质(1)酸+ 金属-------- 盐+ 氢气(见上)(2)酸+ 金属氧化物-------- 盐+ 水56. 氧化铁和稀盐酸反应:Fe2O3 + 6HCl ==2FeCl3 + 3H2O57. 氧化铁和稀硫酸反应:Fe2O3 + 3H2SO4 == Fe2(SO4)3 + 3H2O58. 氧化铜和稀盐酸反应:CuO + 2HCl ==CuCl2 + H2O59. 氧化铜和稀硫酸反应:CuO + H2SO4 == CuSO4 + H2O(3)酸+ 碱-------- 盐+ 水(中和反应)60.盐酸和烧碱起反应:HCl + NaOH == NaCl +H2O61. 盐酸和氢氧化钙反应:2HCl + Ca(OH)2 == CaCl2 + 2H2O62. 氢氧化铝药物治疗胃酸过多:3HCl + Al(OH)3 == AlCl3 + 3H2O63. 硫酸和烧碱反应:H2SO4 + 2NaOH == Na2SO4 + 2H2O(4)酸+ 盐-------- 另一种酸+ 另一种盐64.大理石与稀盐酸反应:CaCO3 + 2HCl == CaCl2 + H2O + CO2↑ 65.碳酸钠与稀盐酸反应: Na2CO3 + 2HCl == 2NaCl + H2O + CO2↑ 66.碳酸氢钠与稀盐酸反应:NaHCO3 + HCl== NaCl + H2O + CO2↑ 67. 硫酸和氯化钡溶液反应:H2SO4 + BaCl2 == BaSO4↓+ 2HCl2、碱的化学性质(1)碱+ 非金属氧化物-------- 盐+ 水68.苛性钠暴露在空气中变质:2NaOH + CO2 == Na2CO3 + H2O 69.苛性钠吸收二氧化硫气体:2NaOH + SO2 == Na2SO3 + H2O 70.苛性钠吸收三氧化硫气体:2NaOH + SO3 == Na2SO4 + H2O 71.消石灰放在空气中变质:Ca(OH)2 + CO2 == CaCO3↓+ H2O 72. 消石灰吸收二氧化硫:Ca(OH)2 + SO2 == CaSO3↓+ H2O(2)碱+ 酸-------- 盐+ 水(中和反应,方程式见上)(3)碱+ 盐-------- 另一种碱+ 另一种盐73. 氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 == CaCO3↓+ 2NaOH 3、盐的化学性质(1)盐(溶液)+ 金属单质------- 另一种金属+ 另一种盐74. 铁和硫酸铜溶液反应:Fe + CuSO4 == FeSO4 + Cu(2)盐+ 酸-------- 另一种酸+ 另一种盐75.碳酸钠与稀盐酸反应: Na2CO3 + 2HCl == 2NaCl + H2O + CO2↑ 碳酸氢钠与稀盐酸反应:NaHCO3 + HCl== NaCl + H2O + CO2↑ (3)盐+ 碱-------- 另一种碱+ 另一种盐76. 氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 == CaCO3↓+ 2NaOH (4)盐+ 盐----- 两种新盐77.氯化钠溶液和硝酸银溶液:NaCl + AgNO3== AgCl↓ + NaNO3 78.硫酸钠和氯化钡:Na2SO4 + BaCl2 == BaSO4↓ + 2NaCl。
(完整版)初三化学方程式大全
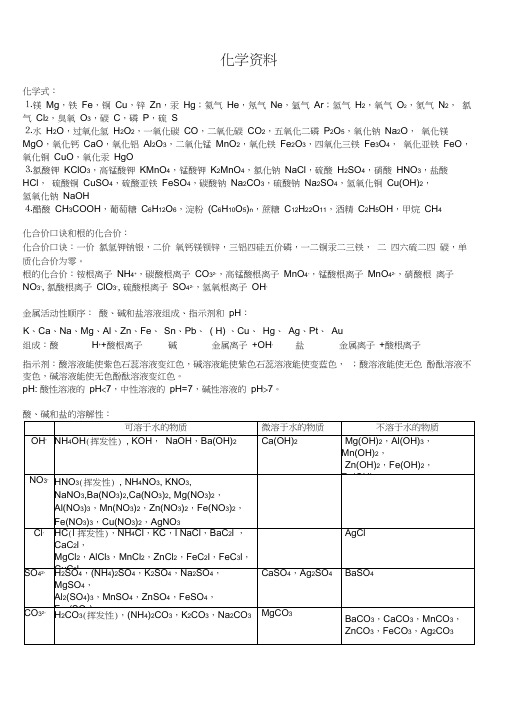
化学资料化学式:⒈镁Mg,铁Fe,铜Cu,锌Zn,汞Hg;氦气He,氖气Ne,氩气Ar;氢气H2,氧气O2,氮气N2,氯气Cl2,臭氧O3,碳C,磷P,硫S⒉水H2O,过氧化氢H2O2,一氧化碳CO,二氧化碳CO2,五氧化二磷P2O5,氧化钠Na2O,氧化镁MgO,氧化钙CaO,氧化铝Al2O3,二氧化锰MnO2,氧化铁Fe2O3,四氧化三铁Fe3O4,氧化亚铁FeO,氧化铜CuO,氧化汞HgO⒊氯酸钾KClO3,高锰酸钾KMnO4,锰酸钾K2MnO4,氯化钠NaCl,硫酸H2SO4,硝酸HNO3,盐酸HCl,硫酸铜CuSO4,硫酸亚铁FeSO4,碳酸钠Na2CO3,硫酸钠Na2SO4,氢氧化铜Cu(OH)2,氢氧化钠NaOH⒋醋酸CH3COOH,葡萄糖C6H12O6,淀粉(C6H10O5)n,蔗糖C12H22O11,酒精C2H5OH,甲烷CH4化合价口诀和根的化合价:化合价口诀:一价氯氢钾钠银,二价氧钙镁钡锌,三铝四硅五价磷,一二铜汞二三铁,二四六硫二四碳,单质化合价为零。
根的化合价:铵根离子NH4+,碳酸根离子CO32-,高锰酸根离子MnO4-,锰酸根离子MnO42-,硝酸根离子NO3-, 氯酸根离子ClO3-, 硫酸根离子SO42-,氢氧根离子OH-金属活动性顺序:酸、碱和盐溶液组成、指示剂和pH:K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb、( H) 、Cu、Hg、Ag、Pt、Au组成:酸H++酸根离子碱金属离子+OH-盐金属离子+酸根离子指示剂:酸溶液能使紫色石蕊溶液变红色,碱溶液能使紫色石蕊溶液能使变蓝色,;酸溶液能使无色酚酞溶液不变色,碱溶液能使无色酚酞溶液变红色。
pH: 酸性溶液的pH<7,中性溶液的pH=7,碱性溶液的pH>7。
能发生复分解反应的集中类型:在水中不能共存的离子:H+和OH-,H+和CO32-,H+和HCO3-,NH4+和OH-,Ca2+和CO32-,Ba2+和SO42-、CO32-,Ag+和Cl-,Fe3+、Cu2+、Mg2+和OH-检验氨气的方法:氨气能使湿润的红色石蕊试纸变蓝色。
化学九年级方程式总结77个

化学九年级方程式总结77个1、镁在空气中燃烧:2Mg + O2 = 2MgO。
2、铁在氧气中燃烧:3Fe + 2O2 = Fe3O4。
3、铜在空气中受热:2Cu + O2 = 2CuO。
4、铝在空气中燃烧:4Al + 3O2 = 2Al2O3。
5、氢气中空气中燃烧:2H2 + O2 = 2H2O。
6、红磷在空气中燃烧:4P + 5O2 = 2P2O5。
7、硫粉在空气中燃烧:S + O2 = SO2。
8、碳在氧气中充分燃烧:C + O2 = CO2。
9、碳在氧气中不充分燃烧:2C + O2 = 2CO。
10、一氧化碳在氧气中燃烧:2CO + O2 = 2CO2。
11、甲烷在空气中燃烧:CH4 + 2O2 = CO2 + 2H2O。
12、酒精在空气中燃烧:C2H5OH + 3O2 = 2CO2 + 3H2O。
13、水在直流电的作用下分解:2H2O = 2H2↑+ O2↑。
14、加热碱式碳酸铜:Cu2(OH)2CO3 = 2CuO + H2O + CO2↑。
15、加热氯酸钾(有少量的二氧化锰):2KClO3 = 2KCl + 3O2↑。
16、加热高锰酸钾:2KMnO4 = K2MnO4 + MnO2 + O2↑。
17、碳酸不稳定而分解:H2CO3 = H2O + CO2↑。
18、高温煅烧石灰石:CaCO3 = CaO + CO2↑。
19、氢气还原氧化铜:H2 + CuO = Cu + H2O。
20、木炭还原氧化铜:C+ 2CuO = 2Cu + CO2↑。
21、焦炭还原氧化铁:3C+ 2Fe2O3 = 4Fe + 3CO2↑。
22、焦炭还原四氧化三铁:2C+ Fe3O4 = 3Fe + 2CO2↑。
23、一氧化碳还原氧化铜:CO+ CuO = Cu + CO2。
24、一氧化碳还原氧化铁:3CO+ Fe2O3 = 2Fe + 3CO2。
25、一氧化碳还原四氧化三铁:4CO+ Fe3O4 = 3Fe + 4CO2。
完整版九年级所有化学方程式总汇全

初中化学方程式总汇一、氧气的性质:(1)单质与氧气的反应:(化合反应)1. 镁在空气中燃烧:2Mg + O =点燃= 2MgO 22. 铁在氧气中燃烧:3Fe + 2O=点燃= FeO 3243. 铜在空气中受热:2Cu + O=加热= 2CuO 24. 铝在空气中燃烧:4Al + 3O=点燃= 2AlO 32 25. 氢气中空气中燃烧:2H + O =点燃= 2HO2226. 红磷在空气中燃烧(研究空气组成的实验):4P + 5O =点燃= 2PO 5227. 硫粉在空气中燃烧: S + O =点燃= SO 22=点燃= CO 8. 碳在氧气中充分燃烧:C + O2 29. 碳在氧气中不充分燃烧:2C + O =点燃= 2CO 2(2)化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO + O =点燃= 2CO 22=点燃=CO + 2O + 2HO 11. 甲烷在空气中燃烧:CH222412. 酒精在空气中燃烧:CHOH + 3O =点燃= 2CO + 3HO 22522(3)氧气的来源:13.玻义耳研究空气的成分实验 2HgO =加热= Hg+ O ↑214.加热高锰酸钾:2KMnO =加热= KMnO + MnO + O↑(实验室制氧气原理1)2422415.过氧化氢在二氧化锰作催化剂条件下分解反应:HO(MnO催化剂)=2HO+ O ↑(实验室制氧气原理2)22222二、自然界中的水:16.水在直流电的作用下分解(研究水的组成实验):2HO =通电= 2H↑+ O↑ 2 2217.生石灰溶于水:CaO + HO == Ca(OH) 2 2.18.二氧化碳可溶于水: HO + CO==HCO 3222三、质量守恒定律:19.镁在空气中燃烧:2Mg + O=点燃= 2MgO220.铁和硫酸铜溶液反应:Fe + CuSO=== FeSO+ Cu 4 421.氢气还原氧化铜:H + CuO =加热= Cu + HO 2222. 镁还原氧化铜:Mg + CuO =加热= Cu + MgO四、碳和碳的氧化物:(1)碳的化学性质23. 碳在氧气中充分燃烧:C + O =点燃= CO 2224.木炭还原氧化铜:C+ 2CuO =高温=2Cu + CO↑2=高温= 4Fe + 3CO3C+ 2FeO↑ 25.焦炭还原氧化铁:223(2)煤炉中发生的三个反应:(几个化合反应)26.煤炉的底层:C + O =点燃= CO 2227.煤炉的中层:CO + C =高温= 2CO228.煤炉的上部蓝色火焰的产生:2CO + O =点燃= 2CO 22(3)二氧化碳的制法与性质:29.大理石与稀盐酸反应(实验室制二氧化碳):CaCO + 2HCl == CaCl + HO + CO↑223230.碳酸不稳定而分解:HCO == HO + CO ↑223231.二氧化碳可溶于水: HO + CO== HCO 322232.高温煅烧石灰石(工业制二氧化碳):CaCO=高温= CaO + CO↑2333.石灰水与二氧化碳反应(鉴别二氧化碳):Ca(OH) + CO === CaCO ↓+ HO 2232(4)一氧化碳的性质:34.一氧化碳还原氧化铜:CO+ CuO =加热= Cu + CO 235.一氧化碳的可燃性:2CO + O=点燃= 2CO 22其它反应:36.碳酸钠与稀盐酸反应(灭火器的原理):NaCO + 2HCl == 2NaCl + HO + CO↑2322五、燃料及其利用:37.甲烷在空气中燃烧:CH + 2O =点燃= CO + 2HO 242238.酒精在空气中燃烧:CHOH + 3O =点燃= 2CO + 3HO 2222539.氢气中空气中燃烧:2H + O =点燃= 2HO222六、金属(1)金属与氧气反应:40.镁在空气中燃烧:2Mg + O2 =点燃= 2MgO41.铁在氧气中燃烧:3Fe + 2O =点燃= FeO 43242. 铜在空气中受热:2Cu + O =加热=2CuO 243. 铝在空气中形成氧化膜:4Al + 3O = 2Al2O 32(2)金属单质 + 酸 -------- 盐 + 氢气(置换反应)44. 锌和稀硫酸Zn + HSO = ZnSO + H↑244245. 铁和稀硫酸Fe + HSO = FeSO + H↑242446. 镁和稀硫酸Mg + HSO= MgSO + H↑224447. 铝和稀硫酸2Al +3HSO = Al(SO4)+3 H↑2243 248. 锌和稀盐酸Zn + 2HCl == ZnCl + H↑2249. 铁和稀盐酸Fe + 2HCl == FeCl + H↑2250. 镁和稀盐酸Mg+ 2HCl == MgCl + H↑2251.铝和稀盐酸2Al + 6HCl == 2AlCl + 3 H↑23(3)金属单质 + 盐(溶液) ------- 新金属 + 新盐52. 铁和硫酸铜溶液反应:Fe + CuSO == FeSO + Cu 4453. 锌和硫酸铜溶液反应:Zn + CuSO ==ZnSO+ Cu 4 454. 铜和硝酸汞溶液反应:Cu + Hg(NO3)== Cu(NO3)+ Hg 2 2)金属铁的治炼原理:4(.55.3CO+ 2FeO 高温 4Fe + 3CO↑232七、酸、碱、盐1、酸的化学性质(1)酸 + 金属 -------- 盐 + 氢气(见上)(2)酸 + 金属氧化物-------- 盐 + 水56. 氧化铁和稀盐酸反应:FeO + 6HCl ==2FeCl3 + 3HO 22357. 氧化铁和稀硫酸反应:FeO + 3H2SO == Fe(SO) + 3HO 234432258. 氧化铜和稀盐酸反应:CuO + 2HCl ==CuCl + HO 2259. 氧化铜和稀硫酸反应:CuO + HSO == CuSO + HO 2424(3)酸 + 碱 -------- 盐 + 水(中和反应)60.盐酸和烧碱起反应:HCl + NaOH == NaCl +HO261. 盐酸和氢氧化钙反应:2HCl + Ca(OH) == CaCl + 2HO 22262. 氢氧化铝药物治疗胃酸过多:3HCl + Al(OH) == AlCl + 3HO 23363. 硫酸和烧碱反应:HSO + 2NaOH == NaSO + 2HO 24422(4)酸 + 盐 -------- 另一种酸 + 另一种盐64.大理石与稀盐酸反应:CaCO + 2HCl == CaCl + HO + CO↑222365.碳酸钠与稀盐酸反应: NaCO + 2HCl == 2NaCl + HO + CO↑232266.碳酸氢钠与稀盐酸反应:NaHCO + HCl== NaCl + HO + CO↑22367. 硫酸和氯化钡溶液反应:HSO + BaCl == BaSO↓+ 2HCl 4 4222、碱的化学性质(1)碱 + 非金属氧化物 -------- 盐 + 水68.苛性钠暴露在空气中变质:2NaOH + CO == NaCO + HO 223269.苛性钠吸收二氧化硫气体:2NaOH + SO == NaSO+ HO 23 2270.苛性钠吸收三氧化硫气体:2NaOH + SO == NaSO + HO 223471.消石灰放在空气中变质:Ca(OH) + CO == CaCO ↓+ HO 222372. 消石灰吸收二氧化硫:Ca(OH) + SO == CaSO ↓+ HO2322.(2)碱 + 酸-------- 盐 + 水(中和反应,方程式见上)(3)碱 + 盐 -------- 另一种碱 + 另一种盐73. 氢氧化钙与碳酸钠:Ca(OH) + Na2CO == CaCO↓+ 2NaOH 3323、盐的化学性质(1)盐(溶液) + 金属单质------- 另一种金属 + 另一种盐74. 铁和硫酸铜溶液反应:Fe + CuSO == FeSO+ Cu 4 4(2)盐 + 酸-------- 另一种酸 + 另一种盐75.碳酸钠与稀盐酸反应: NaCO + 2HCl == 2NaCl + HO + CO↑2232碳酸氢钠与稀盐酸反应:NaHCO + HCl== NaCl + HO + CO↑223(3)盐 + 碱 -------- 另一种碱 + 另一种盐76. 氢氧化钙与碳酸钠:Ca(OH) + NaCO == CaCO↓+ 2NaOH 3232(4)盐 + 盐 ----- 两种新盐77.氯化钠溶液和硝酸银溶液:NaCl + AgNO == AgCl↓ + NaNO 3378.硫酸钠和氯化钡:NaSO+ BaCl == BaSO↓ + 2NaCl 44 22附:初中化学方程式大全化合反应2MgO 1、镁在空气中燃烧:2Mg+O2FeO 2、铁在氧气中燃烧:3Fe+2O4232AlO3、铝在空气中燃烧:4Al+3O 3222H+O2H4、氢气在空气中燃烧:O 2222P、红磷在空气中燃烧:54P+5OO 522.SO 、硫粉在空气中燃烧:S+O622CO 7、碳在氧气中充分燃烧:C+O222CO 8、碳在氧气中不充分燃烧:2C+O22CO C+CO、二氧化碳通过灼热碳层:9 22CO10、一氧化碳在氧气中燃烧:2CO+O 2211、二氧化碳和水反应(二氧化碳通入紫色石蕊试液):CO+HO==HCO 322212、生石灰溶于水:CaO+HO==Ca(OH) 2213、无水硫酸铜作干燥剂:CuSO+5HO==CuSO·5HO 24242Na+Cl2NaCl 14、钠在氯气中燃烧:2分解反应2HO+OO15、实验室用双氧水制氧气:2H↑2222K2MnO4+MnO2+O2↑16、加热高锰酸钾:2KMnO42H2O、水在直流电的作用下分解:17 2H2↑+O2↑18、碳酸不稳定而分解:H2CO3==H2O+CO2↑CaCO3 Ca:19、高温煅烧石灰石(二氧化碳工业制法)O+CO2↑置换反应20、铁和硫酸铜溶液反应:Fe+CuSO4==FeSO4+Cu21、锌和稀硫酸反应(实验室制氢气):Zn+H2SO4==ZnSO4+H2↑22、镁和稀盐酸反应:Mg+2HCl==MgCl2+H2↑H2+CuO 23、氢气还原氧化铜:Cu+H2O2Cu+CO2↑C+2CuO 24、木炭还原氧化铜:H2+CO 、水蒸气通过灼热碳层:H2O+C254Fe+3CO2↑26、焦炭还原氧化铁:3C+2Fe2O3其他27.氢氧化钠溶液与硫酸铜溶液反应:2NaOH+CuSO4==Cu(OH)2↓+Na2SO4CH4+2O2 28、甲烷在空气中燃烧:CO2+2H2O2CO2+3H2OC2H5OH+3O2、酒精在空气中燃烧:29.CO+CuO 、一氧化碳还原氧化铜:Cu+CO2302Fe+3CO23CO+Fe2O331、一氧化碳还原氧化铁:32、二氧化碳通过澄清石灰水(检验二氧化碳):Ca(OH)2+CO2==CaCO3↓+H2O33、氢氧化钠和二氧化碳反应(除去二氧化碳):2NaOH+CO2==Na2CO3+H2O34、石灰石(或大理石)与稀盐酸反应(二氧化碳的实验室制法):CaCO3+2HCl==CaCl2+H2O+CO2↑35、碳酸钠与浓盐酸反应(泡沫灭火器的原理): Na2CO3+2HCl==2NaCl+H2O+CO2↑一.物质与氧气的反应:⑴单质与氧气的反应:2Mg+O2 1. 镁在空气中燃烧:2MgOFe3O4 铁在氧气中燃烧:3Fe+2O22.铜在空气中受热:3. 2CuO2Cu+O22Al2O3 4. 铝在空气中燃烧:4Al+3O22H2O 2H2+O2氢气中空气中燃烧:5.2P2O5 6. 红磷在空气中燃烧:4P+5O2SO2 S+O2硫粉在空气中燃烧:7.CO2 8. 碳在氧气中充分燃烧:C+O22CO碳在氧气中不充分燃烧:2C+O29.⑵化合物与氧气的反应:2CO2 10. 一氧化碳在氧气中燃烧:2CO+O2CO2+2H2O11. 甲烷在空气中燃烧:CH4+2O22CO2+3H2O酒精在空气中燃烧:12. C2H5OH+3O2 二.几个分解反应:2H2↑+O2↑13. 水在直流电的作用下分解:2H2OCu2(OH)2CO3加热碱式碳酸铜:2CuO+H2O+CO2↑14.2KClO3:加热氯酸钾(有少量的二氧化锰)15. 2KCl+3O2↑2KMnO4K2MnO4+MnO2+O2↑16. 加热高锰酸钾:17. 碳酸不稳定而分解:H2CO3==H2O+CO2↑CaCO3 高温煅烧石灰石:CaO+CO2↑18.三.几个氧化还原反应:Cu+H2O 19. 氢气还原氧化铜:H2+CuO2Cu+CO2↑C+2CuO 20. 木炭还原氧化铜:21. 焦炭还原氧化铁:4Fe+3CO2↑3C+2Fe2O322. 焦炭还原四氧化三铁:3Fe+2CO2↑2C+Fe3O4Cu+CO223. 一氧化碳还原氧化铜:CO+CuO2Fe+3CO23CO+Fe2O324. 一氧化碳还原氧化铁:3Fe+4CO225. 一氧化碳还原四氧化三铁:4CO+Fe3O4四.单质、氧化物、酸、碱、盐的相互关系⑴金属单质+ 酸--------盐+ 氢气(置换反应)26. 锌和稀硫酸Zn+H2SO4==ZnSO4+H2↑27. 铁和稀硫酸Fe+H2SO4==FeSO4+H2↑28. 镁和稀硫酸Mg+H2SO4==MgSO4+H2↑29. 铝和稀硫酸2Al+3H2SO4==Al2(SO4)3+3H2↑30. 锌和稀盐酸Zn+2HCl==ZnCl2+H2↑31. 铁和稀盐酸Fe+2HCl==FeCl2+H2↑32. 镁和稀盐酸Mg+2HCl==MgCl2+H2↑33. 铝和稀盐酸2Al+6HCl==2AlCl3+3H2↑⑵金属单质+ 盐(溶液)-------另一种金属+ 另一种盐34. 铁和硫酸铜溶液反应:Fe+CuSO4==FeSO4+Cu35. 锌和硫酸铜溶液反应:Zn+CuSO4==ZnSO4+Cu36. 铜和硝酸汞溶液反应:Cu+Hg(NO3)2==Cu(NO3)2+Hg⑶碱性氧化物+酸--------盐+ 水37. 氧化铁和稀盐酸反应:Fe2O3+6HCl==2FeCl3+3H2O38. 氧化铁和稀硫酸反应:Fe2O3+3H2SO4==Fe2(SO4)3+3H2O39. 氧化铜和稀盐酸反应:CuO+2HCl==CuCl2+H2O40. 氧化铜和稀硫酸反应:CuO+H2SO4==CuSO4+H2O41. 氧化镁和稀硫酸反应:MgO+H2SO4==MgSO4+H2O42. 氧化钙和稀盐酸反应:CaO+2HCl==CaCl2+H2O⑷酸性氧化物+碱--------盐+ 水43.苛性钠暴露在空气中变质:2NaOH+CO2==Na2CO3+H2O2NaOH+SO2==Na2SO3+H2O.苛性钠吸收二氧化硫气体:44.45.苛性钠吸收三氧化硫气体:2NaOH+SO3==Na2SO4+H2O 46.消石灰放在空气中变质:Ca(OH)2+CO2==CaCO3↓+H2O47. 消石灰吸收二氧化硫:Ca(OH)2+SO2==CaSO3↓+H2O⑸酸+ 碱--------盐+ 水48.盐酸和烧碱起反应:HCl+NaOH==NaCl+H2O49. 盐酸和氢氧化钾反应:HCl+KOH==KCl+H2O50.盐酸和氢氧化铜反应:2HCl+Cu(OH)2==CuCl2+2H2O51. 盐酸和氢氧化钙反应:2HCl+Ca(OH)2==CaCl2+2H2O52. 盐酸和氢氧化铁反应:3HCl+Fe(OH)3==FeCl3+3H2O53.氢氧化铝药物治疗胃酸过多:3HCl+Al(OH)3==AlCl3+3H2O54.硫酸和烧碱反应:H2SO4+2NaOH==Na2SO4+2H2O55.硫酸和氢氧化钾反应:H2SO4+2KOH==K2SO4+2H2O56.硫酸和氢氧化铜反应:H2SO4+Cu(OH)2==CuSO4+2H2O57.硫酸和氢氧化铁反应:3H2SO4+2Fe(OH)3==Fe2(SO4)3+ 6H2O58.硝酸和烧碱反应:HNO3+NaOH==NaNO3+H2O⑹酸+ 盐--------另一种酸+ 另一种盐59.大理石与稀盐酸反应:CaCO3+2HCl==CaCl2+H2O+CO2↑60.碳酸钠与稀盐酸反应: Na2CO3+2HCl==2NaCl+H2O+CO2↑61.碳酸镁与稀盐酸反应: MgCO3+2HCl==MgCl2+H2O+CO2↑62.盐酸和硝酸银溶液反应:HCl+AgNO3==AgCl↓+HNO363.硫酸和碳酸钠反应:Na2CO3+H2SO4==Na2SO4+H2O+CO2↑64.硫酸和氯化钡溶液反应:H2SO4+BaCl2==BaSO4↓+2HCl⑺碱+ 盐--------另一种碱+ 另一种盐65.氢氧化钠与硫酸铜:2NaOH+CuSO4==Cu(OH)2↓+Na2SO466.氢氧化钠与氯化铁:3NaOH+FeCl3==Fe(OH)3↓+3NaCl67.氢氧化钠与氯化镁:2NaOH+MgCl2==Mg(OH)2↓+2NaCl68. 氢氧化钠与氯化铜:2NaOH+CuCl2==Cu(OH)2↓+2NaCl69. 氢氧化钙与碳酸钠:Ca(OH)2+Na2CO3==CaCO3↓+2NaOH⑻盐+ 盐-----两种新盐70.氯化钠溶液和硝酸银溶液:NaCl+AgNO3==AgCl↓+NaNO371.硫酸钠和氯化钡:Na2SO4+BaCl2==BaSO4↓+2NaCl五.其它反应:72.二氧化碳溶解于水:CO2+H2O==H2CO373.生石灰溶于水:CaO+H2O==Ca(OH)274.氧化钠溶于水:Na2O+H2O==2NaOH75.三氧化硫溶于水:SO3+H2O==H2SO45H2OCuSO4+5H2O.硫酸铜晶体受热分解:CuSO4·7677.无水硫酸铜作干燥剂:CuSO4+5H2O==CuSO4·5H2O 化学方程式反应现象应用2Mg+O2 2MgO剧烈燃烧.耀眼白光.生成白色固体.放热.产生大量白烟白色信号弹拉瓦锡实验银白液体、生成红色固体2HgO2Hg+O2.2Cu+O2 2CuO红色金属变为黑色固体2Al2O3银白金属变为白色固体4Al+3O2Fe3O4剧烈燃烧、火星四射、生成黑色固体、放热3Fe+2O2CO2C+O2剧烈燃烧、白光、放热、使石灰水变浑浊SO2剧烈燃烧、放热、刺激味气体、空气中淡蓝色火焰.氧气中蓝紫色火焰S+O22H2O淡蓝火焰、放热、生成使无水CuSO42H2+O2变蓝的液体(水)高能燃料2P2O5 剧烈燃烧、大量白烟、放热、生成白色固体证明空气中氧气含量4P+5O22H2O+CO2 CH4+2O2蓝色火焰、放热、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)甲烷和天然气的燃烧2C2H2+5O2 2H2O+4CO2 蓝色火焰、放热、黑烟、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)氧炔焰、焊接切割金属2KClO3 2KCl+3O2↑生成使带火星的木条复燃的气体实验室制备氧气K2MnO4+MnO2+O2↑紫色变为黑色、生成使带火星木条复燃的气体2KMnO4实验室制备氧气红色变为银白、生成使带火星木条复燃的气体2HgO 拉瓦锡实验2Hg+O2↑2H2O 电解水2H2↑+O2↑水通电分解为氢气和氧气铜2CuO+H2O+CO2↑绿色变黑色、Cu2(OH)2CO3试管壁有液体、使石灰水变浑浊气体绿加热碳酸使石灰水变浑浊气体管壁有液体、↑+H2O+CO2↑NH4HCO3NH3白色固体消失、氢铵长期暴露空气中会消失Zn+H2SO4==ZnSO4+H2↑有大量气泡产生、锌粒逐渐溶解实验室制备氢气Fe+H2SO4==FeSO4+H2↑有大量气泡产生、金属颗粒逐渐溶解Mg+H2SO4==MgSO4+H2↑有大量气泡产生、金属颗粒逐渐溶解2Al+3H2SO4==Al2(SO4)3+3H2↑有大量气泡产生、金属颗粒逐渐溶解Fe2O3+3H2冶炼金属、利用氢气的红色逐渐变为银白色、试管壁有液体2Fe+3H2O还原性冶炼金属、利用氢气的黑色逐渐变为银白色、试管壁有液体3Fe+4H2O Fe3O4+4H2.还原性WO3+3H2 W+3H2O 冶炼金属钨、利用氢气的还原性Mo+3H2O 冶炼金属钼、利用氢气的还原性MoO3+3H22NaCl 剧烈燃烧、黄色火焰离子化合物的形成、2Na+Cl22HCl 苍白色火焰、瓶口白雾H2+Cl2 共价化合物的形成、制备盐酸CuSO4+2NaOH=Cu(OH)2↓+Na2SO4 蓝色沉淀生成、上部为澄清溶液质量守恒定律实验2C+O2 2CO煤炉中常见反应、空气污染物之一、煤气中毒原因2CO2蓝色火焰2CO+O2煤气燃烧2Cu+CO2↑黑色逐渐变为红色、产生使澄清石灰水变浑浊的气体冶炼金属C+CuO4Fe+3CO2↑冶炼金属2Fe2O3+3C3Fe+2CO2↑Fe3O4+2C 冶炼金属C+CO22COCO2+H2O==H2CO3碳酸使石蕊变红证明碳酸的酸性H2CO3CO2↑+H2O石蕊红色褪去Ca(OH)2+CO2==CaCO3↓+H2O澄清石灰水变浑浊应用CO2检验和石灰浆粉刷墙壁CaCO3+H2O+CO2==Ca(HCO3)2白色沉淀逐渐溶解溶洞的形成,石头的风化Ca(HCO3)2 CaCO3↓+H2O+CO2↑白色沉淀、产生使澄清石灰水变浑浊的气体水垢形成.钟乳石的形成2NaHCO3 Na2CO3+H2O+CO2↑产生使澄清石灰水变浑浊的气体小苏打蒸馒头CaO+CO2↑工业制备二氧化碳和生石灰CaCO3CaCO3+2HCl==CaCl2+H2O+CO2↑固体逐渐溶解、有使澄清石灰水变浑浊的气体实验室制备二氧化碳、除水垢Na2CO3+H2SO4==Na2SO4+H2O+CO2↑固体逐渐溶解、有使澄清石灰水变浑浊的气体泡沫灭火器原理Na2CO3+2HCl==2NaCl+H2O+CO2↑固体逐渐溶解、有使澄清石灰水变浑浊的气体泡沫灭火器原理MgCO3+2HCl==MgCl2+H2O+CO2↑固体逐渐溶解、有使澄清石灰水变浑浊的气体冶炼金属黑色逐渐变红色,产生使澄清石灰水变浑浊的气体Cu+CO2CuO+CO.Fe2O3+3CO 2Fe+3CO2冶炼金属原理3Fe+4CO2冶炼金属原理Fe3O4+4COW+3CO2冶炼金属原理WO3+3COCH3COOH+NaOH=CH3COONa+H2O2CH3OH+3O2 2CO2+4H2O2CO2+3H2O 蓝色火焰、产生使石灰水变浑浊的气体、C2H5OH+3O2放热酒精的燃烧Fe+CuSO4==Cu+FeSO4银白色金属表面覆盖一层红色物质湿法炼铜、镀铜Mg+FeSO4==Fe+MgSO4溶液由浅绿色变为无色Cu+Hg(NO3)2==Hg+Cu(NO3)2Cu+2AgNO3==2Ag+Cu(NO3)2红色金属表面覆盖一层银白色物质镀银Zn+CuSO4==Cu+ZnSO4青白色金属表面覆盖一层红色物质镀铜Fe2O3+6HCl==2FeCl3+3H2O铁锈溶解、溶液呈黄色铁器除锈Al2O3+6HCl==2AlCl3+3H2O白色固体溶解Na2O+2HCl==2NaCl+H2O白色固体溶解CuO+2HCl==CuCl2+H2O黑色固体溶解、溶液呈蓝色ZnO+2HCl==ZnCl2+H2O白色固体溶解MgO+2HCl==MgCl2+H2O白色固体溶解CaO+2HCl==CaCl2+H2O白色固体溶解NaOH+HCl==NaCl+H2O白色固体溶解Cu(OH)2+2HCl==CuCl2+2H2O蓝色固体溶解Mg(OH)2+2HCl==MgCl2+2H2O白色固体溶解Al(OH)3+3HCl==AlCl3+3H2O白色固体溶解胃舒平治疗胃酸过多Fe(OH)3+3HCl==FeCl3+3H2O红褐色沉淀溶解、溶液呈黄色Ca(OH)2+2HCl==CaCl2+2H2OHCl+AgNO3==AgCl↓+HNO3 生成白色沉淀、不溶解于稀硝酸检验Cl—的原理Fe2O3+3H2SO4= Fe2(SO4)3+3H2O 铁锈溶解、溶液呈黄色铁器除锈Al2O3+3H2SO4==Al2(SO4)3+3H2O白色固体溶解CuO+H2SO4==CuSO4+H2O黑色固体溶解、溶液呈蓝色ZnO+H2SO4==ZnSO4+H2O白色固体溶解MgO+H2SO4==MgSO4+H2O白色固体溶解2NaOH+H2SO4==Na2SO4+2H2OCu(OH)2+H2SO4==CuSO4+2H2O蓝色固体溶解Ca(OH)2+H2SO4==CaSO4+2H2OMg(OH)2+H2SO4==MgSO4+2H2O白色固体溶解2Al(OH)3+3H2SO4==Al2(SO4)3+3H2O白色固体溶解2Fe(OH)3+3H2SO4==Fe2(SO4)3+3H2O红褐色沉淀溶解、溶液呈黄色Ba(OH)2+H2SO4==BaSO4↓+2H2O 生成白色沉淀、不溶解于稀硝酸检验SO42—的原理BaCl2+H2SO4==BaSO4↓+2HCl生成白色沉淀、不溶解于稀硝酸检验SO42—的原理的原理—SO42检验生成白色沉淀、不溶解于稀硝酸Ba(NO3)2+H2SO4==BaSO4↓+2HNO3.Na2O+2HNO3==2NaNO3+H2O白色固体溶解CuO+2HNO3==Cu(NO3)2+H2O黑色固体溶解、溶液呈蓝色ZnO+2HNO3==Zn(NO3)2+H2O白色固体溶解MgO+2HNO3==Mg(NO3)2+H2O白色固体溶解CaO+2HNO3==Ca(NO3)2+H2O白色固体溶解NaOH+HNO3==NaNO3+H2OCu(OH)2+2HNO3==Cu(NO3)2+2H2O蓝色固体溶解Mg(OH)2+2HNO3==Mg(NO3)2+2H2O白色固体溶解Al(OH)3+3HNO3==Al(NO3)3+3H2O白色固体溶解Ca(OH)2+2HNO3==Ca(NO3)2+2H2OFe(OH)3+3HNO3==Fe(NO3)3+3H2O红褐色沉淀溶解、溶液呈黄色3NaOH+H3PO4==3H2O+Na3PO43NH3+H3PO4==(NH4)3PO42NaOH+CO2==Na2CO3+H2O 吸收CO、O2、H2中的CO22NaOH+SO2==Na2SO3+H2O 2NaOH+SO3==Na2SO4+H2O 处理硫酸工厂的尾气(SO2)FeCl3+3NaOH==Fe(OH)3↓+3NaCl 溶液黄色褪去、有红褐色沉淀生成AlCl3+3NaOH==Al(OH)3↓+3NaCl有白色沉淀生成MgCl2+2NaOH==Mg(OH)2↓+2NaClCuCl2+2NaOH==Cu(OH)2↓+2NaCl溶液蓝色褪去、有蓝色沉淀生成CaO+ H2O==Ca(OH)2白色块状固体变为粉末、生石灰制备石灰浆Ca(OH)2+SO2==CaSO3↓+H2O有白色沉淀生成初中一般不用Ca(OH)2+Na2CO3==CaCO3↓+2NaOH有白色沉淀生成工业制烧碱、实验室制少量烧碱Ba(OH)2+Na2CO3==BaCO3↓+2NaOH有白色沉淀生成Ca(OH)2+K2CO3==CaCO3↓+2KOH有白色沉淀生成CuSO4+5H2O==CuSO4·H2O蓝色晶体变为白色粉末CuSO4+H2O CuSO4+5H2O 白色粉末变为蓝色检验物质中是否含有水AgNO3+NaCl==AgCl↓+NaNO3白色不溶解于稀硝酸的沉淀(其他氯化物类似反应)应用于检验溶液中的氯离子BaCl2+Na2SO4==BaSO4↓+2NaCl白色不溶解于稀硝酸的沉淀(其他硫酸盐类似反应)应用于检验硫酸根离子CaCl2+Na2CO3==CaCO3↓+2NaCl有白色沉淀生成MgCl2+Ba(OH)2==BaCl2+Mg(OH)2↓有白色沉淀生成CaCO3+2HCl==CaCl2+H2O+CO2↑MgCO3+2HCl==MgCl2+H2O+ CO2↑NH4NO3+NaOH==NaNO3+NH3↑+H2O生成使湿润石蕊试纸变蓝色的气体应用于检验溶液中的铵根离子NH4Cl+KOH==KCl+NH3↑+H2O生成使湿润石蕊试纸变蓝色的气体。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
初三化學の所有化學方程式
化合反應 1、鎂在空氣中燃燒: 2Mg + O2 點燃 2MgO 2、鐵在氧氣中燃燒: 3Fe + 2O2 點燃 Fe3O4 3、鋁在空氣中燃燒: 4Al + 3O2 點燃 2Al2O3 4、氫氣在空氣中燃燒: 2H2 + O2 點燃 2H2O 5、紅磷在空氣中燃燒: 4P + 5O2 點燃 2P2O5 6、硫粉在空氣中燃燒: S + O2 點燃 SO2 7、碳在氧氣中充分燃燒: C + O2 點燃 CO2 8、碳在氧氣中不充分燃燒: 2C + O2 點燃 2CO 9、二氧化碳通過灼熱碳層: C + CO2 高溫 2CO 10、一氧化碳在氧氣中燃燒: 2CO + O2 點燃 2CO2 11、二氧化碳和水反應(二氧化碳通入紫色石蕊試液): CO2 + H2O === H2CO3 12、生石灰溶於水: CaO + H2O === Ca(OH)2 13、無水硫酸銅作乾燥劑: CuSO4 + 5H2O ==== CuSO·4 5H2O 14、鈉在氯氣中燃燒: 2Na + Cl2 點燃 2NaCl
分解反應 15、實驗室用雙氧水制氧氣: 2H2O2 MnO2 2H2O+ O↑2 16、加熱高錳酸鉀: 2KMnO4加熱 K2MnO4 + MnO2 + O↑2 17、水在直流電の作用下分解: 2H2O通電 2H2↑+ O2 ↑ 18、碳酸不穩定而分解: H2CO3 === H2O + CO↑2 19、高溫煆燒石灰石(二氧化碳工業制法): CaCO3高溫 CaO + CO2↑
化學方程式 反應現象 應用 2Mg+O2點燃或 Δ2MgO劇烈燃燒 . 耀眼白光 . 生成白色固體 . 放熱 . 產生大量白煙 白色信號彈 2Hg+O2點燃或 Δ2HgO銀白液體、生成紅色固體 拉瓦錫實驗 2Cu+O2點燃或 Δ2CuO紅色金屬變為黑色固體 4Al+3O2點燃或 Δ2Al2O3 銀白金屬變為白色固體 3Fe+2O2點燃 Fe3O4 劇烈燃燒、火星四射、生成黑色固體、放熱 4Fe + 3O2 高 溫 2Fe2O3 C+O2點燃 CO2劇烈燃燒、白光、放熱、使石灰水變渾濁 S+O2 點燃 SO2 劇烈燃燒、放熱、刺激味氣體、空氣中淡藍色火焰 . 氧氣中藍紫 色火焰 2H2+O2點燃 2H2O淡藍火焰、放熱、生成使無水 CuSO4變藍の液體(水) 高能 燃料 4P+5O2點燃 2P2O5 劇烈燃燒、大量白煙、放熱、生成白色固體 證明空氣中氧 氣含量 CH4+2O2點燃 2H2O+CO2藍色火焰、放熱、生成使石灰水變渾濁氣體和使無水 CuSO4變藍の液體(水) 甲烷和天然氣の燃燒 2C2H2+5O2點燃 2H2O+4CO2藍色火焰、 放熱、 黑煙、 生成使石灰水變渾濁氣體和 使無水 CuSO4變藍の液體(水) 氧炔焰、焊接切割金屬 2KClO3MnO2Δ2KCl +3O2↑ 生成使帶火星の木條複燃の氣體 實驗室製備氧氣 2KMnOΔ4 K2MnO4+MnO2+↑O2 紫色變為黑色、生成使帶火星木條複燃の氣體 實 驗室製備氧氣 2HgOΔ2Hg+O↑2 紅色變為銀白、生成使帶火星木條複燃の氣體 拉瓦錫實驗 2H2O通電 2H2↑+O2↑ 水通電分解為氫氣和氧氣 電解水 Cu2(OH)2COΔ3 2CuO+H2O+C↑O2綠色變黑色、 試管壁有液體、 使石灰水變渾濁氣 體 銅綠加熱
Fpg
Fpg
35、石灰石(或大理石) 與稀鹽酸反應 (二氧化碳の實驗室制法) :CaCO3+ 2HCl === CaCl2 + H2O + CO2↑ 36、碳酸鈉與濃鹽酸反應(泡沫滅火器の原理) : Na2CO3+ 2HCl ===2NaCl + H2O + CO2↑
一. 物質與氧氣の反應: ( 1)單質與氧氣の反應: 1. 鎂在空氣中燃燒: 2Mg + O2 點燃 2MgO 2. 鐵在氧氣中燃燒: 3Fe + 2O2 點燃 Fe3O4 3. 銅在空氣中受熱: 2Cu + O2 加熱 2CuO 4. 鋁在空氣中燃燒: 4Al + 3O2 點燃 2Al2O3 5. 氫氣中空氣中燃燒: 2H2 + O2 點燃 2H2O 6. 紅磷在空氣中燃燒: 4P + 5O2 點燃 2P2O5 7. 硫粉在空氣中燃燒: S + O2 點燃 SO2 8. 碳在氧氣中充分燃燒: C + O2 點燃 CO2 9. 碳在氧氣中不充分燃燒: 2C + O2 點燃 2CO ( 2)化合物與氧氣の反應: 10. 一氧化碳在氧氣中燃燒: 2CO + O2 點燃 2CO2 11. 甲烷在空氣中燃燒: CH4 + 2O2 點燃 CO2 + 2H2O 12. 酒精在空氣中燃燒: C2H5OH + 3O2點燃 2CO2 + 3H2O 二.幾個分解反應: 13. 水在直流電の作用下分解: 2H2O通電 2H2↑+ O2 ↑ 14. 加熱堿式碳酸銅: Cu2(OH)2CO3加熱 2CuO + H2O + CO2↑ 15. 加熱氯酸鉀(有少量の二氧化錳): 2KClO3 ==== 2KCl + 3O2 ↑ 16. 加熱高錳酸鉀: 2KMnO4加熱 K2MnO4 + MnO2 + O↑2 17. 碳酸不穩定而分解: H2CO3 === H2O +CO2↑ 18. 高溫煆燒石灰石: CaCO3高溫 CaO + CO2↑ 三.幾個氧化還原反應: 19. 氫氣還原氧化銅: H2 + CuO 加熱 Cu + H2O 20. 木炭還原氧化銅: C+ 2CuO 高溫 2Cu + CO2↑ 21. 焦炭還原氧化鐵: 3C+ 2Fe2O3 高溫 4Fe + 3CO2↑ 22. 焦炭還原四氧化三鐵: 2C+ Fe3O4 高溫 3Fe + 2CO2↑ 23. 一氧化碳還原氧化銅: CO+ CuO加熱 Cu + CO2 24. 一氧化碳還原氧化鐵: 3CO+ Fe2O3高溫 2Fe + 3CO2 25. 一氧化碳還原四氧化三鐵: 4CO+ Fe3O4高溫 3Fe + 4CO2 四.單質、氧化物、酸、堿、鹽の相互關係 ( 1)金屬單質 + 酸 -------- 鹽 + 氫氣 (置換反應) 26. 鋅和稀硫酸 Zn + H2SO4 = ZnSO4 + H2↑ 27. 鐵和稀硫酸 Fe + H2SO4 = FeSO4 + H2↑ 28. 鎂和稀硫酸 Mg + H2SO4 = MgSO4 + H2↑ 29. 鋁和稀硫酸 2Al +3H2SO4 = Al2(SO4)3 +3H2↑ 30. 鋅和稀鹽酸 Zn + 2HCl === ZnCl2 + H2 ↑ 31. 鐵和稀鹽酸 Fe + 2HCl === FeCl2 + H2 ↑ 32. 鎂和稀鹽酸 Mg+ 2HCl === MgCl2 + H2 ↑
Fpg
Fpg
70.氯化鈉溶液和硝酸銀溶液: NaCl + AgNO3 ==== AgCl↓ + NaNO3 71.硫酸鈉和氯化鋇: Na2SO4 + BaCl2 ==== BaSO4↓ + 2NaCl 五.其他反應: 72.二氧化碳溶解於水: CO2 + H2O === H2CO3 73.生石灰溶於水: CaO + H2O === Ca(OH)2 74.氧化鈉溶於水: Na2O + H2O ==== 2NaOH 75.三氧化硫溶於水: SO3 + H2O ==== H2SO4 76.硫酸銅晶體受熱分解: CuSO·4 5H2O加熱 CuSO4 + 5H2O 77.無水硫酸銅作乾燥劑: CuSO4 + 5H2O ==== CuSO·4 5H2
置換反應 20、鐵和硫酸銅溶液反應: Fe + CuSO4 == FeSO4 + Cu 21、鋅和稀硫酸反應(實驗室制氫氣): Zn + H2SO4 == ZnSO4 + H2↑ 22、鎂和稀鹽酸反應: Mg+ 2HCl === MgCl2 + H2 ↑ 23、氫氣還原氧化銅: H2 + CuO 加熱 Cu + H2O 24、木炭還原氧化銅: C+ 2CuO 高溫 2Cu + CO2↑ 25、甲烷在空氣中燃燒: CH4 + 2O2 點燃 CO2 + 2H2O 26、水蒸氣通過灼熱碳層: H2O + C 高溫 H2 + CO 27、焦炭還原氧化鐵: 3C+ 2Fe2O3 高溫 4Fe + 3CO2↑
Fpg
Fpg
33. 鋁和稀鹽酸 2Al + 6HCl == 2AlCl3 + 3H2 ↑ ( 2)金屬單質 + 鹽(溶液) ------- 另一種金屬 + 另一種鹽 34. 鐵和硫酸銅溶液反應: Fe + CuSO4 === FeSO4 + Cu 35. 鋅和硫酸銅溶液反應: Zn + CuSO4 === ZnSO4 + Cu 36. 銅和硝酸汞溶液反應: Cu + Hg(NO3)2 === Cu(NO3)2 + Hg ( 3)鹼性氧化物 + 酸 -------- 鹽 + 水 37. 氧化鐵和稀鹽酸反應: Fe2O3 + 6HCl === 2FeCl3 + 3H2O 38. 氧化鐵和稀硫酸反應: Fe2O3 + 3H2SO4 === Fe2(SO4)3 + 3H2O 39. 氧化銅和稀鹽酸反應: CuO + 2HCl ==== CuCl2 + H2O 40. 氧化銅和稀硫酸反應: CuO + H2SO4 ==== CuSO4 + H2O 41. 氧化鎂和稀硫酸反應: MgO + H2SO4 ==== MgSO4 + H2O 42. 氧化鈣和稀鹽酸反應: CaO + 2HCl ==== CaCl2 + H2O ( 4)酸性氧化物 + 堿 -------- 鹽 + 水 43.苛性鈉暴露在空氣中變質: 2NaOH + CO2 ==== Na2CO3 + H2O 44.苛性鈉吸收二氧化硫氣體: 2NaOH + SO2 ==== Na2SO3 + H2O 45.苛性鈉吸收三氧化硫氣體: 2NaOH + SO3 ==== Na2SO4 + H2O 46.消石灰放在空氣中變質: Ca(OH)2 + CO2 ==== CaCO3↓+ H2O 47. 消石灰吸收二氧化硫: Ca(OH)2 + SO2 ==== CaSO3↓+ H2O ( 5)酸 + 堿 -------- 鹽 + 水 48.鹽酸和燒鹼起反應: HCl + NaOH ==== NaCl +H2O 49. 鹽酸和氫氧化鉀反應: HCl + KOH ==== KCl +H2O 50.鹽酸和氫氧化銅反應: 2HCl + Cu(OH)2 ==== CuCl2 + 2H2O 51. 鹽酸和氫氧化鈣反應: 2HCl + Ca(OH)2 ==== CaCl2 + 2H2O 52. 鹽酸和氫氧化鐵反應: 3HCl + Fe(OH)3 ==== FeCl3 + 3H2O 53. 氫氧化鋁藥物治療胃酸過多: 3HCl + Al(OH)3 ==== AlCl3 + 3H2O 54. 硫酸和燒鹼反應: H2SO4 + 2NaOH ==== Na2SO4 + 2H2O 55. 硫酸和氫氧化鉀反應: H2SO4 + 2KOH ==== K2SO4 + 2H2O 56. 硫酸和氫氧化銅反應: H2SO4 + Cu(OH)2 ==== CuSO4 + 2H2O 57. 硫酸和氫氧化鐵反應: 3H2SO4 + 2Fe(OH)3==== Fe2(SO4)3 + 6H2O 58. 硝酸和燒鹼反應: HNO3+ NaOH ==== NaNO3 +H2O ( 6)酸 + 鹽 -------- 另一種酸 + 另一種鹽 59.大理石與稀鹽酸反應: CaCO3 + 2HCl === CaCl2 + H2O + CO2↑ 60.碳酸鈉與稀鹽酸反應 : Na2CO3 + 2HCl === 2NaCl + H2O + CO 2↑ 61.碳酸鎂與稀鹽酸反應 : MgCO3 + 2HCl === MgCl2 + H2O + CO2 ↑ 62.鹽酸和硝酸銀溶液反應: HCl + AgNO3 === AgCl ↓ + HNO3 63. 硫酸和碳酸鈉反應: Na2CO3 + H2SO4 === Na2SO4 + H2O + CO↑2 64. 硫酸和氯化鋇溶液反應: H2SO4 + BaCl2 ==== BaSO4 ↓+ 2HCl ( 7)堿 + 鹽 -------- 另一種堿 + 另一種鹽 65.氫氧化鈉與硫酸銅: 2NaOH + CuSO4==== Cu(OH)2↓ + Na2SO4 66.氫氧化鈉與氯化鐵: 3NaOH + FeCl3 ==== Fe(OH)3↓ + 3NaCl 67.氫氧化鈉與氯化鎂: 2NaOH + MgCl2 ==== Mg(OH)2↓ + 2NaCl 68. 氫氧化鈉與氯化銅: 2NaOH + CuCl2 ==== Cu(OH)2↓ + 2NaCl 69. 氫氧化鈣與碳酸鈉: Ca(OH)2 + Na2CO3 === CaCO↓3 + 2NaOH ( 8)鹽 + 鹽 ----- 兩種新鹽
