有机化学第三版答案 南开大学出版社第十四章
有机化学第三版答案-上册--南开大学出版社--王积涛等主编

3,3-二甲基戊烷 3,3-dimethylpentane
8)
CH3CH2∣ CHCH2CH3 ∣CH2
CH3
3-乙基戊烷 3-ethylpentane
9)CH3
∣ CH3
C ∣
CH ∣
CH3
CH3 CH3
2,2,3-三甲基丁烷 2,2,3-trimethylbutane
1) 链引发
1 3 0 ℃
① ( C H 3 ) 3 C O - O C ( C H 3 ) 3
2 ( C H 3 ) 3 C O
︱ C H 3
② (C H 3 )3 C O+C H 3 -︱ C -C H 3
(C H 3 )3 C -O H+C H 3 -︱ C H -C H 3
2) 链增长
H
5 0 %
⑶
δ-
δ+
H3C __ Li
δ-
δ+
⑷ NH2 __ H
⑸
δ+
H3C
__
δ-
OH
δ-
δ+
(6) H3C __ MgBr
10、H2N-是一个比HO-更强的碱,对它们的共轭酸NH3 和H2O哪个酸性更强?为什麽?
答:H2O的酸性更强。共轭碱的碱性弱,说明它保 持负电荷的能力强,其相应的共轭酸就更容易 失去H+而显示酸性。
N a + - C N +C H 3 C O O H
p K a : 9 .2
p K a : 4 .7 2
反应向左(即向着生成HCN的方向)进行。
( 2 )C H 3 C H 2 O H +N a + - C N C H 3 C H 2 O - N a + +H C N
有机化学(第三版 马祥志主编)课后习题答案

第一章绪论习题参考谜底之迟辟智美创作1. 某化合物的分子量为60,含碳40.1%、含氮6.7%、含氧53.2%,确定该化合物的分子式.解:①由各元素的百分含量,根据下列计算求得实验式该化合物实验式为:CH2O②由分子量计算出该化合物的分子式该化合物的分子式应为实验式的2倍,即:C2H4O22. 在C—H、C—O、O—H、C—Br、C—N等共价键中,极性最强的是哪一个?解:由表1-4可以查得上述共价键极性最强的是O—H键.3. 将共价键⑴C—H⑵N—H⑶F—H⑷O—H按极性由年夜到小的顺序进行排列.解:根据电负性顺序F > O > N > C,可推知共价键的极性顺序为:F—H > O—H > N—H > C—H4. 化合物CH3Cl、CH4、CHBr3、HCl、CH3OCH3中,哪个是非极性分子?解:CH4分子为高度对称的正四面体空间结构,4个C—H的向量之和为零,因此是非极性分子.5. 指出下列化合物所含官能团的名称和该化合物所属类型.碳碳三键,炔烃羟基,酚酮基,酮羧基,羧酸醛基,醛羟基,醇氨基,胺6. 甲醚(CH3OCH3)分子中,两个O—C键的夹角为111.7°.甲醚是否为极性分子?若是,用暗示偶极矩的方向.解:氧原子的电负性年夜于碳原子的电负性,因此O—C键的偶极矩的方向是由碳原子指向氧原子.甲醚分子的偶极矩是其分子中各个共价键偶极矩的向量之和,甲醚分子中的两个O—C键的夹角为111.7°,显然分子是具有极性的,其偶极矩的方向如下图所示.7. 什么叫诱导效应?什么叫共轭效应?各举一例说明之.(研读教材第11~12页有关内容)8. 有机化学中的离子型反应与无机化学中的离子反应有何区别?解:无机化学中的离子反应是指有离子介入的反应,反应物中必需有离子.而有机化学中的离子型反应是指反应物结构中的共价键在反应过程中发生异裂,反应物自己其实不是一定是离子.第二章链烃习题参考谜底1. 写出分子式为C6H14的化合物的所有碳链异构体的构造式,并按系统命名法命名.解:①所有可能的碳架如下:②所有异构体的构造式及名称:己烷2—甲基戊烷3—甲基戊烷2,3—二甲基丁烷2,2—二甲基丁烷2. 写出下列化合物的结构式或名称,并指出分子中的1°、2°、3°、4°碳原子.3. 将下列化合物的结构式改写成键线式4. 写出分子式为C5H10的所有开链异构体的结构式,并用系统命名法命名.5. 完成下列反应式6. 用化学方法鉴别下列各组化合物(1) 乙烷、乙烯、乙炔解答:分别将三种气体通入溴水中,不能使溴水褪色的是乙烷.将能使溴水褪色的两种气体分别通入银氨溶液中,能使之发生白色沉淀的气体是乙炔,另一个是乙烯.(2) 丁烷、1—丁炔、2—丁炔解答:分别将三种待测物分别与高锰酸钾酸性溶液混合,不能使高锰酸钾紫红色褪色的是丁烷.将能使高锰酸钾褪色的两种待测物分别与银氨溶液混合,能使之发生白色沉淀的是1—丁炔,另一个是2—丁炔.(3) 1,3—丁二烯、1—丁炔解答:分别将两种待测物与氯化亚铜氨溶液混合,能使之发生棕红色色沉淀的是1—丁炔,另一个是1,3—丁二烯.7. 以乙炔、丙炔为原料,合成下列化合物(其他试剂任选).(1) 1,2—二氯乙烷(2) 异丙醇(3) 2,2—二氯丙烷(4) 乙烯基乙炔(5) 丙酮(6) 苯(7) 乙烯基乙醚8. 如何除去乙烷中含有的少量丙烯?解答:将含有少量丙烯的乙烷气体通入硫酸溶液中,其中的丙烯杂质因与硫酸发生加成反应而被吸收.9. 丁烷和异丁烷分子中哪个氢原子最容易发生卤代反应?为什么?解答:异丁烷分子中的叔氢原子最易发生卤代反应.有年夜量实验结果标明,在取代反应中,各种类型氢原子的反应活性顺序为:3°H > 2°H > 1°H .10. 用杂化轨事理论简述甲烷、乙烯、乙炔的分子结构.解答:(1) 甲烷的结构根据杂化轨事理论,甲烷分子中的碳原子采用sp3杂化,4个价电子分别位于4个sp3杂化轨道中.4个sp3杂化电子云在空间呈正四面体排布,各个sp3杂化电子云的年夜头分别指向四面体的四个极点.C与H成键时,4个H原子的s电子云沿着4个sp3杂化电子云的年夜头重叠形成4个s-sp3σ键,因此形成的甲烷分子是正四面体型的,键角为109°28/ .(2)乙烯的结构乙烯分子中的碳原子采用sp2杂化,4个价电子中有3个分别位于3个sp2杂化轨道中,1个位于2p轨道中.3个sp2杂化电子云在空间呈平面三角形分布,各sp2杂化电子云的年夜头指向三角形的3个极点,2p电子云对称轴垂直穿过3个sp2杂化电子云所在的平面.11. 乙烯和乙炔都能使溴水褪色,两者的反应速度有何区别?为什么会有此不°同?解答:乙烯使溴水褪色的速度较乙炔的快.乙炔碳碳键长(0.120nm)较乙烯碳碳键的键长(0.133nm)短,因此乙炔分子中的π键较乙烯的π键稳定,反应活性低、反应速度慢.12. 乙烯既能使高锰酸钾溶液褪色,也能使溴水褪色.这两个实验的实质有无区别?解答:这两个实验有着实质的区别,乙烯使高锰酸钾溶液褪色是因为乙烯与高锰酸钾发生了氧化还原反应,乙烯使高锰酸钾还原而褪色;乙烯使溴水褪色是因为乙烯与溴发生了加成反应,生成了无色的溴代烷烃.13. 写出分子式C4H6的开链构造异构体的结构式,并用系统命名法命名.1—丁炔2—丁炔1,3—丁二烯1,2—丁二烯14. A,B两化合物的分子式都是C6H12 ,A经臭氧化并与锌和酸反应后的乙醛和甲乙酮,B经高锰酸钾氧化只得丙酸,写出A和B的结构式.解答:顺—3—甲基—2—戊烯反—3—甲基—2—戊烯顺—3—己烯反—3—己烯15. 化合物A 和B 互为同分异构体,二者都能使溴水褪色,A 能与硝酸银的氨溶液反应而B 不能.A 用酸性高锰酸钾溶液氧化后生成(CH3)2CHCOOH 和CO2,B 用酸性高锰酸钾溶液氧化后生成CH3COCOOH 和CO2.试推测A 和B 的结构式和名称,并写出有关的反应式.解答: 化合物A 的有关反应式: 化合物B 的有关反应式:16. 某化合物分子量为82,每摩尔该化合物可吸收2摩尔氢,不与硝酸银的氨溶液反应,当他吸收1摩尔氢时,生成2,3—二甲基—1—丁烯.试写出该化合物的结构式. 解答: 第三章 脂环烃习题参考谜底1. 命名下列化合物2. 写出下列化合物的结构(1) 3—甲基环丁烯 (2) 5—甲基二环[]—2—辛烯3. 用化学方法鉴别下列各组化合物解答:将上述三种试剂分别通入溴水中,不能使溶液棕红色褪色的是CH3CH2CH3;将能使溴水褪色的两种试剂分别通入高锰酸钾酸性溶液中,能使溶液紫红色褪色的是CH3CH =CH2 .(2) 1,1—二甲基环丙烷和环戊烯A. B. CH 2 C CH CH 2CH 3(CH 3)2CHC CH 3—甲基—1—丁炔2—甲基—1,3—丁二烯 CH 2 C C CH 2CH 3CH 3解答:将两种试剂与高锰酸钾酸性溶液混合,能使溶液紫红色褪色的是环戊烯,不能使溶液褪色的是1,1—二甲基环丙烷.4. 完成下列反应式5. 完成苯基环丙烷与下列试剂的反应.(1) HCl(2) Cl2(Cl4)(3) Br2(FeBr3)(4) H2SO46. 回答下列问题:(1) 在环丙烷中含有少量杂质丙烯,在提纯环丙烷时如何去除杂质?解答:将含有少量丙烯杂质的环丙烷气体通入高锰酸钾溶液,丙烯因为与高锰酸钾反应而被溶液吸收去除,然后用排水集气法收集获得不含丙烯的环丙烷气体.(2) 解释环丙烷的稳定性解答:环丙烷的3个碳原子在同一平面上,其每一个碳原子的sp3杂化电子云夹角为105.5°.因此,当做键时,两个成键电子云是以弯曲方式重叠,形成“弯曲σ键”.与以“头仇家”方式正面重叠形成的一般σ键相比,弯曲σ键重叠水平低,而且具有恢复正常重叠方式的自在趋势力——张力,因此不稳定.环丙烷的3个“弯曲σ键”的不稳定决定了环丙烷分子的不稳定性,它容易发生开环加成反应.7. 有一化合物分子式为C7H14,此化合物发生如下反应:(1) 可以催化加氢,产物分子式为C7H16;(2) 在室温下不能使高锰酸钾溶液褪色;(3) 能与HBr 反应得产物2—溴—2,3—二甲基戊烷.写出该化合物的结构.解答: 或 第四章 芳香烃习题参考谜底 1. 命名下列化合物.对乙基甲苯 对异丙基甲苯 4—乙基—2—溴甲苯2—环戊基甲苯 对二氯苯 三苯甲基游离基6—溴—1—萘磺酸 2,4—二硝基甲苯2. 写出下列化合物的结构.(1) 间甲乙苯 (2) β-萘酚 (3) 4-氯-2,3-二硝基甲苯(4) 环戊二烯负离子 (5) 间二乙烯苯 (6) 邻二异丙苯(7) 6-氯-1-萘磺酸 (8) 环丙烯正离子3. 完成下列反应.4. 写出下列反应所需试剂,并完成反应,(1) 苯→甲苯→氯苄(2) 甲苯→苯甲酸→邻、对硝基苯甲酸(3) 硝基苯→间硝基氯苯(4) 萘→邻苯二甲酸5. 用化学方法鉴别下列各组化合物.CH 3CH 3CH 3H 3C H 3C CH 3CH 3(1) 甲苯、1-甲基环己烯、甲基环己烷解答:取三种待测物少许,分别与溴水混合,能使溴水迅速褪色的是1-甲基环己烯;将不能使溴水褪色的两种待测物分别与高锰酸钾溶液混合加热,能使高锰酸钾紫红色褪色的是甲苯,余者为甲基环己烷.(2) 苯、1,3-己二烯解答:取两种待测物少许,分别与高锰酸钾酸性溶液混合,能使溶液紫红色褪色的是1,3-己二烯.6. 二甲苯的邻、间、对位三个异构体,在进行硝化时,分别获得一个一硝基产物,二个一硝基产物和三个一硝基产物,写出相对应的二甲苯结构.解答:得一个硝基产物的是对二甲苯:得二个硝基产物的是邻二甲苯:得三个硝基产物的是间二甲苯:7. 依照亲电取代反应活性由强到弱的顺序排列下列化合物.(1) 甲苯、苯、氯苯、硝基苯、苯酚解答:亲电取代反应活性顺序为苯酚> 甲苯> 苯> 氯苯> 硝基苯(2) 溴苯、苯甲酸、间二甲苯、甲苯、间硝基苯甲酸解答:亲电取代反应活性顺序为间二甲苯> 甲苯> 溴苯> 苯甲酸> 间硝基苯甲酸8. 判断下列化合物有无芳香性.(1) 环戊二烯解答:环戊二烯分子中没有闭合的共轭年夜π健结构,故不具有芳香性.(2) 环戊二烯负离子解答:环戊二烯负离子具有闭合的6电子共轭年夜π健结构,且π电子数6符合“4n+2”.因此根据休克尔规则,环戊二烯负离子具有芳香性.(3) 环戊二烯正离子解答:环戊二烯正离子具有闭合的4电子共轭年夜π健结构,但其π电子数4不符合“4n+2”.因此根据休克尔规则,环戊二烯正离子不具有芳香性.(4) 1,2,3,4-四氢萘解答:1,2,3,4-四氢萘保管了一个完整的苯环,因此具有芳香性.(5) 1,3,5,7-环辛四烯解答:1,3,5,7-环辛四烯π电子数8不符合“4n+2”.因此根据休克尔规则,1,3,5,7-环辛四烯不具有芳香性.(6) 环丙烯正离子解答:环丙烯正离子具有闭合的2电子共轭年夜π健结构,且π电子数2符合“4n+2”.因此根据休克尔规则,环丙烯正离子具有芳香性.9. 以苯为主要原料合成下列化合物.(1) 叔丁基苯(2) 2,4-二硝基苯甲酸(3) 间硝基苯甲酸(4) 2-甲基-5-硝基苯磺酸(5) 环戊基苯10. 某芳烃A分子式为C8H10,被酸性高锰酸钾氧化生成份子式为C8H6O4的B.若将B进一步硝化,只获得一种一元硝化产物而无异构体,推出A、B的结构并写出反应式.解答:A和B的结构分别为:相关反应式如下:第五章芳香烃习题参考谜底1. 简述卤代烃的结构特点、分类,并举例说明.(拜会教材第62页)2. 写出分子式为C4H9Br所有异构体及名称,并指出它们分别属于伯、仲、叔卤烃的哪一种?解答:所有可能的碳链如下所有异构体如下1-溴丁烷2-溴丁烷2-甲基-1-溴丙烷2-甲基-2-溴丙烷(伯卤烃)(仲卤烃)(伯卤烃)(叔卤烃)3. 解释下列名词并举例说明:(1) 亲核试剂(2) 亲核取代反应(3) 反应底物(4) 中心碳原子(5) 离去基团(6) 消除反应(拜会教材)4. 叙述卤代烷的单分子亲核取代反应(SN1)机理和双分子亲核取代反应(SN2)机理.(拜会教材)解答:1.单分子亲核取代反应(SN1)以叔溴丁烷的水解反应为例加以讨论.叔溴丁烷的水解反应的分两步进行.第一步:叔丁基溴的C—Br键发生异裂,生成叔丁基碳正离子和溴负离子,此步反应的速率很慢.第二步:生成的叔丁基碳正离子很快地与进攻试剂结合生成叔丁醇.2. 双分子亲核取代反应(SN2)实验证明,溴甲烷水解反应的机制为SN2,反应一步完成:该反应的反应速率与溴甲烷和碱的浓度有关,称为双分子亲核取代反应,用SN2(2代表决定反应速率所涉及的两种分子)暗示.在该反应过程中,OH-从Br的反面进攻带部份正电荷的α-C,C—O键逐渐形成,C—Br键逐渐变弱形成一个过渡状态;然后C—Br键迅速断裂,C—O键形成,完成取代.5. 简述卤代烷的消除反应和亲核取代反应及二者之间的关系.(拜会教材)6. 用系统命名法命名下列化合物.(1)(2)(3)CH3C(CH3)2CH2Br CH3CH2CHBrCH2I CH2CHCH2CH3Cl2,2-二甲基-1-溴丙烷2-溴-1-碘丁烷1-苯基-2-氯丁烷3-甲基-3-碘-1-戊烯3-氯环己烯2-甲基-1-溴萘间溴甲苯1-环戊基-2-溴乙烷7. 写出下列化合物的结构式.(1) 二碘二溴甲烷(2) 叔丁基溴(3) 烯丙基氯(4) 氟烷(5) 1-溴-1-丙烯(6) 2,4-二氯甲苯(7) 苄基氯(8) 5-溴-1,3-环己二烯8. 完成下列反应式9. 完成下列转变解答:解答:解答:解答:10. 用化学方法鉴别下列各组化合物.(1) 氯苯、苄基氯、1-苯基-2-氯丙烷解答:各取待测物少许分别与硝酸银醇溶液混合,室温下立即发生白色沉淀的为苄基氯;加热后发生白色沉淀的为1-苯基-2-氯丙烷,余者为氯苯.(2) 溴苯、溴乙烯、异丙基溴解答:各取待测物少许分别与硝酸银醇溶液混合加热,发生淡黄色沉淀的为异丙基溴;将剩余2种待测物分别与高锰酸钾酸性溶液混合,能使高锰酸钾紫红色褪色的是溴乙烯,余者为溴苯.(3) 2-氯丙烯、2-氯丙烷、3-氯丙烯、3-碘环戊烯解答:各取待测物少许分别与硝酸银醇溶液混合,立即发生黄色沉淀的为3-碘环戊烯,立即发生白色沉淀的为3-氯丙烯,加热后发生白色沉淀的为2-氯丙烷,余者为2-氯丙烯.(4) 4-溴-1-丁炔、2-溴-2-丁烯、3-溴环戊烯解答:各取待测物少许分别与硝酸银醇溶液混合,立即发生淡黄色沉淀的为3-溴环戊烯,立即发生白色沉淀的为4-溴-1-丁炔,余者为2-溴-2-丁烯.11. 下列卤代烃与氢氧化钾醇溶液发生消除反应,按反应速率由年夜到小排列顺序.2-甲基-1-氯丁烷、2-甲基-2-氯丁烷、2-甲基-3-氯丁烷解答:2-甲基-2-氯丁烷> 2-甲基-3-氯丁烷> 2-甲基-1-氯丁烷12. 下列卤代烃与硝酸银醇溶液反应,按生成沉淀的快慢顺序排列.1-溴环己烯、4-溴环己烯、溴化苄、1-甲基-1-溴环己烷解答:溴化苄> 1-甲基-1-溴环己烷> 4-溴环己烯> 1-溴环己烯第六章醇酚醚习题参考谜底1. 写出下列化合物的名称或结构简式2,2-二甲基-3-戊烯-1-醇甲基异丙基醚2. 完成下列反应式3. 用化学方法区别下列化合物(1) 正丁醇、仲丁醇和叔丁醇解答:各取待测物少许分别与卢卡斯试剂(浓盐酸+无水ZnCl2)混合,室温下立即呈现沉淀的是叔丁醇,过5~10分钟呈现沉淀的是仲丁醇,无沉淀的是正丁醇.(2) 苯甲醇和对甲苯酚解答:各取待测物少许分别与FeCl3混合,呈现显著颜色变动的是对甲苯酚.(3) 1,3-丁二醇和2,3-丁二醇解答:各取待测物少许分别与新制Cu(OH)2混合并振摇,Cu(OH)2溶解并获得深蓝色溶液的是2,3-丁二醇,余者为1,3-丁二醇.4. 苯甲醇和苯酚都含有苯环和羟基,为什么他们性质有很年夜分歧?解答:苯酚中的羟基与苯环发生了p-π共轭,而苯甲醇中的羟基与苯环相隔一个碳原子没有共轭发生,因此他们的性质年夜相径庭.5. 推导结构化合物A(C9H12O)与NaOH、KMnO4均不反应,遇HI生成B 和C,B遇溴水立即酿成白色浑浊,C经NaOH水解,与Na2Cr2O7的H2SO4溶液反应生成酮D,试写出A、B、C、D的结构简式与相应反应式.解答:A、B、C、D的结构简式为相关反应式如下:A B CD第七章醛酮醌习题参考谜底1. 写出下列化合物的结构式(1)4-甲基-3-戊烯-2-酮(2)α,γ-二甲基己醛(3)甲基异丁基酮(4)3-硝基苯乙酮(5)环己酮腙2. 命名下列化合物2,4-戊二酮对甲氧基苯甲醛3-环己基丙醛3-戊烯-2-酮2,8-二羟基-9,10-蒽醌对苯醌单肟3. 写出苯甲醛和环己酮分别与下列化合物的反应(如果有的话)所得产物的结构式.(1) 托伦试剂苯甲醛与托伦试剂作用的产物是:环己酮与托伦试剂不反应.(2) KMnO4,H+,加热环己酮一般条件下不容易被氧化.(3) 2,4-二硝基苯肼(4) NaHSO3(5) LiAlH4(6) 浓NaOH苯甲醛与之作用的产物为:环己酮与之不反应.(7) 乙醇,HCl苯甲醛与之作用的产物为:环己酮与之不反应.(8) 乙基溴化镁苯甲醛与之作用的产物为:环己酮与之作用的产物为:(9) 稀NaOH苯甲醛和环己酮与稀碱均不作用.4. 完成下列反应式.5. 依照与HCN反应的活性,由高至低顺序排列下列各组化合物.解答:空间位阻的分歧造成上述顺序.解答:硝基的吸电子作用增加了羰基碳原子的正电荷有利于亲和加成反应;甲氧基通过p,π-共轭效应供电子使羰基碳原子的正电荷降低晦气于亲核加成反应.解答:空间位阻的分歧是造成上述顺序的主要因素.6. 用简双方法区别下列各组化合物.(1) 苯甲醛、苯乙酮、环己酮解答:分别取上述待测物质少许与托伦试剂混合后水浴加热,呈现银镜的为苯甲醛.将剩余两种待测物分别与碘的碱溶液混合,呈现黄色沉淀的为苯乙酮,余者为环己酮.(2) 乙醛、丙醛、丁酮、二乙酮解答:取上述待测物少许分别与托伦试剂混合后水浴加热,呈现银镜的是乙醛和丙醛,未有银镜呈现的是丁酮和二乙酮.将乙醛和丙醛少许分别与碘的氢氧化钠溶液混合,呈现黄色沉淀的乙醛,另一个为丙醛.将丁酮和二乙酮少许分别滴入饱和NaHSO3溶液,呈现白色结晶的为丁酮,未有沉淀的是二乙酮.(3) 甲醛、仲丁醇、丁醛、3-戊酮解答:取上述待测物少许分别与西夫试剂混合,呈现紫红色的是甲醛和丁醛,然后加入浓硫酸,紫色不退色的为甲醛,紫色褪去的为丁醛.与西夫试剂混合后未有颜色变动的是仲丁醇和3-戊酮.各取它俩少许分别与2,4-二硝基苯肼混合,呈现黄色结晶沉淀的为3-戊酮,余者为仲丁醇.(4) 2-丁烯醛、异丁醛、3-戊酮、异丁醇解答:各取上述待测物少许,分别与溴水混合,能使溴水棕色褪至无色的是2-丁烯醛.将剩余3待测物少许分别与托伦试剂混合后水浴加热,发生银镜的是异丁醛.将最后2个待测物少许分别与2,4-二硝基苯肼混合,呈现黄色结晶沉淀的是3-戊酮.7. 用6个碳以下的直链醛或酮合成下列化合物,无机试剂任选.请写出各步反应式.(1) 2-辛醇(2) 3-甲基-3-己醇(3) 正庚醇(4) 异己烷解答:(1)合成2-辛醇的方法首先制得格氏试剂己基溴化镁:然后用己基溴化镁与乙醛反应制得2-辛醇:(2)合成3-甲基-3-己醇的方法首先制得格氏试剂丙基溴化镁:然后用丙基溴化镁与丁酮反应制得3-甲基-3-己醇:(3)合成正庚醇的方法首先制得格氏试剂己基溴化镁(见前题).然后用己基溴化镁与甲醛作用制得正庚醇:(4)合成异己烷的方法首先制得2-甲基-3-戊酮:然后用克莱门森还原法制得异己烷:8. 某化合物化学式为C5H12O(A),A 氧化后得一产物C5H10O(B).B 可与亚硫酸氢钠饱和溶液作用,并有碘仿反应.A 经浓硫酸脱水得一烯烃C ,C 被氧化可得丙酮.写出A 可能的结构式及有关反应式.解答:A 的结构式为: 有关反应式如下:9. 某化合物A (C6H10O2)可使溴水褪色,可与2,4-二硝基苯肼发生沉淀,并能与三氯化铁显色,无银镜反应.试写出A 的结构式.解答:A 的结构式为:第八章 羧酸及其衍生物习题参考谜底1. 命名下列化合物β-甲基丁酸 对苯二甲酸 3-苯基丁酸3,7—壬二烯酸 丙酰氯对甲基苯甲酰氯 乙丙酐 二甲基丙二酸二乙酯乙酸异丙酯 丙酰胺2. 写出下列化合物的结构式(1) 2,3-二甲基戊酸 (2) 反-2-甲基-2-丁烯酸(当归酸) (3) α,α-二氯丁酸CH 3CHCH(CH 3)2OH(4) 丙二酸甲乙酯 (5) 邻苯二甲酸酐 (6) 丙烯酰氯3. 比力下列化合物酸性的强弱(1) 丙酸 丙二酸 乙二酸解答:乙二酸 > 丙二酸 > 丙酸(2) α-氯丙酸 α,α-二氯丙酸 丙酸 β-氯丙酸解答:α,α-二氯丙酸 >α-氯丙酸>β-氯丙酸> 丙酸4. 写出乙酸与下列试剂的反应方程式.(1) 乙醇(2) 五氯化磷 (3) 氨 (4) 氢化锂铝 5. 用化学方法鉴别下列各组化合物(1) 甲酸 乙酸 乙醛解答:取上述待测物少许,分别与石蕊试剂混合,不呈现红色的是乙醛.将能使石蕊变红的两个化合物分别与高锰酸钾溶液混合,能使高锰酸钾紫红色褪色的是甲酸,余者为乙酸.解答:取上述待测物少许,分别与2,4-二硝基苯肼混合,能使之呈现黄色结晶状沉淀的是对-羟基苯乙酮.将余下两种待测物分别与溴水混合,能使溴水褪色的是乙烯基对苯二酚,余者为对甲基苯甲酸.6. 写出下列反应的主要产物或反应所需的条件7. 完成下列转化 +CH 3COOH CH 3CH 2CH 3COOC 2H 5+H 2O +CH 3COOH CH 3COCl +HClPCl +POCl 3+CH 3COOHCH 3COONHNH 3+CH 3CONH 2H 2O CH 3COOH LiAlH4CH 3CH 2OH(1) 由异丁烯制备2,2-二甲基丙酸解答: (2) 由乙炔制乙酸乙酯 解答: (3) 由丙二酸二乙酯制丁酸解答:8. 写出分子式为C5H6O4的不饱和二元羧酸的各种异构体的结构式,如有顺反异构,则注明Z 、E 构型.解答:9.有三种化合物的分子式均为C3H6O2,其中A 能与NaHCO3反应放出CO2,B 和C 则不能.B 和C 在NaOH 溶液中加热均可发生水解,B 的水溶液蒸馏出的液体能发生碘仿反应,而C 的则不能.试推测A 、B 、C 的结构式.解答:第九章 取代羧酸习题参考谜底1. 命名下列化合物.β-羟基丁酸 γ-戊酮酸 3-甲基-4-羟基丁酸2-氨基-3-(4-羟基苯基)丙酸 α-甲基-γ-戊酮酸 4-甲基-3-氯戊酸2. 写出下列化合物的结构式.3. 完成下列反应式.4. 用简单化学方法鉴别下列每组化合物.Mg CO 2H 2O CH 3C CH 2CH 3HBr CH 3C CH 3CH 3Br(CH 3)3(CH 3)3CCOOHKMnO 4 , H H 2O , Hg 2+HC CH CH 3CH 3COOH +CH 3COOC 2H 5解答:各取三种待测物少许分别与FeCl3溶液混合,没有呈现显色现象的是乳酸;将与FeCl3溶液显色的2种待测物分别与2,4-二硝基苯肼试剂作用,呈现黄色结晶的是乙酰乙酸乙酯,余者为水杨酸.解答:各取2种待测物少许分别与FeCl3溶液混合,呈现显色现象的是2,4-戊二酮,另一个就是丙酮.(3) 丙二酸二乙酯与乙酰乙酸乙酯解答:各取2种待测物少许,分别与2,4-二硝基苯肼试剂作用,呈现黄色结晶的是乙酰乙酸乙酯,另一个为丙二酸二乙酯.5. 将下列化合物按其酸性从年夜到小次第排列.6. 将下列化合物写成酮式与烯醇式的互变平衡体系.7. 用乙酰乙酸乙酯及其他需要的试剂合成下列化合物.解答:解答:解答:解答:8. 化合物A(C9H10O3),它不溶于水,稀盐酸及稀碳酸氢钠溶液,但能溶于氢氧化钠溶液.A与稀氢氧化钠共热后,冷却酸化得一沉淀B(C7H6O3),B能溶于NaHCO3溶液,并放出气体,B遇FeCl3溶液发生紫色,B的一种衍生物是经常使用药物APC的成份之一.试写出A、B的结构式及各步反应式.解答:A、B的结构式为:有关反应式如下:第十章立体化学习题参考谜底1. 下列化合物中,哪些是旋光性物质?哪些是非旋光性物质?为什么?解答:(1)是非旋光性物质,因为以其结构中的碳原子和2个氯原子所确定的平面是分子的对称面,具有对称面的分子不具有手性.(2)、(3)、(4)、(5)和(6)均是旋光性物质,其中(2)、(3)、(4)分子中均含有多个分歧的手性碳原子,属于手性分子.(5)和(6)两个化合物的空间结构不含有对称面和对称中心等对称因素,因而属于手性分子.2. 下列各对化合物哪些互为对映异构体?哪些互为非对映异构体?哪些为同一化合物?同一个化合物互为对映体互为对映体互为非对映体3. 写出下列旋光性物质所有的光学异构体的费歇尔投影式,并指出它们之间的关系.解答:(1)的所有光学异构体的费歇尔投影式如下:Ⅰ与Ⅱ互为对映体;Ⅲ是内消旋体,不具有旋光性.Ⅰ与Ⅲ、Ⅱ与Ⅲ的关系为非对映体.(2)的所有光学异构体的费歇尔投影式如下:Ⅰ与Ⅱ、Ⅲ与Ⅳ互为对映体;Ⅰ和Ⅱ中的任意一个与Ⅲ和Ⅳ中的任意一个互为非对映体.4. 用R、S构型标示方法标示下列化合物中手性碳原子的构型.R S R。
《有机化学-结构和性质相关分析与功能》第三版_课本答案全

第一章绪 论问题一部分参考答案μ=0。
1. (1) sp 3 (2) sp (3) sp 2 (4) sp(5) sp 3 (6)sp 22. (1),(3),(6)互为同分异构体;(2),(4),(5),(7)互为同分异构体。
3. (1)醇类 (2)酚类 (3)环烷烃 (4)醛类 (5)醚类 (6)胺类4.π键的成键方式:成键两原子的p 轨道沿着与连接两个原子的轴垂直的方向“肩并肩”重叠而形成。
π键特点:①电子云平面对称;②与σ键相比,其轨道重叠程度小,对外暴露的态势大,因而π键的可极化度大,在化学反应中易受到亲电试剂的进攻而发生共价键的异裂;③由于总是与σ键一起形成双键或叁键,所以其成键方式必然限制σ键单键的相对旋转。
5. (1) (2) (5)易溶于水;(5) (4) (6)难溶于水。
6.C 6H 67.C 3H 6F 2第三章开链烃问题三参考答案3-1(1) 3,3-二甲基己烷(2) 2,2,4,9-四甲基癸烷3-4 (1) 2,4,4-三甲基-1-戊烯(2) 4,6-二甲基-3-庚烯3-5 2-己烯有顺反异构:3-8 在较高温度和极性溶剂条件下,1,3-戊二烯同溴化氢主要发生1,4加成:习题三参考答案1.(1) 2-甲基-4,5-二乙基庚烷(2) 3-甲基戊烷(3) 2,4-二甲基-3-乙基戊烷(4) (顺)-3-甲基-3-己烯or Z-3-甲基-3-己烯(6) (Z)-3,5-二甲基-3-庚烯(7) 2,3-己二烯(8) 3-甲基-2-乙基-1-丁烯(9) 2,5,6-三甲基-3-庚炔(10)1-丁炔银(11)3-甲基-1,4-戊二炔(12) 3-甲基-1-庚烯-5-炔2.3.4.(Z)-2-戊烯(E)-2-戊烯(Z)-3-甲基-3-己烯(E)-3-甲基-3-己烯(Z)-3-甲基-4-乙基-3-庚烯(E)-3-甲基-4-乙基-3-庚烯(Z)-5-甲基-3-乙基-2-己烯(E)-5-甲基-3-乙基-2-己烯(Z)3-甲基-1,3-戊二烯(E)3-甲基-1,3-戊二烯5.2,3,3-三甲基戊烷2,3-二甲基-3-乙基戊烷2,3-二甲基-1-戊烯6-甲基-5-乙基-2-庚炔二乙基-1-己烯-4-炔6. (1)和(3) (2)和(4) (5)和(6)7.8.1-庚烯2-庚烯3-庚烯2-甲基-1-己烯3-甲基-1-己烯4-甲基-1-己烯5-甲基-1-己烯2-甲基-2-己烯3-甲基3-甲基-3-己烯2,3-二甲基-1-戊烯2,4-二甲基-1-戊烯3,5-二甲基-1-戊烯3,3-二甲基-1-戊烯2-乙基-1-戊烯3-乙基-1-戊烯2,3-二甲基-2-戊烯2,4-二甲基-2-戊烯3,4-二甲基-2-戊烯3-乙基-2-戊烯3-甲基-2-乙基-1-丁烯9.(1) 官能团位置异构(2) 顺反异构(3) 碳胳异构(4) 官能团异构(5) 碳胳异构(6) 碳胳异构10.该化合物的分子式为C14H3011.12.13. (CH 3)22CH 3 > CH 3CH 3 >C(CH 3)4 > CH 4烷烃的卤代反应机理为自由基取代反应。
有机化学第三版答案 南开大学出版社第十四章

分子内的氢键抑制了邻二甲苯酸的二级电离。
4. 下列个对化合物中哪个是较强的碱?
(1). CH3CH2O- ,CH3CO2- ;
(2). ClCH2CH2CO2- , CH3CHCO2Cl
解:ClCH2CH2CO2 >CH3CHCO2
解: 3CH2O- >CH3CO2- ; CH
Cl
(3). HC
CCH2CO2- ,CH3CH2CH2CO2- ;
解:HC
2011-5-26
CCH2CO2- < CH3CH2CH2CO2- ;
宁夏大学化学化工学院 4
(4).
COO-
, 环乙烷酸负离子
解:
COO- << 环乙烷酸负离子
(5). HOCH2CO2-
, CH3CO2-
HOCH2CO2- < CH3CO2解:
在比较体系的碱性强弱时要注意: 在比较体系的碱性强弱时要注意 体系保持负电荷的能力越强,其碱性越弱。 体系保持负电荷的能力越强,其碱性越弱。
CH3 (4). C CH3 OH CHCH3 I2—NaOH <参 P351> H
+
CH3O C CH3 COH
13.
由甲苯,不超过三个碳的醇及其它必要无机试剂合成。
O NO2 CH3
宁夏大学化学化工学院
(1).
C
2011-5-26
21
解: CH3 O C CH3 混酸 KMnO4 O COH O PCl3 CCl NO2 CH3 CH3 AlCl3
2011-5-26
CH2CH2OH 说明: LiAlH4为负氢离子给予体只还 原极性不饱和键而不还原C=C CH=CHCH2CH2OH CH2CO2H
有机化学第三版答案-下册---南开大学出版社---王积涛等编

解:
O
CH-OCH2CH2CH3
OH
8. 化合物A(C6H12O3)在1710cm-1有强的红外吸收峰。 A和 I2/NaOH溶液作用给出黄色沉淀。A与吐伦试剂无银镜 反应,但 A用稀H2SO4处理后生成化合物B与吐伦试剂 作用有银镜生成。A的1H NMR数据为 δ2.1(单峰,3H), δ2.6(双峰,2H), δ3.2(单峰,6H), δ4.7(三重峰, 1H)。写出A,B的结构式及有关反应式。
5 . 按 碱 性 强 弱 排 列 下 列 化 合 物
( 1 ) . α - 溴 代 苯 乙 酸 , 对 溴 苯 乙 酸 , 对 甲 基 苯 乙 酸 , 苯 乙 酸 。
解 :B r-CH2H COC2C H2O H C2C H2O H
C2C H2O H
>
>
>
B r
C3H
( 2 ) . 苯 甲 酸 , 对 硝 基 苯 甲 酸 , 间 硝 基 苯 甲 酸 , 对 甲 基 苯 甲 酸 。
α , α '— 二 甲 基 己 二 酸 ( 2 , 5 — 二 甲 基 己 二 酸 )
2 . 写 出 下 列 化 合 物 的 结 构 式 。
( 1 ) . 4 — 乙 基 -2 -丙 基 辛 酸 ;( 2) .
O CH 3(C2H)2CH 2CHC-H 2-CH C-OH CH3C
CH 2CH 3 CH 2CH 2CH3
O
O
O H C C H 2C C H 3
1.Ag(N H 3)2O H 2.H +
H O O C C H 2C C H 3
9. 有一化合物的IR在1690 ㎝-1和826 ㎝-1有特征吸收峰。 1H NMR数据为δ7.60(4H), δ2.45(3H)。它的质谱较强 峰m/e183相对强度100(基峰),m/e 198相对强度 26,m/e200相对强度25。写出它的结构式。
《有机化学》第十四章氨基酸、多肽与蛋白质课后习题答案(第三版)

第十四章 氨基酸、多肽与蛋白质14.2 写出下列氨基酸分别与过量盐酸或过量氢氧化钠水溶液作用的产物。
a. 脯氨酸b. 酪氨酸c. 丝氨酸d. 天门冬氨酸 答案:N H 2COOHNCOO -HOCH 2CHCOOHb.a.O -CH 2CHCO O -c.CH 2-CH-COOHOH+NH 3CH 2-CH-COO -OHNH 2d.HOOC-CH 2-CH-COOH+NH 3-OOC-CH 2-CH-COO -NH 2++NH 3NH 214.3 用简单化学方法鉴别下列各组化合物:a.CH 3CHCOOH N H 2H 2NCH 2CH 2COOHN H 2b. 苏氨酸 丝氨酸c. 乳酸 丙氨酸 答案:a.CH 3CHCOOHNH 2(A)H 2NCH 2CH 2COOH(B)NH 2(C)A BCA Bb.OH NH 2NH 2苏氨酸H 3CCH-CHCOOH丝氨酸HOCH 2CHCOOHI 2/NaOHCHI 3无变化c.乳酸H 3CCHCOOHOH丙氨酸H 3CCHCOOHNH 2茚三酮显色不显色14.4 写出下列各氨基酸在指定的PH 介质中的主要存在形式。
a. 缬氨酸在PH 为8时b. 赖氨酸在PH 为10时c. 丝氨酸在PH 为1时d. 谷氨酸在PH 为3时 答案: (CH 3)2CHCH(NH 2)COOH (CH 3)2CHCH(NH 2)COO -H 2N(CH 2)4CH(NH 2)COOHH 2N(CH 2)4CHCOO -NH 2IP 5.96PH=8时主要存在形式b. 赖氨酸IP 9.74 PH=10时a. 缬氨酸CH 2-CHCOOHCH 2-CHCOOHOHN H 2OH N H 3c. 丝氨酸IP 5.68 PH=1时+HOOC(CH 2)2CHCOOHHOOC(CH 2)2CHCOOHNH 2d.. 谷氨酸IP 3.22 PH=3时NH3+14.5 写出下列反应的主要产物a.CH 3CHCO 2C 2H 5+H 2ONH 2b.CH 3CHCO 2C 2H 5+NH 2(CH 3CO)2O c.CH 3CHCONH 2NH 2+HNO 2(过量)d.CH 3CHCONHCHCONHCH 2COOHH 2OH +NH 2CH 2CH(CH 3)2e.CH 3CHCOOHNH 2++CH 3CH 2COClf.(亮氨酸)CH 3OH +(过量HClg.(异亮氨酸)CH 3CH 2I (过量h.(丙氨酸)i.Br 2--H 2O酪氨酸j.(丙氨酸)+O 2NNO 2Fk.NH 2CH 2CH 2CH 2CH 2COOH l.CH 2COOHNH 2.HCl+SOCl 2+答案:a.CH 3CHCO 2C 2H 5+H 2ONH 2CH 3CHCOOH+NH 3Cl -b.CH 3CHCO 2C 2H 5+NH 2(CH 3CO)2O CH 3CHCO 2C 2H 5NHCOCH 3c.CH 3CHCONH 2NH 2+HNO 2(过量)CH 3CHCOOHOHd.CH 3CHCONHCHCONHCH 2COOHH 2OH +NH 2CH 2CH(CH 3)2CH 3CHCOOH +NH 3H 3N +CH 2COO H +(CH 3)2CHCH 2CHCOOH+NH 3e.CH 3CHCOOHNH 2+++CH 3CH 2COCl CH 3CHCOOHNHCOCH 2CH 3f.(亮氨酸)(CH 3)2CHCH 2CHCOOH NH 2CH 3OH (CH 3)2CHCH 2CHCOOCH 3+(过量HClNH 2g.(异亮氨酸)CH 3CH 2CH-CHCOOH +CH 3CH 2I (过量CH 3CH 2CH-CHCOOHCH 3NH 2CH 3+N(CH 2CH 3)3h.(丙氨酸)CH 3CHCOOHNH 2i.HOCH 2CH(NH 2)COOHBr 2--H 2OHO CH 2CH(NH 2)COOHBr Br酪氨酸HC HNC CHNH C CH 3H 3COO j.(丙氨酸)CH 3CHCOOHNH 2+O 2NNO 2F NO 2O 2NCH 3CHNHCOOHk.NH 2CH 2CH 2CH 2CH 2COOH H NOl.CH 2COOHNH 2.HCl+SOCl 2CH 2COClNH 2.HCl14.6 某化合物分子式为C 3H 7O 2N ,有旋光性,能分别与NaOH 或HCl 成盐,并能与醇成酯,与HNO 2作用时放出氮气,写出此化合物的结构式。
有机化学第三版答案-下册---南开大学出版社---王积涛等编

C4H9 -H2 C4H7 m/e 55 - CH2 C3H7 m/e 43
-H2 C3H5
m/e 41
习题与解答
1.利用λmax计算规律预测下列化合物的紫外最大吸收 波长。
O
解:该化合物λmax: 317nm。计算过程如下: 215(母体烯酮)+5(一个环外反键)+30 (一个延伸共轭双键)+39(同环二烯)+10 (α-位烃基取代)+18(δ-位烃基取代) =317nm 2.化合物C7H12O紫外最大吸收波长为248nm写出该化合 物的结构式。
5 . 按 碱 性 强 弱 排 列 下 列 化 合 物
( 1 ) . α - 溴 代 苯 乙 酸 , 对 溴 苯 乙 酸 , 对 甲 基 苯 乙 酸 , 苯 乙 酸 。
解 :B r-CH2H COC2C H2O H C2C H2O H
C2C H2O H
>
>
>
B r
C3H
( 2 ) . 苯 甲 酸 , 对 硝 基 苯 甲 酸 , 间 硝 基 苯 甲 酸 , 对 甲 基 苯 甲 酸 。
解:
Br
O C-CH3
IR: 1690cm-1 与苯环共轭的羰基吸收。 826 cm-1对二取代苯环上氢的面外弯曲。
MS: m/e 198 , m/e 200 其强度比为:26:25说 明分子中含有Br
基峰 m/e 183 为 Br
CO
产生 m/e 198 为 79Br
O CC3H
m/e 200 为
10.化合物C6H14Br的13C NMR谱图如下,写出它的结构式
解:δ =70为C-O吸收化合物为: CH3 CH3
CH3-CH-O-CH-CH3
11.化合物C9H10O2.的13C NMR谱图如下,写出它的结构式。
《有机化学》第三版 王积涛 课后习题答案 南开大学 无水印版本
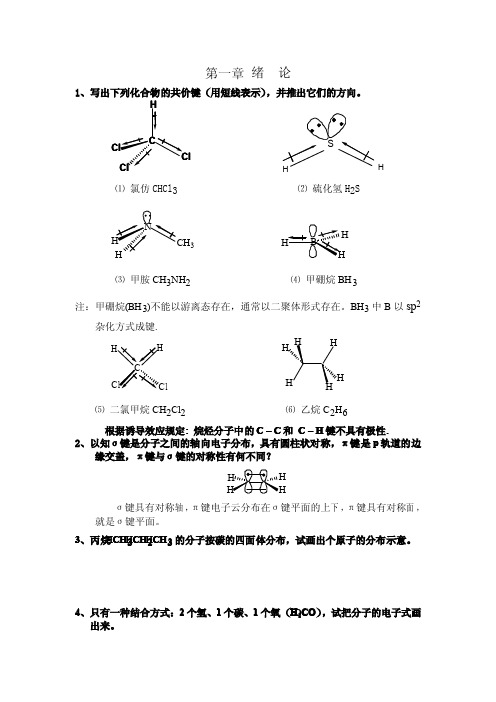
130 (CH3)3CO-OC( CH3)3
2( CH3)3CO
异丁烷和才 CCl4 的混合物在 130℃~140℃时十分稳定。假如加入少量叔丁 基过氧化物就会发生反应,主要生成叔丁基氯和氯仿,同时也有少量叔丁醇 (CH3)3C-OH,其量相当于所加的过氧化物,试写出这个反应可能机理的所 有步骤。
_
CH3 CH3CH-CH3
ci s-3-heptene
(
):
2-
1
(2) Cl2 (3) Br2
CH3 CH3-C=CH2
Cl2
CH3 CH3-C-CH2
Cl Cl
1, 2- -2-
CH3 CH3-C=CH2
Br2
CH3 CH3-C-CH2
BrBr
1, 2- -2-
(4) I2
CH3
I2
CH3-C=CH2
|CH3 |CH3 5) CH3CHCH2CHCH3
2,4-二甲基戊烷 2,4-dimethylhentane
CH3 | CH3CCH2CH2CH3 | 6) CH3
CH3
|
CH3CH2CCH2CH3
|
7)
CH3
2,2-二甲基戊烷 2,2-dimethylhentane 3,3-二甲基戊烷 3,3-dimethylhentane
的远离,可想像 2 个 sp 杂化轨道之间的夹角应互为 1800,sp 杂化的碳原子
应为直线型构型。
8、 二氧化碳的偶极矩为零,这是为什麽?如果 CO2 遇水后形成 HCO3-或 H2CO3,
这时它们的偶极矩还能保持为零吗?碳酸分子为什麽是酸性的?
O = C = O 化合物分子的偶极矩是分子中所有键偶极矩的矢量和,二氧化碳分
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
12 .完 成 下 列 转 化 OH
OH
( 1 ) .
K H O 3 CC 2 H 5 OH
+C 2O OH
H 2 S O 4
参 书 P 3 0 0K o lb e -S c h m itt反 应 OH
C 2 C O 2 H 5
( 2 ) .2 C H 3 C H 2 C H O - O - H 2 O H C H 3 C H 2 C H = C - C H O M O 2C n H 3 C H 2 C H = C - C O O H
出产生两个不等强度的裂分;
B中含有的异丙基在此区域内则产生两个等强度的 吸收峰。
C的直链的烷基在此区域不产生裂分峰。
14.12.2020
h
15
9 .4 - 羟 基 戊 酸 用 微 量 硫 酸 在 苯 溶 液 中 处 理 发 生 下 列 反 应 , 提 出 它 的 反 应 机 理 。
OH C3 C HH 2 C C 2 C H H 2 H O H +
说 明 这 个 实 验 事 实 。
14.12.2020
h
3
解:
O CO- H -H+ CO- H
O
O CO-CO- H
O
O CO--
H CO-
O
分子内的氢键抑制了邻二甲苯酸的二级电离。
4 . 下 列 个 对 化 合 物 中 哪 个 是 较 强 的 碱 ?
( 1 ) .C H 3 C H 2 O -, C H 3 C O 2 -; ( 2 ) . C lC H 2 C H 2 C O 2 -, C H 3 C H C O 2 -
( 2) ( C H 3) 2C H C H 2C O O H B r2/P O
( C H 3) 2C =C H -C O C 2H 5
K O H -醇( C H 3) 2C =C H C O O - C 2H 5O H H 2S O 4
14.12.2020
h
19
O ( 3 ) ( C H 3 ) C H C H 2 C O H + P b ( O A c ) 4 + L iC l 8 0 0 C ( C H 3 ) 2 C H C H 2 C l
C 3H
C 3H
14.12.2020
h
20
(3 ).
OO C H 3 C O 2 H
O O
H 3 + O
O H
O
C H 2 C H 2 C H 2 C O H
(1 )
C2 B H r OH
C2 C H2 H O ;
OH
( 2) C3H C2H C HC 3 H B r
O (3)CH 3CC2H CH 2CH 2I
C H 3C2H CH2H COБайду номын сангаас
C3H O C 3CHC2H CH 2CH2CO 2H;
(4)
CH 2CH 2Br OC3H
CH 2CH 2CO2H OC3H
α , α '— 二 甲 基 己 二 酸 ( 2 , 5 — 二 甲 基 己 二 酸 )
2 . 写 出 下 列 化 合 物 的 结 构 式 。
14.12.2020
h
2
( 1 ) . 4 — 乙 基 -2 -丙 基 辛 酸 ;( 2) .
O CH 3(C2H)2CH 2CHC-H 2-CH C-OH CH3C
CH=CHCH2CHO
CH2CH2CH2CH2OH
14.12.2020
h
8
CHO
CO 2H CHO
CO 2H
(5).
Ag2O /-O H
KM nO 4
CH3
CH3
CH3
CO 2H
O
CH3
CO2H
CO
(6)
KMnO4/H+
CO2H △
C=O
CO2H
C=O
CH3
CO2H
CO
O
O
O
N a B H 4
H + / C H 2 -C
( 3 ) ( C H 3 ) 2 C H C H 2 C l ; ( 4 ) ( C H 3 ) 2 C H C H 2 C H 2 C H (B r)C H 2 B r。 解: 以CH3CHCH2COOH为 原 料 合 成 :
CH3
( 1)( C H 3) 2C H C H 2C O O H LiA lH 4 ( C H 3) 2C H C H 2C H 2O H
习题与解答
14.12.2020
h
1
1. 写出下列化合物的名称:
( 1)CH3CH2CH2CHCH2CH2CH3 (2) HO
CO2H
C2H C2O H
3-丙基戊酸
NO2
2-羟 基 -5-硝 基 苯 甲 酸
(3)
CO2H
C2 O H C2 O H (4). CH3CHCH2CH2CHCH3
(E)-环癸烯羧酸
14.12.2020
h
5
5 . 按 碱 性 强 弱 排 列 下 列 化 合 物
( 1 ) . α - 溴 代 苯 乙 酸 , 对 溴 苯 乙 酸 , 对 甲 基 苯 乙 酸 , 苯 乙 酸 。
解 :B r-CH2H COC2C H2O H C2C H2O H
>
>
>
C2C H2O H
B r
C3H
( 2 ) . 苯 甲 酸 , 对 硝 基 苯 甲 酸 , 间 硝 基 苯 甲 酸 , 对 甲 基 苯 甲 酸 。
CH 2CH 3 CH 2CH 2CH3
2-已 烯 -4-炔 酸
O
C-CH=CH-COH
(3). 6-羟 基 -1-萘 甲 酸 ;
COOH
(4) 对 乙 酰 基 苯 甲 酸
COOH
HO
O C- CH 3
3 . 邻 苯 二 甲 酸 p K 2 为 5 .4 , 对 苯 二 甲 酸 p K 2 为 4 .8 ,
CH3CH2CHCO2H CH 3
O
O
( 3 ) C H 3 C C H 2 C H 2 C H 2 I N a C NH 3 + OC H 3 C C H 2 C H 2 C H 2 C O O H
( 4 ) C H 2 C H 2 B r M g ( 1 ) C O 2
O C H 3
乙 醚( 2 ) H 3 + O
14.12.2020
h
4
(4).
CO - O , 环 乙 烷 酸 负 离 子
解 : CO - < O <环 乙 烷 酸 负 离 子
( 5 ) .H O C H 2 C O 2 - , C H 3 C O 2 解 : H O C H 2 C O 2 -< C H 3 C O 2 -
在比较体系的碱性强弱时要注意: 体系保持负电荷的能力越强,其碱性越弱。
14.12.2020
h
17
解:(1)、(3)应选用腈的水解法,避免格式试剂的分解和与羰基的 加成;(2)、(4)可用格式试剂制备,可避免 NaCN与卤代烷作用 时消除反应的发生。
(1) CH 2Br NaCN OH
H3+O
(2)CH3CH2CHCH3 Mg 乙醚
Br
(1)CO2 (2)H3+O
CH 2COOH OH
D.
COOH
OH
不显色 A. KMnO4
C
不退色
C
14.12.2020
h
13
(3 )
O C O 2 H , O , O
O H , H O
O H
C H 3
解 : 加 入 N a H C O 3 放 出 C O 2 者 为 C O O H ; 剩 下 三 者 : 分 别 加 入
N O 2
N O 2
N H N H 2, 生 成 黄 色 沉 淀 者 为 H O
(4) (CH3)2CHCH2COH LiAlH4
HBr
Li
(CH3)2CHCH2CH2Br
CuI[(CH3)2CHCH2CH2]2CuLi CH2=CHBr (CH3)2CHCH2CH2-CH=CH2Br2 CCl4
(CH3)2CHCH2CH2-CHCH2(注:本合成通过二烷基铜锂的偶联反应来建造分子骨架。) Br Br
h
11
解:
甲酸 乙酸 乙醛
NaHCO3 CO2 CO2
Ag+(NH3)2 Ag
Ag
14.12.2020
h
12
( 2 ) 肉 桂 酸 , 苯 酚 , 苯 甲 酸 , 水 杨 酸
解:
A. B. C.
CH=CHCOOH OH COOH
CO2 D 显色 B. Na2CO3
D. FeCl 3
不反应 B 退色 A
(7 ).C H 3 C O C H 2 C H 2 C O 2 H
C H 3 C H C H 2 C H 2 C O H
O
O H
C H 2 -C H -C H 3
14.12.2020
h
9
(8 ).C H 3 C O 2 H +H O
O H + C 2 O HHC 3 C HO 2 CO HH
(9). CH3CH2CH2CO2H + Br2
COOH COOH
解 : >
N2O
> N2O
6. 完 成 下 列 反 应 式 。
COOH COOH > C3H
14.12.2020
h
6
CC ( H 3)3
CC ( H 3)3
