第28讲 卤代烷烃的亲核取代反应
卤代烃的取代反应

影响亲核取代反应的因素(一)卤代烷的结构●对S N2,主要因素是空间效应:α—C(或β—C)上的取代基越多、越大,亲核试剂越不易进攻,反应越难进行。
电子效应(次要):α—C取代基越多,越不利于Nu¯进攻α—C。
故,S N2反应的顺序:CH3X>1°RX>2°RX>3°RX●对S N1,碳正离子越稳定,反应就越容易进行。
因,碳正离子稳定性:3°>2°>1°>CH3+故,S N1反应的顺序:3°RX>2°RX>1°RX>CH3X.(二)离去基团的影响底物中离去基团的离去能力越强,对S N2和S N1均有利。
但S N1反应速率主要取决于基团离去这一步,而S N2决定速率的步骤还有亲核试剂的参与,所以,S N1机制受离去基团的影响更大。
离去基团的碱性越弱,离去能力就越强,就越容易离去。
如:碱性F¯>Cl¯>Br¯>I¯,活性顺序RI>RBr>RCl>RF当离去基团的碱性大于亲核试剂的碱性时,反应不易发生。
(三)亲核试剂的影响●对S N2,因为决定速率的步骤有亲核试剂的参与,故对反应有很大影响;试剂的亲核性强,浓度低,体积小,有利于进攻α碳,形成S N2过渡态。
对S N1,反应速率只取决于卤代烷的解离,故影响不大。
●亲核性强弱取决于试剂的碱性、可极化性和溶剂化作用。
亲核性与碱性的一般规律:(1)中心原子为同种元素的亲核试剂,其亲核性与碱性的强弱一致;C2H5O¯>HO¯>C6H5O¯>CH3COO¯>NO3¯(2)中心原子处于同一周期并且有相同电荷的亲核试剂,按周期表的位置从左到右,亲核性与碱性一致递减;R3C¯>R2N¯>RO¯>F¯(3)中心原子处于同一族的亲核试剂,其亲核性与碱性强弱受溶剂的影响,在质子溶剂中亲核性与碱性顺序相反(变形性大,亲核性强)在质子溶剂中,一些常用亲核试剂强弱次序:RS¯≈ArS¯>CN¯>I¯>NH3(RNH2)>RO¯≈OH¯>Br¯>PhO¯>Cl¯>H2O>F¯(四)溶剂的影响●质子性溶剂:指分子中含有可形成氢键的氢原子溶剂。
卤代烃及亲核取代反应PPT课件

叔丁基溴SN1水解反应的反应进程势能曲线
第42页,共95页。
单分子亲核取代反应(SN1)特点
在亲核取代反应中,在决速步骤中发生共价键变化 的只有一种分子,把这种反应称为单分子反应历程
A.反应分二步进行
(SN1)
B.反应速度只与反应物浓度有关;
C.反应有碳正离子产生。
可以得到“构型保持”和“构型转化”两种产物(卤代烃中 卤素所连的碳为手性碳,经SN1反应后,得到的产物基本上 是外消旋化的)。有重排产物(SN1 反应的标志).
第35页,共95页。
8.5 饱和碳原子上的亲核取代反应机理
X + Nu-
Nu + X
CH3Br + OH―→ROH + Br―
底物的浓度
υ = κ [CH3Br][OH―]
(CH3)3CBr + OH― → (CH3)3COH + Br―
υ = κ [(CH3)3CBr] 反应的级数
碱的浓度
第36页,共95页。
(CH2O)n HCl
NaCN CH2Cl
CH2CN
CH2CN
H+ ,H2O
CH2COOH
第24页,共95页。
3.与醇钠作用 ( Nu=RO-)
RX + RONa
ROR' + NaX
Williamson醚合成法; RX——伯卤烷。
ONa
O
+
Br
第25页,共95页。
4.与氨作用 ( Nu=NH3)
过渡态
CH3
CH3
........OH
CH3
过渡 态
CH3
CH3
+ + Br
02-卤代烃的亲核取代反应课件

卤烷的化学性质
结构
X
C
X=F,Cl,Br,I
键的极性 C F C Cl C Br C I
化学性质
亲核取代反应
Nu - + R-X
R-Nu + X -
Nu + R-X
R-Nu+ + X -
亲核试剂:带负电荷的试剂(OH-,RO-,CN-,HS-)或 具有未共用电子对的试剂(H2O,ROH,NH3)
2. 卤烃的氰解
• 卤代烷与氰化钠或氰化钾的醇溶液中反应,生成腈。
RX + NaCN
RCN + NaX
• 此反应是非常有用的一个反应,可以增加分子中碳 链的长度,每次可以增加一个碳原子,是增长碳链 的反应之一。
CH3CH2Cl + NaCN
CH3CH2CN + NaCl
3. 卤烃的氨解
• 此反应既可用氨反应,也可用氨的衍生物反应,来 制取伯、仲、叔胺。
1. 卤烃的水解
• 卤代烃与水作用,水解为醇,反应是可逆反应。如:
CH3CH2Br + H2O
CH3CH2OH + HBr
在一般情况下,此反应很慢。为增大反应速率, 提高醇的产率,常加入强碱(氢氧化钠),使生成 的HX与强碱反应,可加速反应并提高了醇的产率。
CH3CH2Br + NaOH
CH3CH2OH + NaBr
• 卤代烃与硝酸银的醇溶液发生亲核取代反应,生成 硝酸酯和卤化银沉淀。可用于卤烃的定性鉴别。
RX + AgNO3
RONO2 + AgX
卤代烃—亲核取代反应(有机化学课件)

卤代烃在有机合成的多种用途
灭火器
制冷剂
管材
薄膜
墙板地板
日用品
目录CONTENT来自01亲核取代反应
02
亲核取代反应实例
01
亲核取代反应
亲核取代反应 1.卤代烷结构分析
导入动画
结论:卤代烃的取代是一个亲核取代的过程。
亲核取代反应 2. 定义 亲核取代反应(SN):
有机化合物分子中的原子或原子团被亲核试剂取代的反应。
2. 被烷氧基取代
卤代烷与醇钠作用,卤原子被烷氧基取代而生成醚类化合物。
+ R X
△ R'ONa
+ ROR'
NaX
Williamson 醚合成法
伯卤代烷 > 仲卤代烷 > 叔卤代烷
亲核取代反应实例
3. 被氰基取代
卤代烷与氰化钠或氰化钾在乙醇溶液中共热回流,卤原子被氰基(—CN)取代,
得到腈。
乙醇
+ RX
亲核取代反应实例
6. 卤化物的互换
氯代烷或溴代烷的丙酮溶液与碘化钠共热,可生成氯化钠和溴化钠沉淀。
丙酮
+ RCl NaI
丙酮
+ RBr NaI
+ RI
NaCl
+ RI
NaBr
卤代烷的 定性鉴定
伯卤代烷>仲卤代烷>叔卤代烷
小结
100% 80% 60% 40% 20%
R-X
NaOH
ROH 醇类
R’ONa ROR’ 醚类
NaCN
+ RCN
NaX
乙醇
+ CH 3CH 2CH 2Cl
NaCN
有机化学基础知识点整理卤代烃的消除反应和亲核取代反应

有机化学基础知识点整理卤代烃的消除反应和亲核取代反应有机化学基础知识点整理:卤代烃的消除反应和亲核取代反应有机化学中,卤代烃是一类重要的化合物。
它们包含有一个或多个卤素原子,如氯、溴、或碘,与碳原子相连。
在有机合成和反应中,卤代烃经常被用作起始物质或中间体。
在本文中,我们将重点介绍卤代烃的消除反应和亲核取代反应两个重要的基础知识点。
一、卤代烃的消除反应卤代烃的消除反应是指在适当的条件下,卤素原子与相邻碳原子之间的化学键断裂,从而形成一个双键或三键,并且卤素原子被去除。
常见的消除反应有β-消除反应和氢化物消除反应。
1. β-消除反应β-消除反应是指当卤代烃的邻碳上有一个或多个氢原子时,卤素和一个氢原子同时被去除,形成一个双键。
常见的β-消除反应有氢氧化钠和氨水处理。
例如,当2-溴丙烷与氢氧化钠反应时,产物为丙烯和溴化钠:CH3CHBrCH3 + NaOH → CH2=CHCH3 + NaBr + H2O2. 氢化物消除反应氢化物消除反应是指当卤代烃中没有邻碳上的氢原子时,卤素与一个氢化物离子(如乙醇钠)同时被去除,形成烯烃。
例如,当1,2-二溴乙烷与乙醇钠反应时,产物为乙烯和溴化钠:CH2Br-CH2Br + 2 NaOEt → CH2=CH2 + 2 NaBr + EtOH二、卤代烃的亲核取代反应卤代烃的亲核取代反应是指一个亲核试剂与卤代烃发生反应,亲核试剂的亲电子进攻和取代卤素原子,形成一个新的化合物。
亲核取代反应是有机合成中最常见的反应之一。
1. SN1 亲核取代反应SN1 亲核取代反应是指在两步反应中,第一步生成一个稳定的卤代烷离子,然后在第二步中,亲核试剂攻击离子,取代卤素原子。
SN1亲核取代反应通常发生在三级卤代烷上,存在亲核试剂的浓度低的情况下。
例如,当溴代异丙基反应生成异丙基碳离子,然后氢氧化钠攻击碳离子,形成异丙醇:(CH3)3C-Br + NaOH → (CH3)3C-OH + NaBr2. SN2 亲核取代反应SN2 亲核取代反应是指在一步反应中,亲核试剂直接攻击卤素原子,并取代它。
卤代烃的亲核取代反应

卤代烃的亲核取代反应亲核取代反应是有机化学中一种重要的反应类型,其中卤代烃作为反应物参与。
这类反应是通过亲核试剂与卤代烃之间的反应来实现,产物通常是新生成的化学键。
在本文中,我们将详细探讨卤代烃的亲核取代反应及其应用。
一、亲核取代反应简介亲核取代反应是一种通过亲核试剂攻击含有可离子性卤素的有机化合物的取代反应。
在这种反应中,亲核试剂以亲核性离子或亲核中心作为活性试剂,攻击卤代烃中的卤素离子,从而将卤素离子取代为新的官能团或基团。
这种取代反应的产物往往具有更加活泼和活性的性质。
二、亲核试剂的选择在亲核取代反应中,选择合适的亲核试剂非常重要。
常见的亲核试剂包括碱(如氢氧化钠、氢氧化钾)、醇类、胺类、硫醇、卤代醇和卤代胺等。
亲核试剂的选择应根据反应的需求以及亲核试剂的性质来确定。
三、亲核取代反应的机理亲核取代反应的机理主要有两种类型:亲核取代SN2反应和亲核取代SN1反应。
1. SN2反应机理:在SN2反应中,亲核试剂以一个步骤进攻卤代烃的碳中心,同时将离去基团踢出。
这种反应机理通常发生在较低的温度下,并且是一种立体选择性反应。
2. SN1反应机理:在SN1反应中,卤代烃首先发生解离,形成卤素离子和一个碳阳离子中间体。
随后,亲核试剂攻击碳阳离子,生成产物。
这种反应机理常发生在较高的温度下,并且不具有立体选择性。
四、亲核取代反应的应用1. 制备醇类化合物:通过亲核取代反应,可以将卤代烃与醇反应,生成醇类化合物。
这种反应常用于有机合成中,特别是制备醇类溶剂或中间体。
2. 制备胺类化合物:亲核取代反应对于合成胺类化合物也非常常见。
卤代烃与胺反应,可以得到相应的胺化合物,该反应广泛用于制备医药和农药中的胺类化合物。
3. 制备酯类化合物:通过卤代烃与醇类反应,可以得到酯类化合物。
这种反应常用于合成食品添加剂、香料以及某些有机合成反应的催化剂。
4. 制备硫醚化合物:卤代烃与硫醇反应,可以生成硫醚化合物。
硫醚是一类重要的有机溶剂和催化剂,具有广泛的应用。
卤代烃的亲核取代反应机制综述
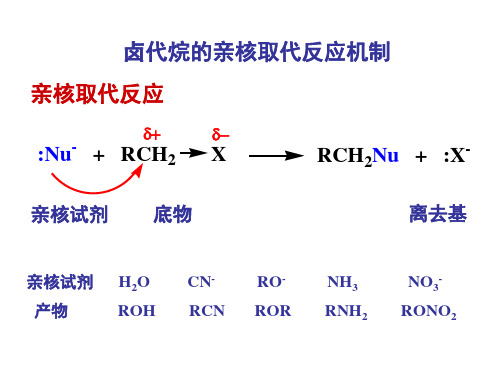
CH3Br
+
υ
HO
CH3OH + Br
-
= k [ CH3 Br ] [ HO- ]
SN2 反应机制
δ+δ-
过渡态
H HO C H H Br
氯甲烷的水解反应动画
构型相反 • 瓦尔登转化
SN2反应的能量变化曲线
H HO C Br H H
OH C CH3 CH2CH2CH3 CH2CH3
H3C
+
CH3 C
CH2CH2CH3 CH2CH3
OH +
A
OHCH3 C OH
CH2 CH3 CH2 CH2 CH3
S
构型转化
制作:邓健 出版:人民卫生出版社 10
SN1反应的特点:
①属于单分子反应。 ②反应分两步进行,决定步骤是活泼中间体-正碳 离子的形成。 ③产物构型外消旋化。
(CH3)3C
Br
(CH3)3C+ + Br叔丁基正碳离子
过渡态A
第二步
(CH3)3C + OH
+ -
快
+
-
(CH3)3C OH 过渡态B
(CH3)3C OH
叔丁基溴水解反应动画
SN1反应的能量变化曲线
上页
下页
首页
SN1反应立体化学
R
C CH3CH2CH2 CH3CH2 Br
Br
反应动画
R
构型保持
-
SN2
E CH3Br + OH-
活化能
CH3OH + Br反应进程
卤代烃的亲核取代反应和消除反应(共74张PPT)

2-bromobutane
(2-溴 丁烷) sec-butyl bromide
(仲丁基溴)
H Cl
CH3 H
(1R,3R)-1-chloro-3-methylcyclopentane
trans-1-chloro-3-methylcyclopentane
(1R,3R)-1-甲基-3-氯环戊烷
Br
CH3CH2OH
C3H C2H CH C2H19%
3) Formation of organometallic compounds 4) (形成有机金属化合物) (T2: p234; T1 p 420 10-8, 9 )
RM
+
CM
M: Li, Na; Mg; B, Al, Ga; Si, Ge, Sn, Pb; P, As, Sb; etc.
• 在铜丝上燃烧时产生绿色火焰, 可用于鉴定卤素.
4.3 Preparation of alkyl halides (6-6)
(Reading material: text 1 6-6, p 220-223)
1) Free-radical halogenation (自由基卤代) 6-6A
hv +C l2
Chapter 4
Alkyl halides (卤代烷): Nucleophilic substitution and elimination (亲核取代和消除)
Text 1: chapter 6 Text 2: 第九章
Contents
➢Classification and Nomenclature of Alkyl halides
CC +N u -
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
煤化工技术专业教学资源库
主讲教师:田苗
第六章
卤代烃
ξ 6.3 卤代烷烃的亲核取代反应
X原子被—OH、—CN、—NH2、—OR、—ONO2等基团所取代,生成了醇、腈、胺、 醚、硝酸酯。
不同卤代烃烷烃表现的活性顺序为:C-I>C-Br>C-Cl。
第六章
卤代烃
一、水解反应 卤代烃与强碱水溶液共热,分子中的卤原子可被羟基取代生成醇。
(1) KOH(水)
(2) 浓KOH(醇),加热
(3) Mg,乙醚
(4) NaCN
(5) AgNO3/C2H5OH,加热
(6) NaI/丙酮
卤代烃
四、醇解反应(威廉姆逊(Williamson)合成法)
第六章
卤代烃
思考:叔卤代烷烃在碱性条件下为什么更有利于发生 消去反应 ?
碱性条件下,更有利于去掉 分子内的氢质子,从而形成 稳定的烯烃。
CH3
CH3 CH2 C Cl
CH3
NaOH或 RONa 或 NaCN或 NH3
CH3
CH3 C CH CH3 + HCl
第六章
卤代烃
水解、氰解、氨 解、醇解反应
卤代烷烃 的亲核取 代反应
与硝酸银的反应 与NaI的反应
第六章
卤代烃
课后习题
1、下列卤代烷中与硝酸银反应最快的是(
(1) CH3CH2CH2Cl
(2) CH3CH2CH2I
),反应最慢的是( (3) CH3CH2CH2Br
)。
2、写出CH3CH2CH2CH2Br与下列化合物反应的主要产物。
常用于制备 特殊的醇
例:
第六章
卤代烃
二、氰解取代
用途:① 增长碳链。 ② 制备羧酸(-COOH)、伯胺(-CH2NH2)和酰胺(-CONH2)等化合物
第六章
卤代烃
三、氨解反应
卤代烷过量,产物是各种取代的伯、仲、叔胺及季铵盐。
RNH2
RX
ROH
R2NH
RX
ROH
R3N
RX
ROH
+-
R4N X
第六章
第六章
卤代烃
五. 与硝酸银反应
此反应可用于卤代烷的定性鉴定。
ห้องสมุดไป่ตู้
反应活性次序:RI>RBr>RCl;叔卤代烷>仲卤代烷>伯卤代烷。根据生成 AgX沉淀的速率和颜色鉴别卤代烷烃的结构。
六、与碘化钠的丙酮溶液反应
R X + NaI
R I + NaX (X=Cl或 Br)
丙酮
① 实验室制备碘代烷烃
② 有机分析上用来检验氯代烷烃和溴代烷烃
