弱电解质的电离知识要点与方法指导
弱电解质的电离平衡知识点推荐文档

弱电解质的电离平衡知识点推荐文档弱电解质是指在溶液中只部分电离的化合物,其电离度较低。
而强电解质则是指能够完全电离成离子的化合物。
弱电解质的电离平衡是指在溶液中,弱电解质分子部分电离成离子的过程,同时溶液中形成的离子也会重新组合反应生成原来的弱电解质分子。
弱电解质的电离平衡有以下几个重要的知识点:1.弱电解质的电离度:弱电解质的电离度往往都比较低,即只有一小部分分子能够电离成离子,其余的分子保持着原始的分子状态。
电离度的大小与溶液浓度、温度等因素有关。
2.平衡常数:对于弱电解质的电离平衡反应,可以建立相应的平衡常数表达式。
平衡常数描述了电离反应达到平衡时,溶液中离子和分子之间的关系以及它们的浓度之间的比例关系。
平衡常数可以通过实验测定得到。
3.离子产生的平衡常数:对于弱电解质AHA的电离反应,可以表示为:AHA⇌A-+HA+。
其中,AHA为弱电解质分子,A-和HA+分别为产生的阴离子和阳离子。
相应的,可以建立如下的平衡常数表达式:K=[A-][HA+]/[AHA]。
其中,K为平衡常数,[]表示浓度。
对于不同的弱电解质电离反应,平衡常数的大小不同。
4.电离度与平衡常数的关系:电离度和平衡常数之间存在一定的关系。
在电离平衡时,溶液中离子的浓度与电离度之间存在着明确的关系。
通常情况下,电离度越高,平衡常数越大。
推荐文档:1. Bockris, J. O. M., & Reddy, A. K. N. (2000). Modern Electrochemistry. Springer Science & Business Media.这本书是一本经典的电化学教材,涵盖了电离平衡的相关知识,包括弱电解质的电离,并详细介绍了电离平衡的理论基础和实验方法。
这本化学教材提供了详细的化学知识和概念,包括弱电解质的电离平衡。
书中用简洁明了的语言解释了电离平衡的基本概念,并通过示例和练习题加深理解。
3. Cotton, F.A., & Wilkinson, G. (1980). Advanced Inorganic Chemistry. John Wiley & Sons.这是一本高级无机化学教材,包含了广泛的无机化学知识,其中包括弱电解质的电离平衡。
高三化学弱电解质的电离平衡要点与解例知识点分析
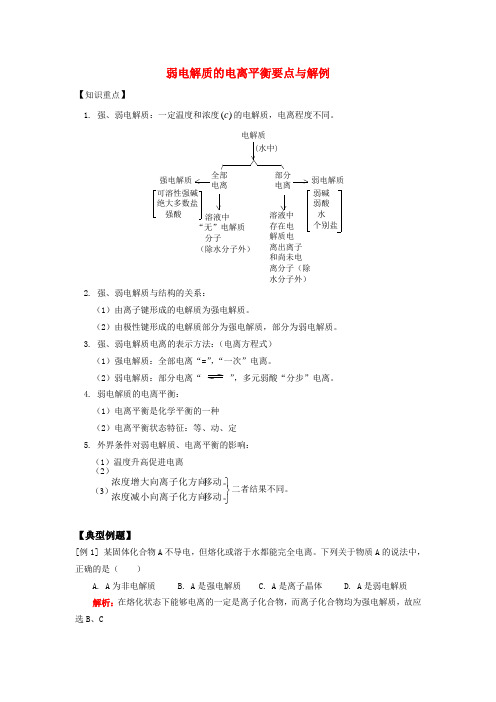
(2)(3) 弱电解质的电离平衡要点与解例【(1)强电解质:全部电离“=”,“一次”电离。
(2)弱电解质:部分电离“”,多元弱酸“分步”电离。
4. 弱电解质的电离平衡: (1)电离平衡是化学平衡的一种 (2)电离平衡状态特征:等、动、定5. 外界条件对弱电解质、电离平衡的影响:(1)温度升高促进电离 ⎭⎬⎫移动。
浓度减小向离子化方向移动。
浓度增大向离子化方向二者结果不同。
【典型例题】[例1] 某固体化合物A 不导电,但熔化或溶于水都能完全电离。
下列关于物质A 的说法中,正确的是( )A. A 为非电解质B. A 是强电解质C. A 是离子晶体D. A 是弱电解质 解析:在熔化状态下能够电离的一定是离子化合物,而离子化合物均为强电解质,故应选B 、C[例2][例3] A. )(23O H NH C ⋅ B. )(4-OH C C.)()(423+⋅NH C O H NH C D. )(-OH C解析:一水合氨是弱电解质,加水稀释,一水合氨的电离平衡右移,)(-OH n 和)(4+NH n 增大,但)(-OH C 和)(4+NH C 减小。
A 、B 、C 各项中,分子、分母同乘溶液体积,浓度比等于其物质的量之比。
A 中)()(23O H NH C OH C ⋅-)()(23O H NH n OH n ⋅=-,随加水量增大比值增大,B 中)()()()(44-+-+=OH n NH n OH C NH C 随加水量增大,比值几乎不变,C 中)()()()(423423++⋅=⋅NH n O H NH n NH C O H NH C ,随加水量增大,比值减小。
D 中)(-OH C 减小。
答案:A【模拟试题】1. 下列物质中,导电性最差的是( )A. 熔融氢氧化钠B. 石墨棒C. 盐酸D. 固体氯化钾 2. 下列叙述中正确的是( )A. 氯化钠溶液中,氯化钠在电流的作用下电离成钠离子或氯离子B. 溶于水后能电离出氢离子的化合物都是酸C. 硫酸钡难溶于水,但硫酸钡是强电解质D. 2SO 溶于水后部分电离,故二氧化硫属于弱电解质 3. 下列事实中能证明氯化氢是共价化合物的是( ) A. 氯化氢极易溶于水 B. 液态氯化氢不导电 C. 氯化氢不易分解 D. 氯化氢溶液可以电离4. 某物质的水溶液能导电,且该物质属于非电解质,溶于水时化学键被破坏的是( ) A. 液溴 B. 干冰 C. 蔗糖 D. 硫酸钡5. 下列各组物质反应后,溶液的导电性比反应前明显增强的是( ) A. 向亚硫酸钠溶液中加液态溴 B. 向硝酸银溶液中通入少量氯化氢 C. 向氢氧化钠溶液中通入少量氯气 D. 向硫化氢饱和溶液中通入少量氯气6. 相同温度下,两种稀氨水A 和B ,浓度分别为12.0-⋅L mol 和1.01-⋅L mol ,则A 、B 的-OH 浓度之比为( )A. 大于2B. 小于2C. 等于2D. 不能肯定 7. 下列电离方程式正确的是( ) A. 43PO H -++343PO H B. 3CaCO -++232CO CaC. NaHS-++++2S H Na D. 3)(OH Fe -++OH Fe 338. 对某弱酸稀溶液加热时,下列叙述错误的是( )A B C D 11. 写出下列电离方程式:(均为L mol /1.0) (1)42HPO Na (2)4NaHSO其中在水中存在电离平衡的是 。
选修1 弱电解质的电离知识点(1)

弱电解质的电离一、强弱电解质:1.电解质与非电解质(1)电解质:在水溶液中或熔融状态下能导电的化合物。
(常见电解质:酸、碱、盐、金属氧化物、水。
)(2)非电解质:在________________都不导电的化合物。
(常见非电解质:大多数有机物(如:蔗糖、酒精)、非金属氧化物、NH3。
)2.强电解质和弱电解质(1)强电解质①定义:在水溶液中能够完全电离的电解质。
②常见的强电解质:强酸、强碱和大多数盐。
(2)弱电解质①定义:在水溶液中只能部分电离的电解质。
②常见的弱电解质:弱酸、弱碱、少部分盐(HgCl2)和水。
二、弱电解质的电离平衡1.电离平衡状态的含义在一定条件(如温度、浓度一定)下,弱电解质在溶液中电离成离子的速率和离子结合成分子的速率相等,电离过程就达到了平衡状态。
提醒:一定条件下,弱电解质达到电离平衡后,还会继续电离,只是电离成离子的速率和离子结合成分子的速率相等。
2.强、弱电解质电离方程式的书写规则(1)强电解质完全电离,在写电离方程式时,用“”。
H2SO4 2H++SO42-Ba(OH)2 2OH-+Ba2+NH4Cl NH4++Cl-(2)弱电解质部分电离,在写电离方程式时,用“”。
①一元弱酸、弱碱一步电离。
CH3COOH ⇋CH3COO-+ H+NH 3·H 2O ⇋ NH 4++OH -②多元弱酸分步电离,必须分步写出,不可合并(其中以第一步电离为主)。
H 2CO 3⇋ HCO 3-+ H +(主);HCO 3-⇋ CO 32-+ H +(次)。
③多元弱碱分步电离(较复杂),在中学阶段要求一步写出。
Fe(OH)3 ⇋ Fe 3++3OH - 三、电离常数 1.表示方法 对于ABA++B −,K=。
3.有关电离平衡常数的计算以弱酸HX 为例:(1)已知c (HX)和c (H +),求电离平衡常数HXH + + X -起始:c (HX) 0 0 平衡:c (HX)-c (H +c (H +) c (H +)则:K == 由于弱酸只有极少一部分电离,c (H +)的数值很小,可做近似处理:c (HX)-c (H +)≈c (HX),则K = ,代入数值求解即可。
弱电解质的电离平衡考点归纳

弱电解质的电离平衡考点归纳弱电解质电离平衡是电解质理论的基础,也是中学化学基本理论中的重要组成部分,近几年高考命题中反复考查。
在学生已经学过化学平衡理论并了解电解质在水溶液中发生电离和离子间发生反应等知识的基础上,进一步学习弱电解质的电离平衡。
高考命题的热点主要有影响弱电解质电离平衡因素,通过图象分析弱电解质和强电解质,电离常数和电离度等,为了更好的学习这一部分内容,本文做了详细的总结和归纳,希望对同学们的学习有所启发,达到触类旁通的效果。
一、弱电解质电离平衡1.电离平衡概念一定条件(温度、浓度)下,分子电离成离子的速率和离子结合成分子的速率相等,溶液中各分子和离子的浓度都保持不变的状态叫电离平衡状态,简称电离平衡。
任何弱电解质在水溶液中都存在电离平衡,达到平衡时,弱电解质在该条件下的电离程度最大。
2.电离平衡的特征电解质的电离平衡属于化学平衡中的一种形式,具有以下一些特征:“逆”——弱电解质的电离是可逆的,存在电离平衡“动”——电离平衡是动态平衡“等”——v(=v(分子化)≠0离子化)“定”——达到电离平衡状态时,溶液中分子和离子的浓度保持不变,是一个定值“变”——电离平衡是相对的,外界条件改变时,平衡被破坏,发生移动形成新的平衡。
二、影响弱电解质电离平衡的因素(符合勒?夏特列原理)1.内因:弱电解质本身的性质,是决定性因素。
2.外因①温度: 升高温度,由于电离过程吸热,平衡向电离方向移动,电离程度增大。
②浓度: 加水稀释,使弱电解质的浓度减小,电离平衡向电离的方向移动,电离程度增大。
因为溶液浓度越小,离子相互碰撞结合成分子的机会越小,弱电解质的电离程度就越大;所以,稀释溶液会促进弱电解质的电离。
例如:在醋酸的电离平衡CH3COOH CH3COO-+H+A 加水稀释,平衡向正向移动,电离程度变大,但c(CH3COOH)、c(H+)、c(CH3COO-)变小;B 加入少量冰醋酸,平衡向正向移动,c(CH3COOH)、c(H+)、c(CH3COO-)均增大但电离程度小;③外加相关物质(同离子效应)例如:0.1 mol/L的CH 3COOH溶液CH3COOH CH3COO-+ H+向其中加入CH3COONa固体,溶液中c(CH3COO-)增大,CH3COOH的电离平衡向左移动,电离程度减小,c(H+)减小,pH增大。
弱电解质的电离

练习
2.下列说法不正确的是
①②③④⑤
(
)
①将 BaSO4 放入水中不能导电,所以 BaSO4 是非电解质 ②氨溶于水得到的氨水能导电,所以氨水是电解质 ③固态共价化合物不导电,熔融态的共价化合物可以导 电 ④固态的离子化合物不导电,熔融态的离子化合物也不 导电 ⑤强电解质溶液的导电能力一定比弱电解质溶液的导电 能力强
3.外界条件对电离平衡的影响 (1)内因:弱电解质本身的性质。 (2)外因:
(1)温度 电离过程是吸热过程,温度升高,平衡向 电离方向移动。 (2)浓度 弱电解质浓度越大,电离程度越小。 (3)其他因素 同离子效应(即在弱电解质溶液中加入同弱 电解质具有相同离子的强电解质,使电离 平衡向逆方向移动)
电解质 强电解质 判 电离特点 别 据
=
弱电解质※
部分电离存在水 之外的电离平衡
非电解质
不电离 非金属氧化 物、多数有 机物、NH3等
完全电离不存在水之外 的电离平衡
强酸、强碱、大 依 物质类别 部分盐、活泼金 属的氧化物 溶液中存 在的微粒 化合物类型 阴、阳离子 离子化合物、 部分共价化合物
弱酸、弱碱、 水 既有离子(少), 又有分子(大部分) 共价化合物
第一节 弱电解质的电离
1.了解电解质的概念;了解强、弱电解 质的概念。 2.了解电解质在水溶液中的电离以及电 解质溶液的导电性。 3. 了 解 弱 电 解 质 在 水 溶 液 中 的 电 离 平 衡。 4.了解电离平衡常数。
重点:弱电解质的电离平衡,
主要考点有四个: 一、是强、弱电解质的判断与比较; 二、是外界条件对电离平衡的影响,常结合图像进行 考查,同时考查溶液 pH 变化及导电性; 三、是电离平衡常数,这是高考新增考点,主要考查 有关计算。 四、预测弱电解质的电离平衡与生物酸碱平衡相结合 的命题在今后的高考中可能出现。
《化学反应原理》复习之《弱电解质的电离平衡》知识要点

《弱电解质的电离平衡》知识要点一、强电解质和弱电解质1、电解质【提醒】常见的强弱电解质(1)强电解质:①强酸:HCl、H2SO4、HNO3、HClO4、HBr、HI、HMnO4②强碱:NaOH、Ca(OH)2、Ba(OH)2、KOH、RbOH…③大部分盐:(2)弱电解质:①弱酸:如H2S、H2CO3、CH3COOH、HF、HCN、HClO等。
HF酸是具有强极性共价键的弱电解质。
H3PO4、H2SO3从其酸性强弱看属于中强酸,但仍属于弱电解质、②弱碱:NH3·H2O,多数不溶性的碱[如Fe(OH)3、Cu(OH)2等]、两性氢氧化物[如Al(OH)3、Zn(OH)2等]。
③个别的盐:如HgCl2,HgBr2等。
④水:是由强极性键构成的极弱的电解质。
2、电离方程式的书写:(1)强电解质用“=”,H2SO4===2H++SO错误!;弱电解质用“” CH3CO OHCH3COO-+H+(2)多元弱酸分步电离,且第一步电离程度远远大于第二步电离,如碳酸的电离:H2CO3H++HCO错误!HCO错误!H++CO错误!(3)多元弱碱的电离分步进行,为书写方便写成一步,如氢氧化铁的电离方程式为 Fe(OH)3Fe3++3OH-(4)可溶性酸式盐电离时,①强酸的酸式盐完全电离。
例如:NaHSO4=== Na++H++SO2-4。
②弱酸的酸式盐中酸式根不能完全电离。
例如:NaHCO3=== Na++HCO错误!HCO错误!H++CO2—3 (5)Al(OH)3存在酸式与碱式电离两种形式:H++AlO错误!+H2O错误!Al(OH)3错误!Al3++3OH-酸式电离碱式电离二、弱电解质的电离平衡1。
电离平衡的建立在一定条件(如温度、浓度)下,当弱电解质分子电离成离子的速率和离子重新结合成分子的速率相等时,电离过程就达到了平衡状态—-电离平衡、(一种特别的化学平衡)2。
电离平衡的特点:逆:弱电解质的电离可逆过程等:V(电离)=V(结合)≠0动:电离平衡是一种动态平衡定:条件一定,平衡体系中分子与离子的浓度一定变:条件改变时,电离平衡发生移动。
【知识解析】弱电解质的电离

弱电解质的电离1 电离方程式(1)相关概念电解质在水溶液中或熔融状态下产生自由移动的离子的过程叫做电离。
表示电解质在水溶液中或熔融状态下电离成能够自由移动的离子的式子叫做电离方程式。
(2)电离方程式的书写①强电解质:完全电离,用“===”。
如: HCl===H ++Cl -NaOH===Na ++OH -NaNO 3===Na ++NO - 3 ②弱电解质:部分电离,用“”。
如:CH 3COOH CH 3COO -+H +NH 3·H 2ONH + 4+OH -③多元弱酸的电离分步进行,以第一步电离为主。
如: H 2CO 3H ++HCO - 3(主要) HCO 3-H ++CO 2- 3(次要)④多元弱碱的电离也分步进行,但是一般用一步电离表示。
如: Cu (OH )2Cu 2++2OH -深化理解(1)酸式盐:强酸的酸式盐完全电离,一步完成。
如:NaHSO 4===Na ++H ++SO 2- 4(水溶液),NaHSO 4===Na ++HSO - 4(熔融状态)。
弱酸的酸式盐强中有弱,分步完成。
如:NaHCO 3===Na ++HCO - 3,HCO 3-H ++CO 2- 3。
(2)两性化合物:双向电离。
如:。
2 电离平衡(1)概念电离平衡:一定条件(如一定温度、浓度)下,当弱电解质分子电离成离子的速率和离子重新结合成弱电解质分子的速率相等时,电离过程就达到了平衡状态,这叫做电离平衡。
图3-1-1(2)特征弱电解质电离平衡的特征可概括为六个字——“弱”“逆”“等”“动”“定”“变”。
具体特征为3 弱电解质电离平衡的影响因素注意弱电解质的电离是吸热过程,即ΔH>0。
但也有极少数弱电解质,其电离是放热过程.如HF(aq)H+(aq)+F-(aq)ΔH<0。
(1)内因:电解质本身的性质决定了弱电解质在水中达到电离平衡时电离程度的大小。
(2)外因①温度:一般情况下,由于弱电解质的电离过程吸热,因此升高温度,电离平衡向电离方向移动,电离程度增大。
弱电解质的电离平衡知识点

一、弱电解质的电离1、定义:电解质:在水溶液中或熔化状态下自身能够电离出自由移动离子的化合物;叫电解质..非电解质:在水溶液中且熔化状态下自身都不能电离出自由移动离子的化合物..概念理解:①电解质、非电解质都是化合物;能导电的物质可能是溶液混合物、金属单质;但他们不属于电解质非电解质的研究对象;因此他们既不是电解质也不是非电解质;②自身电离:SO2、NH3、CO2、等化合物能和水反应形成酸或碱;但发生电离的并不是他们本身吗;因此属于非电解质;③只能在水中发生电离的电解质有酸或者某些易溶于水高温下易分解的盐;如液态氯化氢是化合物;只存在分子;没有发生电离;因此不能导电;又如NaHCO3在高温时即分解;不能通过熔融态证明其为电解质;只能在熔融状态下电离的电解质是活泼金属氧化物;如Na2O、CaO;他们在溶液中便不存在;要立刻反应生成键;因此不能通过溶液中产生离子证明;既能在水溶液中又能在溶液中发生电离的物质是某些高温难分解盐;绝大多数盐溶解在水中都能发生完全电离;某些盐熔融时也发生电离;如BaSO4..④电离不需要通电等外界条件;在熔融或者水溶液中即能够产生离子;⑤是电解质;但是要产生离子也要在溶液状态或者熔融状态;否则即便存在离子也无法导电;比如NaCl;晶体状态不能导电..⑥电解质的强弱与导电性、溶解性无关..如如BaSO4不溶于水;但溶于水的BaSO4全部电离;故BaSO4为强电解质..导电性与自由移动离子的浓度和带电荷数等有关..强电解质:在水溶液里全部电离成离子的电解质..弱电解质:在水溶液里只有一部分电离成离子的电解质 ..2.常见的电解质为酸碱盐、活泼金属氧化物、水;其中强电解质与偌电解质常见分类:3、电离方程式的书写——“强等号;弱可逆;多元弱酸分步离”①强电解质:如H2SO4:H2SO4===2H++SO错误! ..②弱电解质a.一元弱酸;如CH3COOH:CH3COOH CH3COO-+H+..b.多元弱酸;分步电离;分步书写且第一步电离程度远远大于第二步的电离程度;如H2CO3:H2CO3H++HCO错误!、HCO错误!H++CO错误!..原因是上一级电离出的H+是下一级电离的产物;对下一级电离电离有抑制作用c .多元弱碱;虽然分布电离;但是书写时一步到位..如FeOH 3:FeOH 3Fe 3++3OH -.. ③酸式盐a .强酸的酸式盐b .弱酸的酸式盐:“强中有弱”;如NaHCO 3:NaHCO 3===Na ++HCO 错误!、HCO 错误!H ++CO 错误! ..4.弱电解质的电离平衡 1电离平衡的建立在一定条件如温度、浓度等下;当弱电解质分子电离成离子的速率和离子结合成弱电解质分子的速率相等时;电离过程就达到平衡..平衡建立过程如图所示..2电离平衡的特征3影响弱电解质电离平衡的因素内因:弱电解质本身的性质;是决定因素..4电离过程是可逆过程;可直接用化学平衡移动原理分析电离平衡..以0.1 mol·L -1CH 3COOH 溶液为例:CH 3COOH CH 3COO -+H +正向吸热..实例稀溶液CH 3COOHH ++CH 3COO - ΔH >0平衡移动方导电能1.表达式1对于一元弱酸HAHA H++A-;平衡常数K a=错误!..2对于一元弱碱BOHBOH B++OH-;平衡常数K b=错误!..2.特点1电离平衡常数错误!2多元弱酸是分步电离的;各级电离平衡常数的大小关系式是K1K2 K3……;所以多元弱酸的酸性决定于其第一步电离..3.意义相同条件下;K值越大;表示该弱电解质越易电离;所对应的酸性或碱性相对越强..如相同条件下常见弱酸的酸性强弱:H 2SO3>H3PO4>HF>CH3COOH>H2CO3>H2S>HClO..4.实例1填写下表2CH 3COOH 酸性大于HClO 酸性填“大于”“小于”或“等于”;判断的依据:相同条件下;电离常数越大;电离程度越大;c H +越大;酸性越强..3磷酸是三元中强酸①磷酸的电离方程式是H 3PO 4H ++H 2PO 错误!、H 2PO 错误!H ++HPO 错误!、HPO 错误!H ++PO 错误!..②电离平衡常数表达式是:K a1=错误!;K a2=错误!;K a3=错误!.. ③比较大小:K a1>K a2>K a3.. 5.电离常数的计算 以弱酸HX 为例:1已知c HX 和c H +;求电离常数 HXH + + X -起始mol·L -1:c HX 0 0 平衡mol·L -1:c HX -c H + c H + c H + 则:K =错误!=错误!..由于弱酸只有极少一部分电离;c H +的数值很小;可做近似处理:c HX -c H +≈c HX;则K =错误!;代入数值求解即可..2已知c HX 和电离常数;求c H +HXH + + X -起始: c HX 0 0 平衡: c HX -c H + c H + c H +则:K=错误!=错误!由于K值很小;c H+的数值很小;可做近似处理:c HX-c H+≈c HX;则:c H+=错误!;代入数值求解即可..强酸与弱酸或强碱与弱碱的比较1.一元强酸与一元弱酸的比较判断一种酸是强酸还是弱酸时;其实质就是看它在水溶液中的电离程度;完全电离即为强酸;不完全电离即为弱酸..还可以证明溶液中是否存在该电解质的电离平衡;存在电离平衡的为弱电解质;反之为强电解质..最常用实验验证方法有:1测0.01 mol·L -1 HA 溶液的pH;若pH =2;HA 是强酸;若pH>2;HA 是弱酸..2测NaA 溶液的pH;若pH =7;HA 为强酸;若pH>7;则HA 为弱酸.. 3.稀释时溶液pH 变化特点比较如图:a 、b 分别为pH 相等的NaOH 溶液和氨水稀释曲线..c 、d 分别为pH 相等的盐酸和醋酸溶液稀释曲线..请体会图中的两层含义:1加水稀释相同倍数后的pH 大小:氨水>NaOH 溶液;盐酸>醋酸溶液..若稀释10n倍;盐酸、NaOH 溶液pH 变化n 个单位;但pH<7或pH>7;不能pH =7;而氨水与醋酸溶液pH 变化不到n 个单位..2稀释后的pH 仍然相等;则加水量的大小:氨水>NaOH 溶液;醋酸溶液>盐酸..易错警示 1酸碱的强弱和溶液酸碱性的强弱不是等同关系;前者看电离程度;后者看溶液中c H +和c OH -的相对大小..强酸溶液的酸性不一定比弱酸溶液的酸性强..2弱酸、弱碱是弱电解质;但它们对应的盐一般为强电解质;如醋酸铵:CH 3COONH 4===NH 错误!+CH 3COO -..强、弱电解质的判断方法1在相同浓度、相同温度下;比较导电能力的强弱..如同体积同浓度的盐酸和醋酸;前者的导电能力强于后者..2在相同浓度、相同温度下;比较反应速率的快慢;如将锌粒投入到等浓度的盐酸和醋酸中;速率前者比后者快..3浓度与pH 的关系;如0.01 mol·L -1的醋酸溶液pH>2;说明醋酸是弱酸..4测对应盐的酸碱性;如CH 3COONa 溶液呈碱性;则证明醋酸是弱酸.. 5稀释前后的pH 与稀释倍数的变化关系..如将pH =2的酸溶液稀释1000倍;若pH<5;则证明酸为弱酸;若pH =5;则证明酸为强酸..6采用实验证明存在电离平衡;如醋酸溶液中滴入石蕊试液变红;再加CH 3COONH 4晶体;颜色变浅..7利用较强酸碱制备较弱酸碱判断电解质强弱..如将CO 2通入苯酚钠溶液中;出现浑浊..说明碳酸酸性大于苯酚..8同pH 的强酸和弱酸;分别加该酸的钠盐固体;溶液的pH 增大的是弱酸;pH 几乎不变的是强酸..9pH 相同、体积相同的强酸和弱酸与碱反应时消耗碱多的为弱酸..二、极弱电解质--水的电离和溶液的酸碱性水的电离1.电离方程式水是一种极弱的电解质;电离方程式为2H 2O H 3O ++OH -;简写为H 2OH ++OH -..2.水的离子积常数K w =c H +·c OH -..1室温下:K w=1×10-14..2影响因素:只与温度有关;温度一定;则K值一定..水的电离是吸热W过程;升高温度;K w增大..= H+·OH- = 110-1425℃时; H+=OH- =10-7 mol/L ; KW3适用范围:K w不仅适用于纯水;也适用于稀的电解质水溶液..3.关于纯水的几个重要数据4.影响水的电离平衡的因素和影响K w的因素1加热;促进水的电离;K w增大..2加入酸或碱;抑制水的电离;K w不变..3①加入强酸强碱的正盐;不影响水的电离..②加入强酸的酸式盐;抑制水的电离..③加入可水解的盐如FeCl 3、Na 2CO 3、NH 4Cl;促进水的电离.. 4加入与水反应的活泼金属如Na 、K;促进水的电离..易错警示 1任何情况下水电离产生的c H +和c OH -总是相等的.. 2水的离子积常数适用于任何酸、碱、盐的稀溶液..即K w =c H +·c OH-中的c H +、c OH -分别是溶液中H +、OH -的总浓度;不一定是水电离出的c H +和c OH -..3水中加酸或碱对水的电离均有抑制作用;因此;室温下;若由水电离出的c H +<1×10-7 mol·L -1;该溶液可能显酸性;也可能显碱性..小结:常温下水电离产生c H +和c OH -计算的5种类型任何水溶液中水电离产生的c H +和c OH -总是相等的;有关计算有以下5种类型以常温时的溶液为例..1中性溶液:c OH -=c H +=10-7 mol·L -1.. 2酸的溶液——OH -全部来自水的电离..实例:pH =2的盐酸中c H +=10-2 mol·L -1;则c OH -=K w /10-2=1×10-12mol·L -1;即水电离出的c H +=c OH -=10-12 mol·L -1.. 3碱的溶液——H +全部来自水的电离..实例:pH =12的NaOH 溶液中c OH -=10-2 mol·L -1;则c H +=K w /10-2=1×10-12mol·L -1;即水电离出的c OH -=c H +=10-12 mol·L -1..4水解呈酸性的盐溶液——H +全部来自水的电离..实例:pH =5的NH 4Cl 溶液中;由水电离出的c H +=10-5 mol·L -1;因部分OH -与部分NH 错误!结合使c OH -=10-9 mol·L -1..5水解呈碱性的盐溶液——OH-全部来自水的电离..实例:pH=12的Na2CO3溶液中;由水电离出的c OH-=10-2mol·L-1;因部分H+与部分CO错误!结合使c H+=10-12mol·L-1..注意:要区分清楚溶液组成和性质的关系;酸性溶液不一定是酸溶液;碱性溶液不一定是碱溶液..。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
【选修四】弱电解质的电离知识要点与方法指导【知识要点】一、电解质有强弱之分(不同的电解质在水溶液中的电离程度是不一样的)1、知识回顾:电解质:在水溶液中或熔化状态下能够导电的化合物例:酸、碱、盐、H2O等非电解质:在水溶液和熔化状态下都不能导电的化合物例:大多数有机物、SO3、CO2等2、强、弱电解质:⑴观察试验3-1:得出强电解质与弱电解质的概念实验3-1:体积相同、浓度相同的盐酸和醋酸与等量镁条(Mg条使用前应用砂纸除去表面的氧化膜)反应,并测量溶液的pH值。
实验表明浓度相同的盐酸和醋酸溶液的pH值不同,并且1mol/L HCl与镁条反应剧烈,而1 mol/L CH3COOH与镁条反应较慢。
说明两种溶液中的H+浓度是不同的。
1 mol/L HCl 溶液中氢离子浓度大,氢离子浓度为1 mol/L,说明HCl完全电离;1mol/L CH3COOH溶液中氢离子浓度较盐酸小,小于1 mol/L,说明醋酸在水中部分电离。
所以不同电解质在水中的电离程度不一定相同。
注:反应速率快慢与Mg条的表面积大小及H+浓度有关⑵强、弱电解质的概念根据电解质在水溶液中离解成离子的程度大小分为强电解质和弱电解质:①强电解质:在水分子作用下,能完全电离为离子的电解质。
包括大多数盐类、强酸、强碱、部分碱性氧化物等例:NaCl电离方程式NaCl = Na++Cl-②弱电解质:在水分子作用下,只有部分分子电离的电解质。
包括弱酸(如HAc、H2S)、弱碱(如NH3·H2O) 、Al(OH)3、H2O等例:CH 3COOH电离方程式 CH3COOH CH3COO-+H+小结:二、弱电解质的电离过程是可逆的(属于化学平衡的一种,符合平衡移动原理)弱电解质溶于水时,在水分子的作用下,弱电解质分子电离出离子,而离子又可以重新结合成分子。
因此,弱电解质的电离过程是可逆的。
分析CH3COOH的电离过程:CH3COOH的水溶液中,既有CH3COOH分子,又有CH3COOH电离出的H+和CH3COO-,H+和CH3COO-又可重新结合成CH3COOH分子,因此CH3COOH分子电离成离子的趋向和离子重新碰撞结合成CH3COOH分子的趋向并存,电离过程是可逆的,同可逆反应一样,最终也能达到平衡。
1、弱电解质的电离平衡定义:在一定条件(如温度、浓度)下,当电解质分子电离成离子的速率和离子重新结合成分子的速率相等时,电离过程就达到了平衡状态例:CH3COOH的电离平衡的建立过程,开始时c(醋酸)最大,而离子浓度最小——为0,所以弱电解质分子电离成离子的速率从大到小变化;离子结合成电解质分子的速率从小到大变化。
2、弱电解质的电离平衡特征:弱电解质的电离平衡属于化学平衡中的一种,具有以下一些特征:“逆”——弱电解质的电离是可逆的“动”——电离平衡是动态平衡“等”——v(离子化)=v(分子化)≠0“定”——在电离平衡状态时,溶液中分子和离子的浓度保持不变。
“变”——电离平衡是相对的、暂时的,当外界条件改变时,平衡就会发生移动3、电离方程式的书写弱电解质的电离是可逆的,存在电离平衡,电离平衡与化学平衡类似,书写电离方程式时也要用“”表示。
例:CH 3COOH CH3COO- + H+NH 3·H 2ONH 4+ +OH -H 2O H + + OH - 多元弱酸分步电离,多元弱碱一步电离例: H2CO 3HCO 3- + H + HCO 3- CO 32- + H +三、电离常数(可用于比较不同弱电解质的相对强弱、电离程度的相对大小)与化学平衡常数相似,在弱电解质溶液中也存在着电离平衡常数,叫做电离常数。
电离常数只与温度有关,能用来计算弱酸溶液中的H +的浓度及比较弱酸酸性的相对强弱例如,醋酸、碳酸和硼酸298K 时的电离常数分别是1.75×10-5,4.4×10-7(第一步电离)和5.8×10-10,由此可知,醋酸、碳酸和硼酸的酸性依次减弱1、一元弱酸和弱碱的电离平衡常数HA H ++ A -MOHM ++OH -注: ①K 越大,离子浓度越大,表示该弱电解质越易电离。
所以可以用K a 或K b 的大小判断弱酸或弱碱的相对强弱。
②K 只与温度有关,不随浓度改变而改变。
2、多元弱酸(碱)分步电离,酸(碱)性主要由第一步电离决定。
例:H 3PO 4的电离:H3PO 4H + + H 2PO 4-K 1 H2PO 4- H + + HPO 42- K 2HPO42- H + + PO 43- K 3注:第一步电离产生的H +对第二步、第三步电离产生抑制,一般K 1K 2 K 3 ,所以多元弱酸(碱)分步电离,酸(碱)性主要由第一步电离决定。
[方法指导]一、电解质与非电解质注意的几个问题 ①电解质与非电解质都是化合物,单质和混合物既不是电解质也不是非电解质例:石墨能导电,但不是电解质;盐酸能导电,但不是电解质②CO 2、NH 3等溶于水得到的水溶液能导电,但它们不是电解质,因为导电的物质不是其本身例:H 2CO 3、NH 3·H 2O 都是电解质,而CO 2、NH 3都是非电解质③难溶的盐(BaSO 4等)虽然水溶液不能导电,但是在融化时能导电,也是电解质。
二、强、弱电解质的区别电解质的强弱由物质内部结构决定,强、弱电解质区别在于水溶液中的电离程度:电解质强电解质弱电解质键型离子键、极性键极性键电离程度完全电离部分电离电离过程不可逆过程可逆过程,存在电离平衡表示方法电离方程式用“=”电离方程式用“”电解质在溶液中的存在形式水合离子分子、水合离子三、电解质的强弱与导电性的关系强、弱电解质的区分依据不是看该物质溶解度的大小,也不是看其水溶液导电能力的强弱,而是看溶于水的部分是否完全电离。
CaCO3、Fe(OH)3的溶解度都很小,CaCO3属于强电解质,而Fe(OH)3属于弱电解质;CH3COOH、HCl的溶解度都很大,HCl属于强电解质,而CH3COOH 属于弱电解质。
电解质的强弱在一定情况下影响着溶液导电性的强弱。
导电性的强弱是由溶液中离子浓度大小决定的。
如果某强电解质溶液浓度很小,那么它的导电性可以很弱(CaCO3、AgCl);而某弱电解质虽然电离程度小,但浓度较大时,该溶液的导电能力也可以较强。
因此,强电解质溶液的导电能力不一定强,弱电解质溶液的导电能力也不一定弱。
四、弱电解质电离平衡的影响因素电离平衡是化学平衡的一种,符合平衡移动原理。
弱电解质电离程度的大小主要决定于本身,但受外界条件的影响①浓度:弱电解质溶液中,水越多,浓度越稀,则弱电解质的电离程度越大。
例:CH3COOH溶液加水浓度变稀,会使平衡右移,电离程度增大。
CH3COO-、H+的物质的量增加,但浓度减小②温度:电离过程需吸收能量,所以升高温度,电离程度增加。
由于电离过程中热效应较小,温度改变对电离常数的影响不大,其数量级一般不变,所以室温范围内可以忽略温度对电离平衡的影响。
③同离子效应:若向弱电解质溶液中加入与弱电解质相同的离子,则会使平衡左移,弱电解质的电离程度减小。
④离子反应效应:若向弱电解质溶液中加入能与弱电解质的离子结合的离子,则会使平衡右移,弱电解质的电离程度变大例:0.1 mol/L的CH 3COOH溶液 CH3COOH CH3COO-+ H+电离程度n(H+)c(H+)导电能力加水增大增多减小减弱升温增大增多增大增强加CH3COONa减小减少减小增强加HCl减小增多增大增强加NaOH增大减少减小增强[经典例题]例题1、下列物质中①NaCl溶液、②NaOH 、③H2SO4、④Cu、⑤CH3COOH、⑥NH3·H2O、⑦CO2、⑧乙醇、⑨水,____________是电解质;__________是非电解质;____________既不是电解质,也不是非电解质。
思路点拨:本题考察基本概念的记忆与理解,电解质指的是在水溶液中或熔化状态下能够导电的化合物;而非电解质指的是在水溶液和熔化状态下都不能导电的化合物解析:首先判断是否是化合物,然后判断水溶液中或熔化状态下能否导电,是化合物的有②③⑤⑥⑦⑧⑨【答案】②③⑤⑥⑨;⑦⑧;①④总结升华:一种物质是电解质还是非电解质,前提首先应该是化合物。
只要在水溶液中、熔化状态下任一条件导电,就是电解质,比如某些共价化合物熔化状态下都不导电,但溶于水可以导电,所以就是电解质;水溶液中、熔化状态下都不导电才是非电解质举一反三:下列事实中能证明氯化氢是共价化合物的是().A、氯化氢极易溶于水B、液态氯化氢不导电C、氯化氢不易分解D、氯化氢溶液可以电离【答案】B 解析:液态时能导电的化合物一定是离子化合物,所以B选项正确例题2、下列物质能导电的是______,属于强电解质的是______,属于弱电解质的是________,属于非电解质的是_______。
a.铜丝b.金刚石c.石墨d.NaCle.盐酸f.蔗糖g.CO2h.Na2O i.硬脂酸j.醋酸l.碳酸氢铵m.氢氧化铝 n.氯气 o. BaSO4思路点拨:注意概念的区分,能否导电与是否强、弱电解质无关系解析:铜丝是金属能导电,石墨能导电,盐酸是溶液能导电,其他的根据所学概念仔细辨析【答案】ace;dhlo;ijm;fg总结升华:即使是电解质也必须在某种特定条件下才能导电,例:NaCl是电解质,但必须在熔化状态下或在溶液中才能导电;强、弱电解质本质区别是在水溶液中的电离程度,而不是在水溶液中的导电性举一反三:在甲酸的下列性质中,可以证明它是弱酸的是()A、1 mol/L的甲酸溶液中c(H+)约为1×10-2 mol/LB、甲酸能与水以任意比例互溶C、1 mol/L的甲酸溶液10 mL恰好与10 mL 1 mol/L的NaOH溶液完全反应D、在相同条件下,甲酸溶液的导电性比盐酸弱解析:甲酸为一元酸,AD选项证明甲酸溶液未完全电离【答案】AD例题3、把0.05 mol NaOH固体分别加入到100 mL下列液体中,溶液的导电能力变化最小的是()A、自来水B、0.5 mol/L盐酸C、0.5 mol/L CH3COOH溶液D、0.5 mol/L KCl溶液思路点拨:溶液导电能力大小主要取决于溶液中离子浓度大小,离子浓度越大,导电能力就越强;反之,导电能力就越弱。
解析:由于自来水几乎不导电,加入0.05 mol NaOH后,导电性突然增大;醋酸是弱电解质,加入NaOH后,生成强电解质CH3COONa,导电性明显增强;0.5 mol/L的KCl中加入0.05 mol NaOH固体后,离子浓度增大,导电能力增强;只有0.5 mol/L的盐酸,能与NaOH 反应生成强电解质NaCl,不影响导电性。
