合成氨工艺原理
布朗工艺合成氨

布朗工艺合成氨
布朗工艺合成氨是工业上生产氨的主要方法之一,下面将为大家详细介绍其原理、过程和性能。
一、原理
布朗工艺合成氨的原理是利用催化剂(通常为铁、铑、钒等)使氮气与氢气在高压、高温条件下发生反应生成氨气。
这是一种可逆反应,温度、压力和催化剂等因素均会影响反应的实际情况。
二、过程
布朗工艺合成氨的过程可以分为以下几个步骤:
1.准备原料:将氮气和氢气进行净化、压缩和加热,使其达到合适的反应条件。
2.反应器:将准备好的原料送入反应器进行反应。
反应器内通常采用填充式催化剂床,反应物质流经催化剂并在催化剂表面发生反应。
3.分离:反应产物在反应器内逐渐积累,需要及时进行分离。
常用的分离方法包括冷凝、吸附等。
4.再生:分离出的副产物可进一步回收利用,催化剂因为反应后表面的玻璃化碳堆积而失去活性,需要进行再生。
三、性能
布朗工艺合成氨具有以下优点:
1.反应速度快:由于催化剂的存在,反应速度大大加快。
2.运行成本低:布朗工艺合成氨的原材料易于获得,且反应过程中不需要大量的能源支持。
3.产品纯度高:反应后产生的氨气往往非常纯,只需一些简单的操作就可以达到工业使用标准。
以上就是关于布朗工艺合成氨的原理、过程和性能的详细介绍。
合成氨工艺及反应原理简介

合成氨工艺及反应原理简介合成氨工艺采用烃类蒸汽转化法。
天然气经加压至4.05MPa,经预热升温在脱硫工序脱硫后,与水蒸汽混合,进入一段转化炉进行转化制H2,随后进入二段转化炉,在此引入空气,转化气在炉内燃烧放出热量,供进一步转化,同时获得N2。
工艺气经余热回收后,进入变换系统,将CO变为CO2,随后经脱碳、甲烷化反应除去CO和CO2,分离出的CO2送往尿素工艺。
工艺气进入分子筛系统除去少量水份,为合成氨提供纯净的氢氮混合气。
氢氮混合气经压缩至14MPa,送入合成塔进行合成氨的循环反应,少量惰性气体经过普里森系统分离进行回收利用。
产品氨送往尿素工艺和氨罐保存。
合成氨工艺的5个过程:1、天然气脱硫:R-SH+H2=RH+H2S H2S+ZnO=H2O(汽)+ZnS2、转化CH4+H20(汽)=CO+3H2 CH4+2H2O(汽)=CO2+4H2 (H2+ 1/2 O2=H2O)3、变换:CO+H2O(汽)=CO2+H24、脱碳:1)K2CO3+CO2+H2O⇔2KHCO32KHCO3⇔K2CO3+CO2+H2O2)甲烷化:CO+3H2=CH4+H2O CO2+4H2=CH4+2H2O5、N2+3H2=2NH31 脱硫系统工艺流程及原理1.1流程天然气进入界区后分为两路:一路作原料气,另一路作燃料气。
原料天然气进入原料气压缩机吸入罐116-F,除去携带的液体,经过原料气压缩机102-J被压缩到4.05MPa(G),经过原料气预热盘管预热到399℃,接着原料气与来自合成气压缩机103-J一段的富氢气混合。
经过Co-Mo加氢器101-D把有机硫转换成H2S,将3 ml/m3的有机硫转化为无机硫,原料气中总硫为30~90ml/m3左右,经氧化锌脱硫槽脱硫至总硫小于0.5mg/m3。
随后进入氧化锌脱硫槽,天然气中的硫化物被ZnO所吸附,制得合格原料气。
ZnO脱硫槽共二个,可以串联或并联操作,一般串联操作。
阀门及管线的配置可以使任何一个脱硫槽停止使用而另一个继续运转。
合成氨生产工艺
合成氨生产工艺合成氨生产原理:氨是一种重要的化工原料,特别是生产化肥的原料,它是由氢和氮合成。
合成氨工业是氮肥工业的基础。
为了生产氨,一般均以各种燃料为原料。
首先,制成含H2和CO等组分的煤气,然后,采用各种净化方法,除去气体中的灰尘、H2S、有机硫化物、CO、CO2等有害杂质,以获得符合氨合成要求的洁净的1:3的氮氢混合气,最后,氮氢混合气经过压缩至15Mpa以上,借助催化剂合成氨。
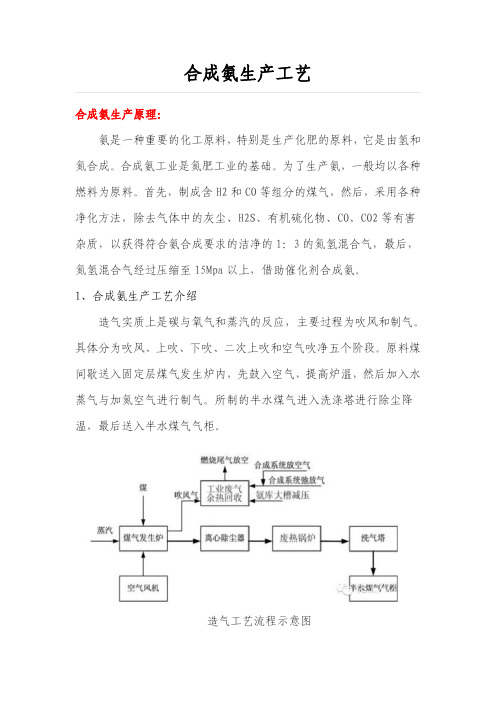
1、合成氨生产工艺介绍造气实质上是碳与氧气和蒸汽的反应,主要过程为吹风和制气。
具体分为吹风、上吹、下吹、二次上吹和空气吹净五个阶段。
原料煤间歇送入固定层煤气发生炉内,先鼓入空气,提高炉温,然后加入水蒸气与加氮空气进行制气。
所制的半水煤气进入洗涤塔进行除尘降温,最后送入半水煤气气柜。
造气工艺流程示意图2、脱硫工段煤中的硫在造气过程中大多以H2S的形式进入气相,它不仅会腐蚀工艺管道和设备,而且会使变换催化剂和合成催化剂中毒,因此脱硫工段的主要目的就是利用DDS脱硫剂脱出气体中的硫。
气柜中的半水煤气经过静电除焦、罗茨风机增压冷却降温后进入半水煤气脱硫塔,脱除硫化氢后经过二次除焦、清洗降温送往压缩机一段入口。
脱硫液再生后循环使用。
脱硫工艺流程图3、变换工段变换工段的主要任务是将半水煤气中的CO在催化剂的作用下与水蒸气发生放热反应,生成CO2和H2。
河南中科化工有限责任公司采用的是中变串低变工艺流程。
经过两段压缩后的半水煤气进入饱和塔升温增湿,并补充蒸汽后,经水分离器、预腐蚀器、热交换器升温后进入中变炉回收热量并降温后,进入低变炉,反应后的工艺气体经回收热量和冷却降温后作为变换气送往压缩机三段入口。
变换工艺流程图4、变换气脱硫与脱碳经变换后,气体中的有机硫转化为H2S,需要进行二次脱硫,使气体中的硫含量在25mg/m3。
脱碳的主要任务是将变换气中的CO2脱除,对气体进行净化,河南中科化工有限责任公司采用变压吸附脱碳工艺。
来自变换工段压力约为1.3MPa左右的变换气,进入水分离器,分离出来的水排到地沟。
在合成氨过程中,需要不断分离出氨的原因

在合成氨的工业生产过程中,需要不断分离出氨的原因有很多。
下面将从化学反应原理、工艺流程和工业需求三个方面进行详细阐述。
一、化学反应原理1. 氨的合成反应合成氨的主要反应是哈柏-博士过程,即N2 + 3H2 ⇌ 2NH3。
这是一个可逆反应,根据Le Chatelier原理,当氨逸出或过量氢气进入反应环境时,平衡会向右移,有利于生成更多氨。
2. 反应平衡的影响由于哈柏-博士反应是可逆的,反应达到平衡后会有一定比例的氮气、氢气和氨气存在于反应容器中。
为了增加产量,需要不断抽取、分离和收集生成的氨气,以减少反应物浓度和促进正向反应进行。
二、工艺流程1. 催化剂固定床反应器合成氨的工艺通常采用催化剂固定床反应器,将氮气和氢气通过铁、铑或钨等催化剂的作用转化为氨气。
在反应过程中,产生的氨气需要及时从反应器中分离出来,以避免对反应平衡产生负面影响。
2. 低温高压条件为了获得较高的氨合成速率和产率,工艺流程通常在较低的温度(400-550°C)和较高的压力(10-30 MPa)下进行。
在这种条件下,尤其需要不断分离出氨气,以保持反应的正常进行。
三、工业需求1. 提高氨产率工业生产中通常追求较高的氨产率,这就要求不断分离氨气,将产生的氨气从反应系统中剔除,从而减少对平衡位置的影响,提高氨的产率。
2. 安全生产合成氨的生产过程中,氨气是一种具有刺激性气味和腐蚀性的气体,必须将其及时分离并储存,以确保生产场所的安全。
氨气的分离也可以减少对环境的污染。
3. 产品纯度要求在一些工业领域,对合成氨的纯度要求较高,因此需要对合成氨进行分离和精馏,以获得高纯度的产品。
总结:在合成氨的工业生产过程中,需要不断分离出氨的原因主要包括化学反应原理、工艺流程和工业需求。
通过分离氨气,可以调节反应平衡、提高产率、保证安全和获得高纯度产品。
在合成氨生产过程中,对氨气的分离是一个至关重要的环节。
在合成氨的工业生产过程中,需要不断分离出氨的原因是多方面的,包括化学反应原理、工艺流程和工业需求。
合成氨工艺原理

合成氨工艺原理合成氨是一种重要的化工原料,广泛应用于肥料、化肥、炸药、染料、医药和塑料等工业领域。
合成氨工艺是通过氮气和氢气在催化剂的作用下发生反应,生成氨气的过程。
下面将介绍合成氨工艺的原理及相关知识。
首先,合成氨工艺的原理是利用哈伯-玻希过程进行氮气和氢气的催化反应。
在工业上,通常采用铁-钼催化剂,通过高温高压条件下进行反应。
氮气和氢气在催化剂的作用下,发生氮氢键的断裂和氢氮键的形成,生成氨气。
这个过程是一个放热反应,需要一定的温度和压力条件才能进行。
其次,合成氨工艺的原理还涉及到氮气和氢气的摩尔比。
在理想的情况下,氮气和氢气的摩尔比应该是1:3,这是为了保证所有的氮气都能够和氢气完全反应,生成氨气。
但在实际生产中,为了提高反应的效率和产量,通常会使用过量的氢气,以保证氮气得到充分利用。
另外,合成氨工艺的原理还涉及到催化剂的选择和运行条件的控制。
催化剂的选择对于反应的速率和选择性有着重要的影响。
铁-钼催化剂是目前应用最广泛的催化剂,它能够在较低的温度和压力下实现高效的氨气合成。
同时,工艺中的温度、压力、气体流速等参数的控制也是十分重要的,它们直接影响着反应的进行和产物的选择性。
最后,合成氨工艺的原理还涉及到反应平衡的问题。
氮气和氢气的反应是一个可逆反应,在一定条件下会达到动态平衡。
为了提高氨气的产量,通常会采取一些措施,如通过改变温度、压力或者利用吸收剂来移除产物,以促进反应向产物的方向进行。
综上所述,合成氨工艺的原理涉及到催化剂的选择、反应条件的控制、反应平衡的问题等多个方面。
通过合理的设计和操作,可以实现高效的合成氨反应,为相关工业领域提供重要的化工原料。
希望本文的介绍能够帮助大家更好地理解合成氨工艺的原理及相关知识。
合成氨工艺原理

合成氨工艺原理合成氨不论采用什么原料和生产方法,大体上包括三个工艺过程:(1)原料气的制造;( 2)原料气的净化(包括脱硫、变换脱除 CO,碳化、脱碳脱除 CO2,精炼脱除微量的 CO、 CO2、 H2S、 O2等);(3)氨的合成和为了满足气体净化及合成各工序工艺条件提供能量补偿的压缩工序。
生产出氨以后再根据需要加工成碳铵、尿素、硝铵等。
其详细原理如下(以煤为原料):一、造气工段合成氨生产所用的半水煤气,要求气体中(CO+H2)与 N2的比例为 3:1 左右。
因此生产上采用间歇地送入空气和蒸汽进行气化,将所得的水煤气配入部分吹风气制成半水煤气。
即以石灰碳化煤球、无烟块煤为原料,在高温下交替与空气和过热蒸汽进行气化反应( C+O2点燃 CO2+Q 、2C+O点燃 2CO+Q、2CO+O2点燃 2CO+Q2H2O(气) +C△CO+2H-Q 制得半水煤气,半水煤气经过除尘,余热回收,水洗降温制得合格的半水煤气,供后工段使用。
二、脱硫工段从造气工段的半水煤气中,除氢气和氮气外,还含有 27%左右 CO、9%左右的 CO2以及少量的硫化物,这些硫化物对合成氨生产是有害的。
它会腐蚀设备、管道,会引起催化剂中毒,会损坏铜液成份。
因此,必须除去少量硫化物,其原理:3用稀氨水(10—15tt )与硫化氢反应(NH3+H2S=NH4HS)将 H2 S 脱除至 0.07g/m (标)以下,使半水煤气净化,以满足合成氨生产工艺要求。
三、变换工段将脱 S 后的半水煤气(含 CO25%—28%)由压缩工段加压后经增温、加热,在一定的温度和压力下,在变换炉内借助催化剂的催化作用,使半水煤气中 CO与 H2O (气)进行化学反应,转变为 CO2和 H2(CO+H2O(气)催化剂高温 CO2+H2+Q),制得合格的变换气,以满足后工段的工艺要求。
其次,系统中设有饱和热水塔、甲交、一水加、二水加、冷却塔等换热设备,以便合理利用反应热和充分回收余热,降低能耗,同时降低变换气温度。
工业合成氨知识点总结

工业合成氨知识点总结一、引言合成氨是一种重要的化工原料,广泛用于化肥、塑料、药品和其他化工产品的生产中。
而工业合成氨主要是通过哈伯-玻斯曼过程进行生产。
在这个过程中,氮气和氢气以高压、高温和催化剂的作用下,发生反应,生成氨气。
因此,工业合成氨的生产涉及了高压、高温、催化剂和气体分离等方面的工艺技术。
二、合成氨的反应原理工业合成氨的反应过程是氮气和氢气在催化剂的作用下,发生氧化还原反应,生成氨气。
这是一个放热反应,反应方程式为:N₂ + 3H₂ → 2NH₃ + 92.6kJ/mol从反应方程式可以看出,该反应需要大量的氢气,而氮气对反应也起到了催化作用。
在实际生产过程中,合成氨的反应条件一般为300-500°C的温度和100-250atm的压力,同时需要使用铁、钨或镍等金属为催化剂。
三、工业合成氨的生产工艺工业合成氨的生产工艺主要包括氢气制备、氮气制备、合成氨反应和氨气的提取等步骤。
1. 氢气制备氢气是工业合成氨的主要原料之一,通常是通过天然气重整法或电解水法进行制备。
a. 天然气重整法天然气经催化剂重整反应制得合成气,合成气中含有一定比例的氢气。
然后通过甲醇水煤气变换反应得到富含氢气的气体。
b. 电解水法将水分解为氧气和氢气的方法,使用电解槽进行电解水反应,得到纯度高的氢气。
2. 氮气制备氮气是工业合成氨的另一主要原料,一般是从空气中分离得到。
a. 常用的氮气制备方法包括分子筛吸附法、柱塔分离法等。
b. 分子筛吸附法:将空气经过分子筛吸附塔,通过吸附分离得到富含氮气的气体。
c. 柱塔分离法:通过茧状分离塔或塔内吸附塔将空气中的氮气和氧气分离出来。
3. 合成氨反应使用氢气和氮气作为原料,在高压、高温和催化剂(通常是Fe3O4、K₂O、CaO、Al₂O₃或者Ni)的作用下进行反应,得到氨气。
合成氨反应通常分为两个主要阶段:合成氨反应和氨气的提取。
在合成氨反应过程中,氮气和氢气以1:3的比例进入反应器,在压力为100-250bar、温度为300-500°C下进行化学反应。
合成氨工艺原理

合成氨工艺原理合成氨是一种重要的化工原料,广泛应用于农业肥料、化肥、医药和化工等领域。
合成氨工艺是通过将氮气和氢气在一定条件下进行催化反应,生成氨气的过程。
本文将介绍合成氨工艺的原理及其相关知识。
合成氨的工艺原理主要包括氮气和氢气的制备、反应条件和催化剂的选择。
首先,氮气的制备通常采用空分设备从空气中分离得到。
空气中约占78%的氮气,通过空分设备可以将氮气分离出来,纯度达到99.99%以上。
而氢气的制备则通常采用天然气蒸汽重整法或电解水法得到,纯度一般在99.9%以上。
其次,合成氨的反应条件主要包括温度、压力和催化剂。
在工业生产中,通常采用哈伯-玻斯曼工艺,反应温度在400-500摄氏度,压力在100-300大气压。
催化剂通常采用铁-铝催化剂或铁-钼-钾催化剂,能够提高反应速率和选择性。
合成氨的反应过程是一个放热反应,根据Le Chatelier原理,在高温高压条件下,反应达到平衡时,氨气的生成量会增加。
同时,催化剂的选择也会影响反应速率和选择性,合适的催化剂能够提高反应效率和减少副反应产物的生成。
合成氨工艺的原理虽然简单,但在实际应用中仍然面临着一些挑战。
例如,如何提高反应速率和选择性,如何减少能耗和资源消耗,如何处理反应产物中的杂质等问题都是需要解决的。
因此,合成氨工艺的研究仍然具有重要意义。
总之,合成氨工艺是一项重要的化工工艺,其原理涉及氮气和氢气的制备、反应条件和催化剂的选择。
在实际应用中,需要综合考虑反应速率、选择性、能耗和资源消耗等因素,不断优化工艺条件,提高生产效率,减少环境污染,推动合成氨工艺的发展。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
合成氨工艺原理
合成氨不论采用什么原料与生产方法,大体上包括三个工艺过程:(1)原料气的制造;(2)原料气的净化(包括脱硫、变换脱除CO,碳化、脱碳脱除CO
2
,精炼脱
除微量的CO、CO
2、H
2
S、O
2
等);(3)氨的合成与为了满足气体净化及合成各工序
工艺条件提供能量补偿的压缩工序。
生产出氨以后再根据需要加工成碳铵、尿素、硝铵等。
其详细原理如下(以煤为原料):
一、造气工段
合成氨生产所用的半水煤气,要求气体中(CO+H
2)与N
2
的比例为3:1左右。
因
此生产上采用间歇地送入空气与蒸汽进行气化,将所得的水煤气配入部分吹风气制成半水煤气。
即以石灰碳化煤球、无烟块煤为原料,在高温下交替与空气与过
热蒸汽进行气化反应(C+O点燃CO
2+Q 、2C+O点燃2CO+Q 、2CO+ O点燃2CO
2
+ Q
2H
2O(气)+C△CO+2H
2
-Q制得半水煤气,半水煤气经过除尘,余热回收,水洗降温制
得合格的半水煤气,供后工段使用。
二、脱硫工段
从造气工段的半水煤气中,除氢气与氮气外,还含有27%左右CO、9%左右的CO
2
以及少量的硫化物,这些硫化物对合成氨生产就是有害的。
它会腐蚀设备、管道,会引起催化剂中毒,会损坏铜液成份。
因此,必须除去少量硫化物,其原理:用
稀氨水(10—15tt)与硫化氢反应(NH
3+H
2
S=NH
4
HS)将H
2
S脱除至0、07g/m3(标)以下,
使半水煤气净化,以满足合成氨生产工艺要求。
三、变换工段
将脱S后的半水煤气(含CO25%—28%)由压缩工段加压后经增温、加热,在一定的温度与压力下,在变换炉内借助催化剂的催化作用,使半水煤气中CO与H
2
O(气)
进行化学反应,转变为CO
2与H
2
(CO+H
2
O(气)催化剂高温CO
2
+H
2
+Q),制得合格的变
换气,以满足后工段的工艺要求。
其次,系统中设有饱与热水塔、甲交、一水加、二水加、冷却塔等换热设备,以便合理利用反应热与充分回收余热,降低能耗,同时降低变换气温度。
四、碳化与脱碳工段
1、碳化
将变换气中26%左右的CO
2用浓氨水与其反应(CO
2
+ H
2
O+ NH
3
=NH
4
HCO
3
)生成
碳酸
氢铵副产品,同时制得合格的原料气。
2、脱碳工段
用MEDA脱碳溶液将变换气中26%左右的CO
2
除去,制成合格的原料气,供后工段使用。
五、压缩机工段
合成氨原料气的制备、净化及氨的合成都要在一定的压力下进行。
为适应变换、碳化、脱碳、精炼、合成等工段的工艺要求,要把气体加压,并按需要的不同压力分别输送到以上各工段,这些工作必须通过压缩机来完成。
因此,压缩工段就就是运送气体与提高气体压力,以满足合成氨生产的原料气制备、净化与氨合成工段的需要。
六、精炼工段
用醋酸铜氨液来吸收经碳化、脱硫后的原料气中少量CO
2、CO、H
2
S等,制得
合格的精炼气,供合成工段使用。
七、合成工段
合成工段在合成氨生产中就是最后一道工序,它就是在高温、高压与有催化剂存在的条件下,将由精炼工段来的经过一系列处理的合格氢氮混合气体在合成
塔内进行化合反应,合成为氨。
(3H
2+N
2
催化剂高温高压2 NH
3
),气态氨经冷凝
分离得液氨,液氨在氨冷器中气化后,送经碳化、精炼用。
多余的液氨作为商品氨。
未合成氨的氢、氮混合气继续在合成系统中循环。
合成放空气与氨罐弛放气回收利用。
八、冰机岗位
将气氨压缩、冷凝使之液化,然后将液氨送往氨贮槽或直接送入氨冷器蒸发制冷以满足合成氨生产中冷量的需要。
